Cho a mol Al tan hoàn toàn vào dung dịch chứa b mol HCl thu được dung dịch Y chứa 2 chất tan có cùng nồng độ mol. Thêm từ từ dung dịch NaOH vào dung dịch Y ta có đồ thị sau:
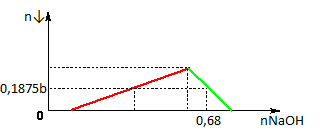
Cho a mol Al phản ứng với dung dịch hỗn hợp chứa 0,15b mol FeCl3 và 0,2b mol CuCl2. Sau khi phản ứng kết thúc thu được x gam chất rắn. Giá trị của x là:
A. 11,776. B. 12,896.
C. 10,874. D. 9,864.
Câu trả lời tốt nhất
Dung dịch Y chứa nAlCl3 = nHCl = a
Bảo toàn Cl —> 4a = b (1)
nOH- = nH+ + 4nAl3+ – nAl(OH)3
⇔ 0,68 = a + 4a – 0,1875b (2)
(1)(2) —> a = 0,16 và b = 0,64
Vậy: nFeCl3 = 0,096 và nCuCl2 = 0,128
Sau phản ứng dung dịch thu được chứa Cl- (0,544), Al3+ (0,16), bảo toàn điện tích —> nFe2+ = 0,032
—> Chất rắn gồm Fe (0,096 – 0,032 = 0,064) và Cu (0,128)
—> m rắn = 11,776
Admin cho em hỏi, dạng bài tập kết tủa Al(OH)3 tan trong NaOH/HCl đã được giảm tải vào năm 2020, nhưng năm nay các trường vẫn ra đề thi thử có dạng này. Cho em hỏi có nên ôn dạng bài tập này không ạ, vì nếu đã giảm tải thì không thi nữa ạ.
