Hình vẽ minh họa sau đây dùng để điều chế và thu khí SO2 trong phòng thí nghiệm.
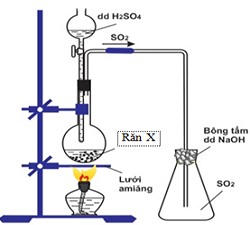
1. Nêu tên các dụng cụ thí nghiệm trong hình vẽ.
2. Viết 2 phương trình phản ứng minh họa tương ứng với các hóa chất A, B.
3. Nêu vai trò của bông tẩm dung dịch D, viết phương trình minh họa.
4. Làm thế nào để biết bình đã đầy khí SO2.
5. Cho 2 hóa chất là dung dịch H2SO4 đặc và CaO rắn. Hóa chất nào được dùng và không được dùng để làm khô khí SO2. Giải thích?
6. Bộ dụng cụ ở trên còn được dùng để điều chế khí hiđroclorua. Viết phương trình phản ứng minh họa.
Câu trả lời tốt nhất
Các dụng cụ: Phễu có khóa, bình cầu, bình tam giác, giá đỡ, ống thủy tinh, đèn cồn, bông.
Na2SO3 + H2SO4 —> Na2SO4 + SO2 + H2O
NaHSO3 + H2SO4 —> Na2SO4 + SO2 + H2O
Bông tẩm dung dịch NaOH để ngăn SO2 thoát ra ngoài:
SO2 + NaOH —> Na2SO3 + H2O
SO2 + H2O + Na2SO3 —> NaHSO3
Nhỏ thêm 1 giọt phenolphtalein vào bông tẩm NaOH, không thấy màu hồng chứng tỏ khí SO2 đã đầy (lúc này dung dịch ở bông là NaHSO3, có tính axit yếu)
Dùng H2SO4 đặc làm khô SO2 vì H2SO4 đặc không phản ứng với SO2. Không dùng CaO làm khô vì CaO có phản ứng:
CaO + SO2 —> CaSO3
Điều chế HCl từ bộ dụng cụ trên:
MnO2 + HCl —> MnCl2 + Cl2 + H2O
