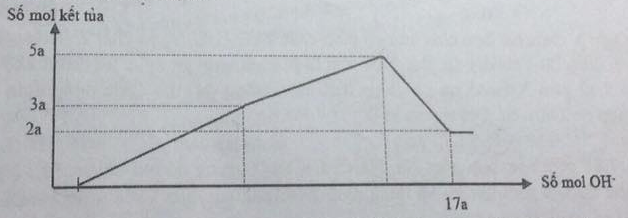
Hòa tan hết 12,06 gam hỗn hợp gồm Mg và Al2O3 trong dung dịch chứa HCl 0,5M và H2SO4 0,1M. Sau khi kết thúc phản ứng thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào dung dịch X, phản ứng biểu diễn theo đồ thị sau:
Nếu cho từ từ V ml dung dịch NaOH 0,3M và Ba(OH)2 0,1M vào dung dịch X, thu được lượng kết tủa lớn nhất, lấy kết tủa nung ngoài không khí đến khối lượng không đổi thu được m gam rắn khan. Giá trị m là
A. 37,860 B. 41,940 C. 48,152 D. 53,124
Câu trả lời tốt nhất
Đặt 5x và x là mol của HCl và H2SO4
Dựa vào đồ thị ta thấy nMg(OH)2 = 2a và n↓ max = 5a —> nAl(OH)3 = 3a
Vậy ban đầu nMg = 2a và nAl2O3 = 1,5a
—> 24.2a + 102.1,5a = 12,06
—> a = 0,06
Dung dịch X chứa Mg2+ (0,12); Al3+ (0,18); Cl- (5x); SO42- (x) —> nH+ = 7x – 0,78
—> nOH- = 17.0,06 = 7x – 0,78 + 0,12.2 + 0,18.4
—> x = 0,12
—> X chứa Mg2+ (0,12); Al3+ (0,18); Cl- (0,6); SO42- (0,12); H+ (0,06)
nNaOH = 3y & nBa(OH)2 = y —> nBa2+ = y và nOH- = 5y
Khi BaSO4 đạt max tại y = 0,12:
nOH- = 0,6 < nH+ + 2nMg2+ + 3nAl3+ = 0,84 —> Hidroxit chưa đạt max
—> Khi nOH- = 0,84 thì các kết tủa đều cực đại, bao gồm BaSO4 (0,12); Mg(OH)2 (0,12), Al(OH)3 (0,18)
Nung thu được m rắn = 41,94
