Hòa tan hoàn toàn hỗn hợp gồm Al và Al2O3 trong dung dịch chứa x mol HCl và y mol H2SO4 loãng, thu được khí H2 và dung dịch X. Thực hiện hai thí nghiệm sau:
– Cho từ từ dung dịch NaOH đến dư vào dung dịch X.
– Cho từ từ dung dịch Ba(OH)2 đến dư vào dung dịch X.
Sự phụ thuộc số mol kết tủa với số mol NaOH hay số mol Ba(OH)2 ở hai thí nghiệm trên được biểu thị theo hai đồ thị sau:
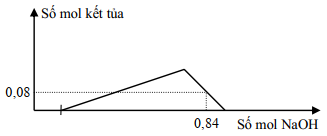

Tỉ lệ x : y là
A. 2 : 1. B. 3 : 2. C. 1 : 1. D. 3 : 1.
Câu trả lời tốt nhất
Đồ thị 2, tại đoạn 1:
H+ + OH- —> H2O
Ba2+ + SO42- —> H2O
nBa(OH)2 = 0,06 —> nH+ dư = 0,12
Đồ thị 1: nOH- = nH+ + 4nAl3+ – nAl(OH)3
Với nOH- = 0,84, nH+ = 0,12 và nAl(OH)3 = 0,08 —> nAl3+ = 0,2
Vậy X chứa Al3+ (0,2), H+ (0,12), Cl- (x) và SO42- (y)
Bảo toàn điện tích —> x + 2y = 0,2.3 + 0,12 (1)
Đồ thị 2, khi dùng 0,41 mol Ba(OH)2 thì Al(OH)3 đang bị hòa tan nhưng chưa hết.
nBaSO4 = y —> nAl(OH)3 = 0,34 – y
nOH- = nH+ + 4nAl3+ – nAl(OH)3
⇔ 0,41.2 = 0,12 + 4.0,2 – (0,34 – y) (2)
(1)(2) —> x = 0,24; y = 0,24
—> x : y = 1 : 1
