[2025 – 2026] Thi học sinh giỏi lớp 12 cụm TP Hải Phòng (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Tổng hợp đề hsg theo năm học
⇒ Mã đề 011-H12A năm 2025-2026
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1A | 2A | 3B | 4D | 5B | 6B | 7D | 8A | 9B | 10A |
| 11B | 12C | 13A | 14B | 15C | 16D | 17D | 18A | 19A | 20D |
| Câu 21 | Câu 22 | Câu 23 | Câu 24 | Câu 25 | |
| (a) | S | S | S | Đ | S |
| (b) | S | S | Đ | S | Đ |
| (c) | Đ | Đ | S | Đ | S |
| (d) | S | S | S | S | Đ |
| 26 | 27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 |
| 20,2 | 1 | 842 | 3 | 9 | 0,12 | 421 | 33 | 7,8 | 41 |
PHẦN 1: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 20. Mỗi câu hỏi thí sinh chỉ lựa chọn một phương án.
(Xem giải) Câu 1: Trong nước sinh hoạt, tiêu chuẩn hàm lượng ammonium (NH4+) cho phép là 1,0 mg/L. Để loại bỏ ion ammonium trong nước thải, người ta cho dư dung dịch NaOH vào nước thải cho đến pH = 11, sau đó cho nước chảy từ trên xuống trong một tháp tiếp xúc, đồng thời không khí được thổi ngược từ dưới lên để oxi hoá NH3. Phương pháp này loại bỏ được 95% lượng ammonium trong nước thải. Phân tích mẫu nước thải ở hai nguồn khác nhau chưa qua xử lý có kết quả như sau:
| Mẫu | Nguồn nước | Hàm lượng ammonium |
| 1 | Nhà máy phân đạm | 18 mg/L |
| 2 | Bãi chôn lấp rác | 160 mg/L |
Tiến hành xử lý hai mẫu nước thải bằng phương pháp trên, sau khi xử lý, mẫu nào đạt tiêu chuẩn cho phép về hàm lượng ammonium?
A. Mẫu 1. B. Mẫu 2. C. Cả 2 mẫu. D. Không mẫu nào.
(Xem giải) Câu 2: Cho X, Y, T là ba nguyên tố liên tiếp nhau trong một chu kì của bảng tuần hoàn các nguyên tố hóa học. Tổng số các hạt mang điện trong thành phần cấu tạo nguyên tử của X, Y, T bằng 72. Phát biểu nào sau đây không đúng?
A. Bán kính ion theo thứ tự tăng dần là X+ < Y2+ < T3+.
B. Các ion X+, Y2+, T3+ có cùng cấu hình electron 1s2 2s2 2p6.
C. Bán kính của nguyên tử theo thứ tự giảm dần là X > Y > T.
D. Nguyên tố X, Y, T đều có tính chất hóa học cơ bản là tính kim loại.
(Xem giải) Câu 3: Phân bón là sản phẩm có chức năng cung cấp chất dinh dưỡng cho cây trồng hoặc có tác dụng cải tạo đất. Phát biểu nào sau đây sai?
A. Không nên bón vôi sống (thành phần chính là CaO) cùng với phân đạm ammonium.
B. Nên bón phân ngay trước hoặc sau khi mưa to, khi thời tiết nắng nóng.
C. Phân superphosphate đơn chứa nhiều calcium sulfate ít tan, tích tụ trong đất, làm đất dần trở lên chai cứng.
D. Việc bón dư thừa phân bón vô cơ, hàm lượng chất dinh dưỡng dư thừa bị rửa trôi, đặc biệt là dinh dưỡng chứa nitrogen và phosphorus gây ra hiện tượng phú dưỡng ở các ao, hồ.
(Xem giải) Câu 4: Cho phản ứng: Na2SO3 + NaHSO4 + KMnO4 → Na2SO4 + MnSO4 + K2SO4 + H2O. Tổng hệ số của các chất (là những số nguyên, tối giản) trong phương trình phản ứng đó là
A. 21. B. 47. C. 23. D. 27.
(Xem giải) Câu 5: Cho thông tin như hình dưới đây:
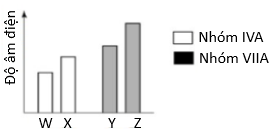
Trong bảng tuần hoàn, W, X, Y, Z thuộc chu kì 2 hoặc 3. Cho các phát biểu sau:
(a) Bán kính nguyên tử: Z > X > Y > W.
(b) Hydroxide ứng với hoá trị cao nhất của Z có công thức là HZO4.
(c) Hợp chất của X với hydrogen là thành phần chính của khí thiên nhiên và khí dầu mỏ.
(d) Hợp chất HZ có tính acid mạnh nên ăn mòn thuỷ tinh vô cơ.
(e) Oxide ứng với hoá trị cao nhất của W là WO2.
Số các phát biểu đúng là
A. 4. B. 2. C. 3. D. 1.
(Xem giải) Câu 6: Cho sơ đồ chuyển hóa sau:
X(l) + 2NaOH(aq) → CH2(COONa)2(aq) + CH3OH(aq) + C2H5OH(aq)
Nhận xét nào sau đây sai về chất X?
A. Công thức cấu tạo của X là:
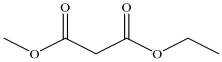
B. Tên của X là ethyl methyl oxalate.
C. Các phân tử X không tạo được liên kết hydrogen với nhau.
D. X là ester no, có hai nhóm chức, công thức phân tử là C6H10O4.
(Xem giải) Câu 7: Cho các vật liệu polymer thuộc loại chất dẻo mô tả như hình sau.

Các polymer này có thể tái chế được, các kí hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng như thuận lợi trong việc thu gom và tái chế. Phát biểu nào sau đây đúng?
A. Các polymer trên đều được tổng hợp từ phản ứng trùng hợp các monomer tương ứng.
B. Trong 6 polymer trên, có 3 polymer nhiệt dẻo và 3 polymer nhiệt rắn.
C. Loại polymer 3 là nguyên liệu chính để sản xuất túi nylon, màng bọc thực phẩm…
D. Hộp xốp đựng thực phẩm chế biến sẵn thường làm bằng polymer số 6, và không nên sử dụng các hộp này để đựng thức ăn nóng hoặc cho hộp vào lò vi sóng.
(Xem giải) Câu 8: Năm 2020, một vụ nổ tại Thủ đô Beirut, Lebanon đã cướp đi sinh mạng hàng trăm người. Nguyên nhân vụ nổ được cho là do sự phân huỷ 2750 tấn ammonium nitrate trên một tàu hàng bỏ hoang theo phương trình hoá học sau: NH4NO3(s) → N2O(g) + 2H2O(g)  = -36 kJ
= -36 kJ
Nhiệt của vụ nổ trên tương đương lượng nhiệt của bao nhiêu tấn thuốc nổ TNT (2,4,6-trinitrotoluene), biết nhiệt tỏa ra khi 1 kg TNT phát nổ là 1,165 MJ. Biết 1 MJ = 1.10^6 J (làm tròn đến hàng đơn vị)
A. 1062. B. 1500. C. 1400. D. 1620.
(Xem giải) Câu 9: Một bạn học sinh thực hiện thí nghiệm như hình vẽ và đưa ra các nhận định sau:
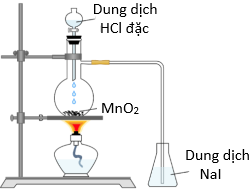
Điều chế và thử tính chất khí chlorine trong phòng thí nghiệm
(1) Khi khí chlorine sinh ra tác dụng với dung dịch NaI có thể dùng hồ tinh bột để chứng tỏ sự tạo thành I2.
(2) Có thể thay dung dịch HCl đặc bằng dung dịch H2SO4 đặc.
(3) Thí nghiệm trên chứng tỏ tính oxi hoá của iodine mạnh hơn chlorine.
(4) Để thu được khí chlorine tinh khiết thì đưa ống dẫn khí vào lần lượt hai bình đựng dung dịch H2SO4 đặc và dung dịch NaCl, rồi thu khí.
(5) Khi kết thúc thí nghiệm nên tắt đèn cồn trước rồi tháo ống dẫn khí sau.
(6) Trong công nghiệp, chlorine được sản xuất bằng cách điện phân dung dịch muối ăn bão hoà không cần màng ngăn giữa các điện cực.
Số nhận định đúng là
A. 3. B. 1. C. 5. D. 4.
(Xem giải) Câu 10: Sorbic acid hay hexa-2,4-dienoic acid là carboxylic acid đơn chức. Sorbic acid được dùng làm chất bảo quản trong đồ uống từ sữa, các loại phomat, quả khô, mứt, kẹo cao su, mỳ ống, mỳ sợi,… Theo TT 24/2019/TT-BYT về mức sử dụng tối đa phụ gia trong thực phẩm (ML) thì sorbic acid có giá trị ML là 1000 mg.kg-1 đối với đồ uống từ sữa dạng lỏng có hương vị (sữa tươi có hương vị, sữa chua vị trái cây,…). Cho các phát biểu sau:
(1) Sorbic acid có công thức phân tử là C6H8O4.
(2) Dung dịch sorbic acid làm phenolphtalein chuyển sang màu hồng.
(3) Khi phân tích một lô sữa tươi có khối lượng 180 gam/hộp, được kết quả thành phần trong một hộp có chứa 160,5 mg sorbic acid. Vậy lô sữa tươi này có lượng sorbic acid nằm trong mức được phép sử dụng phụ gia theo TT 24/2019/TT-BYT.
(4) Trên thực tế, việc chuyển hóa sorbic acid thành muối sorbate giúp cải thiện tính hòa tan, ổn định và hiệu quả bảo quản của sản phẩm, đồng thời hạn chế ảnh hưởng xấu đến hương vị của thực phẩm. Khi cho 22,4 gam sorbic acid phản ứng hoàn toàn với dung dịch KOH dư thì sẽ thu được 38,2 gam muối potassium sorbate.
Số phát biểu đúng là
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 11: Arachidonic acid (ARA) là một acid béo thiết yếu có vai trò quan trọng trong việc kích hoạt các dây thần kinh trong não và hỗ trợ cho nhiều chức năng khác như hệ miễn dịch, tạo mạch máu, phát triển xương và hoạt động của tim. ARA có công thức cấu tạo như hình dưới đây:
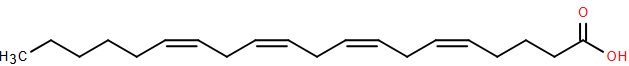
Cho các phát biểu sau:
(1) ARA thuộc loại acid béo omega-6.
(2) Trong một phân tử ARA có 11 nhóm methylene.
(3) Triester của glycerol với ARA có công thức phân tử C63H92O6.
(4) a mol ARA tác dụng tối đa với 4a mol H2 (xt, t°, p).
(5) Dầu cá biển chứa nhiều acid béo omega-6; các loại dầu thực vật (dầu mè, dầu đậu nành, dầu hướng dương,…) chứa nhiều acid béo omega-3.
Số phát biểu sai là
A. 4. B. 3. C. 2. D. 1.
(Xem giải) Câu 12: Biểu tượng (1) và (2) dưới đây lần lượt đại diện tương ứng cho yếu tố nào trong phản ứng cháy?

A. chất cháy và nhiên liệu. B. chất cháy và chất oxi hóa.
C. chất oxi hóa và chất cháy. D. chất oxi hóa và nhiên liệu.
(Xem giải) Câu 13: Squalene là một hydrocarbon mạch hở, là chất lỏng, sánh, không màu ở điều kiện thường, có tác dụng dưỡng ẩm, chống oxi hóa, tăng cường miễn dịch… Kết quả phân tích nguyên tố cho thấy trong phân tử Squalene chứa 87,80% carbon về khối lượng. Từ phổ khối lượng (MS), xác định được phân tử khối của Squalene là 410. Khi cho 0,1 mol Squalene tác dụng với nước bromine, thấy lượng Br2 phản ứng tối đa là x mol. Giá trị của x là
A. 0,6. B. 0,5. C. 0,3. D. 0.4.
(Xem giải) Câu 14: Cho các phát biểu sau:
(1) Phản ứng CH4 + Cl2 → CH3Cl + HCl xảy ra theo cơ chế gốc (SR).
(2) Trong phản ứng hữu cơ, tác nhân electrophile là tác nhân có ái lực với hạt nhân.
(3) Phản ứng cộng vào nối đôi C=C của alkene với halogen, với halogen halide, với nước (trong môi trường acid) xảy ra theo cơ chế cộng nucleophile.
(4) Trong cơ thể con người, gốc tự do được sinh ra từ các quá trình trao đổi chất, trong đó tồn tại gốc tự do có lợi và có hại. Để giảm thiểu tác động tiêu cực của gốc tự do, chúng ta có thể sử dụng các chất chống oxi hoá như vitamin C, E, và β-carotene.
Phát biểu đúng là
A. (2), (4). B. (1), (4). C. (2), (3). D. (1), (3).
(Xem giải) Câu 15: Một nhà máy nhiệt điện khí có sản lượng điện 10^6 kWh/ngày (1kWh = 3600 kJ) đã sử dụng khí thiên nhiên hóa lỏng LNG (chứa 96% CH4, 4% C2H6 về thể tích) làm nhiên liệu. Các nhiên liệu bị đốt cháy hoàn toàn tạo ra sản phẩm khí (biết 64% nhiệt lượng tỏa ra của quá trình đốt cháy được chuyển hóa thành điện năng). Khối lượng khí CO2 mà nhà máy này thải ra trong 1 tháng (30 ngày) ngày là m tấn (làm tròn kết quả đến hàng phần trăm). Biết nhiệt bay hơi của H2O(l) ở 25°C và 1 bar là 44 kJ/mol; CH4 và C2H6 cháy theo các phương trình nhiệt hóa học:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)  = -893 kJ
= -893 kJ
C2H6(g) + 3,5O2(g) → 2CO2(g) + 3H2O(l)  = -1560 kJ
= -1560 kJ
Giá trị của m là
A. 3139,50. B. 1791,20. C. 9304,51. D. 9101,51.
(Xem giải) Câu 16: Cho sơ đồ xen phủ các orbital nguyên tử tạo liên kết sau:
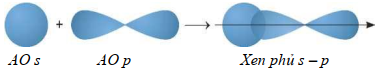
Liên kết giữa các nguyên tử trong phân tử nào dưới đây phù hợp với sơ đồ trên?
A. Chlorine. B. Nitrogen. C. Hydrogen. D. Hydrogen chloride.
(Xem giải) Câu 17: X là một disaccharide có công thức cấu tạo sau:
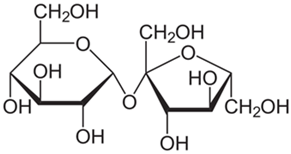
Cho các nhận định sau:
a) Phần trăm khối lượng của carbon trong X là 42,11% (làm tròn kết quả đến hàng phần trăm).
b) Dung dịch của X hòa tan Cu(OH)2 trong môi trường kiềm tạo dung dịch màu xanh lam.
c) Trong phân tử X có chứa liên kết α-1,4-glycoside.
d) Thủy phân hỗn hợp gồm 0,01 mol chất X và 0,02 mol maltose trong môi trường acid, với hiệu suất đều là 60% theo mỗi chất, thu được dung dịch A. Trung hòa dung dịch A thu được dung dịch B, sau đó cho toàn bộ B tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, đun nóng thu được m gam Ag. Giá trị của m là 7,776.
Số nhận định đúng là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 18: Năm 1918, E. Rutherford và các cộng sự đã phát hiện ra hạt X khi dùng hạt α bắn phá nitrogen. Phương trình phản ứng hạt nhân như sau: ![]() +
+ ![]() →
→ ![]() + X. Kí hiệu của X là
+ X. Kí hiệu của X là
A. p. B. n. C. e. D. ![]() .
.
(Xem giải) Câu 19: Cho hình vẽ sau:
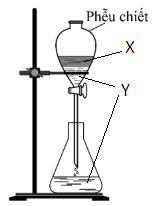
X, Y có thể là những chất nào?
A. Tinh dầu sả chanh và nước cất. B. Acetic acid và ethanol.
C. Ethanol và nước cất. D. Nước đường và nước cất.
(Xem giải) Câu 20: X là hợp chất mạch hở (chứa C, H, O) có phân tử khối bằng 90. Cho X tác dụng với Na dư thu được số mol H2 bằng số mol X phản ứng. Mặt khác, X có khả năng phản ứng với NaHCO3. Số công thức cấu tạo của X có thể là
A. 5. B. 4. C. 2. D. 3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 21 đến câu 25. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 21: Cùng một lượng kim loại Zn phản ứng với cùng một thể tích dung dịch H2SO4 1M, nhưng ở hai nhiệt độ khác nhau theo phản ứng: Zn + H2SO4 → ZnSO4 + H2. Thể tích khí H2 sinh ra ở mỗi thí nghiệm theo thời gian được biểu diễn ở đồ thị sau:

a) Đồ thị (1) mô tả phản ứng xảy ra ở nhiệt độ thấp hơn phản ứng xảy ra ở đồ thị (2).
b) Thể tích khí sinh ra ở đồ thị (1) luôn nhiều hơn thể tích khí sinh ra ở đồ thị (2).
c) Kết thúc phản ứng, lượng muối ZnSO4 thu được ở cả hai thí nghiệm là như nhau.
d) Trong một thí nghiệm, người ta đo được tốc độ trung bình của phản ứng zinc (dạng bột) với dung dịch H2SO4 loãng là 0,005 mol/s. Nếu ban đầu cho 0,4 mol zinc (dạng bột) với dung dịch H2SO4 ở trên thì sau 1 phút còn lại 0,05 mol zinc.
(Xem giải) Câu 22: Sulfuric acid là hoá chất hàng đầu được dùng trong nhiều ngành sản xuất. Sulfuric acid được dùng để sản xuất phân bón, chất giặt rửa tổng hợp, tơ sợi hoá học, chất dẻo, sơn màu, phẩm nhuộm, dược phẩm, chế biến dầu mỏ,… Trong công nghiệp, sulfuric acid chủ yếu được sản xuất bằng phương pháp tiếp xúc theo sơ đồ sau:
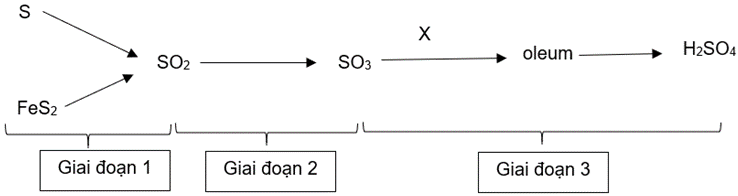
a) Trong sơ đồ trên, tất cả các phản ứng xảy ra đều là phản ứng oxi hoá – khử.
b) Để tiết kiệm hoá chất, giai đoạn 3 chất X có thể lấy là H2O.
c) Khi bị bỏng sulfuric acid thì thao tác đầu tiên là nhanh chóng rửa ngay với nước lạnh nhiều lần.
d) Để xác định công thức của một oleum (H2SO4.nSO3), người ta pha loãng 8,36 gam oleum đó vào nước thành 1,0 lít dung dịch sulfuric acid, sau đó tiến hành chuẩn độ mỗi 10,0 mL dung dịch acid này bằng dung dịch NaOH 0,10M. Thể tích dung dịch NaOH trung bình cần sử dụng để chuẩn độ là 20,01 mL. Giá trị của n xác định được là 3.
(Xem giải) Câu 23: Biodiesel (diesel sinh học) là một loại nhiên liệu lỏng, thân thiện hơn với môi trường so với diesel truyền thống. Biodiesel được sản xuất thông qua phản ứng giữa chất béo với các alcohol mạch ngắn (thường là methanol), với xúc tác là kiềm, thu được biodiesel (ester của acid béo) và glycerol. Một nhà máy tái chế dầu ăn đã qua sử dụng để sản xuất biodiesel theo phương trình phản ứng tổng quát sau:
(RCOO)3C3H5 + 3CH3OH (NaOH) → 3RCOOCH3 + C3H5(OH)3 (1)
a) Biodiesel có thành phần nguyên tố giống dầu diesel truyền thống.
b) Phương pháp trên giúp tận dụng dầu ăn đã qua sử dụng, giảm ô nhiễm môi trường do dầu ăn thải gây ra.
c) Phản ứng (1) sinh ra sản phẩm là ethanol được ứng dụng làm rượu, bia.
d) Từ 500 kg một loại dầu ăn đã qua sử dụng có chứa 86% chất béo (phân tử khối trung bình của chất béo là 860 amu), còn lại là tạp chất không có khả năng chuyển hóa thành biodiesel, có thể tạo tối đa 432 kg biodiesel dạng methyl ester với hiệu suất chuyển hóa là 90%.
(Xem giải) Câu 24: Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 ml dung dịch X. Lấy chính xác 10 ml dung dịch X, thêm 10 ml dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như sau:
| Lần chuẩn độ | 1 | 2 | 3 |
| V dung dịch KMnO4 (mL) | 16,0 | 16,1 | 16,0 |
Cho các phát biểu:
a) Dung dịch H2SO4 được thêm vào dung dịch chuẩn độ để tạo thành môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành Mn2+.
b) Có thể thay dung dịch H2SO4 bằng dung dịch acid mạnh như HCl, HNO3 nhưng phải đảm bảo lượng H+ dư sau phản ứng.
c) Trong mỗi lần chuẩn độ, dung dịch KMnO4 được xem là phản ứng vừa đủ với muối Mohr (điểm dừng) khi giọt dung dịch KMnO4 cuối cùng nhỏ vào dung dịch Y không mất màu.
d) Theo kết quả chuẩn độ ở trên, trong số các giá trị: 93,32; 98,45; 97,36; 99,87 độ tinh khiết (% khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr có giá trị gần nhất với 98,45.
(Xem giải) Câu 25: Adipic acid là hóa chất quan trọng được dùng trong sản xuất vải sợi (nylon-6,6) và nhiều sản phẩm thông dụng khác như thảm, dây thừng hay lông bàn chải đánh răng… Các nhà nghiên cứu thuộc Viện Công nghệ sinh học và Công nghệ Nano (IBN) của Singapore vừa phát hiện một sơ đồ hóa học mới có thể chuyển hóa đường glucose thành adipic acid như sau:
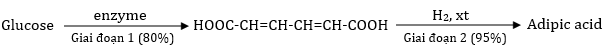
Trong công nghiệp adipic acid được dùng để sản xuất poly(hexamethylene adipamide) qua phản ứng trùng ngưng giữa hexamethylenediamine và adipic acid với hiệu suất đạt 90%.
a) 1,0 mol mucic acid làm mất màu tối đa 2,0 mol Br2 tạo ra chất hữu cơ có phần trăm khối lượng bromine là 68,67% (Kết quả được làm tròn đến hàng phần trăm).
b) Hiện nay, nylon-6,6 được dùng để sản xuất chỉ nha khoa chứa 90% poly(hexamethylene adipamide). Lượng adipic acid được tạo ra từ 216 kg glucose theo sơ đồ (1) có thể sản xuất được 206 kg chỉ nha khoa (Kết quả làm tròn đến phần nguyên).
c) Trong 1 phân tử adipic acid có 16 liên kết sigma.
d) Tơ nylon-6,6 thuộc loại tơ tổng hợp.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 26 đến câu 35.
(Xem giải) Câu 26: Rutin là hợp chất hữu cơ có trong nụ hoa hòe, nó có tác dụng làm giảm các chứng suy giảm tĩnh mạch, giảm cholesterol trong máu. Ngoài ra rutin còn được dùng để điều chế thuốc quercetin có tác dụng chống oxy hóa mạnh, kháng viêm, chống dị ứng, ngăn ngừa tế bào ung thư. Công thức cấu tạo của rutin và quercetin như hình dưới đây:
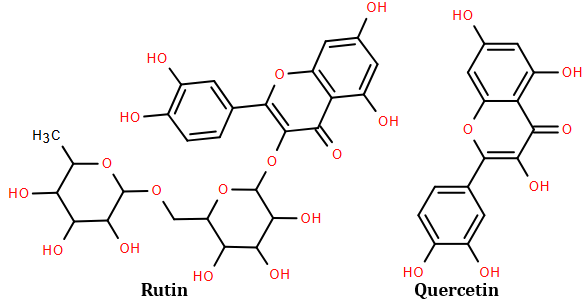
Trong môi trường acid, một phân tử rutin phản ứng với hai phân tử nước thu được sản phẩm gồm quercetin, glucose và rhamnose. Biết hàm lượng quercetin trong một viên thuốc có khối lượng 500 mg là 96,64% về khối lượng, phần còn lại là tá dược khác. Để sản xuất 5 triệu viên thuốc trên, cần bao nhiêu tấn bột hoa hòe? (Biết hàm lượng rutin trong bột hoa hòe là 30,20%, phần còn lại không tạo ra quercetin; hiệu suất toàn bộ quá trình sản xuất đạt 80%) (Làm tròn kết quả đến hàng phần mười).
(Xem giải) Câu 27: Ethylene được ứng dụng rộng rãi trong việc sản xuất bao bì, dệt may, điện tử, vận chuyển, sử dụng cho ngành chất dẫn xuất và ngành hóa dầu. Ethylene tham gia vào các phản ứng tạo ra hóa chất, tổng hợp các chất hữu cơ như: ethylene glycol, ethanol,… Sơ đồ dưới đây tổng hợp một số chất hữu cơ từ ethylene:
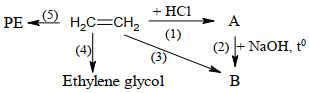
Biết rằng A, B đều là các chất hữu cơ. Cho các phát biểu sau:
(a) Phản ứng (5) thuộc loại phản ứng trùng ngưng.
(b) Hợp chất hữu cơ B là CH3CH2OH.
(c) Tên thay thế của chất A là ethyl chloride.
(d) Các phản ứng (1), (2), (3), (4) đều là phản ứng cộng.
Có bao nhiêu phát biểu đúng?
(Xem giải) Câu 28: Sử dụng vôi sữa là phương pháp phổ biến để xử lý khí thải SO2. Với sản phẩm thu 90% khí SO2 theo phương trình hóa học: Ca(OH)2 + SO2 → CaSO3 + H2O. CaSO3 bị oxi hóa hoàn toàn thành CaSO4 dưới tác dụng của O2. Sau đó, CaSO4 được lọc tách, làm sạch, nung khô và thu hồi dưới dạng thạch cao thương phẩm (2CaSO4.H2O) với hiệu suất 80%. Một nhà máy trong một ngày thải ra 2000 m³ (đkc) khí thải chứa 1% về thể tích là SO2. Bằng phương pháp trên, tính khối lượng (kg) 2CaSO4.H2O thu được trong 10 ngày? (Làm tròn kết quả đến hàng đơn vị).
(Xem giải) Câu 29: Khảo sát một số tính chất của ba chất X, Y, Z được ghi lại trong bảng sau:
| Chất | Nhiệt độ nóng chảy (°C) | Quỳ tím |
| X | -6,3 | Không đổi màu |
| Y | 233 | Không đổi màu |
| Z | 247 | Màu hồng |
Biết X, Y, Z là một trong ba chất glycine (Gly), aniline, glutamic acid (Glu). Cho các nhận định sau:
a) Ở pH < 6, Y nhận proton trở thành cation và di chuyển về cực âm khi đặt trong điện trường.
b) X tác dụng với nitrous acid ở nhiệt độ thấp (0-5°C) tạo thành muối diazonium (thường được dùng tổng hợp phẩm nhuộm azo và dược phẩm).
c) Thuỷ phân hoàn toàn 1,0 mol peptide A thu được 3,0 mol Y và 2,0 mol Z. Mặt khác, nếu thuỷ phân không hoàn toàn A thu được hỗn hợp các peptide và các α-amino acid, trong đó có tripeptide Gly-Glu-Glu. Có 2 công thức A thoả mãn tính chất trên.
d) Hỗn hợp M gồm Lys-Y-Ala, Lys-Ala-Lys-Lys-Lys-Y và Ala-Y trong đó oxygen chiếm 19,9% về khối lượng. Cho 0,1 mol M tác dụng vừa đủ với dung dịch HCl thu được m gam muối. Giá trị của m là 67,5 (Làm tròn kết quả đến hàng phần mười).
Số nhận định đúng là bao nhiêu?
(Xem giải) Câu 30: Xăng E5 được sản xuất bằng cách phối trộn xăng khoáng RON 92 với ethanol (D = 0,8 gam/ml) theo tỉ lệ thể tích tương ứng là 95 : 5. Ethanol được sản xuất từ tinh bột bằng phương pháp lên men. Tinh bột có nhiều trong sắn, ngô. Cho bảng thông tin sau:
| Nguyên liệu | Sắn tươi (khoai mì) | Ngô khô (bắp khô) |
| Hàm lượng tinh bột | 30% | 75% |
| Giá 1 kilogam nguyên liệu | 1850 đồng | 6500 đồng |
Biết hiệu suất của toàn bộ quá trình sản xuất từ sắn tươi đạt 79,83%, từ ngô khô đạt 84,783%. Để điều chế 50000 lít xăng E5 từ sắn tươi cần chi x triệu đồng, từ ngô khô cần chi y triệu đồng. Chênh lệch tiền nguyên liệu là z (triệu đồng) khi dùng sắn tươi so với dùng ngô khô để sản xuất. Tính giá trị của z (Làm tròn kết quả đến phần nguyên, chỉ lấy giá trị chênh lệch không lấy dấu).
(Xem giải) Câu 31: Cho phản ứng: CO(g) + Cl2(g) ⇋ COCl2(g) được thực hiện trong bình kín dung tích 1 lít ở nhiệt độ không đổi. Khi phản ứng đạt trạng thái cân bằng, nồng độ của các chất là: [CO] = 0,2M; [Cl2] = 0,1M; [COCl2] = 0,2M. Nếu bơm thêm vào bình 14,2 gam Cl2 thì nồng độ mol/L của CO ở trạng thái cân bằng mới là bao nhiêu? (kết quả làm tròn đến hàng phần trăm)
(Xem giải) Câu 32: Hydrocarbon M có công thức đơn giản nhất là C3H4. M chuyển hoá thành hai chất hữu cơ X và Y theo chuyển hoá:
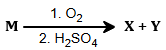
Chất X và Y kết hợp với nhau theo phương trình:
X + 2Y → bisphenol A + H2O
Sự hiện diện bất thường của X trong nước tiểu là một dấu hiệu của bệnh tiểu đường và được phát hiện qua việc xét nghiệm nước tiểu (chỉ số KET). Bisphenol A được dùng nhiều trong công nghiệp điều chế nhựa epoxy. Cho các phát biểu:
(1) Chất Y là chất rắn ở nhiệt độ thường, tan tốt trong nước nóng.
(2) Chất X phản ứng với iodine trong môi trường kiềm tạo kết tủa iodoform màu vàng.
(3) Dung dịch chất Y trong dung môi ethanol có tối đa 3 liên kết hydrogen.
(4) Poly (phenol formaldehyde) được điều chế trực tiếp từ formaldehyde và Y có mặt xúc tác acid, đun nóng.
(5) Trong công nghiệp để điều chế được 1,0 tấn Y với hiệu suất 95% thì cần dùng 1,44 tấn M. (Làm tròn kết quả đến hàng phần trăm).
(6) Từ 1,0 tấn M người ta điều chế bisphenol A theo chuyển hoá (1) và phương trình (2) với hiệu suất lần lượt là 95% và 80%, khối lượng bisphenol A thu được là 1444 kg.
Liệt kê theo thứ tự giảm dần các phát biểu đúng?
(Xem giải) Câu 33: Cho phổ khối lượng MS của silver (Ag) ở hình dưới đây:
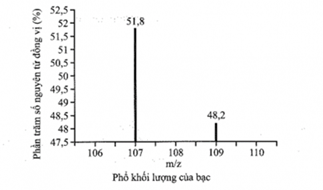
Tính phần trăm khối lượng của đồng vị 47Ag107 trong phân tử silver nitate? (Làm tròn kết quả đến hàng đơn vị). Cho nguyên tử khối trung bình của N = 14; O = 16.
(Xem giải) Câu 34: Mùn là loại vật chất hữu cơ phức tạp trong đất, độ màu mỡ của đất phụ thuộc vào hàm lượng mùn trong đất. Xác định carbon trong đất để tính hàm lượng mùn trong đất theo phương pháp Tiurin như sau:
• Bước 1: Cân 0,35 gam một mẫu đất khô rồi cho phản ứng với 11,7 mL dung dịch K2Cr2O7 0,1 M trong H2SO4 loãng, dư, đun nóng (cho biết có 90% lượng carbon đã bị oxi hóa ở phản ứng này) thu được dung dịch X, sơ đồ phản ứng xảy ra như sau:
K2Cr2O7 + C + H2SO4 → K2SO4 + Cr2(SO4)3 + CO2 + H2O (1)
• Bước 2: Chuẩn độ dung dịch X thu được ở bước 1 bằng dung dịch FeSO4 0,1221 M trong H2SO4 loãng với chất chỉ thị thích hợp (cho biết phản ứng xảy ra hoàn toàn) thì dùng hết 18,7 mL, sơ đồ phản ứng xảy ra như sau:
K2Cr2O7 + FeSO4 + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O (2)
Theo phương pháp Tiurin, khối lượng mùn trong đất bằng khối lượng carbon trong đất nhân với hệ số 1,724 và từ đó xác định được hàm lượng mùn trong đất là a% khối lượng. Giá trị của a bằng bao nhiêu? (Không làm tròn khi tính toán và kết quả cuối cùng làm tròn đến hàng phần mười)
(Xem giải) Câu 35: Nung 25 gam một mẫu quặng malachite có thành phần chính là Cu(OH)2.CuCO3 (còn lại là tạp chất trơ) trong không khí đến khối lượng không đổi, theo sơ đồ phản ứng:
Cu(OH)2.CuCO3 → 2CuO + H2O + CO2
Cho toàn bộ lượng chất rắn thu được (gồm CuO và tạp chất trơ) vào cốc thủy tinh, sau đó cho từ từ dung dịch H2SO4 19,6% vào cốc cho đến khi chất rắn không tan thêm được nữa thì dừng lại, lọc bỏ tạp chất trơ thu được dung dịch X. Làm lạnh toàn bộ dung dịch X xuống 10°C thu được dung dịch Y có nồng độ 14,16% và tách ra 25 gam tinh thể CuSO4.5H2O. Biết x% là phần trăm theo khối lượng của Cu trong 25 gam mẫu quặng malachite trên. Tính giá trị của x. (Làm tròn kết quả đến hàng đơn vị).


Bình luận