[2026] Thi thử TN chuyên Lương Văn Chánh – Đắk Lắk
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 098
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2D | 3A | 4B | 5C | 6D | 7C | 8D | 9A |
| 10A | 11A | 12C | 13A | 14C | 15D | 16C | 17C | 18D |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | Đ | Đ | Đ |
| (b) | S | Đ | Đ | Đ |
| (c) | S | S | Đ | S |
| (d) | S | Đ | S | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 0,44 | 0,51 | 8,11 | 48,9 | 2 | 24,7 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho phổ hồng ngoại của butan-1-ol như sau:

Peak nào giúp dự đoán được trong hợp chất này có nhóm chức hydroxyl (OH-)?
A. peak 1073 cm-1. B. peak 3333 – 3323 cm-1.
C. peak 901 cm-1. D. peak 1466 cm-1.
(Xem giải) Câu 2. Đun nước cứng lâu ngày, trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là
A. CaCl2. B. Na2CO3. C. CaO. D. CaCO3.
(Xem giải) Câu 3. Alcohol bị oxi hoá bởi CuO đun nóng tạo thành ketone là
A. CH3CH(OH)CH3. B. CH3OH. C. CH3CH2CH2OH. D. CH3CH2OH.
(Xem giải) Câu 4. Kim loại nào sau đây dẫn điện tốt nhất?
A. Cu. B. Ag. C. Au. D. Fe.
(Xem giải) Câu 5. Cho các phát biểu sau khi nói về tính chất của ethylamine C2H5NH2
(1) Ethylamine có khả năng tạo được liên kết hydrogen liên phân tử.
(2) Khi hòa tan vào trong nước, dung dịch ethylamine làm giấy quỳ tím hóa xanh.
(3) Khi cho ethylamine phản ứng với NaNO2/HCI ở nhiệt độ thường thu được sản phẩm chứa ethanol.
(4) Phản ứng của AlCl3 với dung dịch ethylamine cho phức chất màu xanh tím.
Số phát biểu đúng là
A. 4. B. 1. C. 3. D. 2.
(Xem giải) Câu 6. Tác nhân của phản ứng nitro hóa benzene là
A. H2SO4. B. NO2. C. NO2-. D. NO2+.
(Xem giải) Câu 7. Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng chất X cho kết quả như hình dưới đây:
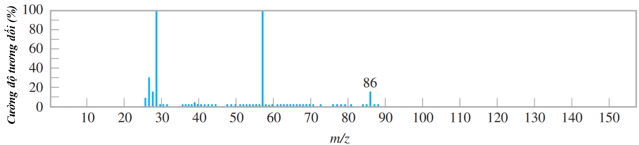
Chất X có thể là
A. C2H5COOH. B. CH3COOH. C. CH3COOC2H3. D. CH3COOC2H5.
(Xem giải) Câu 8. Fructose là một loại monosaccharide có nhiều trong mật ong, vị ngọt sắc. Số nguyên tử hydrogen có trong phân tử của fructose là
A. 11. B. 6. C. 24. D. 12.
(Xem giải) Câu 9. “…(1)… là những hợp chất hữu cơ trong phân tử có nhóm hydroxy liên kết với nguyên tử carbon no”. Nội dung phù hợp trong chỗ trống (1) là
A. Alcohol. B. Aldehyde. C. Phenol. D. Ketone.
(Xem giải) Câu 10. Cho phản ứng C(s) + 2H2(g) ⇋ CH4(g). Biểu thức hằng số cân bằng (Kc) của phản ứng là
A. [CH4]/[H2]². B. [CH4]/[C][H2]. C. [CH4]/[C][H2]². D. [CH4]/[H2].
(Xem giải) Câu 11. Trong phân tử phức chất, cầu nội bao gồm ion trung tâm và các phối tử liên kết trực tiếp, cầu ngoại là các ion liên kết với cầu nội bằng lực tĩnh điện.
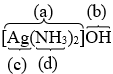
Tên gọi của các thành phần (a), (b), (c) và (d) trong phức chất hình bên lần lượt là
A. cầu nội, cầu ngoại, nguyên tử trung tâm và phối tử.
B. cầu nội, cầu ngoại, phối tử và nguyên tử trung tâm.
C. cầu ngoại, cầu nội, phối tử và nguyên tử trung tâm.
D. cầu ngoại, cầu nội, nguyên tử trung tâm và phối tử.
(Xem giải) Câu 12. Phức chất [Cu(H2O)6]2+ có 6 liên kết cho – nhận giữa 6 phối tử H2O với nguyên tử trung tâm. Nguyên tử trung tâm của phức chất [Cu(H2O)6]2+ là
A. OH-. B. Cu. C. Cu2+. D. H2O.
(Xem giải) Câu 13. Xét phản ứng nhiệt phân NaHCO3 thành Na2CO3 trong quá trình Solvay:
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(g)  = +135,6kJ.
= +135,6kJ.
Nhiệt lượng cần cung cấp để nhiệt phân 1kg NaHCO3 theo phản ứng trên là
A. 807,1 kJ. B. 403,6 kJ. C. 1210,7 kJ. D. 1614,3 kJ.
(Xem giải) Câu 14. Tên thay thế của alanine là
A. α–aminopropanoic acid. B. 2–aminopropionic acid.
C. 2–aminopropanoic acid. D. α–aminopropionic acid.
(Xem giải) Câu 15. Trong các kim loại sau, kim loại nào có thể được điều chế bằng phương pháp thủy luyện?
A. Al. B. K. C. Mg. D. Cu.
(Xem giải) Câu 16. Cation M2+ có cấu hình electron: 1s2 2s2 2p6. Số hiệu nguyên tử của M là
A. 9. B. 11. C. 12. D. 10.
(Xem giải) Sử dụng thông tin cho dưới đây để trả lời các câu 17 – 18: Quá trình sản xuất gang và thép là hai giai đoạn nối tiếp nhau trong ngành luyện kim đen, với mục tiêu cuối cùng là biến quặng sắt tự nhiên thành các sản phẩm gang thép.
Nguyên liệu để sản xuất gang chủ yếu là quặng sắt và than cốc. Trong lò luyện gang khi than cốc cháy tạo ra chất khử CO và nhiệt. Chất khử CO khử oxide của sắt tạo ra sắt nóng chảy trộn lẫn từ 2% đến 5% khối lượng carbon tạo gang lỏng. Gang lỏng chuyển sang lò luyện thép. Khí oxygen được thổi vào lò, lúc gang ở trạng thái nóng chảy thì các tạp chất trong gang sẽ bị oxi hóa bởi O2 ta thu được thép (carbon chiếm dưới 2% về khối lượng).
Câu 17. Cho các phát biểu sau về sản xuất gang, thép.
(a) Trong lò luyện gang người ta sử dụng phương pháp nhiệt luyện để tách sắt ra khỏi oxide của sắt.
(b) Trong lò luyện gang người ta sử dụng phương pháp điện phân nóng chảy để tách sắt ra khỏi quặng.
(c) Vai trò than cốc trong quá trình luyện gang gồm: tạo nhiệt, tạo chất khử, tạo gang.
(d) Khi phân tích 30 gam hợp kim của sắt ta thấy có chứa 0,85 gam carbon, vậy mẫu hợp kim đem phân tích là thép.
Số phát biểu đúng là
A. 3. B. 1. C. 2. D. 4.
Câu 18. Để chống ăn mòn kim loại người ta bảo vệ các công trình, phương tiện bằng thép nằm trong nước biển bằng cách gắn vào công trình hoặc phương tiện tại vị trí nằm trong nước biển mẫu kim loại Zn. Nhận định nào sau đây đúng?
A. Tại anode xảy ra quá trình khử Fe thành Fe2+.
B. Tại cathode xảy ra quá trình C + O2 → CO2.
C. Phương pháp bảo vệ kim loại trên là phương pháp phủ bề mặt.
D. Phương pháp bảo vệ kim loại trên là phương pháp điện hóa.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Trong công nghiệp, xút (sodium hydroxide) được sản xuất bằng phương pháp điện phân dung dịch sodium chloride có màng ngăn xốp. Bằng phương pháp này, người ta cũng thu được khí chlorine. Chất khí này được làm khô (loại hơi nước) rồi hoá lỏng để làm nguyên liệu quan trọng cho nhiều ngành công nghiệp chế biến và sản xuất hoá chất.
Từ quá trình điện phân nêu trên, một lượng chlorine và hydrogen sinh ra được tận dụng để sản xuất hydrochloric acid đặc thương phẩm (37%, D = 1,19 g/mL ở 20°C).
Một nhà máy với quy mô sản xuất 200 tấn xút mỗi ngày thì đồng thời sản xuất được V m³ acid thương phẩm trên (ở 20°C). Biết rằng, tại nhà máy này, 60% khối lượng chlorine sinh ra được dùng tổng hợp hydrochloric acid và hiệu suất của toàn bộ quá trình từ chlorine đến acid thương phẩm là 80%.
a) Có thể dùng sulfuric acid đặc làm khô khí chlorine thoát ra.
b) Trong thí nghiệm điện phân thì Cl2 sẽ thoát ra tại cực cathode.
c) Nếu không sử dụng màng ngăn xốp thì phương trình điện phân dung dịch NaCl là: 2NaCl + 2H2O → 2NaOH + H2 + Cl2.
d) Giá trị của V là 237 (làm tròn đến hàng phần mười).
(Xem giải) Câu 20. Pin Lithium-ion hoạt động dựa trên sự di chuyển của các ion Li+ qua lại giữa hai điện cực có cấu trúc dạng lớp. Thông thường, cực âm (anode) được làm bằng than chì ngậm lithium (LiC6) và cực dương (cathode) là oxide kim loại (như LiCoO2). Chất điện phân (thường là LiPF6 trong dung môi hữu cơ) đóng vai trò dẫn truyền ion Li+. Phản ứng ở các điện cực khi pin hoạt động (xả pin) như sau:
Cathode: CoO2 + Li+ + 1e → LiCoO2
Anode: LiC6 → C6 + Li+ + 1e
Phản ứng hoá học đầy đủ xảy ra trong trong pin như sau:
LiC6(s) + CoO2(s) ⇋ C6(s) + LiCoO2(s) (∗)
a) Trong quá trình xả pin, tại anode xảy ra quá trình oxi hoá LiC6.
b) Khi xả pin, số oxi hoá của nguyên tố Cobalt (Co) giảm từ +4 xuống +3 .
c) Để có một viên pin đạt dung lượng 4000 mAh, khối lượng LiCoO2 tối thiểu là khoảng 16,4 gam. Biết rằng 1 mol electron có điện lượng là 96485C và 1C = 1A.s (MLi = 7, MCo = 59; MO = 16). (Chỉ làm tròn đến hàng chục ở phép tính cuối cùng).
d) Trong phương trình phản ứng tổng quát (∗), chiều nghịch biểu diễn cho quá trình sạc pin.
(Xem giải) Câu 21. Áp dụng kiến thức về các yếu tố ảnh hưởng đến tốc độ phản ứng trong phần tổng hợp ester, một nhóm học sinh dự đoán “nhiệt độ càng cao, hiệu suất ester hóa càng cao”. Để kiểm chứng cho dự đoán trên, nhóm đã tiến hành thí nghiệm phản ứng tổng hợp propyl acetate từ alcohol và acid tương ứng với nồng độ không đổi ở các điều kiện nhiệt độ khác nhau tương ứng theo phương trình:
CH3COOH + CH3CH2CH2OH ⇋ CH3COOCH2CH2CH3 + H2O (1)
Kết quả thu được như bảng:
| Nhiệt độ (°C) | 60 | 65 | 70 | 75 | 80 | 85 |
| Thể tích ester (mL) | 26,0 | 30,5 | 35,0 | 40,0 | 36,5 | 31,0 |
Cho độ tan trong 100 gam nước của các chất như bảng sau
| Chất | CH3COOH | CH3CH2CH2OH | CH3COOCH2CH2CH3 |
| Độ tan (gam – ở 25°C) | Vô hạn | Vô hạn | 1,6 |
a) Từ kết quả trên, dự đoán của học sinh là sai.
b) Trong phản ứng (1), H2O được tạo thành từ -OH của acid và -H của alcohol.
c) Có thể dùng phương pháp chiết lỏng – lỏng để tách CH3COOCH2CH2CH3 ra khỏi hỗn hợp sản phẩm.
d) Vì CH3COOH và CH3CH2CH2OH đều có nhóm -OH nên không thể dùng phương pháp phổ hồng ngoại (IR) để nhận biết 2 chất trên.
(Xem giải) Câu 22. Polymer Y được dùng làm hộp đựng thực phẩm, đồ chơi trẻ em, vỏ đĩa CD, DVD,… Trong công nghiệp sản xuất chất dẻo, polymer Y được điều chế theo sơ đồ sau:
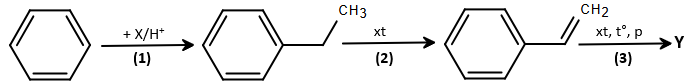
a) Phản ứng (3) trong sơ đồ thuộc loại phản ứng trùng hợp.
b) Từ 100 kg benzene và 32 m³ khí X (ở 25°C, 1 bar), với hiệu suất mỗi quá trình (1), (2), (3) lần lượt là 60%, 55% và 60%, thu được 26,4 kg polymer Y.
c) Trong sơ đồ trên, X là ethane; Y có ký hiệu là PE.
d) Polymer Y có tính đàn hồi cao, dùng để sản xuất cao su, vật liệu chống thấm, lốp xe,…
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Phân bón NPK là hỗn hợp các muối NH4NO3, (NH4)2HPO4, KCl và một lượng phụ gia không chứa các nguyên tố dinh dưỡng. Trên các bao bì phân NPK thường có kí hiệu bằng những chữ số nhằm cho biết tỉ lệ khối lượng các thành phần trong phân bón. Việc bón phân NPK cho cây cà phê sau khi trồng 4 năm được chia thành ba thời kì như sau:
| Thời kì | Lượng phân bón |
| Bón thúc ra hoa | 0,5 kg phân NPK 10.12.5/cây |
| Bón đậu quả, ra quả | 0,7 kg phân NPK 12.8.2/cây |
| Bón thúc quả lớn, tăng dưỡng chất cho quả | 0,6 kg phân NPK 16.16.16/cây |
Tổng khối lượng đạm (N) và lân (P2O5) đã cung cấp cho cây cà phê trong cả ba thời kì là bao nhiêu kg? (kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 24. Lắp ráp pin điện hóa Zn-Ni ở điều kiện chuẩn. Cho biết các giá trị thế điện cực chuẩn: E°Zn2+/Zn = -0,763V và E°Ni2+/Ni = -0,257V. Sức điện động chuẩn của pin điện hóa trên là bao nhiêu? (Kết quả được làm tròn đến hàng phần trăm).
(Xem giải) Câu 25. Phần trăm khối lượng nguyên tố hydrogen trong methyl acetate là a%. Giá trị của a là bao nhiêu? (Kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 26. Cần mạ bạc (silver) lên một vật hình trụ, đáy hình tròn với bán kính 3 cm, chiều cao hình trụ 0,3 cm, lớp mạ bạc dày 0,01 cm, tiến hành điện phân dung dịch AgNO3 dư với cường độ dòng điện không đổi 2A. Khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết thời gian là t phút. Biết khối lượng riêng của silver là 10,5 gam/cm³, hiệu suất điện phân là 100%, số mol electron (n) đi qua dây dẫn được tính theo công thức n = It/F với I là cường độ dòng điện (A), t là thời gian (s), F là hằng số Faraday (F = 96500 C/mol), π = 3,14. Giả thiết lớp mạ dày như nhau, toàn bộ lượng silver tạo ra đều bám hết vào vật hình trụ. Tính thời gian t cần mạ. (kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 27. Malic acid là một loại acid tự nhiên, thường được tìm thấy trong các loại trái cây, đặc biệt là quả táo và các loại rau. Công thức cấu tạo của malic acid được cho trong hình minh họa dưới đây. Vậy 1,0 mol malic acid phản ứng được tối đa với bao nhiêu mol KOH?

(Xem giải) Câu 28. Nescafe đã sản xuất thành công lon coffee tự làm nóng. Để làm nóng coffee, chỉ cần ấn nút (trên lon) để trộn nguyên liệu gồm dung dịch KOH hoặc NaOH rất loãng và CaO; 180 mL coffee trong lon sẽ được làm nóng đến khoảng 40°C. Giả sử nhiệt dung riêng của coffee là 4,18 J/g.K (Nhiệt dung riêng là nhiệt lượng cần cung cấp để 1 gam chất tăng lên 1°C). Cho  (kJ/mol) của CaO(s), H2O(l), Ca(OH)2(aq) lần lượt là: -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Khối lượng CaO cần cung cấp để làm nóng 180 mL coffee (d = 1,0 g/mL) từ 10°C đến 40°C là bao nhiêu gam? (kết quả làm tròn đến hàng phần mười).
(kJ/mol) của CaO(s), H2O(l), Ca(OH)2(aq) lần lượt là: -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Khối lượng CaO cần cung cấp để làm nóng 180 mL coffee (d = 1,0 g/mL) từ 10°C đến 40°C là bao nhiêu gam? (kết quả làm tròn đến hàng phần mười).

Bình luận