[2026] Thi thử TN sở GDĐT Điện Biên
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 124
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2D | 3D | 4B | 5C | 6B | 7A | 8A | 9C |
| 10D | 11B | 12D | 13D | 14B | 15A | 16A | 17A | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | Đ | S | S |
| (b) | Đ | S | Đ | Đ |
| (c) | Đ | S | S | S |
| (d) | S | Đ | Đ | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 7 | 115 | 600 | 15 | 4 | 76 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Các kim loại nhóm IA (nhóm kim loại kiềm) và hợp chất của chúng có nhiều ứng dụng như: sản xuất pin lithium, nước Javel, phân kali, tế bào quang điện, đồng hồ nguyên tử,… Nhận định nào sau đây đúng?
A. Trong tự nhiên, các kim loại kiềm tồn tại ở dạng hợp chất và đơn chất.
B. Ở nhiệt độ thường, các ion kim loại nhóm IA đều có màu đặc trưng.
C. Trong các hợp chất, nguyên tố kim loại kiềm chỉ có số oxi hóa là 0 và +1.
D. Các kim loại kiềm có độ cứng thấp do có liên kết kim loại yếu.
(Xem giải) Câu 2. Một người muốn bổ sung omega-3 để cải thiện sức khỏe tim mạch. Trong các thực phẩm sau, thực phẩm nào có hàm lượng omega-3 cao nhất?
A. Thịt bò. B. Dầu đậu nành. C. Dầu dừa. D. Dầu cá hồi.
(Xem giải) Câu 3. Ở nhiệt độ thấp (0 – 5°C), amine X tác dụng với nitrous acid tạo thành muối diazonium. X là
A. trimethylamine. B. dimethylamine. C. methylamine. D. aniline.
(Xem giải) Câu 4. Trong phòng thí nghiệm, dung dịch chất nào sau đây phù hợp để kiểm tra sự có mặt của ion Ca2+(aq)?
A. NaCl. B. Na2CO3. C. NaNO3. D. HCl.
(Xem giải) Câu 5. Xét phản ứng giữa ethene với HBr: CH2=CH2 + HBr → CH3CH2Br
Phản ứng xảy ra theo cơ chế cộng electrophile (tác nhân electrophile là các tiểu phân thiếu electron). Các giai đoạn của cơ chế diễn ra như sau:
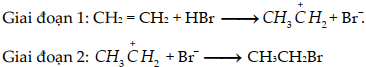
Nhận định nào sau đây đúng?
A. Tác nhân electrophile trong cơ chế trên là Br-.
B. Phản ứng giữa alkene với HBr luôn cho ra một sản phẩm.
C. Giai đoạn 2 là quá trình kết hợp giữa carbocation (tiểu phân mang điện tích dương trên nguyên tử carbon) với Br-.
D. Ở giai đoạn 1 có sự phá vỡ liên kết σ C-C.
(Xem giải) Câu 6. Người ta thường lấy lá chè xanh rửa sạch, có thể vò nhẹ, cho vào ấm rồi đổ nước sôi, ủ từ 3 – 5 phút là có thể sử dụng được làm thức uống rất tốt cho cơ thể. Cách làm này được gọi là hãm chè, dựa trên phương pháp nào sau đây?
A. Chưng cất. B. Chiết lỏng – rắn. C. Kết tinh. D. Cô đặc.
(Xem giải) Câu 7. Phát biểu nào sau đây không đúng?
A. Dùng dung dịch Ca(OH)2 vừa đủ làm mất tính cứng vĩnh cửu.
B. Đun sôi nước cứng làm mất tính cứng tạm thời.
C. Dùng dung dịch Na2CO3 làm mất tính cứng tạm thời và tính cứng vĩnh cửu.
D. Phương pháp trao đổi ion làm giảm tính cứng tạm thời và tính cứng vĩnh cửu
(Xem giải) Câu 8. Ở điều kiện thích hợp, khi cho NH3 tác dụng với H2SO4 theo tỉ lệ mol nNH3 : nH2SO4 = 2 : 1 thì thu được chất nào sau đây?
A. (NH4)2SO4. B. (NH4)2S. C. (NH4)2SO3. D. NH4HSO3.
(Xem giải) Câu 9. Chất nào sau đây là đồng phân của acetic acid?
A. HCOOH. B. CH3CHO. C. HCOOCH3. D. C2H5COOH.
(Xem giải) Câu 10. Cho phản ứng hóa học sau: C(s) + O2(g) → CO2(g). Yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng trên?
A. Diện tích bề mặt carbon. B. Nhiệt độ. C. Áp suất O2. D. Khối lượng carbon.
(Xem giải) Câu 11. Phát biểu nào sau đây đúng?
A. Zn2+ có tính oxi hoá mạnh hơn Fe2+.
B. Cu bị hoà tan trong dung dịch muối Fe(NO3)3 dư.
C. Tính khử của Ag mạnh hơn Zn.
D. Fe – Sn để ngoài không khí ẩm, Sn sẽ bị ăn mòn điện hoá.
(Xem giải) Câu 12. Trong pin nhiên liệu hydrogen, H2 có vai trò tương tự như kim loại mạnh hơn trong pin Galvani. Phản ứng nào sau đây diễn ra ở điện cực âm khi pin nhiên liệu hydrogen hoạt động?
A. 2H+ + 2e → H2. B. O2 + 4H+ + 4e → 2H2O.
C. 2H2 + O2 → 2H2O. D. H2 → 2H+ + 2e.
(Xem giải) Câu 13. Loại carbohydrate mạch phân nhánh, có nhiều trong các loại ngũ cốc là
A. cellulose. B. amylose. C. saccharose. D. amylopectin.
(Xem giải) Câu 14. Phenol là một hợp chất hữu cơ quan trọng, được sử dụng rộng rãi trong sản xuất nhựa, phẩm nhuộm, thuốc nổ và đặc biệt là trong ngành y dược để sản xuất các chất sát trùng, tẩy uế. Để nghiên cứu tính chất hóa học đặc trưng của phenol, một nhóm học sinh tiến hành thí nghiệm sau:
• Bước 1: Cho 1 mL phenol lỏng vào ống nghiệm, sau đó thêm 2 mL nước cất, lắc đều thu được hệ huyền phù (1).
• Bước 2: Thêm từ từ dung dịch NaOH vào ống nghiệm (1), lắc đều cho đến khi chất lỏng trở nên đồng nhất (2).
• Bước 3: Thêm tiếp dung dịch HCl dư vào ống nghiệm (2), lắc đều và để ổn định.
Cho các phát biểu sau:
(a) Sau bước 2, chất lỏng trong ống nghiệm trở thành dung dịch đồng nhất do phenol phản ứng với NaOH tạo thành muối tan.
(b) Ở bước 3, HCl đã đẩy phenol ra khỏi muối, làm dung dịch xuất hiện vẩn đục.
(c) Kết thúc bước 3, nếu để yên ống nghiệm một thời gian, chất lỏng sẽ phân thành hai lớp.
(d) Thí nghiệm trên chứng minh phenol có tính acid và tính acid của nó mạnh hơn acid carbonic (H2CO3).
(e) Nếu thay dung dịch HCl ở bước 3 bằng cách sục khí CO2 dư vào, hiện tượng vẩn đục tương tự vẫn xảy ra.
Số phát biểu đúng là
A. 3. B. 4. C. 2. D. 1.
(Xem giải) Câu 15. Trong các ion sau: Na+, Mg2+, Fe3+, Zn2+, số ion có thể điện phân trong dung dịch nước là
A. 2. B. 1. C. 4. D. 3.
(Xem giải) Câu 16. Phản ứng nào sau đây không thể hiện tính base của amine?
A. CH3NH2 + HNO2 → CH3OH + N2 + H2O.
B. CH3NH2 + H2O → CH3NH3+ + OH-.
C. Fe3+ + 3CH3NH2 + 3H2O → Fe(OH)3 + 3CH3NH3+.
D. C6H5NH2 + HCl → C6H5NH3Cl.
(Xem giải) Câu 17. Trong cơ thể sinh vật, chất X là một α-amino acid đóng vai trò nền tảng để xây dựng nên các chuỗi polypeptide và protein. Kết quả phân tích nguyên tố cho thấy X chứa 40,45% C, 7,87% H, 15,73% N về khối lượng, còn lại là oxygen. Biết rằng 0,1 mol X phản ứng vừa đủ với dung dịch chứa 0,1 mol NaOH. Cho các phát biểu sau:
(a) Tên thay thế của X là acid 2-aminopropanoic; tổng số nguyên tử trong một phân tử X là 13.
(b) Ở điều kiện thường, X là chất lỏng, dễ tan trong nước và có nhiệt độ sôi thấp hơn so với các acid carboxylic có cùng phân tử khối.
(c) Ở môi trường có pH = 2, dưới tác dụng của điện trường X di chuyển về phía cực dương.
(d) Dung dịch X có khả năng hòa tan Cu(OH)2 tạo thành hợp chất màu tím đặc trưng.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 18. Trùng hợp chất nào sau đây thu được polyacrylonitrile dùng để sản xuất tơ nitron?
A. CH2=CHCl. B. CH2=CHCN. C. CH2=CH2. D. CH2=CHCH3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Trong y học hiện đại, poly(lactic acid) (PLA) là một polymer sinh học quan trọng được dùng để sản xuất chỉ khâu phẫu thuật tự tiêu, các thanh cố định xương gãy và máng niềng răng trong suốt. PLA được tổng hợp từ acid lactic (2-hydroxypropanoic acid), nguồn nguyên liệu này thu được từ quá trình lên men các loại nông sản như ngô, sắn. Một ưu điểm vượt trội của PLA là có khả năng bị thủy phân thành các sản phẩm không độc hại và được cơ thể đào thải tự nhiên qua quá trình trao đổi chất.
a) Phản ứng tổng hợp trực tiếp PLA từ các phân tử acid lactic thuộc loại phản ứng trùng ngưng, trong đó có sự tách ra các phân tử nước.
b) Sử dụng các sản phẩm từ PLA giúp giảm thiểu ô nhiễm môi trường do chúng có khả năng bị phân hủy sinh học bởi vi sinh vật.
c) Acid lactic, đơn vị cấu tạo nên PLA, là một hợp chất hữu cơ tạp chức, trong phân tử chứa đồng thời nhóm chức carboxyl (–COOH) và nhóm chức hydroxyl (–OH).
d) Từ 10 kg ngô (chứa 81% tinh bột về khối lượng), nếu hiệu suất toàn bộ quá trình điều chế đạt 80% thì khối lượng polymer PLA thu được là 2,88 kg.
(Xem giải) Câu 20. Melamine (C3H6N6) là hợp chất có hàm lượng nitrogen rất cao (66,67%). Trong một vụ gian lận thực phẩm, kẻ gian đã pha loãng sữa bột tiêu chuẩn (chứa 16% protein theo khối lượng, biết nitrogen chiếm 16% khối lượng protein) bằng cách thay thế một phần sữa bột bằng bột đá (CaCO3) không độc nhưng không có dinh dưỡng, sau đó thêm melamine để bù lại “độ đạm” bị thiếu hụt khi đo bằng máy Kjeldahl.
a) Melamine có tính base yếu, có thể phản ứng với các acid trong dịch vị dạ dày, đây là một trong những nguyên nhân gây rối loạn tiêu hóa trước khi gây sỏi thận.
b) Nếu kẻ gian rút bớt 50% khối lượng sữa bột thật và thay bằng bột đá, sau đó thêm vào một lượng melamine bằng 1,9% khối lượng sữa thật còn lại thì tổng hàm lượng nitrogen đo được vẫn đạt xấp xỉ mức sữa tiêu chuẩn.
c) Để nâng độ đạm tổng số (lượng nitrogen quy đổi) của một mẫu sữa từ 12% lên 16% bằng melamine, người ta chỉ cần pha thêm vào mẫu đó một lượng melamine bằng khoảng 1% khối lượng mẫu ban đầu. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nguyên.)
d) Thí nghiệm cho mẫu sữa trên tác dụng với Cu(OH)2 trong môi trường kiềm sẽ giúp người kiểm định phát hiện ngay sự thiếu hụt protein thật do cường độ màu tím sẽ giảm đi một nửa so với mẫu chuẩn.
(Xem giải) Câu 21. Phèn sắt ammonium (NH4Fe(SO4)2.12H2O) có thể được dùng để loại bỏ các chất lơ lửng trong nước. Khi hòa tan phèn sắt ammonium vào nước được dung dịch có màu vàng, một lúc sau thì xuất hiện kết tủa màu nâu đỏ theo các quá trình sau:
Fe3+(aq) + 6H2O(l) → [Fe(OH2)6]3+(aq) (1)
[Fe(OH2)6]3+(aq) + 3H2O(l) → [Fe(OH)3(OH2)3](s) + 3H3O+(aq)(2)
a) Cation Fe3+ có cấu hình electron là [Ar]3d34s2. (biết số hiệu nguyên tử của Fe là 26)
b) Để hạn chế lượng kết tủa nâu đỏ xuất hiện ở quá trình (2) thì nhỏ thêm vào dung dịch vài giọt dung dịch H2SO4
c) Quá trình (2) chứng minh H2O là một acid theo thuyết Br∅nsted Lowry.
d) Màu vàng của dung dịch là màu phức chất aqua của cation Fe3+.
(Xem giải) Câu 22. Trong các phòng thí nghiệm hoặc điều kiện y tế đặc thù, thiết bị điện phân nước có thể được sử dụng để cung cấp nguồn khí oxygen tinh khiết tức thời. Thiết bị vận hành dựa trên nguyên tắc điện phân dung dịch chất điện ly (thường là dung dịch H2SO4 loãng) với các điện cực trơ. Quá trình điện phân diễn ra theo các bán phản ứng sau:
Tại cathode (–): 2H2O + 2e → H2 + 2OH-
Tại anode (+): 2H2O → O2 + 4H+ + 4e
Máy được thiết kế với bình chứa dung tích 2,5 lít. Để bảo vệ các điện cực và đảm bảo nồng độ chất điện ly không quá đậm đặc, máy được lập trình: Nếu lượng nước bị tiêu thụ vượt quá 80% dung tích ban đầu của bình, hệ thống sẽ tự động ngắt và phát tín hiệu cảnh báo cần bổ sung nước.
a) Giả sử hiệu suất điện phân là 100%, để máy sản xuất đủ 1239,5 lít khí O2 (đkc), tổng khối lượng nước nguyên chất bị tiêu hao do phản ứng điện phân là khoảng 1,89 kg.
b) Khi máy hoạt động, ở vùng dung dịch bao quanh điện cực anode, dung dịch có tính acid mạnh hơn do sự tích tụ tạm thời của ion H+ trước khi khuếch tán ra toàn bình.
c) Acid H2SO4 đóng vai trò là chất dẫn điện để tăng tốc độ quá trình điện phân nước. Vì thế nồng độ mol của acid này không đổi sau quá trình điện phân.
d) Nếu một bệnh nhân cần cung cấp oxygen với lưu lượng 2,0 lít/phút (đkc), máy điện phân sẽ hoạt động liên tục được ít nhất 12 giờ trước khi phát tín hiệu cảnh báo bổ sung nước.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Phức chất [Co(NH3)Clx]y− có dạng hình học bát diện, nguyên tử trung tâm là Co3+. Tổng giá trị của x và y là bao nhiêu?
(Xem giải) Câu 24. Một loại khí thiên nhiên (X) có thành ứng phần phần trăm về thể tích như sau: 85,0% methane, 10,0% ethane, 2,0% nitrogen, 3,0% khí carbon dioxide. Biết rằng: khi đốt cháy 1 mol methane, 1 mol ethane thì lượng nhiệt tỏa ra tương ứng là 880,0 kJ và 1560,0 kJ, để nâng 1 mL nước lên thêm 1°C cần 4,2 J. Giả thiết rằng lượng nhiệt tỏa ra của quá trình đốt cháy X dùng để làm nóng nước với hiệu suất hấp thụ nhiệt khoảng 80%. Thể tích khí X (đkc) cần dùng để đun nóng 10,0 lít nước (khối lượng riêng của nước 1 g/mL) từ 20°C lên 100°C bằng bao nhiêu lít (làm tròn kết quả đến phần nguyên)?
(Xem giải) Câu 25. Aspirin có tác dụng giảm đau, hạ sốt, chống viêm. Aspirin được điều chế từ phenol theo sơ đồ sau:
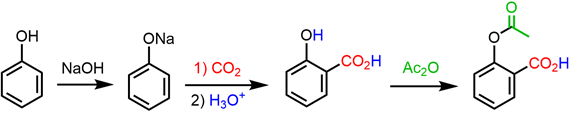
Một viên thuốc aspirin có khối lượng 80 mg. Tính khối lượng (gam) phenol cần thiết để sản xuất 100 lọ aspirin (mỗi lọ có 100 viên) với hiệu suất cả quá trình là 69,63%.
(Xem giải) Câu 26. Nguyên tố X là một nguyên tố thiết yếu trong cơ thể sinh vật, có mặt trong xương, răng và tất cả các tế bào sống. Nguyên tử của nguyên tố X có 3 lớp electron và có 3 electron độc thân. Xác định số hiệu nguyên tử của của X.
(Xem giải) Câu 27. Cho dãy các chất: tripalmitin, phenol, phenylammonium chloride, saccharose, glutamic acid. Có bao nhiêu chất trong dãy phản ứng với dung dịch NaOH?
(Xem giải) Câu 28. Spathose là một loại quặng chứa iron(II) carbanate, FeCO3. Có thể xác định phần trăm FeCO3 bằng phương pháp chuẩn độ với dung dịch potassium dichromate(VI) đã được acid hóa, sử dụng chất xúc tác thích hợp. Sơ đồ phản ứng: Cr2O72- + H+ + Fe2+ → Cr3+ + Fe3+ + H2O.
Thực hiện quy trình như sau:
• Bước 1: Hòa tan 5,00 gam mẫu spathose vào acid phù hợp rồi lọc.
• Bước 2: Pha loãng dung dịch lọc đến 250 mL bằng nước cất.
• Bước 3: Lấy 25 mL dung dịch ở trên đem chuẩn độ thì hết 27,3 mL dung dịch potassium dichromate(VI) 0,02 M.
Cho biết phần trăm iron(II) carbanate có trong mẫu spathose. (Làm tròn kết quả đến hàng đơn vị).

Bình luận