[2026] Thi thử TN sở GDĐT Tuyên Quang (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 118
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2C | 3C | 4C | 5D | 6A | 7C | 8C | 9A |
| 10D | 11C | 12A | 13C | 14A | 15C | 16C | 17B | 18C |
| 19 | 20 | 21 | 22 | |
| (a) | S | Đ | S | Đ |
| (b) | S | S | Đ | S |
| (c) | Đ | S | Đ | Đ |
| (d) | Đ | Đ | S | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 7 | 234 | 3 | 1,00 | 4 | 297 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
| Liên kết | C–H | C–C | C=C | C≡C |
| Năng lượng liên kết Eb (kJ/mol) | 418 | 346 | 612 | 838 |
Biến thiên enthalpy của phản ứng C3H8(g) → CH4(g) + C2H4(g) có giá trị là
A. −80 kJ. B. +103 kJ. C. +80 kJ. D. −103 kJ.
(Xem giải) Câu 2. Hơn 50% sản lượng kẽm trên thế giới được sản xuất bằng phương pháp điện phân dung dịch ZnSO4. Với anode là hợp kim chì-bạc và cathode là các tấm nhôm. Biết các điện cực không tham gia vào quá trình điện phân. Phát biểu nào sau đây không đúng?
A. Ở cathode (điện cực âm) ion Zn2+ bị khử.
B. Dung dịch sau điện phân có pH thấp hơn dung dịch đầu.
C. Ở anode (điện cực dương) ion sulfate bị oxi hoá.
D. Có khí oxygen thoát ra ở điện cực dương.
(Xem giải) Câu 3. Tên thay thế của CH3CH2Cl là
A. chloromethane. B. bromoethane. C. chloroethane. D. ethyl chloride.
(Xem giải) Câu 4. Thực hiện thí nghiệm về tính chất điện di của các amino acid: Glycine, Lysine, Glutamic tại môi trường có pH = 6, cho kết quả như sau:

Phát biểu nào sau đây đúng?
A. Glycine hầu như không dịch chuyển nên glycine tồn tại chủ yếu ở dạng phân tử trung hòa.
B. Các amino acid tồn tại chủ yếu ở dạng ion lưỡng cực nên sẽ di chuyển về hai đầu điện cực.
C. Lysine dịch chuyển về phía cực âm nên lysine tồn tại chủ yếu ở dạng cation.
D. Tại pH = 6, glutamic acid tồn tại chủ yếu ở dạng cation.
(Xem giải) Câu 5. Cho cân bằng (trong bình kín) sau: CO(g) + H2O(g) ⇌ CO2(g) + H2(g) ΔH° < 0. Lần lượt thực hiện các thay đổi sau: (1) tăng nhiệt độ; (2) thêm một lượng hơi nước; (3) thêm một lượng H2; (4) thêm chất xúc tác. Thay đổi nào không làm chuyển dịch cân bằng của hệ?
A. (3). B. (2). C. (1). D. (4).
(Xem giải) Câu 6. Công thức cấu tạo của methyl formate là
A. HCOOCH3 B. HCOOH C. CH3COOH D. CH3COOCH3
(Xem giải) Câu 7. Trong các chất sau, chất nào không phải là hợp chất phenol?

A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 8. Dãy các kim loại được xếp theo thứ tự độ dẫn điện giảm dần từ trái sang phải là
A. Cu, Ag, Au. B. Ag, Au, Cu. C. Ag, Cu, Au. D. Au, Ag, Cu.
(Xem giải) Câu 9. Muối nào sau đây có khả năng làm mất màu thuốc tím trong môi trường sulfuric acid loãng?
A. FeSO4. B. MgSO4. C. Fe2(SO4)3. D. Cr2(SO4)3.
(Xem giải) Câu 10. Sự phân cắt đồng li là sự phân cắt một cách đồng đều đối với hai nguyên tử tham gia liên kết, mỗi nguyên tử chiếm một electron từ cặp electron chung và trở thành tiểu phân mang một electron độc thân. Quá trình nào dưới đây xảy ra sự phân cắt đồng li?
A. CH3C≡CH → CH3C≡C- + H+.
B. CH3CH2Br → CH3CH2+ + Br-.
C. (CH3)3CBr → (CH3)3C+ + Br-.
D. Cl2 → Cl• + Cl•
(Xem giải) Câu 11. Amino acid là hợp chất hữu cơ tạp chức trong phân tử chứa đồng thời hai loại nhóm chức nào sau đây?
A. –OH và –COOH. B. –COOH và –CHO. C. –NH2 và –COOH. D. –NH2 và –OH.
(Xem giải) Câu 12. Nguyên tử X có 17 proton trong hạt nhân và số khối bằng 37. Kí hiệu nguyên tử của X là
A. 17X37 B. 17X20 C. 37X17 D. 20X37
(Xem giải) Câu 13. Phối tử trong phức chất [Fe(CO)5] và [CuCl4]2- lần lượt là
A. Fe và Cu. B. CO và Cl2. C. CO và Cl-. D. CO và Cl.
(Xem giải) Câu 14. Cho các nhận định về tính chất của saccharose:
1) Saccharose phản ứng được với Cu(OH)2 ở điều kiện thường.
2) Khi thủy phân saccharose tạo thành sản phẩm trong đó có glucose.
3) Saccharose tham gia phản ứng tráng bạc.
4) Ở điều kiện thường, saccharose là chất kết tinh, không màu.
Có bao nhiêu nhận định không đúng với tính chất của saccharose?
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 15. Thí nghiệm nào sau đây chỉ xảy ra ăn mòn hóa học?
A. Nhúng thanh Zn vào dung dịch CuSO4.
B. Nhúng thanh Fe vào dung dịch CuSO4 và H2SO4 loãng.
C. Nhúng thanh Cu vào dung dịch Fe2(SO4)3.
D. Nhúng thanh Cu vào dung dịch AgNO3.
(Xem giải) Câu 16. Trong các hợp chất sau đây, hợp chất nào tan tốt trong nước ở điều kiện thường?
A. CaCO3. B. BaSO4. C. NaCl. D. Mg(OH)2.
Sử dụng thông tin dưới đây để trả lời các câu hỏi 17 – 18
Giá trị thế điện cực chuẩn của các kim loại là một đại lượng quan trọng để đánh giá khả năng khử của dạng khử và khả năng oxi hoá của dạng oxi hoá trong điều kiện chuẩn. Khi sắp xếp thế điện cực chuẩn các cặp oxi hoá – khử (Mn+/M) theo chiều tăng dần từ trái sang phải sẽ thu được dãy thế điện cực chuẩn, thường gọi là dãy điện hoá của kim loại.
(Xem giải) Câu 17. Cho các phát biểu sau về ý nghĩa dãy điện hoá của kim loại:
(a) Thế điện cực chuẩn cặp oxi hoá – khử Mn+/M càng lớn, tính khử của kim loại càng mạnh.
(b) Trong điều kiện chuẩn, tất cả kim loại đứng trước đều khử được ion kim loại đứng sau trong dung dịch muối.
(c) Sức điện động chuẩn của pin điện hoá tạo bởi hai cặp oxi hoá – khử luôn có giá trị dương.
(d) Ở điều kiện chuẩn, pin Galvani tạo bởi 2 cặp M+/M và N2+/N (E°M+/M > E°N2+/N) dòng electron chuyển từ thanh kim loại M sang thanh kim loại N.
Số phát biểu đúng là
A. 2. B. 1. C. 3. D. 4.
(Xem giải) Câu 18. Cho biết thế điện cực chuẩn của Ca2+/Ca, Mg2+/Mg và Cu2+/Cu lần lượt là −2,84V, −2,356V và +0,34V. Nhóm học sinh được giao nhiệm vụ tách Cu ở lẫn tạp chất là Ca và Mg. Một bạn học sinh đề xuất “có thể cho hỗn hợp vào dung dịch CuSO4 dư, các kim loại Ca và Mg sẽ tan, lọc dung dịch sau phản ứng sẽ thu được kim loại Cu tinh khiết”. Một số nhận định đồng tình và không đồng tình với đề xuất này được đưa ra như sau:
(1) Sử dụng dung dịch CuSO4 được vì Ca và Mg có tính khử mạnh hơn Cu nên sẽ tan trong dung dịch CuSO4.
(2) Không thể sử dụng vì chất không tan sau phản ứng sẽ gồm Cu, Cu(OH)2 và có thể có CaSO4.
(3) Không thể sử dụng vì Cu có tính khử mạnh hơn Ca và Mg.
(4) Có thể sử dụng vì Ca, Mg khử ion Cu2+ thành kim loại Cu nên chất rắn sau có khối lượng Cu tăng thêm so với khối lượng Cu ban đầu.
Nhận định đúng là
A. nhận định (4). B. nhận định (3). C. nhận định (2). D. nhận định (1).
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Trong thực tế, sự ăn mòn kim loại gây ra tổn thất to lớn về tài nguyên và chi phí sửa chữa, thay thế các chi tiết bị ăn mòn của máy móc, thiết bị. Một trong số các phương pháp bảo vệ chống ăn mòn kim loại được sử dụng rộng rãi là phương pháp bảo vệ cathode. Trong phương pháp này, người ta sẽ hoặc cho kim loại cần được bảo vệ tiếp xúc với kim loại hoạt động hóa học mạnh hơn (kim loại hy sinh).
a) Trong một thí nghiệm nghiên cứu sự ảnh hưởng của kẽm nhằm bảo vệ chống ăn mòn thép. Một khối kẽm có khối lượng 50,0 gam được gắn lên một vật bằng thép đặt trong nước biển. Sau một thời gian, cân lại thì khối kẽm nặng 56,8 gam. Giả thiết trong quá trình đó, toàn bộ Zn chỉ bị oxi hóa thành Zn(OH)2 và hydroxide này bám hết lên khối kẽm. Phần trăm khối lượng kẽm đã bị oxi hóa là 28,46%. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm.)
b) Vật bằng thép bị ăn mòn nhanh hơn khi tiếp xúc với kẽm nhưng bị ăn mòn chậm hơn khi tiếp xúc với kim loại đồng.
c) Trong trường hợp sử dụng kẽm để bảo vệ vật bằng thép khỏi bị ăn mòn thì bản chất là dựa vào hoạt động của pin điện hóa mà trong đó kẽm là anode, vật bằng thép là cathode.
d) Kim loại hy sinh luôn có thế điện cực chuẩn thấp hơn kim loại có thể được bảo vệ.
(Xem giải) Câu 20. Trong vỏ quả cây vanilla có hợp chất mùi thơm dễ chịu, tên thường là vanillin. Công thức cấu tạo của vanillin như hình bên:
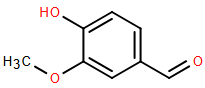
a) Vanillin thuộc loại hợp chất hữu cơ tạp chức.
b) Vanillin có thể bị khử bởi dung dịch AgNO3 trong NH3 tạo thành bạc kim loại.
c) Mẫu vanillin đủ tiêu chuẩn dùng trong công nghiệp sản xuất dược phẩm và thực phẩm cần có trên 99% về khối lượng là vanillin. Để định lượng một mẫu vanillin, người ta làm như sau: Hòa tan 0,120 gam mẫu trong 20 mL ethanol 96% và thêm 60 mL nước cất, thu được dung dịch X. Biết X phản ứng vừa đủ với 7,82 mL dung dịch NaOH nồng độ 0,1M và tạp chất trong mẫu không phản ứng với NaOH. Từ các số liệu trên suy ra mẫu vanillin này không đủ tiêu chuẩn dùng trong công nghiệp sản xuất dược phẩm và thực phẩm.
d) Công thức phân tử của vanillin là C8H8O3.
(Xem giải) Câu 21. Poly(vinyl chloride) (PVC) là một chất dẻo có tính cách điện tốt, không thấm nước, bền với acid vì vậy nó được dùng để sản xuất vật liệu cách điện, ống dẫn nước,… Khi đun nóng, PVC mềm ra rồi nóng chảy và khi để nguội nó lại đóng rắn. Hiện nay, trong công nghiệp sản xuất PVC người ta đi từ nguyên liệu là khí ethylene và chlorine. Quy trình sản xuất thực hiện theo sơ đồ khép kín:

a) Đốt cháy là một trong các phương pháp xử lí chất thải nhựa PVC mà không làm ô nhiễm môi trường.
b) PVC thuộc loại polymer nhiệt dẻo và vật liệu làm bằng PVC có thể tái chế.
c) Phản ứng (3) giúp giảm thải khí gây ô nhiễm môi trường và tăng hiệu quả của quá trình sản xuất.
d) Biết chỉ có 1,4% lượng chlorine bị thất thoát vì vậy để sản xuất 1,3 tấn PVC cần 682 kg chlorine (làm tròn số đến phần mười).
(Xem giải) Câu 22. Hạt chống ẩm đổi màu, một dạng đặc biệt của silica gel được trộn thêm chất chỉ thị màu có khả năng thông báo tình trạng hút ẩm bằng cách thay đổi màu sắc. Một loại phức chất được sử dụng dựa trên cân bằng:
CoCl2(s, màu xanh dương) + 6H2O(l) ⇌ X(aq, màu đỏ hồng) + Y(aq) ![]() < 0
< 0
Biết phức chất X có hình học bát diện.
a) Hạt hút ẩm đổi màu có thể tái sử dụng bằng phương pháp sấy nhiệt.
b) Y là phức chất aqua của anion chloride.
c) Trong phức chất aqua của Co2+, số liên kết σ là 18.
d) X là phức aqua có công thức là [Co(OH2)4]2+.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Số nguyên tử carbon có trong một phân tử toluene là bao nhiêu?
(Xem giải) Câu 24. Cho các phát biểu sau:
(1) Dung dịch ethylamine và dung dịch aniline đều làm xanh giấy quỳ tím.
(2) Nhỏ từ từ đến dư dung dịch methylamine vào dung dịch copper(II) sulfate, ban đầu thấy xuất hiện kết tủa màu xanh nhạt, sau đó kết tủa tan tạo thành dung dịch màu xanh lam.
(3) Cho dung dịch methylamine vào ống nghiệm đựng dung dịch iron(III) chloride thấy xuất hiện kết tủa màu nâu đỏ.
(4) Nhỏ vài giọt dung dịch aniline vào ống nghiệm đựng nước bromine thấy xuất hiện kết tủa trắng.
Gắn số thứ tự theo chiều tăng dần các phát biểu đúng (ví dụ: 123; 134; 234;…).
(Xem giải) Câu 25. Một oleum có công thức H2SO4.nSO3. Hòa tan 7,605 gam oleum này với nước cất thu được 1000 mL dung dịch H2SO4 loãng (dung dịch X). Để xác định nồng độ H2SO4 trong X, người ta tiến hành chuẩn độ như sau:
• Bước 1: Rửa sạch burette loại 25 mL bằng nước cất, tráng lại bằng dung dịch chuẩn NaOH 0,1 M rồi lắp burette lên giá đỡ, cho dung dịch chuẩn NaOH 0,1M vào burette, điều chỉnh dung dịch trong burette đến vạch 0.
• Bước 2: Lấy chính xác 10,0 mL dung dịch X cho vào bình tam giác 250 mL. Thêm 3 – 4 giọt phenolphthalein, lắc đều.
• Bước 3: Mở khóa burette để dung dịch NaOH nhỏ từ từ xuống bình tam giác, lắc đều cho đến khi dung dịch chuyển từ không màu sang màu hồng bền trong khoảng 20 – 30 giây thì dừng lại.
Thể tích dung dịch NaOH đo được trung bình trong ba lần chuẩn độ là 18,0 mL. Giá trị của n bằng bao nhiêu? (Không làm tròn các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
(Xem giải) Câu 26. Theo Thông tư 50/2025/TT-BCT của bộ Công Thương, xăng sinh học E10 bắt buộc sử dụng cho động cơ đốt trong trên toàn quốc từ ngày 1/6/2026 và xăng E5 RON92 vẫn tiếp tục duy trì đến hết ngày 31/12/2030. Biết rằng, xăng E5 chứa 5% thể tích ethanol và 95% thể tích xăng khoáng (giả sử là hỗn hợp các đồng phân của C8H18). Tương tự, xăng E10 chứa 10% thể tích ethanol. Khối lượng riêng của ethanol là 0,789 g/mL và của xăng khoáng là 0,703 g/mL. Giả thiết quá trình pha trộn không làm thay đổi thể tích hỗn hợp. Ở điều kiện chuẩn, nhiệt lượng tỏa ra khi đốt cháy hoàn toàn 1 mol ethanol và 1 mol hỗn hợp đồng phân C8H18 lần lượt là 1276 kJ và 5144 kJ; Gọi V(CO2–E5) và V(CO2–E10) lần lượt là thể tích khí CO2 thu được ở điều kiện chuẩn khi đốt cháy hai loại nhiên liệu trên sao cho chúng toả ra cùng một lượng nhiệt.
Đặt k = V(CO2–E10) / V(CO2–E5) giá trị của k bằng bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
(Xem giải) Câu 27. Có bao nhiêu công thức cấu tạo của carboxylic acid ứng với công thức phân tử C5H10O2?
(Xem giải) Câu 28. Một nhà máy luyện kim sản xuất Zn từ 80 tấn quặng blende (chứa 75% ZnS về khối lượng, còn lại là tạp chất không chứa kẽm) với hiệu suất cả quá trình đạt 95% qua hai giai đoạn sau:
+ Đốt quặng zinc blende: 2ZnS(s) + 3O2(g) → 2ZnO(s) + 2SO2(g)
+ Khử zinc oxide ở nhiệt độ cao bằng than cốc: ZnO(s) + C(s) → Zn(g) + CO(g)
Toàn bộ lượng Zn tạo ra được đúc thành k thanh Zn hình hộp chữ nhật: Chiều dài 120 cm, chiều rộng 30 cm và chiều cao 5 cm. Biết khối lượng riêng của kẽm là 7,14 g/cm³. Tính giá trị của k? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).

Bình luận