[2026] Thi thử TN sở GDĐT Đồng Nai (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 088
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2D | 3B | 4C | 5C | 6C | 7B | 8C | 9C |
| 10A | 11B | 12A | 13D | 14D | 15D | 16D | 17C | 18A |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | Đ | S | S |
| (b) | S | S | S | S |
| (c) | S | S | S | Đ |
| (d) | Đ | Đ | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 2 | 10 | 4 | 104 | 4 | 4,1 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Khi đi từ Lithium (Li) đến Cesium (Cs) trong nhóm kim loại kiềm (nhóm IA), tính khử của các nguyên tử kim loại có xu hướng tăng dần. Nguyên nhân chính giải thích cho quy luật này là:
A. Khối lượng nguyên tử tăng dần, làm cho các kim loại có xu hướng dễ dàng nhường electron hơn trong phản ứng.
B. Nhiệt độ nóng chảy giảm dần, khiến cho mạng tinh thể kim loại dễ bị phá vỡ để giải phóng electron.
C. Điện tích hạt nhân tăng dần, làm cho electron hóa trị có nhiều năng lượng và càng dễ tách ra khỏi nguyên tử.
D. Bán kính nguyên tử tăng đáng kể làm giảm lực hút của hạt nhân đối với electron hóa trị ngoài cùng.
(Xem giải) Câu 2. Cho các quá trình sau:
(1) CH4 + Cl2 → CH3Cl + HCl
(2) C3H8 → C2H4 + CH4
(3) CH4 + 2O2 → CO2 + 2H2O
(4) 2CH4 + 3O2 → 2CO + 4H2O
Các quá trình 1, 2, 3, 4 lần lượt thuộc loại phản ứng nào?
A. Thế; cracking; oxi hoá không hoàn toàn; oxi hoá hoàn toàn.
B. Cộng; cracking; oxi hoá hoàn toàn; oxi hoá không hoàn toàn.
C. Thế; reforming; oxi hoá hoàn toàn; oxi hoá không hoàn toàn.
D. Thế; cracking; oxi hoá hoàn toàn; oxi hoá không hoàn toàn.
(Xem giải) Câu 3. Phát biểu nào sau đây đúng khi so sánh xà phòng và chất giặt rửa tổng hợp?
A. Cả hai đều là muối của axit béo.
B. Xà phòng là muối của axit béo, còn chất giặt rửa tổng hợp thì không.
C. Chất giặt rửa tổng hợp là este, còn xà phòng là ancol.
D. Cả hai đều không tan trong nước.
(Xem giải) Câu 4. Tên gốc – chức của hợp chất CH3CH2NH2 là
A. Methylamine. B. Dimethylamine. C. Ethylamine. D. Propylamine.
(Xem giải) Câu 5. Bình xịt gây tê trong thể thao là dụng cụ y tế khẩn cấp giúp làm đông lạnh cục bộ, tê liệt dây thần kinh cảm giác để giảm đau, sưng tấy tức thì khi bị va chạm, bong gân hoặc căng cơ. Trong một số bình xịt gây tê, người ta sử dụng một hợp chất hữu cơ X. Chất X là
A. CH3OH, vì khi bay tỏa nhiệt mạnh vào môi trường.
B. C2H6, vì không phân cực nên hấp thụ nhiệt tốt.
C. C2H5Cl, vì khi bay hơi thu nhiệt mạnh từ môi trường.
D. C2H5OH, vì có khả năng tạo liên kết hydrogen và sát khuẩn.
(Xem giải) Câu 6. Mùi tanh của cá chủ yếu do các amine (như trimethylamine) gây ra. Để khử mùi tanh này trong quá trình sơ chế, người ta thường dùng giấm ăn (chứa chất X) là do:
A. Acetic acid có trong giấm làm xúc tác cho quá trình phân hủy các amine thành những chất khí không mùi.
B. Acetic acid và nước tạo lớp màng bảo vệ trên bề mặt cá, ngăn không cho các amine tiếp xúc với không khí.
C. Acetic acid có trong giấm ăn phản ứng với các amine tạo thành muối tan trong nước, dễ dàng bị rửa trôi.
D. Nước có trong giấm ăn đã hòa tan các amine thành dung dịch bão hòa, ngăn chặn sự bay hơi của mùi tanh.
(Xem giải) Câu 7. Trong các phân tử sau, phân tử nào có chứa liên kết đôi?
A. CH4 B. CO2 C. H2O D. NH3
(Xem giải) Câu 8. Trong một pin điện hoá Galvani Zn-Cu đang hoạt động tạo ra dòng điện, điện cực kẽm (Zn) có vai trò là:
A. Cathode, nơi xảy ra quá trình khử và đóng vai trò là cực dương của pin.
B. Cathode, nơi xảy ra quá trình oxi hóa và đóng vai trò là cực dương của pin.
C. Anode, nơi xảy ra quá trình oxi hoá và đóng vai trò là cực âm của pin.
D. Anode, nơi xảy ra quá trình khử và đóng vai trò là cực âm của pin.
(Xem giải) Câu 9. Kim loại nào sau đây có tính dẻo cao nhất, có thể dát thành những màng cực mỏng (đến mức ánh sáng có thể xuyên qua được) và thường được ứng dụng để phủ (thếp) lên bề mặt các tác phẩm mĩ nghệ, tượng hoặc các công trình kiến trúc nhằm mục đích trang trí?
A. Ag (Bạc). B. Cu (Đồng). C. Au (Vàng). D. Al (Nhôm).
(Xem giải) Câu 10. Khi quan sát các vật dụng bằng sắt (thép) như đinh, búa, xẻng để lâu ngoài không khí ẩm, ta thường thấy chúng xuất hiện lớp gỉ màu nâu đỏ, xốp và làm vật dụng trở nên giòn, dễ gãy. Phát biểu nào sau đây trình bày đúng khái niệm về hiện tượng ăn mòn kim loại xảy ra trong ví dụ trên?
A. Là sự phá huỷ kim loại hoặc hợp kim do tác dụng hoá học, điện hoá của các chất trong môi trường xung quanh.
B. Là sự biến đổi trạng thái vật lí của kim loại từ rắn sang lỏng do hấp thụ hơi ẩm từ môi trường.
C. Là sự bào mòn bề mặt kim loại do các tác động va đập cơ học trong quá trình con người sử dụng.
D. Là quá trình kim loại tự bay hơi từ từ vào không khí do sự chênh lệch nhiệt độ giữa ngày và đêm.
(Xem giải) Câu 11. Quá trình lưu hoá cao su tự nhiên tạo ra sản phẩm (cao su lưu hoá) có tính đàn hồi, chịu ma sát và chịu nhiệt tốt hơn. Nguyên nhân dẫn đến sự cải thiện tính chất này là do:
A. Sulfur đóng vai trò như một chất xúc tác, làm tăng lực tương tác van der Waals giữa các mạch polymer.
B. Sự hình thành các cầu nối disulfide (-S-S-) liên kết các mạch polymer lại với nhau tạo nên cấu trúc mạng lưới không gian.
C. Sự thay thế các nguyên tử hydrogen trong mạch polymer bằng các nguyên tử sulfur, tạo ra khối vật liệu cứng hơn.
D. Sự cộng hợp nguyên tử sulfur vào toàn bộ các liên kết đôi C=C làm bão hoà hoàn toàn mạch hydrocarbon của cao su.
(Xem giải) Câu 12. Phát biểu nào sau đây đúng?
A. Chất béo là triester của glycerol với acid béo.
B. Acid béo là hợp chất hữu cơ chứa nhiều nhóm –COOH.
C. Ester là hợp chất chỉ chứa nguyên tố C và H.
D. Lipid là những hợp chất hữu cơ tan tốt trong nước và không tan trong dung môi hữu cơ.
(Xem giải) Câu 13. Dựa vào nguồn gốc, các loại tơ được phân chia thành tơ tự nhiên, tơ tổng hợp và tơ bán tổng hợp (tơ nhân tạo). Trong các loại polymer dưới đây, chất nào thuộc loại tơ bán tổng hợp?
A. Tơ nitron. B. Tơ capron. C. Tơ tằm. D. Tơ visco.
(Xem giải) Câu 14. Hợp chất của một kim loại nhóm IIA (nhóm kim loại kiềm thổ) được sử dụng rộng rãi làm vật liệu xây dựng (thành phần chính của đá vôi, vỏ sò, xi măng). Nguyên tố kim loại đó là:
A. Sodium (Na). B. Aluminum (Al). C. Iron (Fe). D. Calcium (Ca).
(Xem giải) Câu 15. Saccharose được dùng phổ biến trong thực phẩm. Phát biểu nào sau đây đúng về saccharose?
A. là disaccharide, không tan trong nước, có vị nhạt.
B. là polysaccharide gồm nhiều đơn vị glucose liên kết α-1,4-glycoside.
C. là monosaccharide, tan tốt trong nước, có vị ngọt.
D. là disaccharide, tạo từ glucose và fructose, tan tốt trong nước.
(Xem giải) Câu 16. Tiến hành điện phân dung dịch CuCl2 với các điện cực trơ. Quan sát thấy tại cathode có lớp kim loại bám vào và anode có khí thoát ra. Nhận định nào sau đây mô tả đúng bản chất các quá trình hoá học xảy ra tại các điện cực?
A. Tại cathode xảy ra quá trình oxi hóa ion Cu2+ và tại anode xảy ra quá trình khử ion Cl-.
B. Tại cathode xảy ra quá trình khử phân tử H2O và tại anode xảy ra quá trình oxi hóa ion Cl-.
C. Tại cathode xảy ra quá trình khử ion Cu2+ và tại anode xảy ra quá trình oxi hóa phân tử H2O.
D. Tại cathode xảy ra quá trình khử ion Cu2+ và tại anode xảy ra quá trình oxi hoá ion Cl-.
(Xem giải) Câu 17. Giá trị pH thích hợp mà tại đó hợp chất amino acid tồn tại chủ yếu ở dạng ion lưỡng cực và có tổng điện tích bằng không gọi là điểm đẳng điện (pI). Khi pH giảm dần thì dạng ion lưỡng cực chuyển dần thành dạng cation, khi pH tăng dần thì dạng ion lưỡng cực chuyển dần thành dạng anion. Dưới tác dụng của điện trường, các ion di chuyển về các điện cực trái dấu với ion. Một số thông tin về các amino acid cho trong bảng sau:
| Amino acid | Glutamic acid | Alanine | Lysine |
| Điểm đẳng điện (pI) | 3,1 | 6,0 | 9,8 |
Phát biểu nào sau đây đúng?
A. Ở pH = 3,1 Alanine chuyển thành cation di chuyển về cực dương.
B. Ở pH = 6,0 Lysine chuyển thành cation di chuyển về điện cực dương.
C. Ở pH = 9,8 Glutamic acid chuyển thành anion di chuyển về cực dương.
D. Ở pH = 6,0 Glutamic acid chuyển thành anion di chuyển về cực âm.
(Xem giải) Câu 18. Phát biểu nào sau đây đúng về tính chất của amoniac (NH3)?
A. NH3 tan tốt trong nước và là base yếu.
B. NH3 không tan trong nước và không có tính base.
C. NH3 không tan trong nước và có tính khử mạnh.
D. NH3 tan tốt trong nước nhưng không có tính khử.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Trong công nghiệp, phần lớn phenol và chất A được sản xuất theo sơ đồ sau:
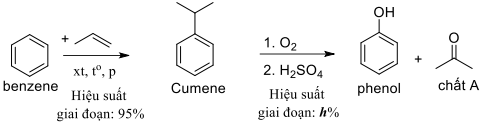
Để sản xuất 650 000 tấn phenol theo sơ đồ trên, nhà máy cần sử dụng 590 000 tấn benzene làm nguyên liệu đầu vào.
a) Giá trị của h là 96. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
b) Trong sơ đồ trên, phản ứng giữa cumene và oxygen là phản ứng oxi hóa hoàn toàn.
c) Chất A có tên thông thường là propan-2-one.
d) Do ảnh hưởng của nhóm –OH nên phản ứng thế nguyên tử hydrogen trên vòng benzene của phenol xảy ra dễ hơn so với benzene.
(Xem giải) Câu 20. Một học sinh quan sát thấy NaOH để ngoài không khí bị chảy rữa, sau đó xuất hiện lớp chất rắn màu trắng. Học sinh này tìm hiểu được hiện tượng này là do việc hấp thu nước và CO2 trong không khí. Học sinh đặt ra giả thuyết: “khối lượng của mẫu NaOH để ngoài không khí tăng với tốc độ không đổi theo thời gian”. Để kiểm chứng giả thuyết học sinh tiến hành thí nghiệm như sau:
• Bước 1: Đặt đĩa thủy tinh lên cân và trừ bì về 0. Mở lọ NaOH, lấy một lượng NaOH cho vào đĩa thấy cân hiển thị đúng 10,350 gam.
• Bước 2: Ngay khi cân xong ở bước 1, bắt đầu bấm giờ.
• Bước 3: Đặt đĩa thủy tinh lên cân để ghi lại khối lượng tại các thời điểm: t = 1; 5; 10; 20; 30 và 60 phút. Quan sát sự thay đổi vật lý của mẫu NaOH trong đĩa thủy tinh.
Từ kết quả thu được học sinh vẽ đồ thị như sau:
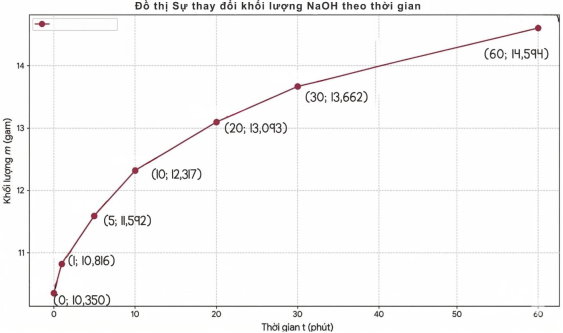
Tốc độ tăng khối lượng trung bình = (m sau – m trước)/(t sau – t trước) (g/phút)
a) Chất rắn màu trắng xuất hiện là muối sinh ra từ phản ứng giữa NaOH và CO2.
b) Kết quả thí nghiệm phù hợp với giả thuyết ban đầu của học sinh.
c) Trong 5 phút đầu tiên từ lúc bấm giờ, tốc độ tăng khối lượng trung bình của mẫu NaOH ở thí nghiệm trên là 0,19 g/phút. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần trăm).
d) Ở bước 1, cần lấy NaOH nhanh chóng và đóng nắp lọ ngay lập tức sau khi lấy xong, nhằm hạn chế tối đa lượng NaOH còn lại trong lọ hấp thụ nước và CO2.
(Xem giải) Câu 21. Thép là hợp kim của sắt (Fe) và carbon, vốn dễ bị ăn mòn khi tiếp xúc với nước biển giàu oxy và muối. Để bảo vệ thép, người ta thường dùng phương pháp điện hóa (gắn khối Mg làm vật hy sinh) hoặc sơn phủ bề mặt. Tuy nhiên, các loại sơn truyền thống chứa chì (Pb) hoặc chromium (Cr) thường gây độc và tích tụ sinh học trong sinh vật biển. Do đó, xu hướng hiện nay là phát triển sơn bio-polymer từ nguyên liệu tái tạo kết hợp với (nano silica SiO2). Loại sơn mới này vừa thân thiện với môi trường, vừa tạo lớp màng ngăn cách có độ bám dính và độ kín khít cao, giúp bảo vệ công trình bền vững hơn.
Bảng: Thế điện cực chuẩn của một số cặp oxi hóa – khử
| Cặp oxi hóa – khử | Mg2+/Mg | Fe2+/Fe | Sn2+/Sn |
| E°(V) | -2,37 | -0,44 | -0,14 |
a) Khi gắn khối Mg vào chân giàn khoan bằng thép, nó sẽ đóng vai trò là cathode và bị oxi hóa thay cho sắt (Fe).
b) Phương pháp bảo vệ bề mặt làm thay đổi thế điện cực chuẩn của kim loại, từ đó hạn chế quá trình oxi hóa xảy ra trên bề mặt kim loại.
c) Gắn thiếc (Sn) lên vỏ tàu thép được xem là phương pháp bảo vệ điện hóa giúp ngăn ngừa quá trình ăn mòn kim loại.
d) Việc lựa chọn sơn bio-polymer nano thay thế cho các dòng sơn chứa chì hay chromium là một phương án đề xuất phù hợp nhằm giải quyết vấn đề ô nhiễm thứ cấp từ kim loại nặng trong môi trường biển.
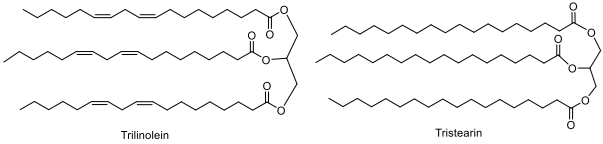
(Xem giải) Câu 22. Omega-3 và omega-6 là hai nhóm acid béo không no thiết yếu, cơ thể người không tự tổng hợp được mà phải lấy từ thức ăn. Omega-3 có nhiều trong dầu cá, dầu hạt lanh; omega-6 có nhiều trong dầu đậu nành, dầu hướng dương. Trong cơ thể, chất béo được thủy phân nhờ enzyme lipase, giải phóng acid béo tự do. Việc cân bằng tỉ lệ omega-6 và omega-3 trong khẩu phần ăn có ý nghĩa quan trọng trong phòng chống viêm nhiễm và bệnh tim mạch. Dưới đây là cấu trúc của hai phân tử chất béo tiêu biểu: một chất béo không no được tạo thành từ acid béo omega-6, và một chất béo no được tạo thành từ acid béo no:
a) Acid béo thuộc nhóm omega‑3 và omega‑6 cũng được sinh ra từ phản ứng thủy phân chất béo trong môi trường base.
b) Dầu cá chứa nhiều omega‑3, còn dầu thực vật như dầu đậu nành chứa chủ yếu omega‑6; do đó để phòng bệnh tim mạch, nên ưu tiên dùng dầu cá hoàn toàn thay thế dầu thực vật.
c) Trilinolein có nhiệt độ nóng chảy thấp hơn so với tristearin.
d) Chất béo tạo từ gốc acid omega‑3 và omega‑6 dễ bị oxi hóa trong không khí, tạo các hợp chất có mùi khó chịu do có chứa liên kết đôi C=C.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Để tìm hiểu những điều kiện cần thiết để ăn mòn điện hóa, một học sinh đã thiết lập thí nghiệm như hình sau:
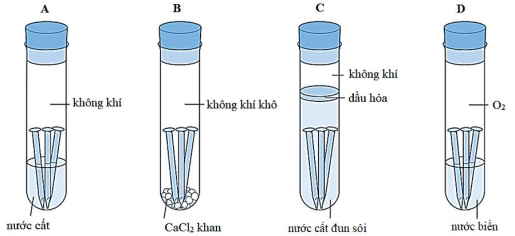
Có bao nhiêu ống nghiệm chứa đinh sắt sẽ bị gỉ sau vài ngày?
(Xem giải) Câu 24. Phương pháp trao đổi ion để làm mềm nước cứng được thực hiện bằng cách cho nước cứng đi qua lớp vật liệu hay màng vật liệu trao đổi ion. Các vật liệu này có chứa cation kim loại, như Na+. Khi cho nước cứng đi qua vật liệu, các cation Ca2+ và Mg2+ đẩy cation Na+ ra khỏi vật liệu. Các cation Ca2+ và Mg2+ bị giữ lại trên vật liệu. Thiết bị làm mềm nước cứng (sử dụng vật liệu trao đổi ion) cần thêm NaCl để thay thế các ion Ca2+ và Mg2+ đang bám trên vật liệu bằng ion Na+, giúp phục hồi vật liệu để tiếp tục làm mềm nước. 50 m³ một loại nước cứng đã được loại bỏ hoàn toàn độ cứng bằng cách cho nước chảy qua thiết bị làm mềm nước. Sau đó, thiết bị làm mềm nước này cần 200 lít dung dịch sodium chloride chứa 150 g/lít NaCl để tái tạo hoàn toàn. Số đơn vị độ cứng của mẫu nước cứng trên là bao nhiêu ? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị). Biết một 1 đơn vị độ cứng tương ứng với tổng số mol của các ion Ca2+ và Mg2+ bằng 0,5 mmol trong 1,0 L nước. Giả sử vật liệu trao đổi ion hoạt động với hiệu suất 100%.
(Xem giải) Câu 25. Trong phòng thí nghiệm, để khảo sát phản ứng thủy phân tinh bột, một nhóm học sinh chuẩn bị ba ống nghiệm, mỗi ống chứa khoảng 2 mL dung dịch hồ tinh bột 1% (đánh số 1, 2, 3) và tiến hành thí nghiệm theo các bước sau:
• Bước 1: thêm khoảng 1 mL dung dịch HCl 1M vào ống nghiệm thứ nhất.
• Bước 2: thêm khoảng 1 mL dung dịch HCl 2M vào ống nghiệm thứ hai.
• Bước 3: Thêm khoảng 1 mL nước cất vào ống nghiệm thứ ba.
• Bước 4: Lắc đều, rồi đặt cả 3 ống nghiệm trong nồi nước nóng, đun cách thủy trong 10 phút. Sau đó để nguội.
• Bước 5: Chia mỗi ống nghiệm thành hai phần:
– Phần 1: cho tác dụng với dung dịch iodine.
– Phần 2: thêm từng giọt dung dịch NaOH 1M cho đến môi trường kiềm, sau đó cho 1 ml thuốc thử Tollens vào, đun cách thủy.
Sau thí nghiệm thu được bảng kết quả:
| Ống | I2 | Tollens |
| (1) | xanh tím | có kết tủa bạc |
| (2) | không đổi màu | có kết tủa bạc |
| (3) | xanh tím | không có kết tủa bạc |
Cho các nhận định sau:
(1) Ở ống nghiệm (1), tinh bột chưa bị thủy phân hoàn toàn thành glucose.
(2) Ở ống nghiệm (2), toàn bộ tinh bột đã bị thủy phân hết.
(3) Ở ống nghiệm (3), không có glucose tạo thành.
(4) Sự có mặt của acid làm phản ứng thủy phân xảy ra nhanh hơn.
(5) Dựa vào phản ứng Tollens, có thể kết luận mẫu không còn tinh bột.
Trong các nhận định trên, có bao nhiêu nhận định đúng?
(Xem giải) Câu 26. Cho cấu tạo của một đoạn mạch trong phân tử polymer X:
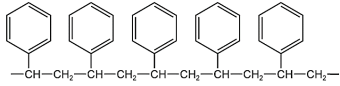
Monomer tổng hợp nên polymer X có phân tử khối bằng bao nhiêu amu?
(Xem giải) Câu 27. Amine X có công thức phân tử là C4H11N. Cho X phản ứng với hỗn hợp dung dịch HCl và NaNO2 ở nhiệt độ thường thấy có khí không màu thoát ra. Có bao nhiêu công thức cấu tạo phù hợp với X?
(Xem giải) Câu 28. Trinitroglycerin, C3H5N3O9 (thường gọi đơn giản là nitroglycerin) là chất nổ mạnh được Alfred Nobel chế tạo thành thuốc nổ dynamite vào năm 1866. Điều khá bất ngờ là nó cũng được sử dụng như một loại thuốc, để giảm đau thắt ngực (đau ngực do động mạch đến tim bị tắc một phần) bằng cách làm giãn mạch máu. Ở điều kiện chuẩn, biến thiên enthalpy của phản ứng phân hủy 1 mol trinitroglycerin tạo thành khí nitrogen, khí carbon dioxide, nước lỏng và khí oxygen là -1541,4 kJ. Để giảm đau thắt ngực, liều chuẩn của trinitroglycerin là 0,60 mg. Nếu liều chuẩn của trinitroglycerin bị phân hủy hoàn toàn trong cơ thể theo phản ứng phân hủy trên thì năng lượng được giải phóng là bao nhiêu J ? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).


Bình luận