[2026] Thi thử TN sở GDĐT Lạng Sơn (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 126
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2C | 3C | 4A | 5C | 6D | 7D | 8D | 9C |
| 10D | 11C | 12C | 13C | 14C | 15A | 16B | 17D | 18D |
| 19 | 20 | 21 | 22 | |
| (a) | S | S | Đ | Đ |
| (b) | S | Đ | S | Đ |
| (c) | Đ | S | S | Đ |
| (d) | Đ | Đ | Đ | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 340 | 4 | 5 | 71,4 | 1,95 | 46,9 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Phát biểu nào sau đây không đúng?
A. Tính chất hoá học của hợp kim thường tương tự tính chất của các kim loại thành phần.
B. Hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn so với kim loại.
C. Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
D. Hợp kim thường dễ bị oxi hoá hơn các đơn kim loại thành phần.
(Xem giải) Câu 2. Ethyl acetate là một chất lỏng không màu có mùi dễ chịu đặc trưng và được sản xuất ở quy mô khá lớn để làm dung môi. Công thức cấu tạo của ethyl acetate là
A. CH3COOCH3. B. C2H5COOCH3. C. CH3COOC2H5. D. HCOOC2H5.
(Xem giải) Câu 3. Trong phản ứng tách kim loại Fe từ Fe2O3 theo phương trình hóa học: Fe2O3(s) + 3CO(g) → 2Fe(l) + 3CO2(g). Phương pháp tách kim loại nào sau đây đã được áp dụng?
A. Điện phân dung dịch. B. Thủy luyện.
C. Nhiệt luyện. D. Điện phân nóng chảy.
(Xem giải) Câu 4. Polystyrene (PS) là chất nhiệt dẻo thường được sử dụng để sản xuất đồ nhựa như: cốc, chén dùng một lần hoặc hộp đựng thức ăn mang về tại các cửa hàng. Monomer được dùng để điều chế PS là
A. C6H5CH=CH2. B. CH2=CH–CH3. C. CH2=CH–CH=CH2. D. CH2=CH2.
(Xem giải) Câu 5. Kim loại tungsten (W) được dùng làm dây tóc bóng đèn sợi đốt. Ứng dụng này dựa trên tính chất nào của kim loại W?
A. Khối lượng riêng lớn. B. Tính dẻo cao.
C. Nhiệt độ nóng chảy cao. D. Độ cứng cao.
(Xem giải) Câu 6. Chất dẻo và rác thải nhựa đang là một trong những nguyên nhân chính gây ô nhiễm môi trường nghiêm trọng, ảnh hưởng đến hệ sinh thái và sức khỏe con người. Việc sử dụng và xử lí rác thải nhựa hợp lí là vấn đề cần được quan tâm. Xét các phát biểu sau:
(a) Các loại nhựa sau khi thải ra môi trường cần thời gian rất dài để phân hủy.
(b) Rác thải nhựa sau khi thu gom nên được đốt hoặc chôn lấp để giảm thiểu ô nhiễm môi trường.
(c) Nên sử dụng vật liệu phân hủy sinh học để thay thế một số loại chất dẻo.
(d) Nên phân loại rác thải tại nguồn để lựa chọn phương pháp xử lí phù hợp.
Số phát biểu đúng là
A. 2. B. 1. C. 4. D. 3.
(Xem giải) Câu 7. Nước ép chanh chứa khoảng 5% citric acid và có độ pH khoảng 2 – 3. Công thức của citric acid được cho như sau:
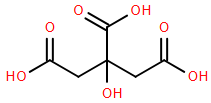
Phát biểu nào sau đây là sai?
A. Citric acid thuộc loại hợp chất hữu cơ tạp chức.
B. Cứ 1 mol citric acid tác dụng được tối đa với 3 mol NaHCO3.
C. Vị chua của nước chanh chủ yếu do citric acid gây ra.
D. Tổng số nguyên tử trong một phân tử của citric acid là 19.
(Xem giải) Câu 8. Nhúng đầu que đốt bằng platinum đã được rửa sạch bằng nước vào dung dịch sodium chloride (NaCl) bão hoà rồi đưa lên ngọn lửa đèn khí sẽ thấy ngọn lửa có màu
A. xanh lam. B. đỏ tía. C. tím nhạt. D. vàng.
(Xem giải) Câu 9. Trong công nghiệp, để sản xuất được bạc (Ag) tinh khiết cần tiến hành các bước sau:
• Bước 1: Nghiền nhỏ 80 kg quặng X (chứa 73,25% Ag2S về khối lượng) rồi cho tác dụng vừa đủ với dung dịch NaCN. Sau khi lọc, thu được dung dịch muối phức chứa bạc theo phản ứng sau:
Ag2S + 4NaCN → 2Na[Ag(CN)2] + Na2S.
• Bước 2: Cho tiếp kim loại Zn dư tác dụng với dung dịch muối phức chứa bạc theo phản ứng:
Zn + 2Na[Ag(CN)2] → Na2[Zn(CN)4] + 2Ag.
Biết hiệu suất mỗi phản ứng trên đều đạt 95%. Khối lượng bạc (kg) thu được sau phản ứng là
A. 24,24. B. 23,03. C. 46,06. D. 48,49.
(Xem giải) Câu 10. Đơn chất của nguyên tố X được dùng làm dây dẫn điện cao thế, hợp kim được dùng chế tạo ô tô, máy bay… Nguyên tử của nguyên tố X có 3 lớp electron, lớp ngoài cùng có 3 electron. Cấu hình electron của X là
A. 1s22s22p63s23p4. B. 1s22s22p63s23p3.
C. 1s22s22p63s23p2. D. 1s22s22p63s23p1.
(Xem giải) Câu 11. Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trong đời sống như kích thích quả mau chín, điều chế nhựa làm sản phẩm gia dụng,… Cơ chế của phản ứng hóa học giữa ethylene với dung dịch Br2 xảy ra như sau:
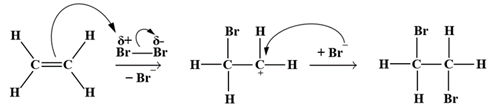
Nhận định nào sau đây không đúng?
A. Phản ứng có sự phân cắt liên kết π giữa hai nguyên tử carbon.
B. Phản ứng trên thuộc loại phản ứng cộng.
C. Sản phẩm của phản ứng có tên gọi là 1,1-dibromoethane.
D. Nếu thay Br2 bằng Cl2, cơ chế phản ứng xảy ra tương tự.
(Xem giải) Câu 12. Carbohydrate là nhóm hợp chất hữu cơ quan trọng, đóng vai trò cung cấp năng lượng chủ yếu cho cơ thể và có nhiều trong các thực phẩm hằng ngày như tinh bột, saccharose, glucose… Xét các phát biểu sau:
(a) Glucose và fructose không tham gia phản ứng thủy phân.
(b) Có thể phân biệt glucose và fructose bằng nước bromine.
(c) Amylopectin được cấu tạo từ các đơn vị α-glucose liên kết với nhau qua liên kết α-1,4-glycoside và α-1,6-glycoside, tạo cấu trúc mạch phân nhánh.
(d) Phân tử saccharose có thể mở vòng tạo nhóm aldehyde, do đó có phản ứng với thuốc thử Tollens.
Số phát biểu đúng là
A. 4. B. 2. C. 3. D. 1.
(Xem giải) Câu 13. Cho phản ứng hoá học sau: C(s) + O2(g) → CO2(g). Yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng trên?
A. Diện tích bề mặt carbon. B. Nhiệt độ.
C. Khối lượng carbon. D. Áp suất O2.
(Xem giải) Câu 14. Một học sinh thực hiện ba thí nghiệm liên quan đến ba kim loại X, Y, Z và dung dịch muối nitrate của chúng ở điều kiện chuẩn, quan sát được các hiện tượng sau:
(1) X không phản ứng được với dung dịch Y(NO3)2 1M.
(2) Y tan trong dung dịch muối ZNO3 1M và xuất hiện tinh thể Z.
(3) Z không phản ứng với dung dịch X(NO3)2 1M.
Thứ tự tăng dần tính khử của ba kim loại là
A. X < Y < Z. B. X < Z < Y. C. Z < X < Y. D. Y < Z < X.
(Xem giải) Câu 15. Để kiểm tra sự có mặt của một số cation kim loại có trong dung dịch ta tiến hành thí nghiệm sau: Cho khoảng 4-6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch cần xác định cation trong muối, thấy có kết tủa màu xanh xuất hiện ngay. Từ kết quả thí nghiệm dự đoán được trong dung dịch này có thể chứa cation nào sau đây?
A. Cu2+. B. Fe3+. C. Zn2+. D. Ag+.
(Xem giải) Câu 16. Phương pháp tách chất bằng cách làm bay hơi một chất lỏng và sau đó ngưng tụ hơi bằng cách làm lạnh được gọi là phương pháp
A. sắc kí cột. B. chưng cất. C. chiết. D. kết tinh.
(Xem giải) Câu 17. Trong thực tế, một số biện pháp được thực hiện để hạn chế sự ăn mòn kim loại như sau:
(a) Tráng kẽm lên vật liệu thép để sản xuất tấm tôn lợp nhà.
(b) Sử dụng các bệ đỡ làm bằng thép hoặc nhôm để đỡ các bức tượng bằng đồng.
(c) Quét sơn kín bề mặt hàng rào bằng thép.
(d) Gắn các khối kẽm lên mặt ngoài của vỏ tàu biển (phần chìm dưới nước).
(e) Rửa sạch và lau khô dao bằng thép sau khi thái, cắt hoa quả.
Trong số các biện pháp trên, những trường hợp nào có mục đích hạn chế (hoặc ngăn cản) sự tiếp xúc của kim loại với dung dịch điện li?
A. (b), (c), (d). B. (a), (c), (d). C. (b), (d), (e). D. (a), (c), (e).
(Xem giải) Câu 18. Hiện nay, trữ lượng các mỏ quặng kim loại ngày càng cạn kiệt, trong khi nhu cầu sử dụng kim loại ngày càng tăng và lượng phế thải kim loại tạo ra ngày càng nhiều. Điều này đòi hỏi cần có các giải pháp tái chế kim loại nhằm giảm sự phụ thuộc vào hoạt động khai thác tài nguyên và bảo vệ môi trường. Cho các phát biểu sau:
(a) Tái chế kim loại vừa tiết kiệm tài nguyên thiên nhiên, vừa gia tăng giá trị kinh tế, bảo vệ môi trường và thực hiện mục tiêu phát triển bền vững.
(b) Tái chế kim loại tiêu thụ ít năng lượng hơn và phát thải ít chất ô nhiễm hơn so với việc sản xuất kim loại từ quặng.
(c) Nhiệt độ ở giai đoạn nấu chảy khi tái chế nhôm, sắt, đồng phụ thuộc chủ yếu vào nhiệt độ nóng chảy của các kim loại tương ứng.
(d) Quá trình tái chế kim loại thủ công không gây ô nhiễm môi trường.
Số phát biểu đúng là
A. 1. B. 4. C. 2. D. 3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Một học sinh tiến hành thí nghiệm với giả thuyết: “Độ tan của CaSO4 giảm khi tăng nhiệt độ” như sau:
• Bước 1: Chuẩn bị 4 bình riêng biệt, mỗi bình đều thêm lượng dư CaSO4.2H2O (3 gam) vào 100 mL nước cất. Đặt mỗi bình ở các mức nhiệt độ khác nhau (cụ thể: 20°C, 40°C, 60°C, 80°C). Khuấy đều trong 15 – 20 phút để đạt cân bằng (đảm bảo vẫn còn chất rắn dư). Duy trì nhiệt độ ổn định ít nhất 10 phút trước khi lọc.
• Bước 2: Lọc nhanh dung dịch bão hòa trong khi vẫn giữ ở nhiệt độ ổn định như ban đầu. Thu lấy phần dịch lọc.
• Bước 3: Lấy 25 mL dung dịch đã lọc và làm bay hơi hết nước rồi cân phần chất rắn khan còn lại. Tính độ tan của CaSO4 theo đơn vị gam chất tan trong 100 mL nước (xem thể tích thay đổi không đáng kể trong quá trình hòa tan). Kết quả như sau:
| Nhiệt độ (°C) | 20 | 40 | 60 | 80 |
| Độ tan (g/100 mL nước) | 0,285 | 0,168 | 0,162 | 0,155 |
a) Từ kết quả cho thấy giả thuyết ban đầu của học sinh là đúng.
b) Ở 60°C, khối lượng chất rắn thu được ở bước 3 là 0,05 gam.
c) Mục tiêu của thí nghiệm là xác định sự thay đổi độ tan CaSO4 theo nhiệt độ.
d) Học sinh lọc dung dịch bão hòa trong điều kiện giữ nhiệt độ ổn định với mục đích tránh kết tinh muối làm sai lệch kết quả.
(Xem giải) Câu 20. Mạ điện là quá trình phủ một lớp kim loại lên bề mặt kim loại khác bằng phương pháp điện phân. Giả sử, người ta cần mạ bạc (Ag) lên hai mặt của một tấm kim loại (mỏng, phẳng) hình tròn có bán kính 30 cm, độ dày lớp mạ là 0,01 mm. Tiến hành điện phân với các điện cực bằng Ag tinh khiết và tấm kim loại cần mạ, dung dịch điện phân là AgNO3. Nếu được cung cấp nguồn điện một chiều có cường độ dòng điện I = 2,5 A thì thời gian cần dùng là t giờ. Biết rằng khối lượng riêng của là 10,5 g/cm³; π = 3,14; hằng số Faraday F = 96500 C/mol; hiệu suất điện phân là 92%, giả sử nước không bị bay hơi trong quá trình điện phân.
a) Có thể thay dung dịch AgNO3 bằng dung dịch Cu(NO3)2.
b) Trong quá trình điện phân, nồng độ ion Ag+ trong dung dịch được coi là không thay đổi.
c) Trong quá trình mạ điện, thanh bạc tinh khiết được dùng làm cathode, tấm kim loại cần mạ được dùng làm anode.
d) Giá trị của t là 6,4 (kết quả cuối cùng làm tròn đến hàng phần mười).
(Xem giải) Câu 21. Chất béo là nguồn dinh dưỡng thiết yếu, không chỉ cung cấp năng lượng mà còn tham gia vào quá trình hấp thụ các vitamin tan trong dầu như A, D, E và K. Về mặt hóa học, chất béo chủ yếu là các triglyceride – triester tạo bởi glycerol và các acid béo. Cho một triglyceride X có công thức cấu tạo như hình sau:
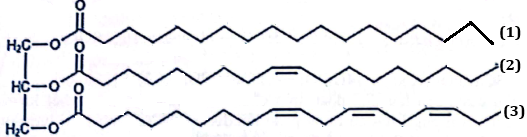
Tiến hành thủy phân hoàn toàn a mol X trong dung dịch NaOH, thu được a mol chất Y và hỗn hợp muối Z.
a) Hỗn hợp muối Z có thể được sử dụng làm nguyên liệu sản xuất xà phòng.
b) Chỉ số xà phòng hóa là tổng số miligam KOH cần để xà phòng hóa triglyceride và trung hòa acid béo tự do trong 1,0 gam chất béo. Một loại chất béo chứa 97,02% chất X và 1,41% oleic acid về khối lượng, còn lại là các tạp chất không tham gia phản ứng với KOH. Chỉ số xà phòng hoá của chất béo trên là 179,2. (Kết quả cuối cùng làm tròn đến hàng phần mười).
c) Dung dịch chất Y khi đun nóng với copper (II) hydroxide trong môi trường base thu được kết tủa đỏ gạch.
d) Acid béo tương ứng với gốc acid ở vị trí (3) thuộc loại acid béo omega-3.
(Xem giải) Câu 22. Cho X, Y, Z, M là các chất khác nhau trong số 4 chất sau: phenol, glycine, aniline, glutamic acid và thông tin về các chất được ghi trong bảng sau:
| Chất | Nhiệt độ nóng chảy (°C) | Cho quỳ tím vào dung dịch các chất |
| X | -6,0 | không làm đổi màu quỳ tím. |
| Y | 233 | không làm đổi màu quỳ tím. |
| Z | 247 | làm quỳ tím chuyển thành màu hồng. |
| M | 43 | không làm đổi màu quỳ tím. |
a) Thuỷ phân hoàn toàn 1,0 mol peptide A trong dung dịch NaOH thu được 3,0 mol muối của chất Y và 2,0 mol muối của chất Z thì lượng NaOH phản ứng tối đa là 7,0 mol.
b) Từ phản ứng trùng ngưng của M với formaldehyde có acid làm xúc tác có thể điều chế nhựa poly(phenol formaldehyde).
c) Cho Z tác dụng với NaOH tỉ lệ mol 1 : 1, thu được chất hữu cơ T. Khi đặt trong điện trường, chất T di chuyển về cực dương.
d) Các chất X, Y, Z, M là chất rắn ở điều kiện thường.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Trong công nghiệp, người ta sản xuất nitric acid (HNO3) từ ammonia theo sơ đồ chuyển hoá sau:
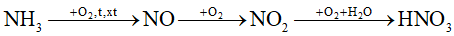
Để sản xuất 1,5 tấn dung dịch HNO3 63%, cần dùng m kg ammonia, biết rằng hiệu suất của toàn bộ quá trình là 75%. Giá trị của m là bao nhiêu (kết quả cuối cùng làm tròn đến hàng đơn vị)?
(Xem giải) Câu 24. Cho các chất: CH2=CH2, CH2=CHCl, CH3COOCH=CH2, C2H5OH, CH2=C(CH3)COOCH3. Có bao nhiêu chất có khả năng trùng hợp tạo polymer?
(Xem giải) Câu 25. Số nguyên tử nitrogen có trong peptide Gly-Ala-Val-Lys là bao nhiêu?
(Xem giải) Câu 26. Theo tiêu chuẩn Việt Nam (TCVN), hàm lượng ion cyanide trong nước thải của các nhà máy phải xử lí trong khoảng 0,05–0,20 mg/L trước khi thải ra môi trường. Phân tích một mẫu nước thải của một nhà máy người ta đo được hàm lượng ion cyanide là x mg/L, vượt mức cho phép. Để làm giảm hàm lượng cyanide đến mức cho phép, người ta bơm sục khí chlorine vào nước thải trong môi trường kiềm hóa thích hợp, có pH = 9. Khi đó ion cyanide chuyển thành nitrogen không độc theo phản ứng:
2CN⁻ + 5Cl2 + 8OH⁻ → 2CO2 + N2 + 10Cl⁻ + 4H2O
Biết rằng thể tích mol khí (ở đkc) là 24,79 L/mol. Lượng CO2 thoát ra được hấp thụ xử lí hoàn toàn, không thải vào môi trường, lượng Cl- sau đó cũng được xử lí đến hàm lượng phù hợp. Dùng 68 m³ khí Cl₂ (ở đkc) để xử lý 400 m³ nước thải. Sau xử lý, còn 0,07 mg/L CN⁻ đạt chuẩn xả thải. Giá trị của x là bao nhiêu? (kết quả cuối cùng làm tròn đến hàng phần mười)
(Xem giải) Câu 27. Một dung dịch NaOH tính toán theo lí thuyết sau khi pha chế có nồng độ là 0,25 M. Để kiểm tra bằng thực nghiệm, người ta chuẩn độ dung dịch NaOH này bằng dung dịch chuẩn HCl 0,20 M với chất chỉ thị phenolphthalein, các bước tiến hành như sau:
• Bước 1: Dùng pipette lấy 10 mL dung dịch NaOH vào bình tam giác (erlen) đã rửa sạch rồi thêm tiếp 2 – 3 giọt chất chỉ thị phenolphthalein.
• Bước 2: Tráng sạch burette (loại 25 mL) bằng nước cất, sau đó tráng lại bằng dung dịch HCl 0,20 M ở trên. Sau khi xả nước tráng, rót dung dịch HCl 0,20 M vào burette rồi điều chỉnh về mức 0.
• Bước 3: Mở từ từ khóa burette, nhỏ từng giọt dung dịch chuẩn vào erlen (lắc đều trong quá trình chuẩn độ) cho đến khi dung dịch vừa mất màu hồng thì dừng chuẩn độ.
• Bước 4: Ghi lại thể tích dung dịch chuẩn đã dùng.
Trong phép chuẩn độ này, thể tích dung dịch HCl đã dùng sau 3 lần thực hiện lần lượt là 12,25 mL; 12,26 mL và 12,26 mL. Nồng độ mol/L của dung dịch NaOH đo bằng thực nghiệm ở trên thấp hơn so với tính toán theo lí thuyết là bao nhiêu %? (kết quả cuối cùng làm tròn đến hàng phần trăm).
(Xem giải) Câu 28. Trong công nghiệp sản xuất đường mía, nước mía sau khi làm sạch được cô đặc để thu dung dịch saccharose bão hòa ở nhiệt độ cao, sau đó làm lạnh để thu tinh thể đường. Biết độ tan của saccharose trong nước ở 20°C là 211,5 gam/100 gam nước và ở 90°C là 420 gam/100 gam nước. Khi làm lạnh 117 tấn dung dịch bão hòa saccharose ở 90°C xuống 20°C, khối lượng saccharose (tấn) kết tinh là bao nhiêu? Giả sử hiệu suất kết tinh là 100% (Kết quả được làm tròn đến hàng phần mười).

Bình luận