[2026] Thi thử TN sở GDĐT Thanh Hóa (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 074
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2B | 3D | 4B | 5C | 6C | 7C | 8C | 9B |
| 10B | 11C | 12C | 13D | 14C | 15D | 16C | 17C | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | Đ | S | 2 | 310 | 4 |
| (b) | S | Đ | S | S | 26 | 27 | 28 |
| (c) | S | S | S | S | 0,26 | 57 | 234 |
| (d) | Đ | Đ | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho peptide X: Lys-Glu-Gly. Trong các phát biểu sau về peptide X:
(a) Công thức phân tử của peptide X là C13H24O6N4.
(b) Mỗi mol peptide X phản ứng tối đa với 3 mol HCl hoặc với 4 mol NaOH.
(c) Peptide X có khả năng hòa tan Cu(OH)2 trong môi trường kiềm tạo thành dung dịch màu tím.
(d) Liên kết giữa các đơn vị amino acid trong peptide X được gọi là liên kết peptide.
Số phát biểu đúng là
A. 1. B. 2. C. 4. D. 3.
(Xem giải) Câu 2. Khi đốt cháy các nhiên liệu hóa thạch (như than đá, dầu mỏ, khí đốt…) thường sinh ra khí X. Khí X không màu, mùi hắc, độc, nặng hơn không khí, là tác nhân chính gây ra mưa acid. Khí X là
A. CO. B. SO2. C. N2. D. NH3.
(Xem giải) Câu 3. Formic acid (methanoic acid) có trong nọc của con kiến. Công thức hóa học của formic acid là
A. CH3COOH. B. CH3OH. C. HCHO. D. HCOOH.
(Xem giải) Câu 4. Phương trình hóa học của phản ứng khi cho ethylene tác dụng với dung dịch Br2 là CH2=CH2 + Br2 → CH2Br-CH2Br. Cơ chế của phản ứng trên xảy ra như sau:
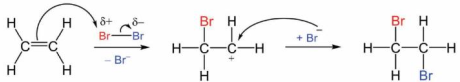
Phát biểu nào sau đây sai?
A. Trong giai đoạn đầu của phản ứng có sự phân cắt liên kết π.
B. Trong giai đoạn hai của phản ứng có sự hình thành liên kết π.
C. Trong giai đoạn đầu của phản ứng có sự hình thành liên kết σ.
D. Phản ứng trên thuộc loại phản ứng cộng.
(Xem giải) Câu 5. Kim loại nào sau đây có độ cứng lớn nhất?
A. Al. B. Mg. C. Cr. D. Na.
(Xem giải) Câu 6. Để bảo vệ vỏ tàu biển làm bằng thép, người ta thường gắn vào vỏ tàu (phần chìm dưới nước) tấm kim loại nào sau đây?
A. Ag. B. Na. C. Zn. D. Cu.
(Xem giải) Câu 7. Kim loại kẽm (Zinc) được sản xuất trong công nghiệp từ quặng sphalerite (có thành phần chính là ZnS) theo sơ đồ:
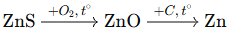
Phương pháp tách kim loại kẽm thuộc phương pháp nào sau đây?
A. Điện phân. B. Thủy luyện. C. Nhiệt luyện. D. Kết tinh.
(Xem giải) Câu 8. Chất nào sau đây thuộc loại hợp chất hữu cơ no, đơn chức, mạch hở?
A. Benzene. B. Glycerol. C. Ethyl alcohol. D. Acrylic acid.
(Xem giải) Câu 9. Từ phổ khối lượng, xác định được phân tử khối của ester X là 88. Công thức phù hợp với X là
A. CH3CH2OH. B. CH3COOC2H5. C. C3H7COOH. D. HCOOC2H5.
(Xem giải) Câu 10. Nước muối sinh lí là dung dịch của chất X với nồng độ 0,9% được dùng trong việc ngăn ngừa nguy cơ mất muối do toát quá nhiều mồ hôi, sau phẫu thuật, do tiêu chảy hay các nguyên nhân khác. Chất X là muối nào sau đây?
A. NaNO3. B. NaCl. C. Na2SO4. D. NaClO.
(Xem giải) Câu 11. Phát biểu nào sau đây đúng?
A. Cellulose thuộc loại disaccharide.
B. Glucose bị thủy phân trong môi trường acid.
C. Dung dịch saccharose hòa tan được Cu(OH)2.
D. Tinh bột là chất lỏng ở nhiệt độ thường.
(Xem giải) Câu 12. Yếu tố nào sau đây luôn không làm chuyển dịch cân bằng của hệ phản ứng?
A. Áp suất. B. Nồng độ. C. Chất xúc tác. D. Nhiệt độ.
(Xem giải) Câu 13. Chlorine (Cl) là chất oxi hóa mạnh, được sử dụng làm chất tẩy trắng và khử trùng nước. Ở trạng thái cơ bản, cấu hình electron của nguyên tử Cl (số hiệu nguyên tử bằng 17) là
A. 1s2 2s2 2p6 3s2 3p4. B. 1s2 2s2 2p6 3s2 3p5 3s3.
C. 1s2 2s2 2p6 3s1 3p6. D. 1s2 2s2 2p6 3s2 3p5.
(Xem giải) Câu 14. Khi nói về liên kết kim loại: “Liên kết kim loại là liên kết hình thành do lực hút tĩnh điện giữa các electron hóa trị …(1)… với các ion …(2)… kim loại ở các nút mạng. Các từ cần điền vào vị trí (1), (2) để được phát biểu đúng là:
A. ngoài cùng, âm. B. ngoài cùng, dương. C. tự do, dương. D. tự do, lưỡng cực.
(Xem giải) Câu 15. Pin Cu-Ag gồm hai điện cực Cu2+/Cu và Ag+/Ag. Cho thế điện cực chuẩn của hai cặp oxi hóa – khử Cu2+/Cu và Ag+/Ag lần lượt là +0,34V và +0,799V. Nhận định nào sau đây đúng?
A. Thanh Ag là cực âm (anode).
B. Sức điện động chuẩn của pin Cu-Ag là -0,459V.
C. Tại điện cực Cu xảy ra sự khử Cu2+.
D. Ag+ dễ bị khử hơn Cu2+.
(Xem giải) Câu 16. Chất nào sau đây được dùng làm thành phần chính của xà phòng?
A. CH3[CH2]11OSO3Na. B. CH3[CH2]16COOH.
C. CH3[CH2]14COONa. D. (CH3COO)3C3H5
Sử dụng thông tin cho dưới đây để trả lời các câu 17 – 18:
Xăng là một trong những thành phẩm của quá trình chưng cất dầu mỏ, được sử dụng như một loại nhiên liệu, chất đốt cho các phương tiện có động cơ đốt trong hoặc một số vật dụng như bật lửa, lò sưởi… Chỉ số octane (octane number) là chỉ số đo lường khả năng chống kích nổ của một nhiên liệu khi nhiên liệu này bốc cháy với không khí bên trong xilanh của động cơ đốt trong. Quy ước chỉ số octane của 2,2,4-trimethylpentane là 100 và của heptane là 0. Chỉ số octane càng cao, hiệu suất cháy của xăng càng cao.
RON là viết tắt của “research octane number”, tức chỉ số octane nghiên cứu. Ví dụ RON 92 thì có chỉ số octane bằng 92, tức là 100 lít xăng RON 92 có thể quy đổi tương ứng với 92 lít xăng có chỉ số octane 100, còn lại là xăng có chỉ số octane bằng 0. Xăng E5 có chứa 5% ethanol và 95% xăng RON 92 theo thể tích, cho biết ethanol có chỉ số octane là 109.
(Xem giải) Câu 17. Cho các phát biểu sau:
(a) Công thức cấu tạo của ethanol là CH3CH2OH.
(b) Chỉ số octane của xăng E5 là 92,85.
(c) Công thức phân tử của 2,2,4-trimethylpentane là C5H12.
(d) Xăng E5 có hiệu suất cháy kém hơn xăng RON 95.
(e) Ứng dụng của phản ứng reforming alkane là để sản xuất xăng có chỉ số octane cao.
Số phát biểu đúng là
A. 3. B. 2. C. 4. D. 5.
(Xem giải) Câu 18. Khi xảy ra cháy xăng dầu, tuyệt đối không được dùng nước để dập lửa vì có thể khiến lửa lan rộng hơn. Thay vào đó, cần sử dụng bọt chữa cháy hoặc cát khô để dập tắt đám cháy. Cho các phát biểu sau:
(a) Xăng dầu nhẹ hơn nước nên sẽ nổi lên trên và tiếp tục cháy nếu dùng nước để dập lửa.
(b) Bọt chữa cháy có tác dụng cách ly nhiên liệu với không khí, giúp dập lửa hiệu quả.
(c) Lớp bọt cũng giúp ngăn chặn hơi xăng dầu thoát ra ngoài, giảm nguy cơ bắt lửa trở lại.
(d) Có thể sử dụng carbon dioxide thay cho bọt chữa cháy để dập tắt các đám cháy do xăng dầu.
Số phát biểu đúng là
A. 2. B. 1. C. 4. D. 3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Nhựa ABS được làm từ polymer có tên đầy đủ là Poly(Acrylonitrile Butadiene Styrene), nhựa ABS có đặc tính cứng, rắn nhưng không giòn, cách điện, không thấm nước, bền với nhiệt độ và hóa chất. Nhựa này được sử dụng khá rộng rãi làm vật liệu xây dựng, đồ chơi trẻ em, đồ gia dụng, mũ bảo hiểm. Công thức cấu tạo của ABS được mô tả như dưới đây:
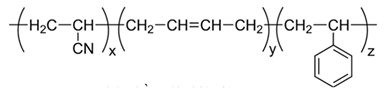
a) Nhựa ABS là vật liệu polymer kém bền với nhiệt độ.
b) Trong Poly(Acrylonitrile Butadiene Styrene) có tỉ lệ khối lượng Acrylonitrile (15,41%), Butadiene (39,24%) còn lại là Styrene thì tỉ lệ giữa các mắt xích x : y : z là 1 : 1,5 : 3.
c) Nhựa ABS là chất dẻo dễ phân hủy sinh học, có thể xử lý bằng cách chôn lấp.
d) Các monomer tạo nên Poly(Acrylonitrile Butadiene Styrene) là: CH2=CH-CN, CH2=CH-CH=CH2, CH2=CH-C6H5.
(Xem giải) Câu 20. Hình vẽ sau đây mô tả quá trình điều chế và thử tính chất hóa học của ethylene:
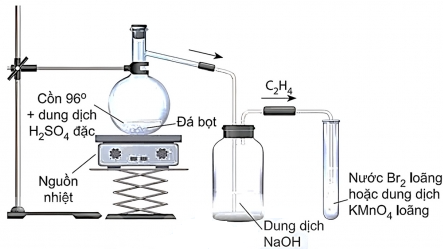
a) Ethylene sinh ra từ phản ứng tách nước của ethanol.
b) Khí ethylene sinh ra làm nhạt màu dung dịch nước bromine.
c) Bình đựng dung dịch NaOH có tác dụng loại bỏ hơi H2SO4 bị lẫn trong ethylene sinh ra.
d) Dung dịch KMnO4 tác dụng với ethylene tạo thành ethylene glycol.
(Xem giải) Câu 21. Trong công nghiệp, sodium hydrogencarbonate (baking soda NaHCO3) và sodium carbonate (soda – Na2CO3) được sản xuất bằng phương pháp Solvay từ nguyên liệu chính là đá vôi, muối ăn, ammonia và nước theo sơ đồ sau:
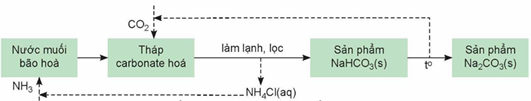
a) Ammonia và carbon dioxide được sử dụng quay vòng trong quá trình sản xuất.
b) Từ 17,55 kg NaCl điều chế NaHCO3 theo phương pháp Solvay thì thu được 25,20 kg NaHCO3 (hiệu suất toàn bộ quá trình là 90%).
c) Phản ứng chuyển hóa NaHCO3 thành Na2CO3 là phản ứng tỏa nhiệt.
d) Trong thực tiễn, NaHCO3 được sử dụng làm bột nở trong chế biến thực phẩm.
(Xem giải) Câu 22. Một quả cầu làm bằng sắt (iron) có bán kính 5cm cần được mạ đồng (copper) để tăng khả năng chống ăn mòn và nâng cao tính thẩm mỹ. Lớp mạ bằng đồng có độ dày là 2.10^-4 cm. Người ta dùng phương pháp điện phân dung dịch CuSO4 dư với cathode là quả cầu sắt và anode là thanh đồng tinh khiết, cường độ dòng điện I = 5A, hiệu suất của quá trình mạ là 80%. Biết khối lượng riêng của Cu là 8,96 g/cm³, công thức tính thể tích hình cầu V = 4πr³/3, π = 3,14 và F = 96500 C/mol.
a) Tại anode, xảy ra quá trình: Cu2+ + 2e → Cu
b) Thể tích quả cầu sau khi mạ xong bằng 524,33 cm³.
c) Thời gian cần thiết để mạ xong quả cầu trên là 7,77 phút.
d) Cathode là quả cầu sắt và anode là thanh đồng tinh khiết.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho dãy các hợp chất của kim loại nhóm IA: Na2CO3, NaCl, NaHCO3, KHCO3, KCl. Có bao nhiêu chất trong dãy trên thỏa mãn cả hai tính chất sau:
– Đốt trên ngọn lửa đèn cồn thấy ngọn lửa có màu vàng.
– Tác dụng với dung dịch HCl tạo ra khí Y làm đục nước vôi trong.
(Xem giải) Câu 24. Các hợp chất của copper(II) được sử dụng rộng rãi trong nông nghiệp như một loại thuốc trừ sâu, diệt nấm. Một ví dụ điển hình là copper(II) sulfate pentahydrate (CuSO4.5H2O), hay còn gọi là “đá xanh”. Chất rắn copper(II) sulfate pentahydrate có thể được điều chế từ copper(II) oxide theo sơ đồ:
CuO(s) → CuSO4(aq) → CuSO4.5H2O(s)
Hòa tan hoàn toàn 2,0 mol CuO bằng một lượng vừa đủ dung dịch H2SO4 20% đun nóng thu được dung dịch X. Làm lạnh X đến 10°C thì có m gam tinh thể CuSO4.5H2O tách ra. Biết ở 10°C, cứ 100 gam H2O hòa tan tối đa được 17,2 gam CuSO4. Giá trị của m là bao nhiêu? (làm tròn đến hàng đơn vị).
(Xem giải) Câu 25. Có bao nhiêu công thức cấu tạo là amine ứng với công thức phân tử là C3H9N?
(Xem giải) Câu 26. Trong quy trình Ostwald để sản xuất nitric acid, khí ammonia (NH3) được oxy hóa để tạo ra khí NO theo phản ứng (1):
(1) 4NH3 + 5O2 → 4NO + 6H2O
Để khơi mào cho phản ứng này, nhà máy sử dụng nguồn nhiệt từ quá trình oxy hóa không hoàn toàn khí methane (CH4) để gia nhiệt hỗn hợp từ 30°C lên 800°C theo công thức Q = m.C(t2 – t1). Biết nhiệt dung riêng C = 1,49 J/g.K. Phản ứng oxy hóa methane:
(2) 2CH4 + 3O2 → 2CO + 4H2O
Hiệu suất (1) là 92%, (2) là 85%. Biết nhiệt tạo thành (kJ/mol) của CH4 là -74,8; CO là -110,5 và H2O là -241,8. Để thu được 3 tấn khí NO cần x tấn khí methane. Giá trị của x là bao nhiêu? (làm tròn đến hàng phần trăm).
(Xem giải) Câu 27. Carboxylic acid X đơn chức có tác dụng kháng khuẩn nhẹ, được sử dụng để điều trị một số loại bệnh. Kết quả phân tích nguyên tố (theo % khối lượng) cho thấy X chứa 53,33% oxygen về khối lượng. Ethanol phản ứng với X ( đặc) tạo thành ester Y theo phương trình sau: C2H5OH(l) + X(l) (H+, t°) ⇋ Y(l) + H2O(l)
Ở nhiệt độ t°C, giá trị Kc của phản ứng trên là 3,4. Nếu cho 46,0 g ethanol phản ứng với 60,0 g X ở t°C thì khối lượng Y thu được trong hỗn hợp ở trạng thái cân bằng là bao nhiêu gam (làm tròn kết quả đến hàng đơn vị)? (Coi tổng thể tích của hệ phản ứng không đổi).
(Xem giải) Câu 28. Cho các dung dịch cùng nồng độ 0,1 mol/L: (1) sodium chloride; (2) glutamic acid; (3) sodium hydroxide; (4) lysine. Liệt kê các dung dịch làm đổi màu quỳ tím theo số thứ tự tăng dần?


Bình luận