[2023 – 2024] Thi học sinh giỏi lớp 12 – Bình Phước
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Thời gian làm bài: 180 phút
⇒ Đề thi, đáp án và giải chi tiết:
Câu 1. (2,0 điểm)
(Xem giải) 1.1. Nguyên tố M tồn tại trong tự nhiên với 2 loại đồng vị X và Y trong đó Y chiếm 27,3% về số nguyên tử. Nguyên tử X có tổng số hạt proton, nơtron, electron là 92, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 24. Số hạt nơtron trong nguyên tử Y nhiều hơn trong nguyên tử X là 2.
a. Tính nguyên tử khối trung bình của nguyên tố M.
b. Viết cấu hình electron và cho biết vị trí của M trong bảng tuần hoàn các nguyên tố hóa học.
(Xem giải) 1.2. Hoàn thành và cân bằng các phản ứng hóa học sau theo phương pháp thăng bằng electron:
a. NO2 + NaOH → NaNO2 + … + H2O
b. Mg + HNO3 → Mg(NO3)2 + NO + N2 + H2O; Trong đó tỉ lệ số mol khí NO : N2 = 2 : 3.
Câu 2. (2,0 điểm)
(Xem giải) 2.1. X, Y, Z, T lần lượt là một trong bốn dung dịch không màu đựng trong các lọ riêng biệt (không theo thứ tự) gồm: Mg(HCO3)2, BaCl2, Na2CO3, NaHSO4. Thực hiện thí nghiệm với bốn dung dịch trên, kết quả được ghi trong bảng dưới đây:
| Mẫu thử | Thí nghiệm | Hiện tượng |
| X hoặc Z | Tác dụng với dung dịch Y | Có kết tủa xuất hiện |
| X hoặc T | Tác dụng với dung dịch Z | Có khí CO2 thoát ra |
| X | Tác dụng với dung dịch T | Có kết tủa xuất hiện |
Xác định các chất X, Y, Z, T (không cần giải thích).
(Xem giải) 2.2. Hòa tan hoàn toàn 2 muối X và Y vào nước thu được dung dịch A chứa các ion sau: Fe3+, NH4+, SO42-, NO3-. Cho 100 ml dung dịch A tác dụng với dung dịch Ba(OH)2 dư sau phản ứng kết thúc thu được 11,46 gam kết tủa và thấy thoát ra 1,792 lít khí (đo ở đktc). Mặt khác, nếu cho 50 ml dung dịch A tác dụng với lượng dư dung dịch BaCl2 thu được 4,66 gam kết tủa. Cho biết các phản ứng xảy ra hoàn toàn. Xác định công thức 2 muối X, Y.
(Xem giải) Câu 3. (2,0 điểm)
Cho phương trình hoá học của phản ứng: N2 (k) + 3H2 (k) ⇋ 2NH3 (k), ΔH° = -92kJ
a. Khi tăng nhiệt độ, cân bằng của phản ứng trên dịch chuyển theo chiều nào?
b. Khi tăng nồng độ của khí hiđro lên 2 lần thì tốc độ phản ứng thuận thay đổi như thế nào?
c. Hỗn hợp khí X gồm N2 và H2 có tỉ khối hơi so với He bằng 1,8. Đun nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối hơi so với He bằng 2. Tính hiệu suất phản ứng tổng hợp NH3.
Câu 4. (2,0 điểm)
(Xem giải) 4.1. Cho sơ đồ chuỗi phản ứng sau:
X + 2KHSO4 → A↓ + B + 2C↑ + 2D
BaCl2 + KHSO4 → A↓ + E + HCl
X + 2KOH → G↓ + H + 2D
H + 2HCl → 2E + C↑ + D
Biết rằng mỗi chữ cái là một chất vô cơ khác nhau và khí C là tác nhân gây hiệu ứng nhà kính.
Xác định các chất X, A, B, C, D, E, G, H. Viết phương trình hóa học các phản ứng theo sơ đồ trên.
(Xem giải) 4.2. Một loại phân NPK có độ dinh dưỡng được ghi trên bao bì 16-16-8. Để cung cấp 8,6 kg nitơ; 1,75 kg photpho và 4,15 kg kali cho một thửa ruộng, người ta sử dụng đồng thời x kg phân NPK (ở trên), y kg đạm urê (độ dinh dưỡng là 45%) và z kg phân kali (độ dinh dưỡng là 75%). Tính tổng giá trị (x + y + z)
Câu 5 (2,0 điểm):
(Xem giải) 5.1. Dung dịch Ringer dùng để rửa vết bỏng và các vết thương trầy xước…được pha chế bằng cách cho 4,300 gam NaCl; 0,150 gam KCl và 0,165 gam CaCl2 vào nước sôi để nguội, pha loãng đến 500ml để sử dụng. Tính nồng độ mol/lít gần đúng của ion Cl- trong dung dịch Ringer.
(Xem giải) 5.2. Điện phân dung dịch X chứa các ion Na+, H+, Cu2+, SO42-, Cl- (với điện cực trơ, có màng ngăn xốp, hiệu suất điện phân là 100%). Lượng khí sinh ra từ quá trình điện phân và lượng Al2O3 bị hòa tan tối đa trong dung dịch sau điện phân được cho ở bảng dưới đây:
| Thời gian điện phân (giây) | t | 2t | 3t |
| Lượng khí sinh ra từ bình điện phân (mol) | 0,31 | x | 1,13 |
| Lượng Al2O3 bị hòa tan tối đa (mol) | 0,075 | y |
Tính giá trị của x và y.
Câu 6. (2,0 điểm)
(Xem giải) 6.1. Viết các công thức cấu tạo của hợp chất hữu cơ thơm, có công thức phân tử C8H10O thỏa mãn tính chất: Tác dụng được với Na nhưng không tác dụng được với dung dịch NaOH.
(Xem giải) 6.2. Cho hai hợp chất hữu cơ X, Y đều đơn chức, mạch hở, chứa ba nguyên tố (C, H, O) và đều có tỉ lệ % khối lượng oxi trong phân tử là 53,33%. Biết MX > MY và X, Y đều tan trong nước. Xác định công thức cấu tạo của X, Y biết nhiệt độ sôi của X và Y lần lượt là 118°C và -19,3°C.
Câu 7. (2,0 điểm)
(Xem giải) 7.1. Cho các hợp chất hữu cơ X, Y, Z có cùng công thức phân tử C4H8O2 đều mạch hở và không phân nhánh. Biết:
– X tác dụng với dung dịch NaHCO3 thấy có khí thoát ra.
– Y tác dụng với dung dịch NaOH thu được hai hợp chất hữu cơ có số nguyên tử cacbon trong phân tử khác nhau.
– Z hòa tan Cu(OH)2 ở điều kiện thường tạo dung dịch màu xanh lam.
Xác định công thức cấu tạo có thể có của X, Y, Z.
(Xem giải) 7.2. Cho X và Y là 2 axit cacboxylic kế tiếp nhau, thuộc cùng dãy đồng đẳng của axit cacboxylic không no (phân tử có 1 nối đôi C=C), đơn chức, mạch hở (MX < MY); Z là ancol no có cùng số nguyên tử cacbon với X; T là este hai chức tạo bởi X, Y và Z (T chỉ chứa chức este, không chứa nhóm chức khác). Đốt cháy hoàn toàn 5,58 gam hỗn hợp E gồm X, Y, Z, T cần 6,608 lít khí O2 (đktc) thu được CO2 và 4,68 gam H2O. Mặt khác 5,58 gam hỗn hợp E trên tác dụng tối đa với 0,02 mol Br2 trong dung dịch. Xác định công thức phân tử của T.
Câu 8. (2,0 điểm)
(Xem giải) 8.1. Viết phương trình phản ứng xảy ra trong các trường hợp sau:
a. Cho CH3COOHN(CH3)3 và Glu-Ala lần lượt tác dụng với dung dịch NaOH dư.
b. Cho C6H5-C≡CH (hợp chất thơm), HCHO lần lượt tham gia phản ứng với dung dịch AgNO3 trong NH3 dư.
(Xem giải) 8.2. Cho các chất lỏng: anilin, lòng trắng trứng, axit axetic và dung dịch glucozơ được kí hiệu ngẫu nhiên là X, Y, Z, T. Kết quả thí nghiệm của các chất với thuốc thử được ghi ở bảng sau:
| Mẫu thử | Thuốc thử | Hiện tượng |
| X | Tác dụng với Cu(OH)2 | Có màu tím |
| Y | CaCO3 | Sủi bọt khí không màu |
| Z | Dung dịch AgNO3 trong NH3, đun nóng nhẹ | Kết tủa Ag trắng sáng |
| T | Dung dịch brom | Kết tủa trắng |
Xác định X, Y, Z, T và viết phương trình hóa học của các phản ứng xảy ra (nếu có).
Câu 9. (2,0 điểm)
(Xem giải) 9.1. Este X mạch hở, có công thức phân tử là C10H12O6. Từ X thực hiện chuỗi phản ứng sau (trong điều kiện thích hợp, theo đúng tỉ lệ mol):
(1) X + 3NaOH → X1 + X2 + X3 + X4
(2) X1 + NaOH (CaO, t°) → CH4 + Na2CO3
(3) X2 + H2SO4 → C2(COOH)2 + Na2SO4
Biết X3, X4 có cùng số nguyên tử cacbon trong phân tử. Tìm công thức cấu tạo của X1, X2 và X.
(Xem giải) 9.2. Cho hỗn hợp X gồm ba este A, B, C. Xà phòng hoá hoàn toàn 7,74 gam X trong dung dịch NaOH vừa đủ thu được 2,82 gam hỗn hợp Y gồm hai ancol mạch hở (tỉ lệ mol 1:3) và dung dịch chứa 9,76 gam hỗn hợp Z gồm ba muối. Đốt cháy hoàn toàn Z thu được Na2CO3, H2O và 0,165 mol CO2. Mặt khác, đốt cháy hoàn toàn 7,74 gam X thu được 14,08 gam CO2 và 3,42 gam H2O. Biết A, B, C chỉ chứa chức este, MA < MB < MC < 200 đvC. Tính thành phần phần trăm về số mol của C trong hỗn hợp X.
(Xem giải) Câu 10. (2,0 điểm)
Tiến hành thí nghiệm điều chế và thử tính chất của hiđrocacbon X theo sơ đồ và các bước sau đây:
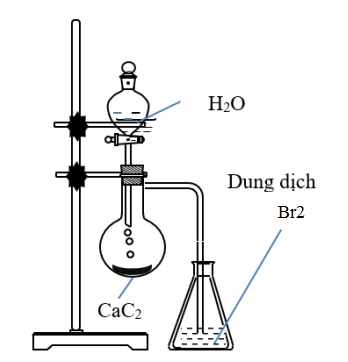
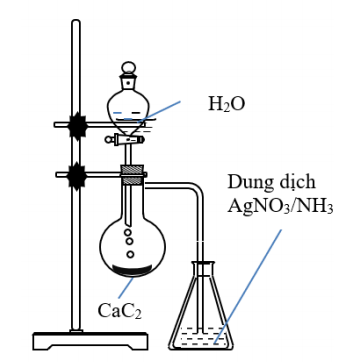
Bước 1: Mở khoá phễu cho H2O chảy từ từ xuống bình cầu đựng CaC2.
Bước 2: Dẫn X vào bình đựng dung dịch A .
Nêu hiện tượng và viết phương trình phản ứng xảy ra ở bước 1 và bước 2 trong hai trường hợp sau:
– Nếu dung dịch A là dung dịch brom dư.
– Nếu dung dịch A là dung dịch AgNO3/NH3.


Bình luận