[2024 – 2025] Thi học sinh giỏi lớp 12 cụm Bắc Ninh
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề 034-H12A năm 2024-2025
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1A | 2A | 3C | 4B | 5A | 6A | 7C | 8B | 9A | 10A |
| 11B | 12D | 13A | 14A | 15D | 16A | 17A | 18D | 19B | 20C |
| 21D | 22B | 23D | 24A | 25B | 26C | 27D | 28D | 29A | 30A |
| 31 | 32 | 33 | 34 | 35 | 36 | 37 | 38 | |
| (a) | Đ | Đ | Đ | S | S | Đ | Đ | S |
| (b) | Đ | Đ | Đ | Đ | S | Đ | Đ | Đ |
| (c) | Đ | S | S | Đ | S | S | S | Đ |
| (d) | Đ | S | Đ | Đ | S | S | Đ | S |
| 39 | 40 | 41 | 42 | 43 | 44 |
| 60 | 8 | 91,8 | 4123 | 362 | 24 |
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 30. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho các phản ứng thuận nghịch đang ở trạng thái cân bằng:
(1) H2 (g) + I2 (g) ⇋ 2HI (g).
(2) Fe2O3 (s) + 3CO (g) ⇋ 2Fe (s) + 3CO2 (g).
(3) 2NO2 (g) ⇋ N2O4 (g).
Yếu tố áp suất ảnh hưởng đến chuyển dịch cân bằng của phản ứng thuận nghịch nào?
A. (3). B. (1). C. (2). D. (2); (3).
(Xem giải) Câu 2. Phát biểu nào sau đây là đúng
A. Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại của các nguyên tố giảm dần.
B. Trong một chu kì, theo chiều giảm dần của điện tích hạt nhân, tính phi kim của các nguyên tố tăng dần.
C. Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, độ âm điện của các nguyên tố tăng dần.
D. Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử giảm dần.
(Xem giải) Câu 3. Đo pH của một cốc nước chanh thấy giá trị pH bằng 2,4. Nhận định nào sau đây không đúng?
A. Nước chanh có môi trường acid.
B. Nồng độ ion [H+] của nước chanh bằng 10^-2,4 mol/L.
C. Nồng độ ion [H+] của nước chanh bằng 2,4 mol/L.
D. Nồng độ ion [OH-] của nước chanh nhỏ hơn 10^-7 mol/L.
(Xem giải) Câu 4. Hạt cau được sử dụng để điều trị tình trạng sâu răng nhờ tính diệt khuẩn và sát trùng, giúp ngăn chặn sự phát triển của vi khuẩn có hại trong khoang miệng. Cách làm, lấy khoảng 20 đến 25 quả cau già, bổ tách lấy hạt và cho vào bình ngâm với 1 lít rượu trắng. Sau khoảng 1 tháng, khi rượu cau bắt đầu chuyển sang màu cánh gián là bạn có thể dùng được. Cách làm rượu hạt cau trên đã áp dụng phương pháp tách biệt nào sau đây?
A. Phương pháp chưng cất. B. Phương pháp chiết.
C. Phương pháp kết tinh. D. Phương pháp sắc kí cột.
(Xem giải) Câu 5. Tên gọi của ester CH3COOCH(CH3)2 là
A. Isopropyl acetate. B. Ethyl acetate.
C. Propyl acetate. D. Propyl formate.
(Xem giải) Câu 6. Vị trí liên kết đôi đầu tiên tính từ nhóm CH3 trong acid béo là n thì acid béo đó gọi là omega-n. Trong các acid béo sau:
CH3(CH2)4CH=CH(CH2)6COOH
CH3CH2CH=CHCH2CH=CHCH2CH=CHCH2CH=CHCH2CH=CH(CH2)3COOH
CH3(CH2)4CH=CHCH2CH=CHCH2CH=CH(CH2)6COOH
CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH
CH3(CH2)7CH=CH(CH2)7COOH
Có bao nhiêu omega-6?
A. 3. B. 2. C. 4. D. 1.
(Xem giải) Câu 7. Phát biểu nào sau đây không đúng:
A. Glucose và fructose là đồng phân của nhau.
B. Saccharose và maltose là đồng phân của nhau.
C. Tinh bột và cellulose là đồng phân của nhau.
D. Trong disaccharide và polysaccharide đều có liên kết glycoside.
(Xem giải) Câu 8. Công thức cấu tạo dạng mạch vòng β-glucose là
A. 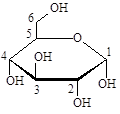 B.
B. 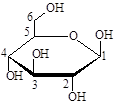
C. 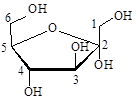 D.
D. 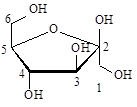
(Xem giải) Câu 9. C4H11N có bao nhiêu đồng phân amine mà khi phản ứng với HNO2 ở điều kiện thường giải phóng khí nitrogen?
A. 4. B. 5. C. 3. D. 2.
(Xem giải) Câu 10. Cho cấu tạo của insulin như sau (gồm hai đoạn mạch A và B, liên kết với nhau qua cầu nối –S-S-).

Tổng số đơn vị aminoacid của Gly; Ala; Val; Glu và Lys trong đoạn mạch B của insulin là
A. 10. B. 8. C. 9. D. 12.
(Xem giải) Câu 11. Phân tử polymer nào sau đây chứa ba loại nguyên tố?
A. Polystyrene. B. Poly(vinyl chloride).
C. Polybuta-1,3-diene. D. Polypropylene.
(Xem giải) Câu 12. Cho E°Zn2+/Zn = -0,762 (V) và E°Cu2+/Cu = +0,34 (V). Nhận xét nào sau đây sai:
A. Tính khử của Zn mạnh hơn của Cu.
B. Tính oxi hóa của Zn2+ yếu hơn của Cu2+.
C. Sức điện động chuẩn của pin Zn-Cu là 1,102V.
D. Zn oxi hóa được Cu2+.
(Xem giải) Câu 13. Khi điện phân dung dịch CuSO4 (với điện cực trơ) thì ở anode xảy ra quá trình
A. oxi hoá H2O. B. oxi hoá ion Cu2+ C. khử ion Cu2+ D. khử H2O.
(Xem giải) Câu 14. Khí H2 được điều chế trong phòng thí nghiệm bằng cách cho Zn tác dụng với dung dịch HCl loãng. Khí H2 sẽ thoát ra nhanh hơn nếu thêm vào hệ phản ứng vài giọt dung dịch nào sau đây?
A. CuSO4 B. MgCl2 C. Al(NO3)3 D. NaCl.
(Xem giải) Câu 15. Thí nghiệm nào sau đây không xảy ra phản ứng ở điều kiện thường?
A. Cho mảnh kim loại đồng vào dung dịch nitric acid đặc.
B. Cho lá nhôm vào dung dịch potassium hydroxide (KOH) loãng.
C. Cho bột sắt vào dung dịch silver nitrate (AgNO3) dư.
D. Cho bột đồng vào dung dịch iron(II) sulfate.
(Xem giải) Câu 16. Trong phân tử chất nào sau đây chứa đồng thời các loại liên kết: liên kết ion, liên kết cộng hóa trị và liên kết cho nhận?
A. NH4Cl. B. NaOH. C. COCl2. D. K2O.
(Xem giải) Câu 17. Trong công nghiệp, ammonia được tổng hợp theo quá trình Haber: nitrogen và hydrogen phản ứng với nhau ở nhiệt độ trên 400°C, áp suất 200 bar với xúc tác bột sắt.
N2 (g) + 3H2 (g) ⇋ 2NH3 (g) ![]() = -91,8 kJ
= -91,8 kJ
Nếu phản ứng đang ở trạng thái cân bằng, yếu tố nào sau đây làm cân bằng dịch chuyển theo chiều nghịch?
A. Tăng nhiệt độ. B. Tăng áp suất.
C. Thêm xúc tác bột sắt. D. Không có yếu tố nào trong ba yếu tố trên.
(Xem giải) Câu 18. Trong quá trình giặt khô, tetrachloroethylene là dung môi được sử dụng phổ biến, và được kí hiệu là PCE. PCE là một dung mỗi hữu cơ dễ bay hơi, ổn định và không cháy. Nhận xét nào sau đây về PCE là sai
A. PCE thuộc loại dẫn xuất halogen của hydrocarbon.
B. Trong phân tử PCE, còn một liên kết π.
C. Các nguyên tử trong phân tử PCE đều nằm trên một mặt phẳng.
D. PCE tan tốt trong nước.
(Xem giải) Câu 19. Tinh bột là loại lương thực quan trọng và là nguyên liệu chủ yếu để sản xuất bánh, kẹo, rượu, bia … Cellulose được sử dụng làm vật liệu xây dựng, sản xuất giấy, sợi tự nhiên và sợi nhân tạo. Phát biểu nào sau đây về tính chất của tinh bột và cellulose là không đúng?
A. Dung dịch hồ tinh bột tạo với iodine hợp chất màu xanh tím. Cellulose không có tính chất này.
B. Tinh bột và cellulose có khả năng tham gia phản ứng tráng bạc.
C. Tinh bột và cellulose có cùng công thức phân tử dạng (C6H10O5)n, nhưng không phải đồng phân của nhau.
D. Thủy phân hoàn toàn tinh bột, cellulose đều thu được sản phẩm glucose.
(Xem giải) Câu 20. Kết quả phân tích nguyên tố trong phân tử chất X như sau: %C = 46,60%; %H = 8,74%; %N = 13,59% (về khối lượng); còn lại là oxygen. Từ phổ khối lượng (MS), xác định được phân tử khối của X bằng 103. Thủy phân X thấy thu được một α-amino acid Y và chất Z có công thức phân tử CH4O. Phát biểu nào sau đây là không đúng?
A. Công thức phân tử của X là C4H9O2N.
B. Có thể điều chế chất X bằng phản ứng của α-amino acid với alcohol tương ứng trong điều kiện thích hợp.
C. Công thức cấu tạo của chất X là H2NCH(CH2CH3)COOH.
D. Công thức cấu tạo của chất X là H2NCH(CH3)COOCH3.
(Xem giải) Câu 21. Polymer X được dùng để sản xuất một loại chất dẻo an toàn thực phẩm. Chất dẻo này được sử dụng để chế tạo chai lọ đựng nước, bao bì đựng thực phẩm. Cho cấu tạo của một đoạn mạch trong phân tử polymer X:
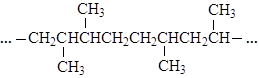
Tên của X là
A. polypropane. B. poly(2,3-dimethylbutane).
C. polyisopentane. D. polypropylene.
(Xem giải) Câu 22. Phát biểu nào sau đây không đúng?
A. Poly(ethylene terephthalate) được điều chế bằng phản ứng trùng ngưng các monomer tương ứng.
B. Trùng ngưng buta-1,3-diene với styrene có xúc tác, thu được cao su buna-S.
C. Tơ cellulose acetate là tơ bán tổng hợp.
D. Trùng hợp acrylonitrile thu được tơ olon.
(Xem giải) Câu 23. Cho biết E°Cu2+/Cu = +0,34 V; E°Fe2+/Fe = -0,440 V; E°Fe3+/Fe2+ = +0,77V. Phản ứng nào sau đây không xảy ra ở điều kiện chuẩn?
A. Fe(s) + 2Fe3+(aq) → 3Fe2+(aq).
B. Cu(s) + 2Fe3+(aq) → Cu2+(aq) + 2Fe2+(aq).
C. Fe(s) + Cu2+(aq) → Fe2+(aq) + Cu(s).
D. 2Fe2+(aq) + Cu2+(aq) → Fe3+(aq) + Cu(s).
(Xem giải) Câu 24. Menthol là một hoạt chất được tìm thấy nhiều trong cây bạc hà. Menthol tạo ra cảm giác mát lạnh, nhờ đó nó giảm sự chú ý của ta khỏi cơn đau và những kích thích khác. Menthol còn có tác dụng kháng khuẩn, chống co thắt và làm giãn cơ. Công thức cấu tạo của menthol như hình sau:
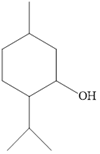
Những phát biểu nào đúng trong các phát biểu sau?
(1) Menthol là alcohol đơn chức.
(2) Công thức phân tử của menthol có dạng CnH2n-1OH.
(3) Tên thay thế của menthol là 2-isopropyl-5-methylcyclohexandiol.
(4) Menthol là alcohol thơm.
(5) Oxi hoá menthol bằng CuO, đun nóng, thu được một aldehyde.
A. (1) và (2). B. (1), (2) và (4). C. (1) và (5). D. (3), (4) và (5).
(Xem giải) Câu 25. Cho các sơ đồ phản ứng sau:
(1) M + NaOH → X + Y
(2) Q + NaOH → X + Z
(3) Y + HCl → T + NaCl
Biết M, Q đều là các hợp chất hữu cơ no, mạch hở, chỉ chứa nhóm chức ester (được tạo thành từ carboxylic acid và alcohol) và trong phân tử có số nguyên tử carbon bằng số nguyên tử oxygen; M và Z có cùng số nguyên tử carbon; MM < MQ < 175. Cho các phát biểu sau:
(a) Nhiệt độ sôi của M thấp hơn nhiệt độ sôi của CH3COOH.
(b) Có duy nhất một công thức cấu tạo của Q thỏa mãn sơ đồ trên.
(c) Hai chất M và T có công thức đơn giản nhất khác nhau.
(d) Đốt cháy hoàn toàn Z, thu được Na2CO3, CO2 và H2O.
(e) X là chất lỏng, giữa các phân tử của X có liên kết hydrogen.
Số phát biểu đúng là
A. 3. B. 4. C. 5. D. 2.
(Xem giải) Câu 26. Cho phương trình nhiệt hóa học của các phản ứng sau:
C2H5OH(l) + O2(g) → CH3COOH(l) + H2O(l) ![]() = -492,6 kJ
= -492,6 kJ
CH3COOH(l) + 2O2(g) → 2CO2(g) + 2H2O(l) ![]() = -874,2 kJ
= -874,2 kJ
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l) ![]() = -2805,0 kJ
= -2805,0 kJ
CO(g) + ½O2(g) → CO2(g) ![]() = -283,0 kJ
= -283,0 kJ
Oxi hoá hoàn toàn 1 gam mỗi chất (giả sử hiệu suất đạt 100%), chất nào giải phóng nhiều năng lượng nhất?
A. C6H12O6. B. CO. C. C2H5OH. D. CH3COOH.
(Xem giải) Câu 27. Bradykinin là một peptide được sản sinh từ huyết thanh trong máu, là chất làm giãn mạch máu và gây co cơn trơn, chất trung gian gây ra tình trạng viêm, có công thức phân tử: C50HyOzNt. Công thức cấu tạo của Bradykinin như sau:
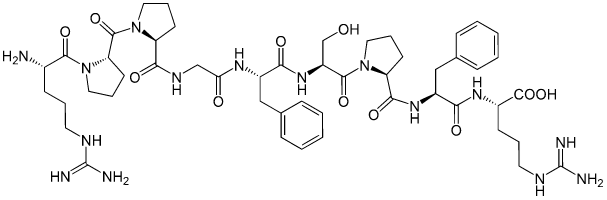
Chọn phát biểu không đúng về bradykinin
A. Trong bradykinin có 2 vòng benzene.
B. Trong một phân tử Bradykinin có một nhóm -OH.
C. Bradykinin có công thức phân tử là C50H73N15O11.
D. Phần trăm khối lượng của nitrogen trong bradykinin là 18,34%.
(Xem giải) Câu 28. Cho một polymer (X) có cấu trúc như sau:
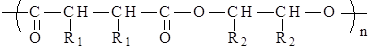
Phát biểu nào sau đây SAI?
A. X là polyester.
B. Giữa các chuỗi của X có tương tác Van der Waals tương đối mạnh.
C. X là copolymer (là loại polymer được tạo thành từ hai hay nhiều loại monomer).
D. X được tạo thành từ phản ứng trùng hợp monomer tương ứng.
(Xem giải) Câu 29. Cho một pin Galvani với điện cực Zn và Cu có sức điện động chuẩn là 1,102 V. Sử dụng pin này để thắp sáng một bóng đèn nhỏ với cường độ dòng điện chạy qua là I = 0,02 A. Nếu điện cực kẽm hao mòn 0,1 mol do pin phóng điện thì thời gian tối đa mà pin thắp sáng được bóng đèn là bao nhiêu giờ? Cho biết các công thức: Q = n.F = I.t, trong đó: Q là điện lượng (C), n là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian (giây), F là hằng số Faraday (96500 C/mol).
A. 268. B. 256. C. 286. D. 298.
(Xem giải) Câu 30. Cho hỗn hợp X gồm Al và Mg tác dụng với 400 ml dung dịch gồm AgNO3 a mol/l và Cu(NO3)2 2a mol/l, thu được 18,08 gam chất rắn Y. Cho Y tác dụng với dung dịch H2SO4 đặc, nóng (dư), thu được 3,4706 lít khí SO2 (ở đkc, là sản phẩm khử duy nhất). Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là
A. 0,30. B. 0,10. C. 0,12. D. 0,08.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 31 đến câu 38. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 31. Một trong những hóa chất dùng phổ biến để xử lí bể bơi là “clo viên” hoặc “TCCA 90” có công thức hóa học là C3Cl3N3O3. Công thức cấu tạo “TCCA 90” như sau:
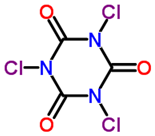
Một viên nén 200 gam có khả năng khử trùng cho 20m³ nước hồ bơi được bán với giá 10 nghìn đồng.
a) Trong “TCCA 90” có 9 liên kết đơn.
b) Phân tử “TCCA 90” có cấu tạo đối xứng.
c) Trong “TCCA 90” có 12 liên kết σ.
d) Nếu một hồ bơi được xây dựng với thể tích nước trong hồ bơi là 300m³ nước thì chi phí mua TCCA 90 cho một lần xử lí là 150 nghìn.
(Xem giải) Câu 32. Một học sinh tiến hành thí nghiệm như hình dưới đây:

• Bước 1: Dây đồng được cuốn thành hình lò xo (1) rồi nung nóng trên ngọn lửa đèn cồn (2).
• Bước 2: Nhúng dây đồng đang nóng vào ống nghiệm chứa ethanol (3), sau đó nhấc ra và nung lại trên ngọn lửa đèn cồn (4). Lặp lại thao tác (3), (4) vài lần.
• Bước 3: Lấy ½ chất lỏng trong ống nghiệm X cho phản ứng với thuốc thử Tollens, đun nóng.
• Bước 4: Lấy ½ chất lỏng trong ống nghiệm X thực hiện phản ứng iodoform.
a) Sau bước 1 dây lò xo đồng có màu đen, khi nhúng vào ống nghiệm chứa ethanol rồi nhấc ra thì dây lò xo đồng có màu đỏ.
b) Sau bước 3 thấy có kết tủa trắng bạc chứng tỏ chất lỏng trong ống nghiệm sau bước 2 có aldehyde.
c) Sau bước 4 không quan sát được hiện tượng gì.
d) Thí nghiệm đã chứng minh alcohol bậc I có tính khử và aldehyde có tính oxi hóa.
(Xem giải) Câu 33. Docosahexaenoic acid (DHA) là một acid béo omega-3 cực kỳ quan trọng cho sự phát triển và hoàn thiện của nhiều bộ phận trong cơ thể. Đặc biệt, DHA được biết đến với vai trò quan trọng trong việc duy trì sức khỏe của mắt và hệ thần kinh. Nó giúp cải thiện thị lực và hỗ trợ chức năng não bộ, đặc biệt là trong giai đoạn phát triển của trẻ em. Ngoài ra, DHA cũng có vai trò quan trọng trong việc bảo vệ sức khỏe tim mạch và hệ tuần hoàn. DHA có công thức cấu tạo như sau:

a) DHA có vai trò duy trì sức khoẻ của mắt, hệ thần kinh và bảo vệ sức khoẻ tim mạch.
b) DHA là một acid béo omega-3 không no, đơn chức, mạch hở và có số nguyên tử carbon chẵn.
c) DHA có thể tác dụng với dung dịch Br2 theo tỉ lệ mol tương ứng là 1 : 7.
d) Triester của glycerol với DHA có công thức phân tử C69H98O6.
(Xem giải) Câu 34. Fructan là polymer tự nhiên, được tìm thấy trong hơn 12% loài thực vật hạt kín, cả thực vật một lá mầm và hai lá mầm như atisô, măng tây, tỏi tây, … Chuỗi fructan chỉ bị phân hủy khoảng 5-15% trong ruột non, sau đó được chuyển xuống ruột già. Vi khuẩn đường ruột ăn những đường này sẽ gây tình trạng đầy hơi, chướng bụng liên tục. Cấu trúc của fructan như hình sau:
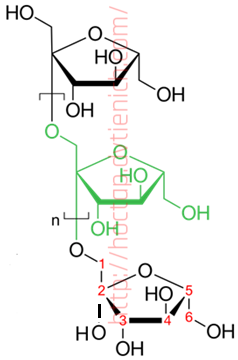
a) Tất cả các mắt xích của fructan đều là glucose.
b) Fructan là polysaccharide.
c) Liên kết giữa các mắt xích trong fructan là β-2,1-glycoside.
d) Sản phẩm thủy phân hoàn toàn fructan là fructose.
(Xem giải) Câu 35. Tryptophan là amino acid thiết yếu có tác dụng duy trì cân bằng nitrogen cho cơ thể và là một chất dẫn truyền thần kinh điều chỉnh cảm giác thèm ăn, cơn buồn ngủ và trạng thái tâm lý.

a) Tryptophan có hai vòng thơm và có số nguyên tử oxygen bằng số nguyên từ nitrogen.
b) Tryptophan có công thức phân tử là C11H14N2O2.
c) Tryptophan tác dụng với HCl trong dung dịch theo tỉ lệ mol tương ứng 1 : 2.
d) Điểm đẳng điện (pI) là giá trị pH mà tại đó aminoacid tồn tại trong dung dịch dạng ion lưỡng cực, dạng ion này có tổng điện tích dương bằng tổng điện tích âm. Tryptophan có điểm đẳng điện pI = 5,88; trong dung dịch có pH = 7,65 tryptophan tồn tại chủ yếu ở dạng cation, di chuyển về phía cực âm dưới tác dụng của điện trường.
(Xem giải) Câu 36. Khi dùng xúc tác Ziegler-Natta (Al(C2H5)3) cho phản ứng trùng hợp ethylene, người ta thấy polyethylene tạo ra có khối lượng riêng khoảng 0,94 g/cm³ (gọi là HDPE), mạch không phân nhánh và không dẫn điện được.
a) Phản ứng điều chế HDPE được biểu diễn như sau: nCH2=CH2 (Al(C2H5)3, t°) → (-CH2-CH2-)n
b) HDPE được dùng để sản xuất xô, chậu nhựa, ống dẫn nước, màng bọc thực phẩm, …
c) HDPE có nhiệt độ nóng chảy xác định và có khả năng tan trong chloroform.
d) Số mắt xích HDPE có trong 1 cm³ nhỏ hơn 2.10²² (mắt xích).
(Xem giải) Câu 37. Lắp đặt thí nghiệm như hình vẽ:

a) Dòng electron chuyển rời từ điện cực kẽm đến điện cực đồng
b) Ở điện cực âm, nguyên tử Zn là bị oxi hóa thành ion Zn2+, nồng độ Zn2+ tăng lên nên ion âm như Cl- di chuyển từ cầu muối đến để cân bằng diện tích.
c) Tại cathode, ion Cu2+ nhường electron bị khử thành nguyên tử Cu nên nồng độ ion dương tăng. Do vậy, các ion âm như Cl- ở cầu muối di chuyển để cân bằng điện tích trong dung dịch.
d) Cầu muối có vai trò cân bằng điện tích ion giữa các dung dịch.
(Xem giải) Câu 38. Một học sinh tiến hành thí nghiệm sau:
Bước 1: Lấy cùng thể tích 10mL dung dịch Fe(NO3)3 0,1M vào cốc (1) và dung dịch AgNO3 0,1M vào cốc (2).
Bước 2: Cho vào cốc (1) một lá sắt và cốc (2) một lá đồng.
a) Dung dịch ở cốc (2) từ màu xanh chuyển thành không màu.
b) Sau khi phản ứng xảy ra hoàn toàn, khối lượng lá sắt ở cốc (1) giảm xuống, khối lượng lá đồng ở cốc (2) tăng lên (giả sử kim loại sinh ra bám vào thanh kim loại).
c) Ở cốc (1) chỉ xảy ra ăn mòn hóa học.
d) Sau khi phản ứng ở hai cốc xảy ra hoàn toàn, nồng độ mol/L của chất tan trong hai cốc bằng nhau vì nồng độ hai muối ban đầu bằng nhau.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 39 đến câu 44.
(Xem giải) Câu 39. Thủy phân 51,3 gam saccharose ở điều kiện thích hợp thu được dung dịch X. Trung hòa dung dịch X bằng dung dịch NaOH, sau đó cho dung dịch thu được tác dụng với thuốc thử Tollens dư, đun cách thủy thu được 31,104 gam bạc (silver). Giả sử hiệu suất của phản ứng tráng bạc là 80%. Tính hiệu suất của phản ứng thủy phân saccharose?
(Xem giải) Câu 40. Lần lượt cho các kim loại Zn, Fe, Cu vào các dung dịch riêng rẽ chứa AlCl3, FeCl3, Pb(NO3)2 và AgNO3. Số trường hợp có xảy ra phản ứng là bao nhiêu?
(Xem giải) Câu 41. Cứ 45,75 gam cao su buna-S phản ứng vừa hết với dung dịch chứa 20 gam Br2 (trong CCl4). Tính phần trăm khối lượng carbon trong loại cao su trên? (Làm tròn kết quả đến hàng phần mười).
(Xem giải) Câu 42. Cho các chất được kí hiệu tương ứng như sau:
(1) HOOC-CH2-CH2-CH(NH2)-COOH (2) HOOC-CH2-CH2-CH(NH2)-COONa
(3) NaOOC-CH2-CH2-CH(NH2)-COONa (4) HOOC-CH2-CH2-CH(NH3Cl)-COOH
Thứ tự pH tăng dần của các chất trên là (VD 1234, 3142, …)
(Xem giải) Câu 43. Một loại chất béo có chứa 75% tristearin về khối lượng (còn lại là tạp chất). Để sản xuất 4 nghìn bánh xà phòng cần dùng tối thiểu x kg loại chất béo trên cho phản ứng với dung dịch NaOH, đun nóng. Biết rằng trong mỗi bánh xà phòng có chứa 70 gam sodium stearate. Tìm x. Kết quả làm tròn đến hàng đơn vị.
(Xem giải) Câu 44. Pin nhiên liệu cung cấp năng lượng điện và giải phóng nhiệt khi pin hoạt động. Ngoài ra, việc vận hành pin nhiên liệu không phát sinh tiếng ồn và giải phóng nước, không làm ô nhiễm môi trường như nhiên liệu hóa thạch.
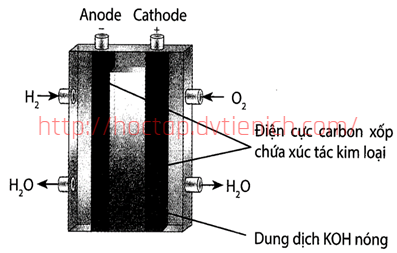
Nhiều hãng sản xuất xe đã nghiên cứu xe sử dụng năng lượng tái tạo là hydrogen, sử dụng tế bào nhiên liệu để chuyển hóa năng lượng và dùng động cơ điện để vận hành.
Anode (–): 2H2 + 4OH- → 4H2O + 4e (E°anode = -0,40V)
Cathode (+): O2 + 4e + 2H2O → 4OH- (E°cathode = 0,83V)
Phương trình hóa học của phản ứng xảy ra: 2H2 + O2 → 2H2O
(1) Sức điện động của pin nhiên liệu trên là 0,43 V.
(2) Pin nhiên liệu có ưu điểm là không phát thải khí gây ô nhiễm môi trường do chỉ thải ra hơi nước.
(3) Về phương diện hóa học, pin nhiên liệu có phản ứng tương đương với sự điện phân.
(4) Pin nhiên liệu có thể bị rò rỉ hydrogen, gây nguy hiểm nếu không được bảo quản đúng cách.
Số phát biểu đúng theo thứ tự từ nhỏ đến lớn là

Bình luận