[2025 – 2026] Thi học sinh giỏi lớp 12 – TP Hải Phòng
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Tổng hợp đề hsg theo năm học
⇒ Mã đề 017-H12A năm 2025-2026
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1D | 2D | 3C | 4B | 5D | 6D | 7A | 8B | 9B | 10A |
| 11C | 12B | 13A | 14A | 15C | 16C | 17A | 18B | 19C | 20D |
| Câu 21 | Câu 22 | Câu 23 | Câu 24 | Câu 25 | |
| (a) | Đ | S | Đ | S | Đ |
| (b) | Đ | Đ | Đ | S | S |
| (c) | S | S | S | S | Đ |
| (d) | Đ | S | Đ | Đ | S |
| 26 | 27 | 28 | 29 | 30 |
| 125 | 63,5 | 1324 | 124 | 1,36 |
| 31 | 32 | 33 | 34 | 35 |
| 40 | 20 | 5,02 | 50 | 18 |
PHẦN 1: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 20. Mỗi câu hỏi thí sinh chỉ lựa chọn một phương án.
(Xem giải) Câu 1. Xăng sinh học E5 là nhiên liệu chứa 5% thể tích ethanol và 95% thể tích xăng truyền thống. Sử dụng xăng sinh học được coi là giải pháp bảo vệ môi trường, giảm sự phụ thuộc vào nhiên liệu hóa thạch. Coi thể tích xăng E5 bằng tổng thể tích xăng truyền thống (D = 0,700 g/cm³) và C2H5OH (D = 0,789 g/cm³). Biết xăng truyền thống là hỗn hợp của C8H18 và C9H20 (tỷ lệ mol tương ứng là 5 : 4). Ở cùng điều kiện phản ứng, đốt cháy hoàn toàn:
| Số mol O2 phản ứng | Thể tích CO2 thu được (đkc) | |
| 25 lít xăng truyền thống | n1 | V1 (lít) |
| 25 lít xăng E5 | n2 | V2 (lít) |
| Giá trị | a = n1 – n2 | b = V1 – V2 |
Giá trị của a và b gần nhất là
A. 32,4 và 470,8. B. 31,5 và 470,8. C. 32,4 và 460,6. D. 31,5 và 460,6.
(Xem giải) Câu 2. Hợp chất X tan trong nước tạo dung dịch không màu. Dung dịch này không tạo kết tủa với dung dịch BaCl2. Khi cho X phản ứng với dung dịch NaOH tạo ra khí có mùi khai. Khi cho X phản ứng với dung dịch HCl tạo ra khí có ứng dụng tẩy trắng giấy và bột giấy. Chất X có công thức là
A. Na2SO3. B. (NH4)2CO3. C. NH4HCO3. D. NH4HSO3.
(Xem giải) Câu 3. Kết quả thí nghiệm của các chất: X, Y, Z, T được sắp xếp ngẫu nhiên methylamine; albumin; aniline; Ala-Gly–Ala như sau:
| Mẫu thử | Thuốc thử | Hiện tượng |
| X | Đun nóng | đông tụ |
| Y | Quỳ tím | không chuyển màu |
| Z | Cu(OH)2/NaOH | dung dịch màu xanh |
| X, T | Cu(OH)2/NaOH | dung dịch màu tím |
Cho các phát biểu sau:
(a) Chất X là hợp chất được cấu tạo nên từ các chuỗi polyamide và thuộc loại protein phức tạp.
(b) Chất T có công thức phân tử là C8H15N3O4.
(c) Chất Y và phenol phản ứng với nước bromine đều thấy xuất hiện kết tủa trắng.
(d) Chất Z có thể được điều chế từ ammonia và iodoform.
Có bao nhiêu phát biểu đúng?
A. 3. B. 4. C. 2. D. 1.
(Xem giải) Câu 4. Linalyl acetate là một trong những chất của tinh dầu cam và mùi thơm của hoa oải hương. Công thức cấu tạo của linlalyl acetate như sau:
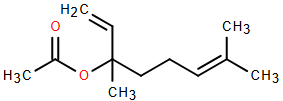
Cho các phát biểu sau:
(a) Linalyl acetate là một carboxylic acid.
(b) Linalyl acetate có 18 nguyên tử hydrogen.
(c) Phân tử khối của Linalyl acetate là 196.
(d) Linalyl acetate có đồng phân hình học.
Số phát biểu đúng là?
A. 4. B. 1. C. 2. D. 3.
(Xem giải) Câu 5. Sulfuric acid là hoá chất quan trọng hàng đầu trong nhiều ngành sản xuất. Trong công nghiệp, sulfuric acid được sản xuất bằng phương pháp tiếp xúc. Phương pháp này gồm 3 giai đoạn chính: Sản xuất SO2 → Sản xuất SO3 → Sản xuất H2SO4.
Ở giai đoạn sản xuất H2SO4: Dùng H2SO4 đặc 98% để hấp thụ SO3, thu được oleum (H2SO4.nSO3). Biết trong oleum, SO3 chiếm 71% về khối lượng. Hòa tan 33,8 gam oleum trên vào nước thành 100 mL dung dịch H2SO4 (dung dịch A). Để trung hòa 10 mL dung dịch A thì cần vừa đủ V mL dung dịch NaOH 2M.
Cho các phát biểu sau:
(a) Oleum có công thức là H2SO4.4SO3.
(b) Giá trị V là 40.
(c) Chất xúc tác ở giai đoạn sản xuất SO3 là V2O5, chất xúc tác cho vào nhằm làm tăng tốc độ phản ứng và làm chuyển dịch cân bằng.
(d) Bình đựng H2SO4 đặc nếu hở nắp để lâu trong không khí ẩm thì khối lượng bình tăng lên.
(e) Có thể dùng bình làm bằng aluminium để đựng dung dịch H2SO4 đặc, nguội.
Số phát biểu sai là
A. 4. B. 3. C. 1. D. 2.
(Xem giải) Câu 6. Alliin là một amino acid có trong tỏi tươi, khi đập dập hay nghiền enzyme alliinase sẽ chuyển hoá alliin thành allicin, tạo ra mùi đặc trưng của tỏi. Alliin và allicin có công thức sau:
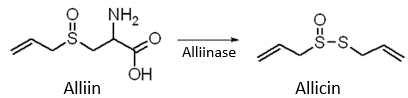
Cho các phát biểu sau đây:
(a) Alliin có công thức phân tử là C6H11O3NS.
(b) Trong mỗi phân tử alliin hoặc allicin đều có chứa 3 liên kết π (pi).
(c) Allicin có tính kháng khuẩn, thường dùng để phòng ngừa và trị cảm cúm.
(d) Alliin có tính chất lưỡng tính.
Có bao nhiêu phát biểu đúng ?
A. 1. B. 2. C. 3. D. 4
(Xem giải) Câu 7. Cho phương trình nhiệt hóa học của phản ứng:
2H2(g) + O2(g) → 2H2O(l) ![]() = -571,68 kJ
= -571,68 kJ
Phản ứng trên là phản ứng
A. tỏa nhiệt.
B. thu nhiệt.
C. có sự hấp thụ nhiệt lượng từ môi trường xung quanh.
D. không có sự thay đổi năng lượng.
(Xem giải) Câu 8. Phân rã tự nhiên 90Th232 tạo ra đồng vị bền 82Pb208, đồng thời giải phóng một số hạt α và β. Số hạt α và β cho quá trình phân rã một hạt nhân 90Th232 lần lượt là
A. 6 và 8. B. 6 và 4. C. 8 và 6. D. 8 và 4.
(Xem giải) Câu 9. Hydrogen sulfide (H2S) là một loại khí độc (gây ngạt) và dễ cháy, thường tích tụ trong các hầm mỏ, đường ống cống ngầm hoặc các trạm xử lý nước thải. Nhằm đảm bảo an toàn cho công nhân trước khi vào ca làm việc, đội giám sát an toàn lao động tiến hành lấy mẫu không khí tại một khu vực hầm mỏ nghi ngờ có khí H2S để xác định hàm lượng có vượt mức cho phép hay không.
Quy trình phân tích như sau: Lấy 50 lít không khí (D = 1,29 g/lít) nhiễm khí H2S cho đi qua thiết bị phân tích có chứa dung dịch CdSO4 dư. Sau đó acid hóa toàn bộ kết tủa thu được và cho tất cả lượng H2S sinh ra hấp thụ hết vào ống dựng 10 ml dung dịch I2 0,015M. Lượng I2 dư tác dụng vừa đủ với 12,0 ml dung dịch Na2S2O3 0,008 M. Các phản ứng xảy ra theo sơ đồ sau:
Cd2+ + H2S → CdS + H+
CdS + H+ → H2S + Cd2+
H2S + I2 → 2H+ + I- + S
I2 + S2O32- → I- + S4O62-
Hàm lượng H2S trong mẫu không khí (số microgam (μg) H2S trong 1 gam mẫu không khí) gần nhất với kết quả nào sau đây?
A. 43,8. B. 53,8. C. 89,6. D. 52,7.
(Xem giải) Câu 10. Sau khi điều chế, khí SO2 có lẫn hơi nước được dẫn qua bình làm khô chứa chất rắn T rồi thu vào bình chứa theo hình dưới đây:
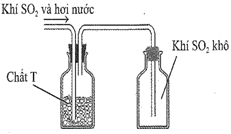
Chất T có thể là
A. P2O5. B. NaOH. C. CaO. D. KOH.
(Xem giải) Câu 11. Một sơ đồ phản ứng: A + B → C có phương trình tốc độ v = k[A]²[B]. Nếu tăng nồng độ A lên 2 lần và giảm nồng độ B đi 2 lần thì tốc độ phản ứng sẽ thay đổi như thế nào?
A. Tăng gấp 4 lần. B. Giảm đi một nửa.
C. Tăng gấp 2 lần. D. Không thay đổi.
(Xem giải) Câu 12. Peptide có nhiều vai trò quan trọng, đặc biệt trong chăm sóc da và tóc, như chống lão hóa, tăng cường sản xuất collagen và elastin, giảm nếp nhăn, sửa chữa các tổn thương… Một peptide A có công thức sau:
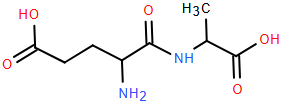
Cho các phát biểu về peptide A:
(a) Peptide A có công thức phân tử là C7H14O5N2.
(b) Peptide A có khả năng phản ứng màu biuret.
(c) Phân tử khối của peptide A là 236.
(d) Peptide A được cấu tạo bởi ba loại α-amino acid khác nhau.
(e) Khi thủy phân hoàn toàn peptide A với dung dịch sodium hydroxide, thu được hỗn hợp các muối X, Y. Cho dung dịch các muối X, Y đặt trong điện trường, thì phần hữu cơ của X, Y sẽ di chuyển về cực (+) của điện trường.
(f) Khi thủy phân hoàn toàn 7,63 gam peptide A với dung dịch hydrochloric acid, thu được 9,27 gam hỗn hợp các muối Z, T.
Có bao nhiêu phát biểu đúng ?
A. 4. B. 1. C. 2. D. 3.
(Xem giải) Câu 13. Bisphenol A là hợp chất được dùng nhiều trong công nghiệp để điều chế nhựa epoxy. Trong công nghiệp oxi hoá 1,0 tấn cumene để điều chế phenol và acetone với hiệu suất 90%. Toàn bộ lượng phenol và acetone thu được ở trên đem điều chế Bisphenol A theo sơ đồ sau:
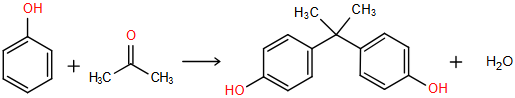
Biết hiệu suất của phản ứng tổng hợp bisphenol A đạt 80%. Khối lượng (kg) bisphenol A thu được là:
A. 684,0. B. 902,5. C. 722,0. D. 744,2.
(Xem giải) Câu 14. Một thửa ruộng có diện tích 10000 m² trồng cây cần được cung cấp 120 kg N, 37,2 kg P và 74,1 kg K. Người ta sử dụng đồng thời ba loại phân bón: Phân hỗn hợp NPK có độ dinh dưỡng ghi trên bao bì là (16-16-8), phân kali (KCl) (độ dinh dưỡng 60%) và urea ((NH2)2CO) (độ dinh dưỡng 46%) trộn lẫn với nhất. Tính tổng khối lượng phân bón cần sử dụng cho thửa ruộng trên (kết quả làm tròn đến hàng đơn vị)
A. 686. B. 605. C. 600. D. 590.
(Xem giải) Câu 15. Sau mỗi trận mưa giông, một lượng nitrogen trong không khí được chuyển hóa thành ion nitrate và hòa tan vào nước mưa. Nguyên tố nitrogen có trong ion nitrate có vai trò thúc đẩy quá trình sinh trưởng và phát triển của cây trồng, làm cho cây trồng ra nhiều lá, cho nhiều củ, quả và hạt hơn. Hàm lượng ion nitrate trung bình trong một mẫu nước mưa là 31 mg/lít nước mưa. Biết rằng, trung bình trong 1 giờ sẽ có 25 m³ nước mưa trên rơi xuống một thửa ruộng. Khối lượng nguyên tố nitrogen mà thửa ruộng đó nhận được khi cơn mưa kéo dài 2 giờ là
A. 1,55 kg. B. 0,175 kg. C. 0,35 kg. D. 0,75 kg.
(Xem giải) Câu 16. Cho hình vẽ mô tả dụng cụ, hoá chất, cách tiến hành thí nghiệm điều chế ethylene và thử tính chất của ethylene:

Tiến hành:
– Cho vài viên đá bọt, 20 mL cồn 96° vào bình cầu. Rót 40 mL dung dịch H2SO4 đặc vào ống đong, sau đó rót từ từ H2SO4 đặc từ ống đong qua phễu vào bình cầu để tránh sự toả nhiệt quá mạnh.
– Lắp bộ dụng cụ như trên.
– Đun nóng đến khi ethylene sinh ra, rồi lần lượt sục vào bình (1) rồi dẫn qua ống nghiệm (2).
– Thay ống dẫn khí thuỷ tinh hình chữ L bằng ống dẫn thuỷ tinh có đầu vuốt nhọn. Dùng que đóm đang cháy để đốt ethylene ở đầu ống dẫn khí.
Cho các phát biểu sau:
(a) Đốt ethylene ở đầu ống dẫn khí, khí ethylene cháy và toả nhiều nhiệt.
(b) Khí ethylene làm mất màu nước Br2 hoặc dung dịch KMnO4 ở ống nghiệm (2).
(c) Vai trò của đá bọt trong bình cầu là để điều hoà quá trình sôi, tránh hiện tượng quá sôi.
(d) Vai trò của NaOH là để trung hoà acid H2SO4 thoát ra.
Số phát biểu đúng là
A. 2. B. 1. C. 3. D. 4.
(Xem giải) Câu 17. Calcium là nguyên tố đóng vai trò quan trọng trong việc hình thành nên xương và răng của con người. Biết rằng, trong tinh thể calcium các nguyên tử là những khối cầu (có bán kính là 0,196 nm) chiếm 74% thể tích tinh thể phần còn lại là khe rỗng. Biết M Ca = 40 g/mol; π = 3,14; NA = 6,022.10²³). Khối lượng riêng của tinh thể calcium là a (g/cm³). Tính a. (Kết quả làm tròn đến hàng phần trăm).
A. 1,56. B. 1,96. C. 1,85. D. 1,54.
(Xem giải) Câu 18. Cho đồ thị biểu diễn năng lượng của một phản ứng như sau:
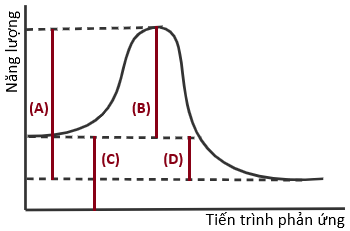
Đoạn nào trên đồ thị tương ứng với năng lượng hoạt hóa của phản ứng?
A. Đoạn (D). B. Đoạn (B). C. Đoạn (A). D. Đoạn (C).
(Xem giải) Câu 19. Tiến hành phản ứng tráng bạc của ethanal với thuốc thử Tollens, người ta tiến hành các bước sau đây:
• Bước 1: Rửa sạch các ống nghiệm bằng cách nhỏ vào mấy giọt dung dịch NaOH, đun nóng nhẹ, tráng đều, sau đó đổ đi và tráng lại ống nghiệm bằng nước cất.
• Bước 2: Nhỏ lần lượt vào ống nghiệm trên: 2 ml dung dịch AgNO3 và 1 ml dung dịch NH3, trong ống nghiệm xuất hiện kết tủa nâu xám của silver hydroxide, nhỏ tiếp dung dịch NH3 đến khi kết tủa tan hết.
• Bước 3: Nhỏ tiếp vào ống nghiệm 2 ml dung dịch CH3CHO và lắc đều.
• Bước 4: Ngâm ống nghiệm trong cốc nước nóng ở nhiệt độ khoảng 70°C – 80°C vài phút.
Cho các phát biểu sau:
(a) Sau bước 4 quan sát thấy thành ống nghiệm sáng bóng như gương.
(b) Ở bước 4 xảy ra phản ứng oxi hóa – khử trong đó ethanal là chất bị khử.
(c) Ở bước 1, vai trò của NaOH và nước cất là để làm sạch bề mặt ống nghiệm.
(d) Trong bước 2, khi nhỏ tiếp dung dịch NH3 vào, kết tủa nâu xám của silver hydroxide bị hòa tan do tạo thành phức [Ag(NH3)4]OH.
(e) Sản phẩm hữu cơ thu được trong dung dịch sau bước 4 có công thức phân tử là C2H7NO2.
(f) Trong bước 4, để kết tủa bạc nhanh bám vào thành ống nghiệm ta phải luôn lắc đều và liên tục hỗn hợp phản ứng.
(g) Ở bước 2 có thể thay dung dịch NH3 bằng dung dịch NaOH.
(h) Ở bước 3 nếu thay ethanal bằng acetone vào ống nghiệm thì thu được hiện tượng tương tự.
Số phát biểu đúng là
A. 5. B. 6. C. 3. D. 4.
(Xem giải) Câu 20. Lactose là một loại đường disaccharide (còn gọi là đường sữa) được tạo thành từ một đơn vị glucose và một đơn vị galactose liên kết với nhau. Lactose chủ yếu được tìm thấy trong sữa và các sản phẩm từ sữa, như phô mai và sữa chua. Đây là nguồn cung cấp năng lượng quan trọng, đặc biệt là cho trẻ sơ sinh và trẻ nhỏ. Tuy nhiên, một số người gặp khó khăn trong việc tiêu hoa lactose do thiếu enzyme lactase, dẫn đến tình trạng không dung nạp lactose, gây ra các triệu chứng như đầy bụng và tiêu chảy khi tiêu thụ các sản phẩm chứa lactose. Trong công nghiệp thực phẩm, lactose được sử dụng như một chất làm ngọt nhẹ và cũng đóng vai trò quan trọng trong việc lên men các sản phẩm từ sữa. Lactose có cấu tạo như sau:
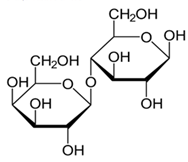
Cho các phát biểu sau:
(a) Lactose có phản ứng với thuốc thử Tollens khi đun nóng.
(b) Thủy phân 1 phân tử lactose trong môi trường acid thu được 2 phân tử glucose.
(c) Trong phân tử lactose có chứa liên kết β-1,2-glycoside.
(d) Độ tan trong nước của lactose ở 60°C là a gam/100 gam H2O; ở 25°C là 18,9 gam/100 gam H2O. Khi làm nguội 274,4 gam dung dịch lactose bão hoà ở 60°C xuống 25°C có tách ra 36,6 gam lactose. Giá trị của a là 37,2.
(e) Công thức phân tử của lactose là C12H22O11.
Số phát biểu đúng là
A. 2. B. 1. C. 4. D. 3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 21 đến câu 25. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 21. Các hợp chất HX (với X là halogen: F, Cl, Br, I), ở điều kiện thường là chất khí được gọi tên là hydrogen halide. Các chất này tan tốt trong nước thành dung dịch tương ứng có tính acid và được gọi là dung dịch hydrohalic acid.
a) Trong dãy HX, tính acid tăng dần từ HF đến HI.
b) Có thể điều chế HF bằng cách cho CaF2 rắn tác dụng với dung dịch H2SO4 đặc, đun nóng.
c) Tất cả các HX đều có tính khử mạnh, có thể tác dụng với dung dịch H2SO4 đặc tạo thành X2.
d) Dung dịch HCl thể hiện tính oxi hóa khi tác dụng với kim loại Mg.
(Xem giải) Câu 22. Tiến hành thí nghiệm chuẩn độ dung dịch FeSO4 nồng độ xM theo các bước sau:
• Bước 1: Dùng pipette hút chính xác 5,00 mL dung dịch FeSO4 nồng độ xM cho vào bình định mức loại 50 mL, dùng nước cất rửa pipette vừa sử dụng, nước rửa đều cho vào bình định mức. Thêm tiếp nước cất vào định mức đến vạch, lắc đều, thu được 50 mL dung dịch Y.
• Bước 2: Lấy 10,00 mL dung dịch Y cho vào bình tam giác, thêm H2SO4 loãng. Tiến hành chuẩn độ, kết quả thấy thể tích trung bình dung dịch KMnO4 0,02M sau 03 lần chuẩn độ là 6,5 mL.
a) Phản ứng chuẩn độ ở trên xảy ra trong môi trường acid nên có thể thay dung dịch H2SO4 bằng dung dịch HCl đặc.
b) Tổng hệ số cân bằng nguyên, tối giản nhất của chất trong phản ứng dạng phân tử xảy ra trong quá trình chuẩn độ là 36.
c) Thời điểm kết thúc chuẩn độ là lúc dung dịch xuất hiện màu tím bền.
d) Giá trị của x bằng 0,065 M.
(Xem giải) Câu 23. Trong tự nhiên nguyên tố sulfur tồn tại 3 đồng vị bền là 32S; 33S; 34S với tỉ lệ phần trăm số nguyên tử tương ứng là 95 : 0,8 : 4,2. Một loại phèn có công thức dạng: aK2SO4.Al2(SO4)3.bH2O. Khi phân tích phèn trên cho kết quả % khối lượng của Al là 5,694% và của S là 13,536%. (Cho: K = 39,000; Al = 27,000; O = 16,000; H = 1,000).
a) Trong tự nhiên, khi có 3,2.10^4 nguyên tử 33S thì số nguyên tử đồng vị 32S và 34S lần lượt là 3,8.10^6 và 1,68.10^5.
b) Trong thực tế phèn trên được dùng làm trong nước, sử dụng trong công nghiệp làm giấy, nhuộm vải, thuộc da…
c) Tổng số nguyên tử oxygen trong một phân tử phèn trên là 28.
d) Nguyên tử khối trung bình của sulfur bằng 32,092.
(Xem giải) Câu 24. Chất béo đóng vai trò là nguồn cung cấp năng lượng cho cơ thể và được xem là nguồn dinh dưỡng quan trọng. Nhiều vitamin như A, D, E và K hoà tan tốt trong chất béo, nên chúng được vận chuyển và hấp thụ cùng với chất béo. Thành phần chính của chất béo là triglyceride. Một triglyceride X có công thức cấu tạo như hình sau:
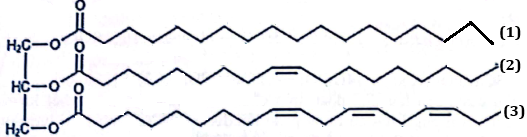
Thuỷ phân hoàn toàn a mol X trong dung dịch NaOH thu được a mol chất Y và hỗn hợp muối Z.
a) Acid béo tương ứng với gốc acid ở vị trí (3) thuộc loại acid béo omega-9.
b) Hỗn hợp muối Z được sử dụng làm chất giặt rửa tổng hợp X.
c) Dung dịch chất Y khi đun nóng với copper (II) hydroxide trong môi trường base sinh kết tủa đỏ gạch.
d) Chỉ số xà phòng hóa là tổng số miligam KOH cần để xà phòng hóa triglyceride và trung hòa acid béo tự do trong 1,0 gam chất béo. Một loại chất béo chứa 97,02% chất X và 1,42% stearic acid về khối lượng, còn lại là các tạp chất không tham gia phản ứng với KOH. Chỉ số xà phòng hoá của chất béo trên là 187,6.
(Xem giải) Câu 25. Kevlar là một polyamide có độ bền rất cao. Loại vật liệu này được dùng để sản xuất áo chống đạn và mũ bảo hiểm cho quân đội. Một đoạn mạch của Kevlar được mô tả như hình sau:
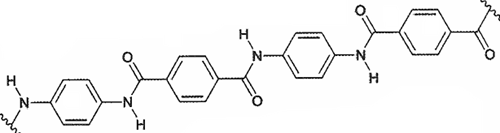
a) Benzene-1,4-diamine thuộc arylamine.
b) Trong số monomer điều chế Kevlar có một monomer có tính acid và một monomer có tính lưỡng tính.
c) Kevlar được tổng hợp trực tiếp từ benzene-1,4-dioic acid với benzene-1,4-diamine bằng phản ứng trùng ngưng.
d) Để sản xuất được 47,6 tấn kevlar với hiệu suất của cả quá trình sản xuất là 80% thì tổng khối lượng tối thiểu của 2 monomer cần dùng là 65,8 tấn.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 26 đến câu 35.
(Xem giải) Câu 26. Hợp chất với hydrogen của các nguyên tố nhóm VA, VIA và VIIA có nhiệt độ sôi được biểu diễn đồ thị sau:

Cho các nhận định sau:
(1) Trừ HF, H2O và NH3 thì nhiệt độ sôi của các hợp chất còn lại trong cùng một nhóm tăng dần do tương tác van der Waals tăng.
(2) Nhiệt độ sôi của H2O cao bất thường so với H2S, H2Se và H2Te là do H2O có liên kết hydrogen liên phân tử.
(3) Ở điều kiện chuẩn, HF và H2O tồn tại ở thể lỏng, các hợp chất còn lại ở thể khí.
(4) H2O có nhiệt độ sôi cao hơn HF là do liên kết H-O phân cực mạnh hơn liên kết H-F.
(5) Hợp chất với hydrogen của các nguyên tố đầu tiên trong mỗi nhóm trên có nhiệt sôi cao do NH3; H2O; HF xuất hiện liên kết hydrogen liên phân tử.
Liệt kê các phát biểu đúng ghi thành dãy các chữ số theo số thứ tự tăng dần? (ví dụ: 1234 hoặc 24,…)
(Xem giải) Câu 27. Để xác định hàm lượng iodine (iodine chỉ tồn tại trong KIO3) của một mẫu “muối i-ốt”. Một sinh viên tiến hành như sau: Cân 30 gam “muối i-ốt” rồi hòa tan hết trong nước cất thu được 100 mL dung dịch X. Lấy 20 mL dung dịch X vào bình nón (có nút nhám), thêm tiếp 1 mL dung dịch KI 1M (dư) và 1 mL dung dịch H2SO4 1M. Đậy nắp và lắc nhanh mẫu, để mẫu nơi tối. Sau 5 phút, thêm tiếp 1 mL dung dịch hồ tinh bột 1% thấy xuất hiện màu xanh tím, rồi đem chuẩn độ chậm (4 giây một giọt) bằng dung dịch Na2S2O3 0,002 mol/L tới khi mất màu thì thể tích dung dịch Na2S2O3 trung bình đã dùng sau 3 lần chuẩn độ là 9,0 mL. Biết trong phép chuẩn độ trên Na2S2O3 bị oxi hóa thành Na2S4O6. Hàm lượng iodine (mg/kg muối) trong mẫu muối i-ốt trên là bao nhiêu?
(Xem giải) Câu 28. Arginine là một trong những amino acid thiết yếu đối với cơ thể con người. Với mỗi môi trường có giá trị pH tương ứng, coi Arginine chỉ tồn tại ở dạng cho dưới đây:
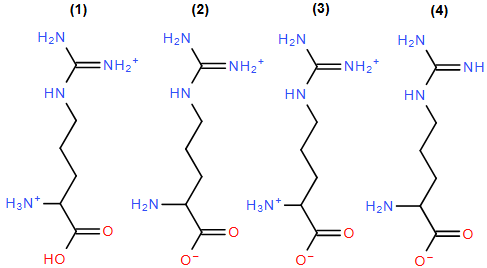
Hãy sắp xếp theo chiều tăng dần pH của các dạng tồn tại đó? (ví dụ: 1234 hoặc 4321,…)
(Xem giải) Câu 29. Kết quả phân tích thành phần một muối sulfate ngậm nước (X) của kim loại M thu được như sau:
| Nguyên tố | M | O | S | H |
| Thành phần khối lượng (%) | 25,6 | 57,6 | 12,8 | 4,0 |
Trong nông nghiệp, muối X được dùng để pha chế thuốc Bordeaux dùng để diệt nấm mốc cho cây trồng. Cách pha chế 10 lít dung dịch Bordeaux 1% như sau:
• Bước 1: Hòa tan 100 gam muối X trong 8,0 lít nước được dung dịch muối X.
• Bước 2: Cho 100 gam vôi sống (CaO) phản ứng hết trong 2,0 lít nước được nước vôi.
• Bước 3: Cho từ từ dung dịch muối X vào nước vội và khuấy đều, thu được dung dịch Bordeaux 1% ở dạng keo, màu xanh nhạt, pH = 7 – 8, độ lắng chậm.
Cho các phát biểu sau:
(1) Một phân tử X có chứa 5 phân tử nước.
(2) Ở bước 2, nếu dùng với tôi (Ca(OH)2) thay cho vôi sống thì cần dùng 132 gam (kết quả làm tròn đến hàng đơn vị).
(3) Có thể sử dụng thùng làm bằng aluminium hoặc iron để pha chế thuốc Bordeaux.
(4) Dung dịch muối X có màu xanh.
Liệt kê các phát biểu đúng ghi thành dãy các chữ số theo số thứ tự tăng dần? (ví dụ: 1234 hoặc 24,…)
(Xem giải) Câu 30. Nến làm từ stearic acid hầu như không bị nhỏ giọt, cháy với ngọn lửa nhỏ, êm dịu và tỏa ra ít khói hơn. Bạn sẽ không mất quá nhiều thời gian để lau sạch những vết sáp trên khăn trải và bàn ăn khi dùng loại nến này. Stearic acid có công thức cấu tạo sau:
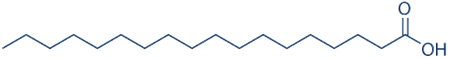
Trong một căn phòng kín, có thể tích không khí 19 m³ ở điều kiện nhiệt độ 21°C, áp suất bằng 98,0 kPa có thành phần, phần trăm thể tích các khí như sau:
| Oxygen | Nitrogen | Các khí khác |
| 21,0 | 78,1 | 0,90 |
Biết các chất khí là khí lý tưởng và tuân theo phương trình: PV = nRT. Hằng số khí R = 8,314 Pa.m³/K.mol. Sau khi 15 cây nến cháy hết hoàn toàn để thắp sáng căn phòng (mỗi cây nến chứa 60 gam stearic acid) thì tỉ lệ số mol của O2 còn lại so với CO2 trong phòng bằng T. Giả sử những cây nến được đốt cháy trong căn phòng không có sự trao đổi khí với môi trường xung quanh, các khí khác không có CO2 và không tham gia phản ứng, quá trình stearic acid cháy chỉ tạo CO2 và H2O. Giá trị của T là bao nhiêu? (Kết quả làm tròn tới hàng phần trăm).
(Xem giải) Câu 31. Từ một loại tinh bột (chứa 19% tạp chất trơ về khối lượng), người ta thủy phân rồi xử lý, thu được glucose monohydrate (gọi là chất X). Hiệu suất quá trình đạt 80%. Pha 27,5 gam X với nước cất pha tiêm (nước cất để pha thuốc tiêm) và tá dược vừa đủ thì thu được 500 mL dung dịch Y. Dung dịch Y dùng truyền vào tĩnh mạch, liều dùng đối với bệnh nhân (người lớn) 30 mL/kg thể trọng/ngày. Với khối lượng tinh bột là 5 kg thì có thể điều chế được lượng dung dịch Y truyền cho bao nhiêu bệnh nhân người lớn có thể trọng 60 kg trong một ngày?
(Xem giải) Câu 32. Trong công nghiệp, ammonia được sản xuất theo phản ứng: N2(g) + 3H2(g) ⇋ 2NH3(g)
Nung nóng hỗn hợp X gồm N2 và H2 trong bình kín có dung tích không đối với xúc tác Fe (có thể tích không đáng kể) sau một thời gian đưa về nhiệt độ ban đầu thu được hỗn hợp khí Y có áp suất giảm 10% so với áp suất ban đầu và tỉ khối của Y so với H2 bằng 85/18. Hiệu suất của phản ứng tổng hợp NH3 là a%. Giá trị của a là bao nhiêu?
(Xem giải) Câu 33. Calcium hydroxyl-apatite [Ca10(PO4)6(OH)2] được ứng dụng làm thành phần chính trong kem đánh răng với mục đích tái khoáng hóa men răng. Calcium hydroxyl-apatite có thể được tổng hợp từ sơ đồ sau:
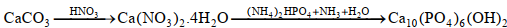
Một nhà máy sản xuất kem đánh răng (loại 75 g/1 tuýp) chứa 8% calcium hydroxyl-apatite về khối lượng. Từ 50 tấn đá vôi (chứa 25% tạp chất trơ không có calcium) nhà máy điều chế đủ lượng [Ca10(PO4)6(OH)2] cho sản xuất x triệu tuýp kem đánh răng trên. Biết hiệu suất cả quá trình đạt 80% và các sản phẩm khác sinh ra trong sơ đồ không chứa nguyên tố Ca. Giá trị của x bằng bao nhiêu?
(Xem giải) Câu 34. Hợp chất hữu cơ đơn chức X ở điều kiện thường là chất lỏng, có mùi thơm hoa quả, được ứng dụng làm dung môi vecni, sơn mài, hương liệu nhân tạo,… Phân tích phần trăm khối lượng các nguyên tố cho thấy X có 64,615% C; 10,760% H, còn lại là O. Từ phổ khối lượng của X xác định được giá trị m/z của peak [M+] bằng 130.
Khi cho X tác dụng với dung dịch NaOH thu được chất hữu cơ Y và muối sodium của carboxylic acid Z. Biết rằng, Y còn được tạo ra khi cho isovaleraldehyde (3-methylbutanal tác dụng với LiAlH4.
Để điều chế X, một học sinh đã tiến hành thí nghiệm cho 12,00 mL Y tác dụng với 6,00 mL Z, có mặt H2SO4 đặc làm xúc tác và đun nóng thu được 7,80 mL X. Cho biết khối lượng riêng (g/mL) của X, Y, Z lần lượt là: 0,875; 0,81; 1,05. Hiệu suất của phản ứng điều chế X là a%. Tính giá trị của a.
(Xem giải) Câu 35. Terephthalic acid là nguyên liệu để tổng hợp nhựa poly(ethylene terephthalate) hay (PET) dùng để sản xuất tơ sợi, chai nhựa. Terephthalic acid có thể được tổng hợp bằng cách oxi hóa arene X có công thức phân tử C8H10 bởi dung dịch KMnO4 theo sơ đồ sau: X (KMnO4/H2SO4) → Terephthalic acid → PET. Số liên kết σ (xích ma) trong 1 phân tử X bằng bao nhiêu?


Bình luận