[2025] Thi thử TN liên trường Nghệ An (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 057
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2B | 3A | 4C | 5A | 6A | 7D | 8B | 9B |
| 10A | 11B | 12A | 13B | 14D | 15B | 16A | 17C | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | S | Đ | 1345 | 172 | 88 |
| (b) | Đ | Đ | Đ | S | 26 | 27 | 28 |
| (c) | Đ | S | S | Đ | 11 | 3 | 1234 |
| (d) | Đ | S | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Artemisinin (X) là hợp chất được chiết xuất từ lá cây thanh hao hoa vàng, đóng vai trò quan trọng trong các loại thuốc điều trị sốt rét hiện nay. Thành phần phần trăm theo khối lượng của X gồm: 63,83% C; 28,37% O và còn lại là H. Khi phân tích X bằng phương pháp khối phổ, peak ion phân tử có giá trị m/z lớn nhất là 282. Công thức phân tử của X là
A. C15H22O4. B. C14H18O6. C. C15H22O5. D. C16H26O4.
(Xem giải) Câu 2. Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch có môi trường kiềm là
A. Na, Cr, K. B. Na, Ba, K. C. Na, Fe, K. D. Ni, Ba, Ca.
(Xem giải) Câu 3. Ion X2- có cấu hình electron ở trạng thái cơ bản 1s2 2s2 2p6. Nguyên tố X là
A. O (Z = 8). B. F (Z = 9). C. Ne (Z = 10). D. Mg (Z = 12).
(Xem giải) Câu 4. Một nhóm nghiên cứu về tốc độ phản ứng đã tiến hành hai thí nghiệm với vụn đá hoa (thành phần chính là Calcium carbonate) và dung dịch hydrochloric acid.
Thí nghiệm 1: Dùng 0,5 gam vụn đá hoa và 50mL dung dịch hydrochloric acid 1M.
Thí nghiệm 2: Dùng 0,5 gam vụn đá hoa đã được nghiền nhỏ và 50mL dung dịch hydrochloric acid 1M.
Sau đó, nhóm nghiên cứu đã đo thể tích khí sinh ra theo thời gian và xây dựng đồ thị như hình dưới.
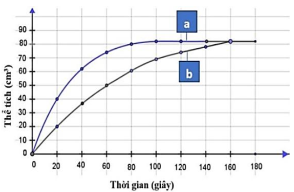
Nhận định nào sau đây là sai?
A. Tốc độ phản ứng trung bình trong 80 giây đầu tiên của thí nghiệm 1 và 2 lần lượt là 0,75 (cm³/s) và 1(cm³/s).
B. Thí nghiệm 1 có đồ thị ứng với đường (b), thí nghiệm 2 ứng với đường (a).
C. Tốc độ thoát khí ở thí nghiệm 1 lớn hơn ở thí nghiệm 2.
D. Trong khoảng thời gian từ 160 giây đến 180 giây, lượng khí thoát ra ở cả hai thí nghiệm không thay đổi.
(Xem giải) Câu 5. Ammonia có nhiều ứng dụng như sản xuất nitric acid, sản xuất phân đạm, làm dung môi, chất gây lạnh,… Trong công nghiệp, quá trình sản xuất ammonia được thực hiện theo phản ứng sau: N2(g) + 3H2(g) ⇌ 2NH3(g) ![]() = –92 kJ
= –92 kJ
Biện pháp được áp dụng để tăng hiệu suất tổng hợp NH3 là
A. Tăng áp suất. B. Tăng nhiệt độ.
C. Giảm nồng độ khí N2. D. Giảm áp suất.
(Xem giải) Câu 6. Cho sơ đồ chuyển hoá sau:
![]()
Biết X, Y, Z, T, E là các hợp chất khác nhau, mỗi mũi tên ứng với một phương trình hoá học. Các chất Z, E thoả mãn sơ đồ trên lần lượt là
A. CO2, KHSO4. B. NaHCO3, Na2CO3. C. Na2CO3, H2SO4. D. CO2, BaSO4.
(Xem giải) Câu 7. Cách nào sau đây không thể làm mềm nước có tính cứng vĩnh cửu?
A. Dùng phương pháp trao đổi ion. B. Dùng dung dịch Na2CO3.
C. Dùng dung dịch Na3PO4. D. Đun sôi nước.
(Xem giải) Câu 8. Hợp chất X không phải là hoạt chất thiết yếu đối với cơ thể người, vì cơ thể có thể tự tổng hợp được. X có công thức cấu tạo như hình bên.
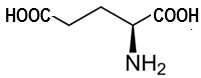
Tên gọi của hợp chất X là
A. Glycine. B. Glutamic acid. C. Alanine. D. Lysine.
(Xem giải) Câu 9. LDPE là một chất dẻo dễ tạo màng, có tính dai bền nên được sử dụng làm túi nylon, màng bọc, bao gói thực phẩm. LDPE thuộc nhóm nhựa PE (polyethylene) và thường được nhận biết qua ký hiệu đặc trưng in trên bao bì như hình bên.

LDPE được tổng hợp từ monomer nào đây?
A. CH2=CH-C6H5. B. CH2=CH2. C. CH2=CH-Cl. D. CH2=CH-CH3.
(Xem giải) Câu 10. Hạt nhân ![]() sau một chuỗi các quá trình phóng xạ α và β− liên tiếp biến đổi thành hạt nhân
sau một chuỗi các quá trình phóng xạ α và β− liên tiếp biến đổi thành hạt nhân ![]() bền theo phương trình chuỗi phản ứng:
bền theo phương trình chuỗi phản ứng: ![]() →
→ ![]() + x
+ x![]() + y
+ y![]() .
.
Trong đó, x và y lần lượt là số lần phóng xạ α và β- trong chuỗi phóng xạ. Giá trị của y là
A. y = 6. B. y = 4. C. y = 8. D. y = 5.
(Xem giải) Câu 11. Chất nào sau đây không phải là ester?
A. CH3COO[CH2]7CH3 (có trong quả cam).
B. CH3COOH (có trong giấm ăn).
C. CH3COOCH2C6H5 (có trong hoa nhài).
D. CH3[CH2]14COO[CH2]29CH3 (có trong mật ong).
(Xem giải) Câu 12. Tiến hành các thí nghiệm sau:
(a) Điện phân dung dịch CuSO4.
(b) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
(c) Nhiệt phân hoàn toàn CaCO3.
(d) Cho kim loại Mg vào lượng dư dung dịch FeCl3.
(e) Dẫn khí H2 dư đi qua bột CuO nung nóng.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kim loại là
A. 3. B. 2. C. 4. D. 1.
(Xem giải) Câu 13. Khí thiên nhiên là nhiên liệu hoá thạch, thường được tìm thấy cùng với các mỏ dầu trong vỏ Trái Đất. Thành phần chính của “khí thiên nhiên” là
A. Ethane. B. Methane. C. Propane. D. Butane.
(Xem giải) Câu 14. Kim loại chuyển tiếp dãy thứ nhất và hợp kim của chúng được sử dụng phổ biến trong chế tạo dụng cụ, thiết bị và phương tiện giao thông nhờ vào các tính chất đặc trưng. Nhận xét nào sau đây là đúng?
A. Trong các kim loại chuyển tiếp dãy thứ nhất, chromium dẫn điện tốt nhất.
B. Sắt thuộc nhóm kim loại nặng và có nhiệt độ nóng chảy cao nhất trong dãy kim loại chuyển tiếp thứ nhất.
C. Các đơn chất kim loại có khối lượng riêng lớn sẽ có độ cứng cao.
D. Chromium có độ cứng cao nên được dùng mạ lên các thiết bị để chống mài mòn.
(Xem giải) Câu 15. Quan sát hình dưới đây:

Trong điều kiện thí nghiệm ở pH = 6, cho các phát biểu sau:
(a) Lysine dịch chuyển về phía cực âm nên lysine tồn tại chủ yếu ở dạng cation.
(b) Glycine hầu như không dịch chuyển nên glycine tồn tại chủ yếu ở dạng ion lưỡng cực.
(c) Glutamic acid dịch chuyển về phía cực dương nên glutamic acid tồn tại chủ yếu ở dạng anion.
(d) Thí nghiệm trên chứng minh tính điện li của các phân tử amino acid.
Số phát biểu đúng là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 16. Carbohydrate là chất dinh dưỡng đa lượng cung cấp năng lượng cho cơ thể. Carbohydrate bao gồm đường, tinh bột và chất xơ có trong thực phẩm. Trong mật ong, carbohydrate có hàm lượng nhiều nhất (chiếm khoảng 40%) và làm cho mật ong có vị ngọt sắc là
A. Fructose. B. Tinh bột. C. Saccharose. D. Cellulose.
(Xem giải) Dựa vào thông tin dưới đây để trả lời các câu hỏi từ câu 17 – 18:
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
| Cặp | Al3+/Al | Zn2+/Zn | Fe2+/Fe | Cu2+/Cu | Ag+/Ag |
| E° (V) | -1,676 | -0,763 | -0,440 | 0,340 | 0,799 |
Câu 17. Dựa trên bảng thế điện cực chuẩn cho ở trên thì phản ứng nào dưới đây là sai?
A. Zn + Fe2+ → Zn2+ + Fe. B. Al + 3Ag+ → Al3+ + 3Ag.
C. Cu + Fe2+ → Fe + Cu2+. D. Fe + Cu2+ → Fe2+ + Cu.
Câu 18. Sức điện động chuẩn của một pin Galvani được thiết lập từ hai cặp oxi hóa – khử trong số các cặp trên có giá trị 2,475V. Hai cặp oxi hóa – khử hình thành pin lần lượt là
A. Al3+/Al và Cu2+/Cu. B. Zn2+/Zn và Al3+/Al.
C. Al3+/Al và Ag+/Ag. D. Fe2+/Fe và Cu2+/Cu.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Vôi sống (CaO) có nhiều ứng dụng như: sản xuất vật liệu xây dựng, vật liệu chịu nhiệt, khử chua đất trồng, tẩy uế, sát trùng, xử lí nước thải,… Tuy nhiên, các lò nung vôi thủ công hoạt động tự phát có thể gây ô nhiễm môi trường. Ở các lò nung vôi công nghiệp, quy trình kiểm soát phát thải được thực hiện chặt chẽ hơn. Khảo sát một lò nung vôi công nghiệp sử dụng than đá làm nhiên liệu, giả thiết:
– Đá vôi chỉ chứa CaCO3 và cần cung cấp một nhiệt lượng 1800 kJ để phân hủy 1 kg đá vôi.
– Đốt cháy 1 kg than đá giải phóng một nhiệt lượng là 27000 kJ, trong đó 50% lượng nhiệt này được hấp thụ để phân hủy đá vôi.
– Than đá chứa 1% sulfur (ở dạng vô cơ và hữu cơ như FeS2, CaSO4, CxHySH,…) về khối lượng, 80% lượng sulfur bị đốt cháy tạo thành SO2 và 1,6% SO2 sinh ra phát thải vào khí quyển.
– Lò có công suất 420 tấn CaO/ngày.
Nhóm nghiên cứu đã đưa ra các kết luận:
a) Phản ứng nhiệt phân đá vôi là phản ứng tỏa nhiệt.
b) Giả thiết toàn bộ lượng SO2 phát thải trong 30 ngày từ lò nung vôi trên chuyển hết thành H2SO4 trong nước mưa với nồng độ là 2.10-5M. Nếu lượng nước mưa này rơi đều trên một vùng đất rộng 40 km², sẽ tạo ra một trận mưa acid với lượng mưa trung bình là 15 mm.
c) Lượng đá vôi cần sử dụng mỗi ngày là 750 tấn.
d) Lượng than đá tiêu thụ mỗi ngày là 100 tấn.
(Xem giải) Câu 20. Ngô và mía là hai nguyên liệu chính được sử dụng trong sản xuất ethanol. Tuy nhiên, chúng là những loại cây lương thực quan trọng. Trong khi đó, cellulose – một nguồn nguyên liệu dồi dào và dễ tìm – cũng có thể dùng để sản xuất ethanol. Tuy giá thành sản xuất ethanol từ cellulose còn cao, do quá trình nuôi cấy nấm sản sinh enzyme cellulase để thuỷ phân cellulose thành glucose tốn kém nhiều năng lượng, nhưng đây vẫn là một hướng đi đầy hứa hẹn trong tương lai.
a) Với những tiến bộ công nghệ đạt được, người ta tin rằng 0,81 tấn cellulose có thể sản xuất được 345 lít ethanol. Khi đó, hiệu suất của quá trình đạt 60% (cho biết khối lượng riêng của ethanol là 0,8 g/mL).
b) Cellulose là một polymer mạch không phân nhánh.
c) Phân tử cellulose được tạo thành từ nhiều đơn vị α-glucose, nối với nhau qua liên kết α-1,4-glycoside.
d) Cellulose có nhiều trong trái cây chín.
(Xem giải) Câu 21. Hoạt tính xúc tác của enzyme càng cao, tốc độ thủy phân protein càng lớn. Hoạt tính enzyme phụ thuộc vào các yếu tố như nhiệt độ, pH,… Một nhóm học sinh đã khảo sát ảnh hưởng của pH đến hoạt tính của enzyme tiêu hoá protein ở người. Nhóm tiến hành thí nghiệm thuỷ phân albumin (protein có trong lòng trắng trứng) bằng enzyme pepsin ở nhiệt độ không đổi nhưng thay đổi pH của môi trường. Kết quả thu được như sau:
| Ống nghiệm | Thành phần | Thời điểm t = 0 (phút) | Thời điểm t = 20 (phút) |
| 1 | Albumin + Pepsin + HCl 0,01M | Đục | Trong |
| 2 | Albumin + Pepsin + H2O | Đục | Đục |
| 3 | Albumin + Pepsin + NaHCO3 0,01M | Đục | Đục |
Sau đó, nhóm học sinh tiến hành thí nghiệm tương tự với enzyme chymotrypsin, thu được đồ thị như hình bên.
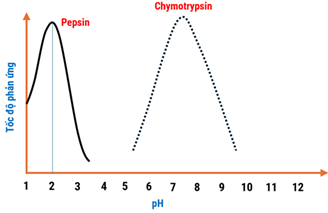
Từ kết quả thí nghiệm, nhóm học sinh đã đưa ra các nhận định sau:
a) Albumin là protein dạng sợi, không tan trong nước nên ban đầu dung dịch bị đục.
b) Pepsin hoạt động tốt nhất ở pH = 2.
c) Từ kết quả thí nghiệm thì enzyme pepsin và chymotrypsin đều hoạt động tốt trong môi trường acid.
d) Ở ống nghiệm 3, nếu thay Pepsin thành Chymotrypsin thì hiện tượng quan sát được là “từ đục thành trong” sau thí nghiệm.
(Xem giải) Câu 22. Pin nhiên liệu hydrogen là một nguồn sản xuất điện sạch với hiệu suất cao. Pin hoạt động thông qua phản ứng điện hoá giữa nhiên liệu là hydrogen và chất oxi hoá là oxygen. Khi pin hoạt động, hydrogen có vai trò tương tự như kim loại mạnh hơn trong pin Galvani; ở cathode, oxygen nhận electron và kết hợp với ion H+ để tạo thành nước. Dòng electron di chuyển qua mạch ngoài tạo ra dòng điện, cung cấp năng lượng cho các thiết bị hoặc động cơ.
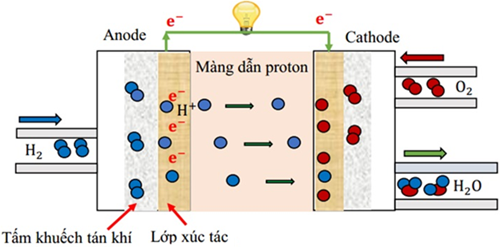
a) Tại cực dương xảy ra quá trình khử: O2 + 4H+ + 4e → 2H2O.
b) Ưu điểm của pin nhiên liệu hydrogen là giá thành rẻ.
c) Phản ứng điện hoá xảy ra trong pin: 2H2 + O2 → 2H2O
d) Giả thiết, một ô tô chạy bằng pin nhiên liệu hydrogen đã nạp vào 0,450 kg H2. Khi vận hành, pin hoạt động với hiệu suất 60% và tạo ra dòng điện có cường độ trung bình 250A để cung cấp cho động cơ. Giả sử không có tổn hao nào khác và các điều kiện khác đầy đủ, thời gian tối đa mà xe có thể chạy liên tục là 28,95 giờ. (Cho biết: điện tích của 1 mol electron là 96500 C/mol; công thức: q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s)).
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Trong công nghiệp, một lượng lớn Na2CO3 (soda ash) và NaHCO3 (backing soda) được sản xuất bằng phương pháp Solvay theo các phương trình hoá học sau:
CaCO3 (t°) → CaO + CO2 (1)
CO2 + H2O + NH3 + NaCl ⇋ NH4Cl + NaHCO3 (2)
2NaHCO3 (t°) → Na2CO3 + CO2 + H2O (3)
2NH4Cl + CaO → 2NH3 + CaCl2 + H2O (4)
Xét các phát biểu sau:
(1) Nguyên liệu chính được sử dụng trong quá trình sản xuất là: NaCl, NH3, CaCO3 và H2O.
(2) Thợ làm bánh dùng Na2CO3 để tạo độ xốp cho bánh nhờ khả năng giải phóng khí và hơi khi bị nhiệt phân hủy của Na2CO3.
(3) Phản ứng (2) xảy ra được là do NaHCO3 có độ tan thấp hơn nên bị kết tinh trước.
(4) Một nhà máy sản xuất soda ash theo phương pháp Solvay sử dụng 1170 kg NaCl (giả thiết không có tạp chất) và thực tế thu được 901 kg Na2CO3, vậy hiệu suất của cả quá trình là 85%.
(5) Phản ứng (3) giải phóng lượng CO2 không vượt quá một nửa lượng đã dùng, khí này được thu hồi và tái sử dụng trong quá trình sản xuất.
Liệt kê các phát biểu đúng theo thứ tự tăng dần (ghi đáp án dạng các chữ số liên tiếp, ví dụ: 1345; 23; 345…).
(Xem giải) Câu 24. PBS – Poly(butylene succinate), có tên thương mại Bionolle, là một polymer phân huỷ sinh học có tính dẻo và bền nhiệt tương tự polyethylene (PE). Nhờ cấu trúc mạch chính chứa các nhóm ester dễ bị thủy phân, PBS có khả năng phân rã trong môi trường tự nhiên. Với đặc tính này, PBS được ứng dụng rộng rãi trong sản xuất bao bì và túi nylon thân thiện với môi trường, trở thành giải pháp tiềm năng thay thế các loại nhựa truyền thống khó phân huỷ. PBS được tổng hợp bằng phản ứng trùng ngưng giữa hai monomer sau:
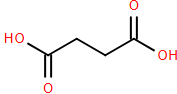
![]()
Tính khối lượng của một mắt xích polymer PBS theo đơn vị amu.
(Xem giải) Câu 25. Cyanide (CN-) là một hoá chất cực độc nhưng vẫn được dùng trong ngành khai thác vàng nhờ khả năng tạo phức mạnh. Một công ty khai thác vàng sử dụng potassium cyanide (KCN) để hoà tan vàng từ quặng, để đảm bảo hiệu quả khai thác và giảm thiểu rủi ro môi trường, họ cần kiểm tra độ tinh khiết của KCN trước khi sử dụng. Hàm lượng ion cyanide có thể xác định bằng phương pháp chuẩn độ Liebig: dùng dung dịch AgNO3 0,1 M làm chất chuẩn.
Phương trình phản ứng chuẩn độ: 2CN- + Ag+ ⇋ Ag(CN)2-
Tại điểm tương đương (phản ứng không làm ảnh hưởng đến thể tích chất chuẩn):
Ag(CN)2- + Ag+ ⇋ Ag[Ag(CN)2]
Một kỹ thuật viên đã thực hiện xác định độ tinh khiết của 0,650 gam mẫu KCN với dung dịch AgNO3 0,1 M.
Chuẩn độ 3 lần thì cho kết quả như sau:
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích chất chuẩn đã dùng (mL) | 43,85 | 44,05 | 44,10 |
Tính độ tinh khiết (%) của mẫu KCN trên (kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 26. Một viên dầu cá “Now Omega-3 Fish Oil” chứa 1000 mg dầu cá, trong đó có 180 mg EPA + 120 mg DHA. Các nghiên cứu cho thấy, việc bổ sung omega-3 liều cao kết hợp EPA + DHA mỗi ngày có thể làm giảm các triệu chứng trầm cảm và lo âu. Một bệnh nhân được chỉ định dùng 1200 mg EPA + DHA mỗi ngày trong suốt 9 tháng (coi như 1 tháng có 30 ngày). Biết rằng cửa hàng không bán lẻ từng viên, hãy tính số lọ dầu cá “Now Omega-3 Fish Oil” loại 100 viên cần mua để đủ liệu trình.
(Xem giải) Câu 27. Naftifine là một chất có tác dụng chống nấm, thường được dùng dưới dạng muối naftifine hydrochloride. Naftifine có cấu tạo như hình dưới đây:
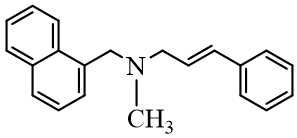
Naftifine thuộc loại amine bậc mấy?
(Xem giải) Câu 28. Bằng cách sử dụng điện cực làm bằng Pt biến tính và chất điện giải NaBr, ta có được một chu trình kết hợp giữa quá trình điện phân và xúc tác để thu được H2 và O2 một cách có hiệu quả.
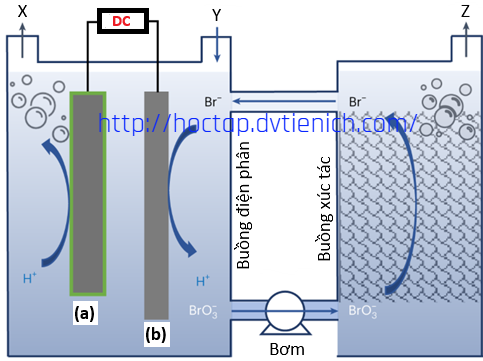
Sơ đồ thiết bị được mô tả như hình trên, biết quá trình xảy ra ở điện cực (b) như sau:
Br- + 3H2O → BrO3- + 6H+ + 6e.
Cho các phát biểu sau:
(1) Tỉ lệ sản phẩm trong pha xúc tác là nZ : nBr- = 3 : 2.
(2) X là khí H2, Z là khí O2.
(3) Điện cực (a) mắc vào cực âm của nguồn.
(4) Phương trình phản ứng trong bình điện phân của hệ là: NaBr + 3H2O → NaBrO3 + 3H2.
(5) Mục đích của việc thêm Y là bổ sung NaBr.
Liệt kê các phát biểu đúng theo thứ tự tăng dần (ghi đáp án dạng các chữ số liên tiếp, ví dụ: 1345; 23; 345…).


Bình luận