[2025] Thi thử TN sở GDĐT Bình Phước (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 063
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2D | 3A | 4C | 5C | 6C | 7D | 8B | 9A |
| 10C | 11B | 12B | 13A | 14D | 15A | 16A | 17C | 18B |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | S | Đ | Đ | 1120 | 0,75 | 2 |
| (b) | Đ | S | S | Đ | 26 | 27 | 28 |
| (c) | S | Đ | S | S | 34 | 234 | 123 |
| (d) | S | Đ | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Xét quá trình điện phân dung dịch NaCl bão hoà không có màng ngăn. Phát biểu nào sau đây đúng?
A. Quá trình xảy ra tại cathode là Na+ + 1e → Na
B. Quá trình xảy ra tại anode là 2H2O + 2e → H2 + 2OH-
C. Dung dịch thu được sau phản ứng là dung dịch NaOH.
D. Cho mẩu giấy màu vào dung dịch sau phản ứng thấy mẩu giấy mất màu.
(Xem giải) Câu 2. Chất thải nhựa và túi nylon (PE, PVC…) gây ảnh hưởng nghiêm trọng đến môi trường còn gọi là “ô nhiễm trắng”. Giải pháp nào sau đây không giúp giảm thiểu tác động của rác thải nhựa đến môi trường?
A. Phân loại rác thải nhựa từ đầu nguồn để tái chế.
B. Tái sử dụng đồ nhựa, chai nhựa làm đồ dùng.
C. Thay thế túi lylon bằng túi giấy, túi vải tái sử dụng nhiều lần.
D. Tiêu huỷ các chất thải nhựa và túi nylon bằng phương pháp đốt hoặc chôn lấp.
(Xem giải) Câu 3. Trong thí nghiệm xác định hàm lượng muối Fe(II) bằng dung dịch thuốc tím, nhận xét nào sau đây là không đúng?
A. Dung dịch muối Fe(II) có màu vàng nhạt. B. Ion Fe2+ là chất bị oxi hóa.
C. Ion MnO4- là chất bị khử. D. H2SO4 là chất tạo môi trường phản ứng.
(Xem giải) Câu 4. Khi nói về liên kết kim loại: “ Liên kết kim loại là liên kết hình thành do lực hút tĩnh điện giữa các electron…(1)… với các ion…(2)… kim loại ở các nút mạng. Các từ cần điền vào vị trí (1), (2) để được phát biểu đúng là
A. ngoài cùng, dương B. hóa trị, lưỡng cực.
C. tự do, dương. D. hóa trị, âm.
(Xem giải) Câu 5. Ăn mòn kim loại là hiện tượng phổ biến trong đời sống hàng ngày. Phương pháp nào sau đây có thể góp phần hạn chế sự ăn mòn kim loại?
A. Cuốn sợi dây đồng vào thanh sắt hoặc thanh nhôm.
B. Sử dụng giấy ráp đánh sạch bề mặt kim loại sau mỗi khoảng thời gian nhất định.
C. Phủ một lớp sơn hoặc lớp dầu mỡ lên bề mặt của vật dụng kim loại.
D. Dùng nước muối ăn để diệt các vi khuẩn bám trên bề mặt của các vật dụng kim loại.
(Xem giải) Câu 6. Xử lí chất thải trong chăn nuôi gia súc bằng hầm biogas hoặc túi biogas vừa giảm ô nhiễm môi trường vừa giúp tiết kiệm nhiên liệu. Phương pháp này tiết kiệm nhiên liệu vì khí biogas
A. chứa nhiều C2H5OH, dễ cháy tỏa nhiều nhiệt.
B. chứa nhiều Cl2, vì khả năng sát khuẩn.
C. chứa nhiều CH4, dễ cháy tỏa nhiều nhiệt.
D. chứa nhiều CH4, không độc hại với môi trường.
(Xem giải) Câu 7. Một người thợ sơn cần lựa chọn một dung môi dễ bay hơi và có độ phân cực kém pha vào sơn giúp sơn nhanh khô khi sử dụng. Chất nào sau đây phù hợp?
A. Glucose. B. Nước. C. Acetic acid. D. Isoamyl acetate.
(Xem giải) Câu 8. Cho biết thế điện cực chuẩn của các cặp oxi hoá – khử Zn2+/Zn, Cu2+/Cu lần lượt là -0,76 V và 0,34 V. Sức điện động chuẩn của pin Galvani Zn-Cu có giá trị bằng
A. 0,42. B. 1,10. C. 0,76. D. 0,34.
(Xem giải) Câu 9. Một học sinh thiết lập một pin điện hóa gồm hai mảnh kẽm (Zn) và đồng (Cu) cắm vào một quả chanh và sau đó nối với đầu bên ngoài một ampe kế, thấy kim chỉ thị lệch khỏi vạch 0 (hình vẽ)

Quá trình nào có thể xảy ra tại điện cực đồng?
A. Khử H+ thành khí H2. B. Khử Cu2+ thành Cu.
C. Khử Zn2+ thành Zn. D. Oxi hóa H2O thành O2.
(Xem giải) Câu 10. Sodium hydrogencarbonate là chất được dùng làm bột nở, chế thuốc trị hỗ trợ triệu chứng đau dạ dày do thừa acid. Công thức của sodium hydrogencarbonate là
A. Na2CO3. B. NaOH. C. NaHCO3. D. NaHS.
(Xem giải) Câu 11. Hợp chất nào sau đây là amino acid?
A. HOCH2COOH. B. H2NCH(CH3)COOH.
C. H2NCH2COOCH3. D. CH3NHCH2CH3.
(Xem giải) Câu 12. Một số cơ sở sản xuất dùng formol để giúp các sản phẩm như bún, bánh phở, mì…lâu bị mốc, hỏng vì formol có tính năng diệt khuẩn mạnh, tuy nhiên formol rất độc hại với sức khoẻ con người (gây ung thư), thuộc danh mục hóa chất bị cấm sử dụng trong thực phẩm. Formol là dung dịch của chất nào sau đây?
A. Acetone. B. Formaldehyde. C. Methanol. D. Phenol.
(Xem giải) Câu 13. Nhỏ vài giọt dung dịch iodine vào dung dịch nào sau đây thì thấy xuất hiện màu xanh tím?
A. Hồ tinh bột. B. Glucose. C. Saccharose. D. Lòng trắng trứng.
(Xem giải) Câu 14. Phản ứng chlorine hóa methane khi chiếu sáng xảy ra theo cơ chế gốc gồm ba giai đoạn: khơi mào, phát triển mạch và tắt mạch. Trong đó, giai đoạn phát triển mạch diễn ra như sau:
Cl• + CH4 → HCl + •CH3
•CH3 + Cl2 → CH3Cl + Cl•
Nhận định nào sau đây không đúng về giai đoạn này?
A. Có sự hình thành liên kết H-Cl. B. Có sự hình thành liên kết C-Cl.
C. Có sự phân cắt liên kết C-H. D. Có sự hình thành liên kết Cl-Cl.
(Xem giải) Câu 15. Cho các polymer sau: PE, PVC, cao su buna, poly(methyl methacrylate), tơ olon, tơ nylon-6,6. Số polymer được điều chế bằng phản ứng trùng hợp là
A. 5. B. 2. C. 4. D. 3.
(Xem giải) Câu 16. Thủy phân hoàn toàn tinh bột trong môi trường acid, thu được chất nào sau đây?
A. Glucose. B. Saccharose. C. Glycerol. D. Ethyl alcohol.
(Xem giải) Câu 17. Trong mật ong, carbohydrate có hàm lượng nhiều nhất (chiếm khoảng 40%) và làm cho mật ong có vị ngọt sắc là
A. cellulose. B. saccharose. C. fructose. D. tinh bột.
(Xem giải) Câu 18. Acid béo omega-3 và omega-6 đều có vai trò quan trọng đối với cơ thể, giúp phòng ngừa nhiều loại bệnh. Chất nào sau đây thuộc loại acid béo omega-3?
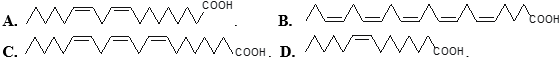
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Cho vào ống nghiệm khoảng 1 mL CuSO4 0,5 M, sau đó thêm từ từ dung dịch HCl đặc, vừa cho vừa lắc ống nghiệm. Xảy ra quá trình sau: [Cu(H2O)6]2+ + 4Cl- ⇋ [CuCl4]2- + 6H2O
a) Số oxi hóa của Cu trong hai phức [Cu(H2O)6]2+ và [CuCl4]2- lần lượt là +2 và -2.
b) Phản ứng trên là phản ứng thay thế phối tử của phức chất trong dung dịch.
c) Khi thêm từ từ dung dịch HCl thì cân bằng dần chuyển dịch sang trái.
d) Phối tử của hai phức [Cu(H2O)6]2+ và [CuCl4]2- lần lượt là H2O và HCl.
(Xem giải) Câu 20. Cho các dữ kiện thực nghiệm về hợp chất hữu cơ đơn chức X, thường được sử dụng làm dung môi, hương liệu:
– Thành phần khối lượng nguyên tố: %C = 54,55%; %H = 9,10%; %O = 36,35%.
– Nhiệt độ nóng chảy là –83,8 °C, nhiệt độ sôi là 77,1 °C.
– Ở 20°C, khối lượng riêng D = 0,90 g/cm³ và độ tan là 8,3 gam/100 gam nước.
– Phổ hồng ngoại và phổ khối lượng:
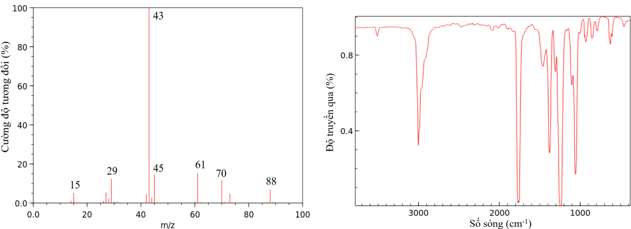
a) X bị thủy phân hoàn toàn trong cả môi trường acid và môi trường kiềm.
b) Ở 20°C, dung dịch X bão hòa có nồng độ phần trăm là 8,3%.
c) X là ester no, đơn chức, mạch hở.
d) X có công thức phân tử là C4H8O2.
(Xem giải) Câu 21. Một học sinh tiến hành thí nghiệm để so sánh tính base trong dung dịch nước của một số amine và ammonia với dự đoán: “Khi số nguyên tử carbon trong phân tử amine tăng thì tính base của amine tăng, pH của dung dịch amin trong nước tăng”. Học sinh tiến hành như sau:
Chuẩn bị các cốc chứa dung dịch nồng độ 0,1M của các chất ở 25°C: NH3; CH3NH2; CH3CH2NH2; (CH3)2NH; CH3CH2CH2NH2. Dùng máy đo pH để do giá trị pH của các dung dịch. Đồ thị thể hiện kết quả thu được như sau:
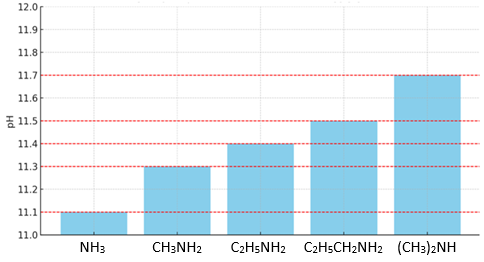
a) Biết Kb = [C2H5NH3+][OH-]/[C2H5NH2] là hằng số cân bằng của quá trình: C2H5NH2 + H2O ⇋ C2H5NH3+ + OH-. Giá trị Kb ở 25°C tính được từ kết quả là 6,5.10^-5.
b) (CH3)2NH có tên thường là ethylamine.
c) Từ kết quả thí nghiệm kết luận được giả thuyết ban đầu của học sinh là hoàn toàn đúng.
d) NH3 có tính base yếu hơn các amine được khảo sát.
(Xem giải) Câu 22. Một học sinh tiến hành thí nghiệm với giả thuyết: “Độ tan của CaSO4 tăng khi tăng nhiệt độ” như sau:
• Bước 1: Thêm lượng dư CaSO4.2H2O (3 gam) vào 100 mL nước cất trong các bình riêng biệt. Đặt mỗi bình ở các mức nhiệt độ khác nhau (cụ thể: 20°C, 40°C, 60°C, 80°C). Khuấy đều trong 15–20 phút để đạt cân bằng (đảm bảo vẫn còn chất rắn dư). Duy trì nhiệt độ ổn định ít nhất 10 phút trước khi lọc.
• Bước 2: Lọc nhanh dung dịch bão hòa trong khi vẫn giữ ở nhiệt độ ổn định như ban đầu. Thu lấy phần dịch lọc.
• Bước 3: Lấy 25 mL dung dịch đã lọc và làm bay hơi hết nước rồi cân phần chất khan rắn còn lại. Tính độ tan theo đơn vị gam chất tan trong 100 mL nước (xem thể tích thay đổi không đáng kể trong quá trình hòa tan).
Kết quả như sau:
| Nhiệt độ (°C) | Độ tan của CaSO4 (g/100 mL nước) |
| 20 | 0,285 |
| 40 | 0,168 |
| 60 | 0,162 |
| 80 | 0,155 |
a) Học sinh lọc dung dịch bão hòa trong điều kiện giữ nhiệt độ ổn định với mục đích tránh kết tinh muối làm sai lệch kết quả.
b) Mục tiêu của thí nghiệm là xác định sự thay đổi độ tan CaSO4 theo nhiệt độ.
c) Từ kết quả cho thấy giả thuyết ban đầu của học sinh là đúng.
d) Ở 40°C, khối lượng chất rắn thu được ở bước 3 là 0,168 gam.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Theo Quy chuẩn Việt Nam về nước sinh hoạt (QCVN 01-1-2018/BYT):
• Tổng nồng độ ion iron (sắt) trong nước uống: ≤ 0,3 mg/L
• Tổng nồng độ ion iron (sắt) trong nước sinh hoạt (tắm, giặt, rửa): ≤ 0,5 mg/L
Nước suối ở những vùng nằm trên nền địa chất có nhiều quặng sắt thường có nồng độ ion sắt rất cao.
Chuẩn độ 20 mL một mẫu nước suối (ở Tây ban Nha), bằng dung dịch KMnO4 0,01M trong môi trường H2SO4 đến khi dung dịch chuyển sang màu hồng (bền trong 20 giây) thì thể tích dung dịch KMnO4 đã dùng là 4 mL. Hỏi nồng độ Fe2+ (mg/L) trong mẫu nước suối đã này vượt gấp bao nhiêu lần so với tổng nồng độ ion sắt tối đa cho phép đối với nước sinh hoạt theo quy chuẩn của Bộ Y tế Việt Nam? (Làm tròn số đến hàng đơn vị)
(Xem giải) Câu 24. Một hợp chất (A) chứa nitrogen có trong cơ thể người và là chất chống oxy hóa quan trọng, bảo vệ tế bào khỏi tổn thương. Công thức của (A) như sau
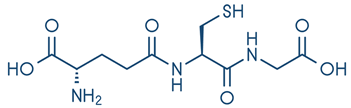
Biết rằng 1 nhóm S-H phản ứng với 1 phân tử NaOH. Khi đun nóng 0,15 mol (A) với dung dịch NaOH thì số mol NaOH phản ứng tối đa là bao nhiêu mol? (Làm tròn số đến hàng phần trăm)
(Xem giải) Câu 25. Ester X có công thức phân tử là C5H10O2¸ xà phòng hóa X bằng dung dịch NaOH thì thu được sodium acetate. Có bao nhiêu đồng phân cấu tạo phù hợp với X?
(Xem giải) Câu 26. Cho các nhận định sau
(1) Cellulose là một loại carbohydrate phổ biến trong thực vật, bị thủy phân thành glucose nên được dùng làm thức ăn cung cấp dinh dưỡng cho cơ thể.
(2) Glycerol là carbohydrate được lưu trữ trong gan và cơ bắp giúp cung cấp năng lượng nhanh chóng cho cơ khi cần.
(3) Quá trình tổng hợp glucose và tinh bột trong cây xanh giúp giảm lượng khí gây hiệu ứng nhà kính trong không khí.
(4) Nước tiểu của người bệnh tiểu đường (đái tháo đường) chứa hàm lượng đường cao, chủ yếu là glucose.
Hãy sắp xếp các phát biểu đúng theo số thứ tự từ nhỏ đến lớn tăng dần (ví dụ: 12, 134,..).
(Xem giải) Câu 27. Để xác định hàm lượng vàng trong một loại vàng hồng (là hợp kim của Au, Cu) người ta tiến hành cân chính xác một mẩu vàng hồng nặng m1 gam, sau đó ngâm mẩu này trong lượng dư dung dịch chất X đến khi khối lượng chất rắn không thay đổi, lọc lấy phần rắn còn lại, rửa sạch làm khô, cân lại được m2 gam và hàm lượng vàng như sau: %Au = 100%.m2/m1
Cho các chất: (1) AgNO3, (2) FeCl3, (3) HNO3, (4) H2SO4 đặc, (5) HCl, (6) AuCl3. Hãy sắp xếp các chất phù hợp với X theo số thứ tự tăng dần (ví dụ: 12, 134, 1456, …).
(Xem giải) Câu 28. Hai chất MnO2 và Fe2O3 đều có khả năng xúc tác cho phản ứng phân hủy H2O2. Đo nồng độ H2O2 theo thời gian, thu được đồ thị sau:
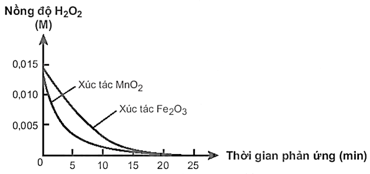
(1) Khi dùng xúc tác MnO2 và Fe2O3 đều làm tăng tốc độ phản ứng.
(2) Trong quá trình phản ứng nồng độ của H2O2 giảm dần.
(3) Xúc tác MnO2 có hiệu quả cao hơn vì đồ thị nồng độ H2O2 theo thời gian khi có mặt MnO2 dốc hơn khi có Fe2O3.
(4) Sau phản ứng khối lượng MnO2 và Fe2O3 giảm.
Hãy sắp xếp các phát biểu đúng theo số thứ tự tăng dần (ví dụ: 12, 134, …).


Bình luận