[2026] Thi thử TN chuyên KHTN Hà Nội (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 067
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2A | 3B | 4C | 5B | 6D | 7A | 8C | 9C |
| 10D | 11A | 12A | 13BD | 14B | 15D | 16D | 17D | 18B |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | S | ||||
| (b) | Đ | Đ | Đ | 26 | 27 | 28 | |
| (c) | S | Đ | Đ | ||||
| (d) | S | S | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Ở điều kiện thường, trong các kim loại sau kim loại nào thể hiện tính dẻo tốt nhất?
A. Ag. B. Cu. C. Al. D. Au.
(Xem giải) Câu 2: Trong phức chất, số liên kết σ (sigma) tạo thành giữa một phối tử với nguyên tử trung tâm được gọi là dung lượng phối trí của phối tử đó. Cấu tạo của phức chất [Fe(C2O4)3]3-) được cho ở hình dưới đây.
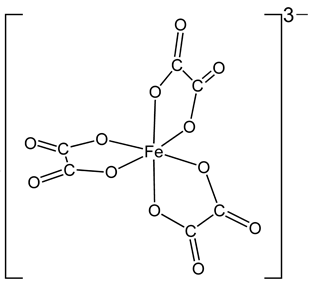
Dung lượng phối trí của mỗi phối tử C2O42- trong phức chất đã cho là
A. 2. B. 6. C. 3. D. 1.
(Xem giải) Câu 3: Phương pháp nào sau đây thường được dùng để nhận biết sự có mặt của ion K+ (aq)?
A. Phương pháp kết tinh. B. Phương pháp thử màu ngọn lửa.
C. Phương pháp điện phân. D. Phương pháp trao đổi ion.
(Xem giải) Câu 4: Phản ứng điều chế isoamyl acetate (dầu chuối) từ acetic acid, isoamyl alcohol, xúc tác H2SO4 đặc thuộc loại phản ứng
A. hydrogen hoá. B. trùng ngưng. C. ester hoá. D. hydrate hoá.
(Xem giải) Câu 5: Trên phổ khối lượng của ester X xác định được peak ion phân tử [X+] với m/z = 88. Công thức phù hợp với X là
A. C5H11OH. B. CH3COOC2H5. C. C3H7COOH. D. HCOOC2H5.
(Xem giải) Câu 6: Tên gọi theo danh pháp thay thế của chất có công thức cấu tạo CH3-CHOH-CH3 là
A. isopropyl alcohol. B. propan-2-one. C. propanoic acid. D. propan-2-ol.
(Xem giải) Câu 7: Cho các phản ứng sau:
(1) CuO + H2 → Cu + H2O;
(2) 2CuSO4 + 2H2O → 2Cu + O2 + 2H2SO4;
(3) Fe + CuSO4 → FeSO4 + Cu;
(4) 2Al + Cr2O3 → Al2O3 + 2Cr.
Số phản ứng có thể sử dụng trong phương pháp nhiệt luyện để điều chế kim loại là
A. 2. B. 3. C. 1. D. 4.
(Xem giải) Câu 8: Cho các phát biểu sau về tính chất của aniline (phenylamine):
(a) Aniline làm giấy quỳ tím ẩm hoá xanh.
(b) Aniline phản ứng được với dung dịch HCl tạo muối tan không màu.
(c) Aniline có tính base mạnh hơn so với methyl amine.
(d) Aniline có phản ứng với nước bromine sinh ra chất kết tủa màu trắng.
Số phát biểu đúng là
A. 4. B. 3. C. 2. D. 1.
(Xem giải) Câu 9: Cho thế điện cực chuẩn của Ag+/Ag và Zn2+/Zn lần lượt là E°1 = +0,799V và E°2 = -0,763V. Sức điện động chuẩn của pin Galvani (E°pin) tạo bởi hai cặp oxi hoá – khử Ag+/Ag và Zn2+/Zn có giá trị là
A. +0,036V. B. -0,036V. C. +1,562V. D. -1,562V.
(Xem giải) Câu 10: Phát biểu nào sau đây về saccharose là không đúng?
A. Saccharose có công thức phân tử C12H22O11.
B. Saccharose phản ứng được với Cu(OH)2 trong môi trường kiềm ở điều kiện thường.
C. Saccharose không phản ứng với [Ag(NH3)2]OH (aq).
D. Saccharose làm mất màu nước bromine ở điều kiện thường.
(Xem giải) Câu 11: Cho phản ứng thuận nghịch sau: H2(g) + I2(g) ⇋ 2HI(g). Ở trạng thái cân bằng, nồng độ (mol/L) của H2(g), I2(g) và HI(g) lần lượt là 0,107M, 0,107M và 0,786M. Giá trị hằng số cân bằng KC của phản ứng là
A. 53,961 B. 68,652. C. 0,019. D. 0,015.
(Xem giải) Câu 12: Số lượng phối tử có trong một phân tử phức chất [Fe(H2O)4(OH)2] là
A. 6. B. 4. C. 2. D. 7.
(Xem giải) Câu 13: Phương trình hóa học của phản ứng thủy phân ethyl bromide là:
CH3CH2Br + NaOH (t°) → CH3CH2OH + NaBr (1)
Một giai đoạn tạo thành sản phẩm trong cơ chế của phản ứng trên xảy ra như sau:
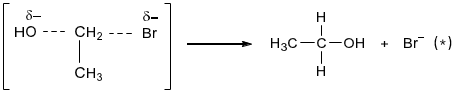
Nhận định nào sau đây là đúng?
A. Trong phân tử ethyl bromide, liên kết C−Br phân cực nên dễ bị phân cắt.
B. Trong giai đoạn (∗), có sự phá vỡ một liên kết σ và hình thành một liên kết π mới.
C. Giai đoạn (∗) biểu diễn sự chuyển hóa chất tham gia phản ứng thành trạng thái chuyển tiếp.
D. Phản ứng (1) thuộc loại phản ứng trao đổi.
(Xem giải) Câu 14: “…(1)… là những nguyên tử, nhóm nguyên tử gây ra phản ứng hóa học đặc trưng cho phân tử hợp chất hữu cơ”. Nội dung phù hợp trong chỗ trống (1) là
A. Nhóm nguyên tố. B. Nhóm chức. C. Nhóm phản ứng. D. Nhóm carboxylic.
(Xem giải) Câu 15: Nhiệt tạo thành chuẩn của MgCO3(s), MgO(s) và CO2(g) lần lượt là –1096,0 kJ/mol; –602,0 kJ/mol và –393,5 kJ/mol. Biến thiên enthalpy chuẩn của phản ứng MgCO3(s) → MgO(s) + CO2(g) là
A. -100,5 kJ. B. -494,0 kJ. C. +494,0 kJ. D. +100,5 kJ.
(Xem giải) Câu 16: Ở trạng thái cơ bản, cấu hình electron của nguyên tử Cl (số hiệu nguyên tử bằng 17) là
A. 1s2 2s2 2p6 3s2 3p7. B. 1s2 2s2 2p6 3s3 3p4.
C. 1s2 2s2 2p6 3p2 3s5. D. 1s2 2s2 2p6 3s2 3p5.
(Xem giải) Câu 17: Dưới đây là sơ đồ của một pin điện hóa và chiều di chuyển của dòng electron.
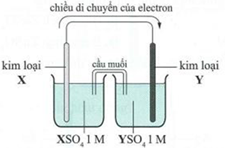
Cặp nguyên tố X và Y nào dưới đây phù hợp với sơ đồ này?
A. Cu và Fe. B. Cu và Zn. C. Fe và Zn. D. Zn và Fe
(Xem giải) Câu 18: Cho bảng thông tin sau:
| Cặp oxi hóa khử | 2H2O/2OH–, H2 | Ni2+/Ni | Sn2+/Sn | Cu2+/Cu | Ag+/Ag |
| Giá trị E° (V) | -0,41 | -0,25 | -0,14 | +0,34 | +0,799 |
Dựa vào thông tin trong bảng hãy cho biết phương trình nào sau đây có thể xảy ra?
A. 2Ag(s) + Cu2+(aq) → Cu(s) + 2Ag+(aq).
B. Sn(s) + Cu2+(aq) → Cu(s) + Sn2+(aq).
C. Ni(s) + 2H2O(l) → Ni(OH)2(s) + H2(g).
D. Cu(s) + Ni2+(aq) → Ni(s) + Cu2+(aq).
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Poly(ethylene terephthalate) (PET) là một polymer nhiệt dẻo phổ biến với nhiều ứng dụng nhờ vào tính chất trong suốt, nhẹ và độ bền cao. PET được tổng hợp theo phương trình hóa học sau:
nHOCH2CH2OH + n(p-HOOC-C6H4-COOH) (xt, t°) → -[CH2CH2-OOC-C6H4-COO]n- + 2nH2O
a) PET được tổng hợp từ phản ứng trùng ngưng giữa terephthalic acid và ethylene glycol, đồng thời giải phóng các phân tử nước.
b) Terephthalic acid có chứa một vòng benzene, do đó, mỗi mắt xích của poly(ethylene terephthalate) cũng sẽ chứa một vòng benzene.
c) Poly(ethylene terephthalate) thuộc loại polyester nên PET là vật liệu bền trong môi trường kiềm.
d) PET là polymer bán tổng hợp.
(Xem giải) Câu 20: Quặng vàng tồn tại trong tự nhiên thường có hàm lượng vàng thấp. Phương pháp tách vàng phù hợp hiện nay là phương pháp Cyanide. Theo phương pháp này, để thu hồi vàng từ quặng, người ta thường nghiền nhỏ quặng rồi hòa tan trong dung dịch KCN (potassium cyanide, rất độc) cùng với dòng không khí liên tục được thổi vào. Khi đó, vàng bị hòa tan tạo thành phức chất (các chất khác trong quặng không phản ứng với KCN):
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
Tiếp theo cho bột kẽm đến dư vào dung dịch phức, thu được bột vàng (có lẫn một ít bột kẽm):
Zn(s) + 2K[Au(CN)2](aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
a) Phương pháp sử dụng để tách kim loại vàng ở trên là phương pháp thủy luyện.
b) Để loại bỏ Zn lẫn trong bột vàng, có thể dùng dung dịch HCl dư.
c) Trong phản ứng số (1), Au là chất bị oxi hóa còn O2 trong không khí là chất bị khử.
d) Ở phản ứng (2), nếu khối lượng bột kẽm thêm vào là 97,5 gam thì sẽ thu được 229,1 gam hỗn hợp kim loại, trong đó có 177,3 gam vàng (hiệu suất phản ứng đạt 100%).
(Xem giải) Câu 21: Kết quả phân tích thành phần của một muối chloride ngậm nước (X) của kim loại M thu được kết quả sau:
| Nguyên tố | M | O | Cl | H |
| Thành phần khối lượng, % | 24,79 | 40,35 | 29,83 | 5,04 |
Trong dung dịch muối X tồn tại cân bằng: [M(H2O)6]2+(aq, màu hồng) + 4Cl-(aq) ⇌ [MCl4]2-(aq, màu xanh) + 6H2O ∆H > 0
Cho vào hai ống nghiệm, mỗi ống khoảng 2 mL dung dịch muối X nồng độ 0,5M. Thêm tiếp vài giọt dung dịch HCl đặc vào ống nghiệm thứ nhất.
a) Công thức của muối chloride ngậm nước (X) là FeCl2.6H2O.
b) Trong các phức chất [M(H2O)6]2+, [MCl4]2- các phối tử đều có dung lượng phối trí là 1.
c) Ngâm ống thứ nhất vào nước lạnh, dung dịch trong đó sẽ chuyển sang màu hồng.
d) Cho vài giọt dung dịch AgNO3 0,1M vào ống thứ hai, kết tủa thu được là hỗn hợp gồm Ag và AgCl.
(Xem giải) Câu 22: Aniline là hóa chất được sử dụng nhiều trong lĩnh vực phẩm nhuộm, dược phẩm. Trong phòng thí nghiệm, quá trình điều chế aniline từ nitrobenzene được thực hiện theo sơ đồ phản ứng sau:
a) Trong phản ứng khử nitrobenzene bằng (Zn + HCl), tác nhân khử là hydrogen mới sinh [H].
b) Trong phản ứng ở giai đoạn (2), cation C6H5NH3+ là một base theo thuyết Brønsted – Lowry.
c) Theo sơ đồ tổng hợp aniline ở trên, từ 61,5 gam nitrobenzene có thể thu được 37,2 gam aniline, với hiệu suất của quá trình tổng hợp aniline từ nitrobenzene là 80%.
d) Phương pháp có thể sử dụng để tách aniline ra khỏi hỗn hợp sau kiềm hóa là phương pháp chiết lỏng – lỏng. Aniline dễ dàng được chiết tách ra khỏi pha nước bằng các dung môi hữu cơ như ether, benzene hoặc dichloromethane.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 1: Có bao nhiêu công thức cấu tạo của carboxylic acid ứng với công thức phân tử C5H10O2?
(Xem giải) Câu 2: Hợp chất hữu cơ (X) có công thức cấu tạo dưới đây. Khi thủy phân không hoàn toàn (X) sẽ thu được tối đa bao nhiêu tripeptide?
(Xem giải) Câu 3: Hợp chất KMnO4 có thể được điều chế từ MnO2 theo các bước sau:
• Bước 1: Đun nóng hỗn hợp gồm KClO3, KOH và 30,20 gam MnO2 trong chén nickel để thực hiện phản ứng:
3MnO2 + KClO3 + 6KOH → 3K2MnO4 + KCl + 3H2O (1)
• Bước 2: Để nguội hỗn hợp, cho nước vào chén nickel, khuấy đều, lọc lấy phần dung dịch. Tiếp đó, sục khí Cl2 dư vào dung dịch nước lọc:
2K2MnO4 + Cl2 → 2KMnO4 + 2KCl (2)
• Bước 3: Làm lạnh để sản phẩm kết tinh, lọc thu lấy tinh thể, sấy khô, thu được 49,95 gam sản phẩm X gồm KMnO4 có lẫn một lượng nhỏ KCl.
Để xác định hiệu suất tổng hợp và độ tinh khiết của sản phẩm KMnO4 thu được ở trên, người ta hòa tan 1,6 gam X vào nước và định mức thành 50 mL dung dịch Y. Chuyển Y lên burette để thực hiện quá trình chuẩn độ 10,0 mL dung dịch H2C2O4 0,5M thì cần vừa đủ 10,0 mL dung dịch Y theo phản ứng:
5H2C2O4 + 2KMnO4 + 3H2SO4 → 10CO2 + K2SO4 + 2MnSO4 + 8H2O (3)
Hiệu suất quá trình tổng hợp KMnO4 và độ tinh khiết của KMnO4 trong X lần lượt là x và y (x, y được làm tròn đến hàng đơn vị). Hãy tính tổng (x + y). (KCl nồng độ nhỏ coi như không có phản ứng với dung dịch KMnO4/H2SO4).
(Xem giải) Câu 4: Xăng RON95 (chỉ số octane bằng 95) có khả năng chịu nén và chống kích nổ tương đương với hỗn hợp hơi xăng gồm 5% heptane (C7H16) và 95% iso-octane (C8H18) về thể tích. Năng suất tỏa nhiệt của một loại xăng RON95 là a.103 kJ/kg, giả thiết loại xăng này có tỉ lệ hơi xăng gồm 5% heptane và 95% iso-octane về thể tích. Biến thiên enthalpy hình thành chuẩn của các chất được cho ở bảng dưới đây, hãy tính giá trị của a. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
| Chất | C7H16(g) | C8H18(g) | CO2(g) | H2O(l) | O2(g) |
| -187,8 | -224,2 | -393,5 | -285,8 | 0,0 |
(Xem giải) Câu 5: Một nhà máy chuyên sản xuất thép (chứa 1% C theo khối lượng) với công nghệ lò luyện thép Martin. Sơ đồ phản ứng luyện thép trong lò là FexOy + C → Fe + CO2. Nguyên liệu nhà máy trên sử dụng để luyện thép gồm sắt phế liệu (chứa 50% Fe3O4; 49% Fe; 1% C theo khối lượng) và gang (chứa 5% khối lượng C còn lại là Fe). Một mẻ luyện thép cần 4 tấn gang và m tấn sắt phế liệu (hiệu suất của quá trình là 100%). Tính giá trị m.
(Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 6: Cho m1 gam dung dịch H2SO4 91% hấp thụ hết m2 gam SO3 tạo thành một loại oleum (H2SO4.nSO3) có chứa 50% khối lượng là SO3. Tính tỉ lệ m2/m1.
(Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).


Bình luận