Quá trình điện phân để mạ đồng lên một chiếc chìa khoá được làm từ thép không gỉ, được mô tả ở hình sau:
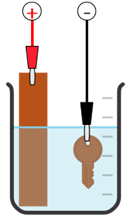
a. Anode được gắn với copper, dung dịch điện phân là dung dịch muối CuSO4.
b. Nếu chiếc chìa khóa có diện tích mỗi mặt là 25 cm2 thì bề dày lớp đồng bám trên chiếc chìa khóa là 0,07 mm. Biết: cường độ dòng điện là 10A, thời gian điện phân là 16 phút 5 giây, Cu
có khối lượng riêng là 8,9 gam/cm³ và nguyên tử khối là 64, F = 96500 C/mol. (Làm tròn kết quả đến hàng phần trăm)
c. Trong quá trình điện phân, điện cực anode tan dần.
d. Khi có dòng điện đi qua, ion Cu2+ di chuyển về cathode và bị oxi hóa thành Cu bám lên bề mặt chiếc chìa khóa.
Câu trả lời tốt nhất
(a) Đúng, anode (cực dương) là thanh đồng nguyên chất. Dung dịch điện phân là dung dịch muối CuSO4, có thể cho thêm H2SO4 để tăng độ dẫn điện.
(b) Sai. Khi mạ 2 mặt chìa khóa với độ dày lớp mạ là 0,007 cm thì:
mCu = 25.2.0,007.8,9 = 3,115 gam
—> t = mCu.2F/(64I) = 939s = 15 phút 39s
(c) Đúng, trong quá trình điện phân, điện cực anode tan dần do Cu bị oxi hóa:
Cu —> Cu2+ + 2e
(d) Sai, ion Cu2+ di chuyển về cathode và bị khử thành Cu bám lên bề mặt chiếc chìa khóa:
Cu2+ + 2e —> Cu
