[2026] Thi thử TN sở GDĐT Hà Tĩnh (Lần 1 – Đề 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 080
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2D | 3D | 4B | 5B | 6D | 7B | 8D | 9A |
| 10D | 11C | 12D | 13D | 14D | 15D | 16D | 17D | 18D |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | Đ | Đ | 47,5 | 1,24 | 37 |
| (b) | S | Đ | S | S | 26 | 27 | 28 |
| (c) | Đ | Đ | Đ | Đ | 3 | 34 | 3,75 |
| (d) | S | Đ | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Hình dưới đây mô tả dụng cụ dùng để tách các chất lỏng ra khỏi nhau.

Cho các phát biểu sau:
(a) Phương pháp được sử dụng trong trường hợp này là phương pháp chưng cất.
(b) Quá trình chuyển trạng thái của chất từ vị trí A sang B là sự ngưng tụ.
(c) Quá trình chuyển trạng thái của chất từ vị trí B sang C là sự bay hơi.
(d) Trong quá trình thí nghiệm, nước làm lạnh được dẫn vào ống sinh hàn ở cửa (2) và thoát ra ở (1).
Số phát biểu đúng là
A. 2. B. 1. C. 3. D. 4.
(Xem giải) Câu 2. Dây cầu chì thường được làm từ các kim loại như Thiếc (Sn), Chì (Pb) và Cadmium (Cd). Khi dòng điện vượt quá mức cho phép, dây chì sẽ nóng chảy và ngắt mạch, ngăn dòng điện tiếp tục lưu thông và tránh nguy cơ cháy nổ. Ứng dụng này dựa trên tính chất nào của các kim loại nói ở trên?
A. Có độ dẫn điện cao. B. Có độ cứng tương đối thấp.
C. Có tính dẻo cao. D. Có nhiệt độ nóng chảy tương đối thấp.
(Xem giải) Câu 3. HCOOCH3 được sử dụng làm dung môi hoà tan cellulose acetate, làm chất tạo bọt và chất xông hơi diệt khuẩn trong nông nghiệp. Tên gọi của HCOOCH3 là
A. ethyl acetate. B. ethyl formate. C. methyl acetate. D. methyl formate.
(Xem giải) Câu 4. Cho các phát biểu sau:
(a) Các kim loại đều tác dụng với oxygen tạo ra oxide.
(b) Tác dụng của chất xúc tác cryolite (Na3AlF6) trong quá trình điện phân nóng chảy Al2O3 là giảm nhiệt độ nóng chảy, tăng độ dẫn điện và bảo vệ Al sinh ra tránh tiếp xúc với oxygen trong không khí.
(c) Miếng gang để trong không khí ẩm chỉ xảy ra ăn mòn hóa học.
(d) Khi điện phân dung dịch CuSO4 (điện cực trơ) ở cathode thu được kim loại.
(e) Kim loại cứng nhất là Cs.
(g) Cho mẩu nhỏ Na vào nước có nhỏ vài giọt phenolphtalein, dung dịch sau phản ứng có màu xanh.
Số phát biểu đúng là?
A. 4. B. 2. C. 5. D. 3.
(Xem giải) Câu 5. Muốn tiến hành mạ đồng lên một chìa khóa làm bằng sắt, một học sinh đã chuẩn bị các thiết bị và hóa chất gồm cốc thủy tinh, nguồn điện một chiều, thanh đồng, dung dịch CuSO4 và dự kiến các cách lắp đặt như sau:
(1) Thanh đồng được đấu nối với cực âm, chìa khóa được đấu nối với cực dương của nguồn điện.
(2) Thanh đồng và chìa khóa không tiếp xúc với nhau được ngâm vào dung dịch CuSO4 trong cùng một cốc.
(3) Thanh đồng được đấu nối với cực dương, chìa khóa được đấu nối với cực âm của nguồn điện.
(4) Thanh đồng và chìa khóa được ngâm vào dung dịch CuSO4 ở hai cốc khác nhau và không có cầu muối.
Cách lắp đặt đúng với mục đích thí nghiệm là
A. (1) và (4). B. (2) và (3). C. (1) và (2). D. (3) và (4).
(Xem giải) Câu 6. Hiện tượng mưa acid là do không khí bị ô nhiễm bởi các khí nào sau đây?
A. NO, CO, CO2. B. CH4, HCl, CO. C. Cl2, CH4, SO2. D. SO2, NO, NO2.
(Xem giải) Câu 7. Nguồn điện nào sau đây không dựa vào các phản ứng hoá học?
A. Pin nhiên liệu. B. Pin mặt trời. C. Pin Galvani. D. Acquy.
(Xem giải) Câu 8. Sự phân cắt đồng li là sự phân cắt một cách đồng đều đối với hai nguyên tử tham gia liên kết, mỗi nguyên tử chiếm một electron từ cặp electron chung và trở thành tiểu phân mang một electron độc thân.
Quá trình nào dưới đây xảy ra sự phân cắt đồng li?
A. CH3C≡CH → CH3C≡C- + H+. B. CH3CH2Br → CH3CH2+ + Br-.
C. (CH3)3CBr → (CH3)3C+ + Br-. D. Cl2 → Cl• + Cl•
(Xem giải) Câu 9. Theo quy định, tất cả các loại chất lỏng, tinh dầu được coi là chất lỏng dễ cháy và là hàng hoá nguy hiểm nếu có điểm chớp cháy nhỏ hơn 60°C không được vận chuyển qua đường hàng không. Cho điểm chớp cháy của một số loại tinh dầu thường gặp như sau:
| Tinh dầu | Trầm hương | Quế | Đinh hương | Tràm gió | Oải hương | Thông |
| Điểm chớp cháy (°C) | 51 | 87 | 87 | 52 | 68 | 65 |
Trong các loại trên, theo quy định có bao nhiêu tinh dầu hành khách được phép mang theo lên máy bay?
A. 4. B. 5. C. 6. D. 2.
(Xem giải) Câu 10. Trong phân tử chất nào sau đây có 1 nhóm amino (NH2) và 2 nhóm carboxyl (COOH)?
A. Alanine. B. Valine. C. Lysine. D. Glutamic acid.
(Xem giải) Câu 11. Thuỷ phân hoàn toàn saccharose thu được X và Y. Để phân biệt X và Y người ta sử dụng
A. Cu(OH)2/OH- đun nóng. B. Cu(OH)2 ở nhiệt độ thường.
C. nước bromine. D. thuốc thử Tollens.
(Xem giải) Câu 12. Trong công nghiệp, khí than ướt được điều chế bằng cách cho hơi nước đi qua than nung nóng theo phương trình phản ứng:
C(s) + H2O(g) ⇋ CO(g) + H2(g) ![]() = 130kJ (1)
= 130kJ (1)
Để cân bằng (1) chuyển dịch theo chiều thuận cần
A. giảm nhiệt độ. B. dùng xúc tác. C. tăng áp suất. D. tăng nhiệt độ.
(Xem giải) Câu 13. Hàng năm nhà máy phân bón sản xuất khoảng 560 000 tấn urea cung cấp ra thị trường. Quá trình sản xuất urea thực hiện theo phản ứng tổng quát sau: CO2(g) + 2NH3(g) → CO(NH2)2 + H2O
Dựa vào công nghệ tuần hoàn mà hiệu suất quá trình tổng hợp tại nhà máy đạt khoảng 98%. Khối lượng NH3 sử dụng để sản xuất được lượng urea trên gần nhất với giá trị nào sau đây?
A. 312000 tấn. B. 340000 tấn. C. 364800 tấn. D. 323800 tấn.
(Xem giải) Câu 14. Trong cơ thể con người, mức độ độc hại của lead (Pb) có thể được giảm bớt bằng cách sử dụng phối tử EDTA4- để tạo phức [Pb(EDTA)]2- rất bền và được thận bài tiết. Phối tử EDTA4- được cung cấp bằng cách tiêm truyền dung dịch Na2[Ca(EDTA)]. Biết phức [Ca(EDTA)]2- tương đối kém bền, sự trao đổi calcium với lead chủ yếu diễn ra trong mạch máu. Hàm lượng lead trong máu của một bệnh nhân là 0,828 μg/mL. Nồng độ lead theo μmol/L trong máu của bệnh nhân này bằng bao nhiêu?
A. 2. B. 2,5. C. 3. D. 4.
(Xem giải) Câu 15. Chất nào sau đây là thành phần chính của chất giặt rửa tổng hợp?
A. (C17H35COO)2Ca. B. C17H35COOK.
C. C15H31COONa. D. CH3[CH2]11C6H4SO3Na.
(Xem giải) Câu 16. Nguyên tố nào sau đây mà nguyên tử có 7 electron ở lớp ngoài cùng?
A. Al (Z = 13). B. Ar (Z = 18). C. Na (Z = 11). D. Cl (Z = 17).
(Xem giải) Câu 17. Ở điều kiện chuẩn xảy ra các phản ứng sau:
(1) Fe2+(aq) + Ag+(aq) → Fe3+(aq) + Ag(s)
(2) Fe(s) + 2Fe3+(aq) → 3Fe2+(aq)
Sắp xếp các cặp oxi – hóa khử nào sau đây đúng theo thứ tự giảm dần thế điện cực chuẩn?
A. Fe3+/Fe2+; Fe2+/Fe; Ag+/Ag. B. Fe3+/Fe2+; Ag+/Ag; Fe2+/Fe.
C. Ag+/Ag; Fe2+/Fe; Fe3+/Fe2+. D. Ag+/Ag ; Fe3+/Fe2+; Fe2+/Fe.
(Xem giải) Câu 18. Nhận định nào sau đây không đúng với tính chất của saccharose?
A. Saccharose phản ứng được với Cu(OH)2.
B. Khi thủy phân saccharose tạo thành sản phẩm trong đó có glucose.
C. Saccharose là chất kết tinh, không màu.
D. Saccharose tham gia phản ứng tráng bạc.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Tiến hành thí nghiệm thử tính chất của cellulose theo các bước sau:
• Bước 1: Cho lần lượt 4,0 ml HNO3, 8,0 ml H2SO4 đặc vào cốc thủy tinh, lắc đều và làm lạnh.
• Bước 2: Thêm tiếp vào cốc một nhúm bông. Đặt cốc chứa hỗn hợp phản ứng vào nồi nước nóng (khoảng 60-70°C) khuấy nhẹ trong 5 phút.
• Bước 3: Lọc lấy chất rắn rửa sạch bằng nước, ép khô bằng giấy lọc sau đó sấy khô (tránh lửa).
a) Sau bước 3, sản phẩm thu được chỉ chứa cellulose trinitrate.
b) Sau bước 3, lấy sản phẩm thu được đốt cháy thấy có khói trắng xuất hiện nhiều.
c) Thí nghiệm trên chứng minh mỗi đơn vị glucose cấu thành phân tử cellulose có ba nhóm hydroxy.
d) Có thể thay thế nhúm bông bằng hồ tinh bột.
(Xem giải) Câu 20. Magnesium là kim loại được ứng dụng để tạo các hợp kim nhẹ, bền, đặc biệt là cho ngành công nghiệp sản xuất ô tô và hàng không vũ trụ. Magnesium được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite. Quá trình được thực hiện qua các giai đoạn sau:
• Giai đoạn 1. Nung quặng dolomite:
MgCO3.CaCO3(s) → MgO(s) + CaO(s) + 2CO2(g)
• Giai đoạn 2. Dùng silicon trong ferrosilicon (Fe, Si) làm chất khử trong điều kiện chân không:
2MgO(s) + 2CaO(s) + Si(s) → 2Mg(g) + Ca2SiO4(s)
Phản ứng chung của quá trình Pidgeon là:
2MgCO3.CaCO3(s) + Si(s) → 2Mg(s) + Ca2SiO4(s) + 4CO2(g) ![]() = 183 kJ
= 183 kJ
a) Trong phản ứng ở giai đoạn 2, MgO dễ bị khử bởi Si hơn CaO.
b) Phản ứng ở giai đoạn 2 thuộc phương pháp nhiệt luyện.
c) Quá trình Pidgeon là quá trình thu nhiệt.
d) Từ 1 tấn quặng dolomite (chứa 92% MgCO3.CaCO3 về khối lượng) thu được 108 kg kim loại magnesium. Hiệu suất của toàn bộ quá trình là 90%.
(Xem giải) Câu 21. Cao su thiên nhiên được sản xuất từ mủ của cây cao su. Mủ cao su là một chất lỏng màu trắng sữa, được khai thác bằng cách cạo vỏ cây. Sau khi thu hoạch, mủ cao su phải trải qua nhiều công đoạn như bảo quản, đông tụ, cán ép, sấy khô và lưu hoá để tạo ra các sản phẩm cao su có tính đàn hồi và độ bền cao, phục vụ cho đời sống và sản xuất. Trong quá trình chế tạo cao su, từ mủ cao su tươi đến cao su khô có hiệu suất trung bình 35%, còn từ cao su khô đến loại cao su có thể dùng để sản xuất lốp xe ô tô có hiệu suất chuyển hoá 90%. Lốp xe ô tô, xe máy… ngoài thành phần là cao su thiên nhiên còn có cao su tổng hợp, than đen, thép, vải, phụ gia… trong đó thành phần cao su thiên nhiên chiếm 50% về khối lượng.
a) Phản ứng lưu hoá cao su là phản ứng tăng mạch polymer.
b) Một nhà máy có quy mô trung bình mỗi ngày sản xuất được 10000 lốp ô tô, mỗi lốp nặng 8 kg thì cần chuẩn bị 125 tấn mủ cao su tươi. (quá trình tính toán chỉ làm tròn bước cuối cùng đến hàng đơn vị)
c) Thành phần chính của cao su thiên nhiên là polyisoprene.
d) Cao su thiên nhiên lưu hoá là polymer bán tổng hợp.
(Xem giải) Câu 22. Để loại bỏ ion ammonium (NH4+) trong nước thải, trước tiên người ta phải kiềm hóa dung dịch nước thải bằng NaOH đến pH = 11, sau đó cho chảy từ trên xuống trong một tháp được nạp đầy các vòng đệm bằng sứ, còn không khí được thổi ngược từ dưới lên để oxi hóa NH3. Phương pháp này loại bỏ được khoảng 92% lượng ammonium trong nước thải.
Kết quả phân tích của ba mẫu nước thải khi chưa được xử lý như sau:
| Mẫu | Hàm lượng ammonium trong nước thải (mg/lít) |
| 1 | 10 |
| 2 | 18 |
| 3 | 125 |
Giả sử tiến hành xử lí ba mẫu nước thải theo phương pháp trên, biết rằng tiêu chuẩn hàm lượng ammonium cho phép là 1,0 mg/lít. Cho các nhận định sau:
a) Tổng lượng ammonium còn lại của mẫu nước thải (1) và (3) là 10,8 mg/lít.
b) Mẫu nước thải (2) đạt tiêu chuẩn cho phép.
c) Phương pháp ngược dòng nhằm mục đích tăng diện tích tiếp xúc giữa ammonia với oxygen không khí.
d) Mục đích của việc kiềm hóa ammonium là để thu được ammonia.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Pin nhiên liệu sử dụng ethanol được đặc biệt quan tâm do có nguồn nhiên liệu sinh học dồi dào. Phản ứng chung trong pin ethanol – oxygen như sau:
C2H5OH(l) + 3O2(g) ⟶ 2CO2(s) + 3H2O (l) ![]() = -1366,7kJ
= -1366,7kJ
Một pin ethanol – oxygen được dùng để thắp sáng 8 bóng đèn LED, mỗi bóng có công suất 3W liên tục trong t giờ, tiêu thụ hết 230 gam ethanol. Biết rằng 60% lượng nhiệt sinh ra từ phản ứng (ở điều kiện chuẩn) được chuyển hoá thành điện năng. Giá trị của t bằng bao nhiêu? (quá trình tính toán chỉ làm tròn bước cuối cùng đến hàng phần mười).
(Xem giải) Câu 24. Cationite là một loại nhựa trao đổi cation được sử dụng để loại bỏ ion Ca2+, Mg2+. Khi nước cứng đi qua cột nhựa, các ion Ca2+, Mg2+ (kí hiệu chung là M2+) sẽ được giữ lại và thay thế bằng các ion H+, Na+ theo sơ đồ sau:
M2+ + 2RSO3X → (RSO3)2M + 2X+ (trong đó X+ là H+ hoặc Na+).
Một loại cationite có % khối lượng sulfur là 7,94% được sử dụng để loại bỏ các ion Mg2+, Ca2+ trong nước cứng. Nếu một cột nhựa trao đổi ion trong thiết bị lọc nước gia đình có chứa 1,00 kg cationite trên thì tổng số mol Mg2+, Ca2+ tối đa có thể được loại bỏ là bao nhiêu? (làm tròn kết quả đến hàng phần trăm).
(Xem giải) Câu 25. Vào mùa lạnh loại coffee tự làm nóng được sử dụng khá nhiều. Để làm nóng coffee, chỉ cần ấn nút (trên lon) để trộn nguyên liệu gồm dung dịch KOH hoặc NaOH rất loãng và CaO; 250 mL coffee trong lon sẽ được hâm nóng đến khoảng 40°C. Giả sử nhiệt dung riêng của coffee là 4,18 J/g.K (Nhiệt dung riêng là nhiệt lượng cần cung cấp để 1 gam chất tăng lên 1°C). Cho ![]() (kJ/mol) của CaO(s), H2O(l), Ca(OH)2(s) lần lượt là -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 25%. Tính khối lượng CaO theo gam cần cung cấp để làm nóng 250 mL coffee từ 10°C đến 40°C (d = 1,0 g/ml). (làm tròn kết quả đến hàng đơn vị).
(kJ/mol) của CaO(s), H2O(l), Ca(OH)2(s) lần lượt là -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 25%. Tính khối lượng CaO theo gam cần cung cấp để làm nóng 250 mL coffee từ 10°C đến 40°C (d = 1,0 g/ml). (làm tròn kết quả đến hàng đơn vị).
(Xem giải) Câu 26. Cho các chất: glucose (1), tinh bột (2), aniline (3), triolein (4), alanine (5), ethyl aceate (6), Ala-Gly (7). Có bao nhiêu chất bị thuỷ phân trong môi trường base?
(Xem giải) Câu 27. Cho các phát biểu sau:
(1) Tất cả các kim loại nhóm IIA đều tan trong nước.
(2) Các kim loại nhóm IA khử được ion kim loại yếu hơn trong dung dịch muối của chúng.
(3) Các ion Na+, Mg2+, Al3+ có cùng cấu hình electron ở trạng thái cơ bản và có tính oxi hoá yếu.
(4) Các kim loại kiềm K, Rb, Cs tự bốc cháy khi tiếp xúc với nước.
(5) Magnesium có E°Mg2+/Mg = -2,356V nên tác dụng mãnh liệt với H2O ở nhiệt độ thường.
Sắp xếp các phát biểu đúng theo thứ tự từ bé đến lớn.
(Xem giải) Câu 28. Methyl cinnamate (ester của cinnamic acid) là chất rắn có mùi thơm nồng. Công thức của methyl cinnamate như hình bên.
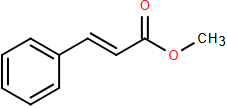
Tỉ lệ khối lượng của carbon và oxygen trong phân tử methyl cinnamate là k. Tìm giá trị của k (làm tròn kết quả đến hàng phần trăm).


Bình luận