[2026] Thi thử TN sở GDĐT Phú Thọ (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 017
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2B | 3A | 4D | 5A | 6B | 7C | 8B | 9A |
| 10D | 11B | 12C | 13A | 14D | 15C | 16C | 17A | 18D |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | Đ | S | 1324 | 1,55 | 84 |
| (b) | Đ | S | S | S | 26 | 27 | 28 |
| (c) | S | Đ | Đ | Đ | 2 | 31,7 | 7,27 |
| (d) | Đ | Đ | S | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Đun nóng ethyl formate với dung dịch NaOH thu được sodium formate và alcohol X. Công thức của X là
A. C2H5OH. B. C2H5COOH. C. HCOOC2H5. D. HCOONa.
(Xem giải) Câu 2: Đại lượng đặc trưng cho độ nhanh hay chậm của một phản ứng hóa học được gọi là
A. quá trình hóa học. B. tốc độ phản ứng. C. cân bằng hóa học. D. biến thiên enthalpy.
(Xem giải) Câu 3: Amine nào sau đây phản ứng được với nitrous acid (HNO2) ở nhiệt độ từ 0 – 5°C tạo thành muối diazonium?
A. Aniline. B. Propylamine. C. Methylamine. D. Ethylamine.
(Xem giải) Câu 4: Chất nào sau đây không có phản ứng thủy phân trong môi trường acid?
A. Maltose. B. Tinh bột. C. Saccharose. D. Glucose.
(Xem giải) Câu 5: Acetic acid được điều chế bằng phương pháp lên men giấm từ dung dịch chất nào sau đây?
A. C2H5OH. B. CH3OH. C. CH3CHO. D. HCOOH.
(Xem giải) Câu 6: Hợp chất carbonyl là các hợp chất hữu cơ trong phân tử có chứa nhóm chức nào sau đây?
A. Carboxyl. B. Carbonyl. C. Hydroxy. D. Amino.
(Xem giải) Câu 7: Dung dịch nào sau đây có pH < 7?
A. Nước vôi trong. B. Nước xà phòng. C. Dịch dạ dày. D. Nước muối (NaCl).
(Xem giải) Câu 8: Phương pháp phổ hồng ngoại (IR) là phương pháp vật lí hiện đại để xác định …(1)… của hợp chất hữu cơ. Nội dung phù hợp trong chỗ trống (1) là
A. công thức tổng quát. B. cấu tạo phân tử. C. công thức phân tử. D. phân tử khối.
(Xem giải) Câu 9: Cấu hình electron nguyên tử của sodium là 1s2 2s2 2p6 3s1. Trong bảng tuần hoàn các nguyên tố hóa học, sodium ở chu kì
A. 3. B. 6. C. 1. D. 2.
(Xem giải) Câu 10: Cây trồng khi thiếu nguyên tố nitrogen, lá sẽ bắt đầu úa vàng từ đỉnh. Để khắc phục tình trạng này, có thể bón cho cây loại phân có thành phần nào sau đây?
A. KCl. B. K2SO4. C. Ca(H2PO4)2. D. (NH2)2CO.
(Xem giải) Câu 11: Cơ chế của phản ứng cộng bromine vào liên kết đôi của ethene gồm hai giai đoạn như sau:
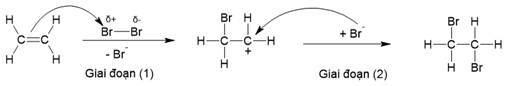
Phát biểu nào sau đây không đúng?
A. Giai đoạn (2) có sự hình thành liên kết σ.
B. Tổng số liên kết trong phân tử ethene và 1,2–dibromoethane bằng nhau.
C. Giai đoạn (1) có sự phân cắt liên kết π.
D. Ethene làm mất màu nước bromine.
(Xem giải) Câu 12: Ester T có khả năng chịu được nhiệt độ cao và được phủ lên bề mặt vật liệu nhằm chống ăn mòn. Thuỷ phân T trong dung dịch NaOH thu được hợp chất X và Y (MX < MY) theo sơ đồ sau:

Phát biểu nào sau đây đúng?
A. Công thức phân tử của T là C14H24O2.
B. X là muối của carboxylic acid và Y là alcohol.
C. 1 mol X có thể tác dụng tối đa với 1 mol Br2 trong CCl4 ở điều kiện thường.
D. Các nguyên tử carbon và hydrogen trong vòng của T, X và Y đều nằm trong cùng một mặt phẳng.
(Xem giải) Câu 13: Trong pin Galvani Cu–Ag, ở anode xảy ra quá trình
A. oxi hóa Cu. B. khử Ag+. C. khử Cu2+. D. oxi hóa Ag.
(Xem giải) Câu 14: Cho các dung dịch sau: lòng trắng trứng, ethylamine, aniline, Ala–Gly–Gly. Số dung dịch hoà tan được Cu(OH)2 trong môi trường kiềm là
A. 1. B. 2. C. 4. D. 3.
(Xem giải) Câu 15: Acquy chì là loại pin sạc lâu đời nhất, có nguyên tắc hoạt động tương tự như pin điện hóa. Cực dương làm từ kim loại Pb được phủ PbO2 và cực âm làm từ Pb nguyên chất dạng xốp, cùng nhúng vào dung dịch H2SO4 nồng độ 38%, hoạt động bằng phản ứng hóa học, được dùng rộng rãi cho ô tô, hệ thống dự phòng. Phản ứng xảy ra khi acquy xả điện là
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l)
Biết rằng PbSO4 sinh ra từ điện cực nào đều bám hết vào điện cực đó.
Phát biểu nào sau đây đúng?
A. Tại anode, Pb bị khử và tạo thành PbSO4.
B. Tại cathode, PbO2 bị oxi hoá và tạo thành PbSO4.
C. Khi acquy xả điện, khối lượng các điện cực đều tăng.
D. Khi acquy xả điện, nồng độ H2SO4 tăng.
(Xem giải) Câu 16: Polymer X có công thức:
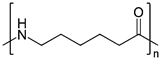
Phát biểu nào sau đây về X không đúng?
A. Có thể tổng hợp X bằng phản ứng trùng hợp hoặc trùng ngưng.
B. Polymer X là tơ tổng hợp.
C. X có liên kết –CO–NH– nên X là polypeptide.
D. X không bền trong môi trường acid hoặc base.
(Xem giải) Câu 17: Glutathione là một chất có khả năng chống oxi hóa tự nhiên trong cơ thể, bảo vệ tế bào khỏi tổn thương, loại bỏ các chất độc hại và các gốc tự do gây hại cho tế bào. Công thức cấu tạo của glutathione như sau:
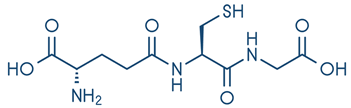
Phát biểu nào sau đây không đúng?
A. Phân tử glutathione có chứa hai liên kết peptide.
B. Khi cho glutathione tác dụng với dung dịch NaOH dư đun nóng, sản phẩm sinh ra có disodium glutamate.
C. Trong cơ thể, nồng độ glutathione thay đổi theo thời gian và điều kiện môi trường sống.
D. Vai trò của glutathione là chất chống oxi hóa, bảo vệ tế bào khỏi gốc tự do.
(Xem giải) Câu 18: Tơ nitron dai, bền với nhiệt, giữ nhiệt tốt, thường được dùng để dệt vải may quần áo ấm. Trùng hợp chất nào sau đây tạo thành polymer dùng để sản xuất tơ nitron?
A. H2N–[CH2]6–NH2. B. H2N–[CH2]5–COOH.
C. CH2=CH–CH3. D. CH2=CH–CN.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 1. Trong phòng thí nghiệm, aniline có thể được điều chế từ benzene theo sơ đồ gồm ba giai đoạn được đánh số (1), (2) và (3) như sau:
Trong một thí nghiệm tổng hợp aniline theo sơ đồ trên, từ 10,0 mL benzene (khối lượng riêng bằng 0,878 g.mL⁻¹) thu được 8,50 gam aniline. Biết các chất vô cơ trong thí nghiệm được lấy dư. Hiệu suất của quá trình tổng hợp aniline từ benzene là h%.
a) Các phản ứng hóa học trong sơ đồ trên đều là phản ứng oxi hóa – khử.
b) Chất X phù hợp với sơ đồ trên là NaOH.
c) Aniline thu được là chất lỏng, không màu, tan tốt trong nước ở nhiệt độ thường.
d) Giá trị của h là 81,2 (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
(Xem giải) Câu 2. Cho mô hình cấu tạo của các phân tử polysaccharide dưới đây:
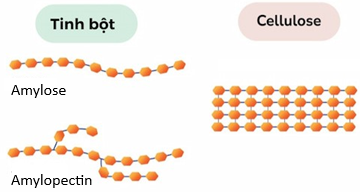
a) Trong cellulose, các nhóm –OH trên các chuỗi liền kề tạo ra liên kết hydrogen, giữ các chuỗi lại với nhau, tạo thành cấu trúc mạng lưới bền chắc.
b) Amylose và cellulose đều có liên kết β–1,4–glycoside giữa các đơn vị glucose, do đó chúng đều tạo thành mạch không phân nhánh và có hoạt tính sinh học giống nhau.
c) Các loại polysaccharide này được tạo thành từ một monosaccharide.
d) Sự khác nhau về kiểu liên kết glycoside (α hay β) làm cho polysaccharide có tính tan và khả năng bị enzyme phân huỷ khác nhau.
(Xem giải) Câu 3. Một nhóm học sinh nghiên cứu quá trình tinh chế đồng từ một mẫu đồng thô (chứa đồng có hàm lượng là x%) bằng phương pháp điện phân và đưa ra giả thuyết “khối lượng mẫu đồng thô giảm bằng khối lượng cathode tăng”. Để kiểm chứng giả thuyết, nhóm học sinh thực hiện thí nghiệm sau:
– Nối mẫu đồng thô với một điện cực và miếng đồng tinh khiết với điện cực còn lại của nguồn điện một chiều, rồi nhúng vào bình điện phân chứa dung dịch copper(II) sulfate trong dung dịch sulfuric acid.
– Tiến hành điện phân với cường độ dòng điện 24A. Sau t giờ, các điện cực được lấy ra, làm khô và đem cân.
– Khối lượng các điện cực trước và sau điện phân được ghi lại trong bảng sau:
| Thời điểm | Khối lượng mẫu đồng thô (g) | Khối lượng miếng đồng tinh khiết (g) |
| Trước điện phân | 103 | 100 |
| Sau t giờ | 8,56 | 182,5 |
Giả sử hiệu suất quá trình điện phân là 100% và phần tạp chất tạp chất trong mẫu đồng không tham gia vào quá trình điện phân. Biết q = ne.F = I.t, trong đó: q là điện lượng (C), ne là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian điện phân (giây), F là hằng số Faraday (F = 96500 C/mol).
a) Giả thuyết của nhóm học sinh sai.
b) Trong thí nghiệm, mẫu đồng thô được nối với cực âm, miếng đồng tinh khiết được nối với cực dương của nguồn điện.
c) Giá trị của x là 80,1. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười)
d) Giá trị của t là 3,3. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười)
(Xem giải) Câu 4. Sulfuric acid (H2SO4) là hợp chất quan trọng trong công nghiệp hoá chất, được sử dụng nhiều trong sản xuất phân bón, khai khoáng, chế biến dầu mỏ,…Trong công nghiệp, sulfuric acid 98% được sản xuất từ sulfur theo phương pháp tiếp xúc, được mô tả như hình dưới đây:
a) Chất xúc tác ở giai đoạn 2 làm tăng tốc độ phản ứng và tăng hiệu suất tổng hợp SO3.
b) Mục đích dùng lượng dư không khí để phản ứng xảy ra hoàn toàn.
c) X là H2SO4 đặc, Y là H2SO4.nSO3 (oleum).
d) Theo tiêu chuẩn quốc tế quy định nếu lượng SO2 vượt quá 1,0.10–5 mol/m3 không khí thì bị coi là ô nhiễm. Kết quả phân tích 50 lít không khí có 0,042 mg SO2, vì vậy không khí bị ô nhiễm.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 1. Cho phương trình hóa học của các phản ứng dưới đây:
(1) CH2OH[CHOH]4CH=O + 2[Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag + 3NH3 + H2O
(2) C6H12O6 → 2CH3CH(OH)COOH
(3) C6H12O6 → 2C2H5OH + 2CO2
(4) C12H22O11 + H2O → 2C6H12O6
Gán số thứ tự phương trình hoá học của các phản ứng theo tên gọi: Phản ứng tráng bạc, phản ứng lên men rượu, phản ứng lên men lactic, phản ứng thủy phân và sắp xếp theo trình tự thành dãy bốn số (ví dụ: 1234, 4321,…).
(Xem giải) Câu 2. Cho pin điện hóa tạo bởi hai cặp oxi hóa–khử ở điều kiện chuẩn: Pb2+/Pb và Al3+/Al với thế điện cực chuẩn tương ứng là –0,126 V và –1,676 V. Sức điện động chuẩn của pin bằng bao nhiêu V?
(Xem giải) Câu 3. Lẩu tự sôi là hộp đựng thực phẩm có khả năng tự làm nóng mà không cần dùng điện hay gas. Cấu trúc hộp gồm 2 tầng: Tầng trên là khay đựng thức ăn, tầng dưới là khay chứa gói tự sôi. Hộp làm nóng sẽ hoạt động khi đổ nước vào tầng dưới, gói tự sôi sẽ xảy ra phản ứng hóa học tỏa nhiệt, làm nóng thức ăn ở tầng trên.
Trong một hộp lẩu tự sôi, người ta sử dụng một gói tạo nhiệt chứa m gam calcium oxide (CaO) nguyên chất. Khi người dùng đổ nước vào khay dưới, xảy ra phản ứng: CaO (s) + H2O(l) Ca(OH)2(s)
Cho biết nhiệt tạo thành chuẩn của các chất như sau:
Chất CaO(s) H2O(l) Ca(OH)2(s)
(kJ mol–1)
–635,1 –285,8 –986,1
Giả sử 80% lượng nhiệt tỏa ra để làm nóng 400 gam nước lẩu ở 25 oC lên 71,7 oC. Biết lượng nhiệt cần thiết để 1 gam nước lẩu thay đổi 1 oC là 4,184 J. Giá trị của m bằng bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị)
(Xem giải) Câu 4. Cho các polymer sau: poly(vinyl chloride), nylon–6,6, polyisoprene, poly(methyl methacrylate), polyacrylonitrile. Có bao nhiêu polymer có tính dẻo?
(Xem giải) Câu 5. Sodium azide (NaN3) là một hợp chất dễ bị phân huỷ. Hỗn hợp chất rắn gồm NaN3, KNO3 và SiO2 được sử dụng để nhanh chóng tạo ra một lượng đủ lớn khí nitrogen trong các túi khí an toàn trên ô tô. Khi bị va đập mạnh, các chất trên sẽ nhanh chóng phản ứng tạo ra khí nitrogen, làm căng đầy túi khí an toàn. Các phản ứng xảy ra được biểu diễn theo các sơ đồ sau:
NaN3 → Na + N2 (1)
Na + KNO3 → K2O + Na2O + N2 (2)
K2O + Na2O + 2SiO2 → K2SiO3 + Na2SiO3 (3)
Nếu lấy 52 gam NaN₃ (các hóa chất khác coi như đã lấy đủ) thì tạo ra được bao nhiêu lít khí nitrogen (ở đkc) cho túi khí an toàn? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười)
(Xem giải) Câu 6. Hợp chất hữu cơ đơn chức E ở điều kiện thường là chất lỏng, có mùi thơm hoa quả, được ứng dụng phổ biến trong ngành thực phẩm, đồ uống, mỹ phẩm, dung môi. Phân tích thành phần khối lượng nguyên tố trong E, thu được kết quả: %C = 64,615%; %H = 10,760% còn lại là oxygen. Phổ MS của E cho thấy peak ion phân tử [M+] có giá trị m/z = 130.
Cho E tác dụng với dung dịch NaOH, thu được muối sodium của carboxylic acid X và chất hữu cơ Y. Trong đó, Y được tạo ra khi khử isovaleraldehyde (3–methylbutanal) bởi LiAlH4.
Khi đun nóng hỗn hợp 8,10 gam X và 7,80 gam Y với xúc tác là H2SO4 đặc, thu được m gam E. Hiệu suất của phản ứng điều chế E là 63,1%. Giá trị của m bằng bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm)


Bình luận