[2025] Thi thử TN sở GDĐT Cần Thơ (Lần 1 – Đề 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 150
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2A | 3A | 4C | 5D | 6D | 7A | 8A | 9A |
| 10D | 11B | 12A | 13B | 14B | 15A | 16D | 17A | 18D |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | S | S | S | 88 | 39,1 | 3 |
| (b) | Đ | Đ | S | Đ | 26 | 27 | 28 |
| (c) | Đ | Đ | Đ | S | 35,6 | 98,3 | 3 |
| (d) | Đ | Đ | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Công thức của ethyl formate là
A. CH3COOCH3. B. HCOOC2H5. C. CH3COOC2H5. D. HCOOCH3.
(Xem giải) Câu 2: Cellulose thuộc loại polysaccharide, là thành phần chính tạo nên màng tế bào thực vật, có nhiều trong gỗ, bông nõn. Công thức của cellulose là
A. (C6H10O5)n. B. C6H12O6. C. C12H22O11. D. C2H4O2.
(Xem giải) Câu 3: Nguyên tử trung tâm của phức chất [PtCl4]2- và [Fe(CO)5] lần lượt là:
A. Pt2+ và Fe. B. Pt2+ và Fe2+. C. Cl và CO. D. Pt2+ và Fe3+.
(Xem giải) Câu 4: Trong phân tử Ala-Gly-Lys-Val, amino acid đầu N là
A. Gly. B. Val. C. Ala D. Lys.
(Xem giải) Câu 5: Phân bón nào sau đây có hàm lượng đạm cao nhất?
A. NaNO3. B. KCl. C. Ca(NO3)2. D. (NH2)2CO.
(Xem giải) Câu 6: Cho bảng giá trị thế điện cực chuẩn của một số cặp oxi hóa – khử như sau:
| Cặp oxi hoá – khử | Li+/Li | Mg2+/Mg | Zn2+/Zn | Ag+/Ag |
| Thế điện cực chuẩn (V) | −3,040 | −2,356 | −0,762 | +0,799 |
Ở điều kiện chuẩn, kim loại nào sau đây khó bị oxi hóa nhất?
A. Zn. B. Mg. C. Li. D. Ag.
(Xem giải) Câu 7: Chất nào sau đây được dùng để làm mất tính cứng vĩnh cửu của nước?
A. Na2CO3. B. NaOH. C. HCl. D. Ca(OH)2.
(Xem giải) Câu 8: Nước muối sinh lí được dùng trong việc ngăn ngừa nguy cơ mất muối do đổ quá nhiều mồ hôi hay do tiêu chảy là dung dịch của chất X với nồng độ 0,9%. Công thức của X là
A. NaCl. B. NaHCO3. C. KCl. D. NaNO3.
(Xem giải) Câu 9: Tiến hành các thí nghiệm theo các bước sau:
• Bước 1: Cho vào hai ống nghiệm (1) và (2) mỗi ống khoảng 2,0 mL ethyl acetate.
• Bước 2: Thêm khoảng 2,0 mL dung dịch H2SO4 20% vào ống nghiệm (1) và khoảng 5,0 mL dung dịch NaOH 30% vào ống nghiệm (2).
• Bước 3: Đun cách thuỷ ống nghiệm (1) và (2) trong cốc thuỷ tinh ở nhiệt độ 60 − 70°C.
Phát biểu nào sau đây đúng?
A. Phản ứng hoá học xảy ra ở ống nghiệm (2) là phản ứng một chiều.
B. Sau bước 2, chất lỏng trong cả hai ống nghiệm đồng nhất.
C. Sau bước 3, sản phẩm thu được ở cả hai ống nghiệm là CH3COOH.
D. Sau bước 3, ống nghiệm (1) tạo thành hỗn hợp đồng nhất.
(Xem giải) Câu 10: Mỗi phân tử hemoglobin (thành phần cấu tạo nên hồng cầu) chứa 4 heme B. Mỗi heme B là phức chất với nguyên tử trung tâm là Fe2+. Cấu hình electron của ion Fe2+ là (cho Fe có Z = 26).
A. [Ar]3d6 4s2. B. [Ar]3d5. C. [Ar]3d8 4s2. D. [Ar]3d6.
(Xem giải) Câu 11: Tên gọi của hợp chất CH3NHCH3 là
A. ethylmethylamine. B. dimethylamine. C. propylamine. D. diethylamine.
(Xem giải) Câu 12: Loại polymer nào sau đây được điều chế bằng phản ứng trùng ngưng?
A. Nylon-6,6. B. PVC. C. PS. D. Cao su buna.
(Xem giải) Câu 13: Nước là chất điện li yếu: H2O ⇌ H+ + OH−
Tích số nồng độ các ion H+ và OH−trong nước nguyên chất ở mỗi nhiệt độ là một hằng sô, gọi là tích số ion của nước, kí hiệu Kw (Kw = [H+][OH−]). Độ acid và độ kiềm của dung dịch có thể được đánh giá bằng nồng độ H+ hoặc quy về một giá trị gọi là pH với quy ước như sau: pH = −lg[H+]. Hình bên biểu diễn sự thay đổi pH của nước tinh khiệt theo nhiệt độ:
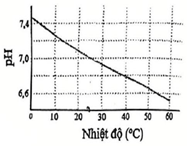
Cho các phát biểu sau:
(a) Nước tinh khiết có [H+] = [OH−].
(b) Quá trình điện li của nưởc là quá trình thu nhiệt.
(c) Ở 25°C, nước tinh khiết có pH = 7.
(d) pH của nước tinh khiết giảm khi tăng nhiệt độ.
Số phát biểu đúng là
A. 3. B. 4. C. 1. D. 2.
(Xem giải) Câu 14: Tùy theo pH của môi trường mà các amino acid có thể tồn tại dưới dạng tích điện âm, tích điện dương hoặc trung hòa về điện (ion luỡng cực). Điểm đẳng điện (pI) là giá trị pH mà tại đó tổng điện tích của một phân tử amino acid bằng không. Giá trị pI của glutamic acid, glycine, lysine được cho ở bảng sau:
| Chất | Glutamic acid | Glycine | Lysine |
| pI | 3,08 | 5,97 | 9,8 |
Phát biểu nào sau đây đúng về quá trình điện di hỗn hợp gồm glutamic acid, glycine và lysine?
A. Với môi trường pH = 5,97 thì không thể tách riêng các amino acid trong hỗn hợp.
B. Với môi trường pH = 5,97, glycine hầu như không di chuyển trong điện trường.
C. Với môi trường pH = 9,8, lysine tồn tại dạng anion và di chuyển về cực dương.
D. Với môi trường pH = 3,08, glutamic acid tồn tại dạng cation và di chuyển về cực âm.
(Xem giải) Câu 15: Đất phèn là loại đất có độ pH nhỏ hơn 6,5. Một mẫu đất có chứa nhiều ion Fe3+ làm giảm độ pH của đất. Chất nào sau đây có thể làm hạ phèn (nâng cao pH) cho mẫu đất trên?
A. CaO. B. HCl. C. NaCl. D. H2SO4.
(Xem giải) Câu 16: Hiện tượng nào sau đây không phải là hiện tượng ăn mòn kim loại?
A. Thép carbon bị gỉ sắt màu nâu đỏ. B. Vòng bằng kim loại bạc bị xỉn màu.
C. Chuông đồng bị gỉ đồng màu xanh. D. Đá vôi bị tan ra bởi mura acid.
(Xem giải) Câu 17: Điện phân dung dịch NaCl bão hòa với điện cực trơ, màng ngăn xốp. Quá trình xảy ra đầu tiên ở điện cực anode là
A. 2Cl− ⟶ Cl2 + 2e. B. 2H2O + 2e ⟶ H2 + 2OH−.
C. Na+ + 1e ⟶ Na. D. 2H2O ⟶ O2 + 4H+ + 4e.
(Xem giải) Câu 18: Độ tan của NaHCO3 theo nhiệt độ được cho trong bảng sau:
| Nhiệt độ (°C) | 20 | 40 | 60 |
| Độ tan (gam/100 gam nước) | 9,6 | 12,7 | 16,5 |
Làm lạnh 1 kg dung dịch NaHCO3 bão hoà ơ 60°C đến khi thu được dung dịch bão hòa ở 40°C thì tách ra m gam NaHCO3. Giá trị của m gần nhất với giá trị nào sau đây?
A. 59,23. B. 16,76. C. 50,48. D. 32,62.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Chất hữu cơ E được tổng hợp từ alcohol X và chất hữu cơ Y (biết Y là hợp chất tạp chức trong phân tử có chứa vòng benzene). Chất E có trong thành phần của một số thuốc giảm đau, xoa bóp, cao dán,dùng để điều trị đau lưng, căng cơ, bong gân. Phân tích nguyên tố cho kết quả phần trăm về khối lượng các nguyên tố trong E như sau: 63,16%C; 5,26%H còn lại là nguyên tố O. Phân tử khối của E được xác định thông qua kết quả phổ khối lượng với peak ion phân tử [M+] có giá trị m/z là 152. Phổ IR của E có các tín hiệu hấp thụ đặc trưng trong khoảng 1750 − 1735 cm−1; 1300 − 1000 cm−1 và 3650 − 3200 cm−1.
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O-H (alcohol) | O-H (carboxylic acid) | C=O (ester, carboxylic acid) | C-O (alcohol, ester, carboxylic acid) |
| Số sóng (cm−1) | 3650 − 3200 | 3300 − 2500 | 1780 − 1650 | 1300 − 1000 |
a) Phản ứng tổng hợp E từ X và Y được gọi là phản ứng thuỷ phân ester.
b) Liên kết O − H trong X hấp thụ số sóng trong khoảng 3650 − 3200 cm−1.
c) Công thức phân tử của E là C8H8O3.
d) Nếu thoa chất E lên vết thương hoặc vùng da bị rạn nứt thì E sẽ làm cho vết thương lâu lành hơn.
(Xem giải) Câu 20: Poly(vinyl chloride) (PVC) là chất dẻo có tính cách điện tốt, không thấm nước, bền với acid vì vậy nó được dùng để sản xuất vật liệu cách điện, ống dẫn nước,… Khi đun nóng, PVC mềm ra rồi nóng chảy và khi để nguội nó lại đóng rắn. Hiện nay, trong công nghiệp sản xuất PVC người ta đi từ nguyên liệu là khí ethylene và chlorine. Quy trình sản xuất thực hiện theo sơ đồ khép kín như sau:
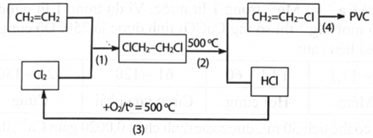
a) Có thể xử lý chất thải nhựa PVC bằng cách đốt cháy vì sản phẩm cháy không gây ô nhiễm môi trường.
b) Phản ứng tổng hợp PVC từ vinyl chloride được gọi là phản ứng trùng hợp.
c) PVC thuộc loại polymer nhiệt dẻo và vật liệu làm bằng PVC có thể tái chế.
d) Từ 2 tấn ethylene có thể sản xuất được 3,24 tấn PVC theo sơ đồ trên với hiệu suất của phản úng (1), (2), (4) lần lượt là 90%, 85% và 95% (làm tròn đến hàng phần trăm).
(Xem giải) Câu 21: Trong công nghiệp, nhôm (Al) được điều chế bằng phương pháp điện phân nóng chảy Al2O3 (tách từ quặng bauxite) với các điện cực bằng than chì. Al2O3 có nhiệt độ nóng chảy rất cao (2050°C) nên được trộn cùng với cryolite (Na3AlF6) để tạo thành hỗn hợp nóng chảy ở khoảng 1000°C. Giải pháp này giúp tiết kiệm nhiều năng lượng cũng như giảm giá thành chế tạo bể điện phân.
a) Sau khi điện phân, nếu khí thu được ở anơde có tỉ khối so với khí H2 bằng 16 thì ở anode chỉ có khí O2.
b) Cryolite làm giảm độ dẫn điện của hỗn hợp nóng chảy.
c) Quặng bauxite có thành phần chính là Al2O3.2H2O.
d) Để sản xuất được 8,1 tấn Al (với hiệu suất chuyển hoá Al2O3 thành Al là 95%) thì cần 16,1 tấn Al2O3 (làm tròn đến hàng phần mười).
(Xem giải) Câu 22: Muối CuSO4 khan màu trắng khi tan vào nước tạo thành dung dịch có màu xanh do hình thành phức chất X. Nhỏ từ từ đến dư dung dịch NH3 đặc vào dung dịch thu được, lúc đầu thấy xuất hiện kết tủa Y màu xanh nhạt, sau đó kết tủa tan dần tạo thành dung dịch màu xanh lam chứa phức chất Z.
a) Công thức của X và Y lần lượt là [Cu(H2O)6]2+ và [Cu(NH3)4]2+.
b) CuSO4 là hợp chất của kim loại chuyển tiếp dãy thứ nhất.
c) Trong phức chất Y, liên kết giữa nguyên tử trung tâm và phối tử là liên kết ion.
d) CuSO4 khan được dùng để phát hiện nước lẫn trong xăng dầu nhờ sự đổi màu khi tiếp xúc với nước.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Ethyl acetate được sử dụng làm dung môi để pha sơn, mực máy in. Phân tử khối của ethyl acetate bằng bao nhiêu?
(Xem giải) Câu 24: Tiến hành sản xuất rượu vang bằng phương pháp lên men rượu với hiệu suất toàn bộ quá trình là 75%. Từ 50 kg quả nho tươi (chứa 22,5% glucose về khối lượng) có thể sản xuất được V lít rượu vang 13,8°. Biết khối lượng riêng của ethyl alcohol là 0,8 g/mL. Giả thiết trong thành phần quả nho tươi chỉ có glucose bị lên men rượu. Giá trị của V bằng bao nhiêu (làm tròn đến hàng phần mười)?
(Xem giải) Câu 25: Cho các chất sau: glucose, fructose, saccharose, amylose, maltose. Có bao nhiêu chất bị thủy phân trong môi trường acid?
(Xem giải) Câu 26: Cho phương trình hoá học của phản ứng nung vôi và đốt cháy methane sau:
(1) CaCO3(s) ⟶ CaO(s) + CO2(g)
(2) CH4(g) + 2O2(g) ⟶ CO2(g) + 2H2O(g)
Biết nhiệt tạo thành của các chất ở điều kiện chuẩn được cho trong bảng sau:
| Chất | CH4(g) | CO2(g) | H2O(g) | CaCO3(s) | CaO(s) |
| −74,6 | −393,5 | −241,8 | -1207 | -635 |
Ở điều kiện chuẩn, để cung cấp nhiệt cho phản ứng nhiệt phân 1 tấn CaCO3 theo phương trình (1), cần phải đốt cháy hoàn toàn m kg CH4 theo phương trình (2). Giả thiết hiệu suất các quá trình đều bằng 100%. Giá trị của m là bao nhiêu (làm tròn đến hàng phần mười)?.
(Xem giải) Câu 27: Thép thường (thép carbon) là hợp kim của Fe, C và một số nguyên tố khác. Tiến hành thí nghiệm sau đây để xác định hàm lượng Fe có trong một mẫu thép:
• Cân 3,56 gam mẫu thép rồi hòa tan hết bằng dung dịch H2SO4 1M, chuyển toàn bộ dung dịch sau hòa tan vào bình định mức 100 mL rồi thêm nước cất tới vạch, thu được 100 mL dung dịch X.
• Chuẩn độ 10,0 mL X (trong môi trường sulfuric acid loãng, dư) bằng dung dịch KMnO4 0,1M đến khi xuất hiện màu hồng nhạt bền trong khoảng 20 giây thì dừng. Thể tích của dung dịch KMnO4 sau 3 lần chuẩn độ như sau:
| Lần chuẩn độ | Lần 1 | Lần 2 | Lần 3 |
| Thể tích dung dịch | 12,6 | 12,4 | 12,5 |
Phần trăm khối lượng của Fe trong mẫu thép là a%. Giá trị của a bằng bao nhiêu (làm tròn đến hàng phần mười)?.
(Xem giải) Câu 28: Cho bảng giá trị thế điện cực chuẩn của một số cặp oxi hóa – khử như sau:
| Cặp oxi hóa – khử | Na+/Na | Mg2+/Mg | Al3+/Al | Fe2+/Fe | Cu2+/Cu |
| Thế điện cực chuẩn (V) | −2,713 | −2,356 | −1,676 | −0,440 | +0,340 |
Trong bảng trên, có bao nhiêu kim loại có thể tách được Cu từ dung dịch CuSO4?

Bình luận