[2026] Thi thử TN trường Hoàng Diệu, Sào Nam – Đà Nẵng (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 075
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2A | 3C | 4A | 5A | 6D | 7D | 8B | 9C |
| 10A | 11B | 12C | 13A | 14B | 15B | 16C | 17B | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | S | Đ | 6 | 4132 | 234 |
| (b) | Đ | S | S | Đ | 26 | 27 | 28 |
| (c) | Đ | Đ | Đ | S | 57,5 | 23,6 | 124 |
| (d) | S | Đ | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Chất nào sau đây được sử dụng làm chất giặt rửa tổng hợp?
A. C15H31COONa. B. C15H31COOCH3. C. CH3[CH2]11OSO3Na. D. CH3COOK.
(Xem giải) Câu 2: Loại carbohydrate mạch phân nhánh, có nhiều trong các loại ngũ cốc là
A. amylopectin. B. saccharose. C. amylose. D. cellulose.
(Xem giải) Câu 3: Số gốc α-amino acid trong phân tử tripeptide mạch hở là
A. 2. B. 4. C. 3. D. 1.
(Xem giải) Câu 4: Polymer nào sau đây thuộc loại polymer tổng hợp?
A. polyethylene. B. tinh bột. C. tơ tằm. D. cellulose.
(Xem giải) Câu 5: Cho một pin điện hoá được tạo bởi các cặp oxi hoá khử Cu2+/Cu, Ag+/Ag ở điều kiện chuẩn. Quá trình xảy ra ở cathode khi pin hoạt động là
A. Ag+ + 1e → Ag. B. Ag → Ag+ + 1e. C. Cu → Cu2+ + 2e. D. Cu2+ + 2e → Cu.
(Xem giải) Câu 6: Cho khối lượng riêng của các chất như bảng sau:
| Chất | Li | Na | K | Ca | Dầu hỏa |
| Khối lượng riêng (g/mL) | 0,53 | 0,97 | 0,86 | 1,54 | 0,80 |
Để bảo quản một số kim loại mạnh, người ta thường ngâm chìm kim loại đó trong dầu hỏa. Trong số các kim loại trên, có bao nhiêu kim loại bảo quản được trong dầu hỏa?
A. 1. B. 4. C. 2. D. 3.
(Xem giải) Câu 7: Phát biểu nào sau đây sai?
A. Tất cả các kim loại nhóm IA đều tan tốt trong nước ở nhiệt độ thường.
B. Nước chứa nhiều ion Ca2+, Mg2+, HCO3-, Cl-, SO42- thuộc loại nước có tính cứng toàn phần.
C. Kim loại nhóm IA đều có cấu trúc mạng tinh thể lập phương tâm khối.
D. Sự tạo thành thạch nhũ trong hang động là do CaCO3 bị phân huỷ thành CaO.
(Xem giải) Câu 8: Nhỏ vài giọt nước bromine vào ống nghiệm chứa 2 mL dung dịch X, thu được kết tủa trắng. Chất nào sau đây phù hợp với X?
A. Methylamine. B. Aniline. C. Ethylamine. D. Dimethylamine.
(Xem giải) Câu 9: Kim loại nào sau đây dẫn điện tốt nhất?
A. Al. B. Cu. C. Ag. D. Au.
(Xem giải) Câu 10: Trong quá trình Solvay, ở giai đoạn tạo thành NaHCO3 tồn tại cân bằng sau: NaCl(aq) + NH3(aq) + CO2(g) + H2O(l) ⇋ NaHCO3(s) + NH4Cl(aq). Khi làm lạnh dung dịch trên, muối bị tách ra khỏi dung dịch là
A. NaHCO3 B. NH4Cl C. NaCl. D. NH4HCO3.
(Xem giải) Câu 11: Hạt nhân 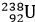 sau một chuỗi các quá trình phóng xạ α và β− liên tiếp biến đổi thành hạt nhân
sau một chuỗi các quá trình phóng xạ α và β− liên tiếp biến đổi thành hạt nhân 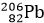 bền theo phương trình chuỗi phản ứng:
bền theo phương trình chuỗi phản ứng: 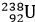 →
→ 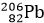 + x
+ x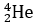 + y
+ y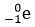 .
.
Trong đó, x và y lần lượt là số lần phóng xạ α và β- trong chuỗi phóng xạ. Giá trị của y là
A. y = 4. B. y = 6. C. y = 8. D. y = 5.
(Xem giải) Câu 12: Trong công nghiệp năng lượng, hydrogen (H2) được sản xuất từ khí tổng hợp thông qua phản ứng water gas shift (WGS): CO(g) + H2O(g) ⇋ CO2(g) + H2(g) ![]() = -41,2 kJ/mol. Khảo sát ảnh hưởng của tỉ lệ hơi nước/CO (R) lên độ chuyển hóa của CO theo nhiệt độ được biểu diễn qua đồ thị bên cạnh:
= -41,2 kJ/mol. Khảo sát ảnh hưởng của tỉ lệ hơi nước/CO (R) lên độ chuyển hóa của CO theo nhiệt độ được biểu diễn qua đồ thị bên cạnh:
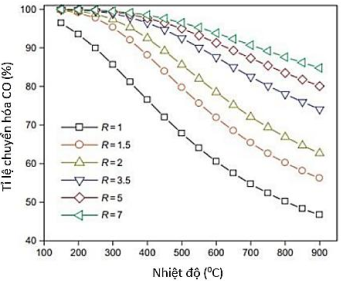
Phát biểu nào sau đây đúng?
A. Phản ứng trên là phản ứng thu nhiệt.
B. Khi tăng áp suất, phản ứng trên chuyển dịch theo chiều thuận.
C. Khi R tăng thì tỉ lệ chuyển hóa của CO tăng.
D. Khi tăng nhiệt độ, tốc độ phản ứng giảm.
(Xem giải) Câu 13: Peptide mạch hở X có cấu trúc phân tử như sau:
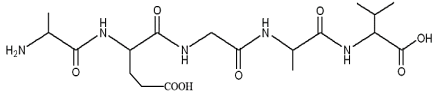
Phát biểu nào sau đây sai?
A. X tác dụng với dung dịch NaOH theo tỷ lệ mol nX : nNaOH = 1 : 5.
B. Trong phân tử X có 4 liên kết peptide.
C. Amino acid đầu C của peptide X là valine.
D. X phản ứng được với Cu(OH)2 trong môi trường kiềm tạo dung dịch màu tím đặc trưng.
(Xem giải) Câu 14: Một học sinh lắp bộ điện phân để mạ đồng lên một chiếc chìa khóa bằng sắt theo sơ đồ sau:
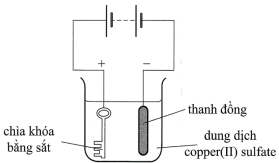
Kết quả của thí nghiệm là không thu được lớp mạ trên chìa khóa. Cần thực hiện thay đổi nào dưới đây để quá trình mạ điện xảy ra được?
A. Tăng điện áp điện phân.
B. Đổi vị trí thanh đồng và chìa khoá sắt cho nhau.
C. Thay dung dịch copper(II) sulfate bằng dung dịch sulfuric acid loãng.
D. Tăng nồng độ dung dịch copper(II) sulfate.
(Xem giải) Câu 15: Cho biết Mg (Z = 12) và Al (Z = 13) là những kim loại quen thuộc. Hợp kim 5005 chứa 99,2% Al và 0,8% Mg theo khối lượng, được ứng dụng làm vật liệu kim loại nhờ các đặc tính như nhẹ và bền. Cho các nhận định sau:
(a) Bán kính nguyên tử của Mg lớn hơn bán kính nguyên tử của Al.
(b) Trong hợp kim 5005, tỉ lệ số nguyên tử Al : Mg bằng 124 : 1.
(c) Do đặc tính bền và nhẹ nên hợp kim 5005 được ứng dụng trong kiến trúc (ốp mặt tiền, trần nhà,…)
(d) Hợp kim 5005 không bị ăn mòn trong dung dịch acid hoặc kiềm.
Các nhận định đúng là
A. (a), (b), (c). B. (a), (c). C. (b), (c). D. (b), (c), (d).
(Xem giải) Câu 16: Có 5 kim loại X, Y, Z, T, Q, tất cả đều có hóa trị II. Tiến hành thí nghiệm như sau:
Thí nghiệm 1. Cho 5 kim loại vào dung dịch hydrochloric acid. Chỉ có Q không có phản ứng, 4 kim loại còn đều có hiện tượng sủi bọt khí.
Thí nghiệm 2. Kim loại X, Y không phản ứng với dung dịch Z2+.
Thí nghiệm 3. Từ 5 kim loại trên, thiết lập các pin điện hóa dạng: M(s) | M2+(aq) || N2+(aq) | N(s). Pin có suất điện động chuẩn lớn nhất là pin của T-Q
Cho các phát biểu sau:
(1) T là kim loại có tính khử mạnh nhất.
(2) Z2+ có tính oxi hóa mạnh nhất trong các ion của 5 kim loại trên.
(3) Q có tính oxi hóa mạnh hơn Y.
(4) Thế điện cực chuẩn của cặp X2+/X lớn hơn Q2+/Q.
(5) Thế điện cực chuẩn của cặp Y2+/Y lớn hơn Z2+/Z.
Số phát biểu sai là
A. 2. B. 1. C. 3. D. 4.
(Xem giải) Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
Nhựa PET (poly(ethylene terephthalate) – kí hiệu số 1 như hình bên) là một polymer được điều chế từ terephthalic acid và ethylene glicol – loại polymer được sử dụng để làm chai lọ, bao bì nhưng lại rất khó phân hủy trong tự nhiên. Gần đây, các nhà khoa học đã phát hiện ra chủng vi khuẩn Ideonella sakaiensis có khả năng tiết ra enzyme có khả năng phân hủy loại nhựa này. Để nghiên cứu tốc độ phân hủy nhựa PET, người ta cho một mảnh nhựa PET dạng tấm hình vuông (cạnh 4,0 cm, độ dày 0,03 cm và khối lượng riêng 1,45 g/cm³) vào một bể chứa lượng lớn vi khuẩn Ideonella sakaiensis. Do mật độ vi khuẩn lớn, chúng bám kín toàn bộ bề mặt của mảnh nhựa nên tốc độ phân hủy nhựa PET của vi khuẩn đạt mức cực đại và gần như không đổi. Thực nghiệm xác định được khối lượng nhựa bị phân hủy trung bình là 8,12 mg/ngày. Sau 12 ngày liên tục, mảnh nhựa trên đã bị vi khuẩn phân hủy a% về khối lượng. Thực hiện thí nghiệm tương tự với những mảnh nhựa PET với độ kết tinh khác nhau, thu được kết quả như đồ thị bên cạnh.
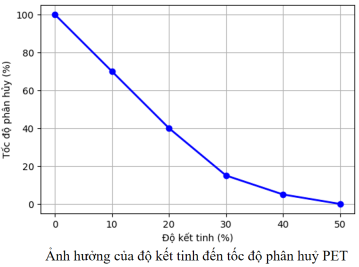
Câu 17: Giá trị của a bằng (kết quả các phép tính trung gian không được làm tròn, kết quả làm tròn đến hàng phần mười)
A. 56,0. B. 14,0. C. 3,5. D. 1,2.
Câu 18: Cho các phát biểu sau về nhựa PET
(1) Phản ứng tổng hợp PET từ terephthalic acid và ethylene glicol thuộc loại phản ứng trùng ngưng.
(2) PET rất khó phân hủy trong tự nhiên vì bền trong môi trường acid.
(3) Tơ được chế tạo từ PET thuộc loại tơ bán tổng hợp.
(4) Số 1 trong kí hiệu nhận dạng cho biết đồ dùng làm từ PET chỉ sử dụng một lần.
(5) Độ kết tinh của nhựa và tốc độ phân huỷ tỷ lệ thuận với nhau.
Số nhận định đúng là
A. 3. B. 2. C. 1. D. 4.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Áp dụng kiến thức về các yếu tố ảnh hưởng đến tốc độ phản ứng trong phần tổng hợp ester, một nhóm học sinh dự đoán “nhiệt độ càng cao, hiệu suất ester hóa càng cao”. Để kiểm chứng cho dự đoán trên, nhóm đã tiến hành thí nghiệm phản ứng tổng hợp propyl acetate từ alcohol và acid tương ứng với nồng độ không đổi ở các điều kiện nhiệt độ khác nhau tương ứng theo phương trình:
CH3COOH + CH3CH2CH2OH ⇋ CH3COOCH2CH2CH3 + H2O (1)
Kết quả thu được như bảng:
| Nhiệt độ (°C) | 60 | 65 | 70 | 75 | 80 | 85 |
| Thể tích ester (mL) | 26,0 | 30,5 | 35,0 | 40,0 | 36,5 | 31,0 |
Cho độ tan trong 100 gam nước của các chất như bảng sau
| Chất | CH3COOH | CH3CH2CH2OH | CH3COOCH2CH2CH3 |
| Độ tan (gam – ở 25°C) | Vô hạn | Vô hạn | 1,6 |
a) Từ kết quả trên, dự đoán của học sinh là sai.
b) Trong phản ứng (1), H2O được tạo thành từ -OH của acid và -H của alcohol.
c) Có thể dùng phương pháp chiết lỏng – lỏng để tách CH3COOCH2CH2CH3 ra khỏi hỗn hợp sản phẩm.
d) Vì CH3COOH và CH3CH2CH2OH đều có nhóm -OH nên không thể dùng phương pháp phổ hồng ngoại (IR) để nhận biết 2 chất trên.
(Xem giải) Câu 20: Trong công nghiệp, kim loại magnesium (Mg) được sản xuất từ quặng carnalite (có thành phần chính là KCl.MgCl2.6H2O) bằng phương pháp điện phân nóng chảy. Trước khi điện phân, carnalite được nung nóng để loại bỏ nước. Khi điện phân, KCl có vai trò hạ nhiệt độ nóng chảy của hỗn hợp, giúp giảm chi phí sản xuất. Sơ đồ thiết bị quá trình điện phân được mô tả như hình bên:
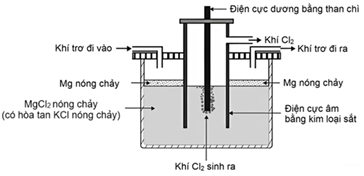
a) Tại cathode xảy ra quá trình khử.
b) Khí trơ được sử dụng trong quá trình điện phân trên là khí nitrogen.
c) Khối lượng riêng của kim loại Mg nóng chảy nhỏ hơn khối lượng riêng của hỗn hợp MgCl2 và KCl nóng chảy.
d) Bằng phương pháp trên, nếu dùng 1 tấn quặng carnalite (chứa 43% KCl.MgCl2.6H2O về khối lượng, còn lại là tạp chất không chứa magnesium) với hiệu suất cả quá trình sản xuất là 75% thì thu được 27,9 kg magnesium. (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 21: Khí thải động cơ xăng (hoặc dầu) ngoài thành phần là carbon dioxide và hơi nước, còn có thể có carbon monoxide, các oxide của nitrogen (NOa) và hydrocarbon (CxHy) chưa bị cháy hết. Để giảm bớt tác hại của khí thải với môi trường, bên cạnh việc tăng hiệu quả đốt cháy, người ta còn sử dụng bộ chuyển đổi xúc tác (đưa chất xúc tác vào ống xả của động cơ) giúp chuyển hóa các chất ô nhiễm, chất độc hại trong khí thải thành những chất ít gây hại hơn. Một bộ chuyển đổi xúc tác được minh họa như hình sau:
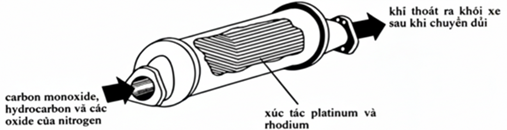
a) Phản ứng tổng quát xảy ra trong bộ chuyển đổi xúc tác là CxHy + NOa → H2O + CO2 + N2.
b) Hàm lượng khí thải chứa nhiều CO2 là nguyên nhân chính gây ra hiện tượng mưa acid.
c) CO là một khí độc, người hít nhiều khí CO sẽ làm giảm khả năng vận chuyển oxygen dẫn đến bị chết ngạt.
d) Một xe ô tô chạy 100 km tiêu thụ hết 5 L xăng (coi như xăng chỉ chứa C8H18), với khối lượng riêng 0,8 gam/mL. Quá trình cháy hoàn toàn lượng xăng nói trên tạo ra hỗn hợp khí thải chứa tỉ lệ số mol như sau: nCO2 : nCO : nNO = 8 : 2 : 3. Thể tích khí oxygen đã tham gia vào các phản ứng trên (đkc) bằng 11221 L. (các phép tính trung gian không làm tròn, kết quả làm tròn đến hàng đơn vị)
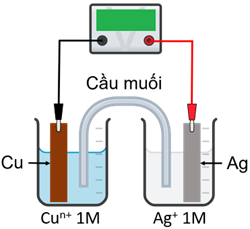
(Xem giải) Câu 22: Một nhóm học sinh thiết lập pin điện hoá với điện cực Cun+/Cu và Ag+/Ag ở điều kiện chuẩn theo sơ đồ như hình dưới. Các giá trị thế điện cực chuẩn và biến thiên enthalpy chuẩn của một số cặp oxi hoá – khử được cho ở trong bảng:
Cu2+(aq) + e → Cu+(aq) E° = +0,16V
Cu2+(aq) + 2e → Cu(s) E° = +0,34V
Cu+(aq) + e → Cu(s) E° = +0,52V
Ag+(aq) + e → Ag(s) E° = +0,80V
a) Khi pin hoạt động, điện cực Ag luôn đóng vai trò là cathode.
b) Với n = 2 sức điện động chuẩn của pin đo được bằng 0,46 V.
c) Khi pin hoạt động sẽ phát sinh dòng điện do sự di chuyển của các ion trong cầu muối về các điện cực.
d) Cầu muối có vai trò khép kín mạch điện và trung hoà điện tích ở hai điện cực.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Ion M3+ có cấu hình electron được biểu diễn dưới dạng orbital (AO) như sau:
![]()
Ở trạng thái cơ bản, nguyên tử M có bao nhiêu ectron độc thân?
(Xem giải) Câu 24: Thực hiện các thí nghiệm được đánh số theo thứ tự sau:
(1) Cho 2 mL dung dịch NaOH 10% vào ống nghiệm, thêm 0,5 mL dung dịch CuSO4 5% vào, lắc nhẹ. Thêm tiếp 3 mL dung dịch saccharose 5% vào ống nghiệm, lắc đều.
(2) Cho khoảng 2 mL dung dịch NaOH 10% và khoảng 0,5 mL dung dịch CuSO4 5% vào ống nghiệm, lắc nhẹ. Cho tiếp khoảng 3 mL dung dịch glucose 2% vào ống nghiệm và lắc đều. Đun nóng nhẹ hỗn hợp trong ống nghiệm trên ngọn lửa đèn cồn vài phút.
(3) Cho khoảng 1 mL nước bromine vào ống nghiệm sau đó thêm vài giọt aniline loãng vào ống nghiệm.
(4) Cho vào ống nghiệm khoảng 1 mL dung dịch I2 trong KI và khoảng 1mL dung dịch NaOH 10%. Nhỏ từ từ 5 giọt acetaldehyde vào ống nghiệm, lắc đều.
Gán số thứ tự của thí nghiệm trên tương ứng với các hiện tượng a, b, c, d được mô tả bên dưới.
a) xuất hiện kết tủa màu vàng.
b) xuất hiện dung dịch màu xanh lam.
c) xuất hiện kết tủa màu trắng.
d) xuất hiện kết tủa đỏ gạch.
(Xem giải) Câu 25: Thực hiện các thí nghiệm sau:
(1) Cho một dây Zinc (Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
(2) Cho một dây Zinc (Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M nhỏ thêm vài giọt dung dịch CuSO4.
(3) Quấn sợi dây đồng trên một đinh sắt, sau đó nhúng vào cốc đựng 2mL dung dịch NaCl.
(4) Cho một đoạn dây thép vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
(5) Cho một dây bạc sạch vào ống nghiệm chứa 2 mL dung dịch CuSO4 0,2 M.
Liệt kê (theo thứ tự tăng dần) số thí nghiệm xuất hiện ăn mòn điện hóa?
(Xem giải) Câu 26: Phản ứng lên men lactic là quá trình chuyển hóa đường glucose thành lactic acid (C3H6O3) nhờ vi khuẩn lactic trong điều kiện kỵ khí, thường gặp trong thực phẩm lên men và cơ bắp khi thiếu oxygen. Lên men lactic gồm hai dạng chính: đồng hình, chỉ tạo lactic acid và dị hình, tạo lactic acid cùng một số sản phẩm khác, được mô tả trong hai sơ đồ sau với đúng tỉ lệ mol:
– Lên men lactic đồng hình: C6H12O6(aq) → 2C3H6O3(aq) ![]() = -115kJ.
= -115kJ.
– Lên men lactic dị hình: C6H12O6(aq) → C3H6O3(aq) + C2H5OH(aq) + CO2(g) ![]() = -91,5kJ.
= -91,5kJ.
Khi vận động mạnh cơ thể không đủ cung cấp oxygen, thì cơ thể sẽ chuyển hoá glucose thành lactic acid từ các tế bào để cung cấp năng lượng cho cơ thể. Biết rằng cơ thể chỉ cung cấp 98% năng lượng nhờ oxygen, năng lượng còn lại nhờ vào sự chuyển hoá glucose thành lactic acid.
Giả sử một người chạy bộ trong một thời gian tiêu tốn 400 kcal và glucose lên men đồng hình và dị hình theo tỷ lệ mol 1 : 1. Tính khối lượng glucose tham gia vào quá trình chuyển hóa đó (biết 1 cal = 4,184 J). (kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 27: Có hai dung dịch X và Y mỗi dung dịch chỉ chứa hai loại cation và hai loại anion trong số các ion sau (X, Y không chứa cùng loại ion):
| Ion | K+ | Mg2+ | Na+ | H+ | HCO3- | SO42- | NO3- | CO32- |
| Số mol | 0,15 | 0,2 | 0,25 | 0,15 | 0,1 | 0,15 | 0,25 | 0,15 |
Biết dung dịch Y hoà tan được Fe2O3. Nếu đun đến cạn dung dịch X thì thu được m gam chất rắn khan. Giá trị m là bao nhiêu? (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 28: Muối Mohr là một dạng muối kép có tác dụng chống lại quá trình oxi hóa bằng không khí. Muối Mohr được tạo thành từ hỗn hợp E cùng số mol gồm iron(II) sulfate ngậm 7 phân tử nước và ammonium sulfate khan. Cân 7,35 gam muối Mohr trên rồi hòa tan vào nước, sau đó định mức trong bình 50 mL. Chuẩn độ 5 mL dung dịch vừa pha cần dùng 12,5 mL dung dịch KMnO4 0,03M trong môi trường H2SO4 loãng, dư theo phương trình:
Fe2+ + MnO4- + H+ → Fe3+ + Mn2+ + H2O (1)
Từ m gam E người ta điều chế muối Mohr với hiệu suất 65%; hòa tan muối Mohr này vào nước thu được dung dịch F. Hạ dần nhiệt độ F xuống 20°C thu được 74,93 gam dung dịch và 31,2 gam muối Mohr kết tinh. Cho biết độ tan muối Mohr ở 20°C là 27 gam. (chỉ làm tròn đến phép tính cuối cùng, các kết quả làm tròn đến hàng phần mười). Cho các phát biểu sau:
(1) Giá trị của m bằng 75,8.
(2) Phần trăm khối lượng của Fe trong muối Mohr tạo thành ở trên bằng 14,3%.
(3) Trong quá trình chuẩn độ Fe2+ bằng KMnO4, có thể thay dung dịch H2SO4 loãng bằng dung dịch HCl.
(4) Tổng hệ số cân bằng (nguyên – tối giản) trong phản ứng (1) bằng 24.
(5) Để bảo quản muối Mohr, có thể bảo quản trong dung dịch có môi trường kiềm.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần.


Bình luận