[2026] Thi thử TN trường Nguyễn Khuyến – Lê Thánh Tông – TP Hồ Chí Minh
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 036
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2B | 3C | 4D | 5D | 6C | 7A | 8C | 9D |
| 10C | 11C | 12A | 13D | 14C | 15C | 16B | 17B | 18B |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | S | Đ | Đ | 2415 | 1 | 8117 |
| (b) | Đ | Đ | Đ | S | 26 | 27 | 28 |
| (c) | S | Đ | S | Đ | 369 | 4 | 3 |
| (d) | S | S | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Amine nào sau đây tạo kết tủa trắng với nước bromine?
A. Methylamine. B. Dimethylamine. C. Phenylamine. D. Ethylamine.
(Xem giải) Câu 2: Ethambutol là một loại thuốc kháng sinh, có tác dụng trong điều trị các bệnh nhiễm trùng do vi khuẩn. Ethambutol có công thức cấu tạo như hình bên.
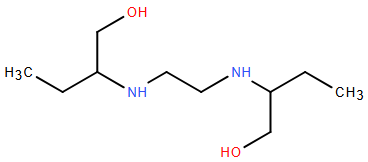
Trong công thức của ethambutol có chứa những loại nhóm chức nào?
A. Nhóm chức amine và nhóm OH của phenol.
B. Nhóm chức amine và nhóm OH của alcohol.
C. Nhóm chức amide và nhóm chức ester.
D. Chỉ có nhóm OH của alcohol.
(Xem giải) Câu 3: Cho glucose (C6H12O6) vào ống nghiệm chứa Cu(OH)2 và dung dịch NaOH, đun nóng xảy ra phản ứng sau:
HOCH2[CHOH]4CHO + 2Cu(OH)2 + NaOH → HOCH2[CHOH]4COONa + Cu2O + 3H2O
Chất bị oxi hóa trong phản ứng trên là
A. NaOH. B. Cu(OH)2. C. C6H12O6. D. H2O.
(Xem giải) Câu 4: Để phân biệt dung dịch ethylamine và dimethylamine, có thể dùng thuốc thử là dung dịch chất nào sau đây?
A. HCl. B. FeCl3. C. HNO3. D. HNO2.
(Xem giải) Câu 5: Trong phân tử glutamic acid (2-aminopentan-1,5-dioic acid) có bao nhiêu nguyên tử oxygen?
A. 2. B. 6. C. 3. D. 4.
(Xem giải) Câu 6: Biết những chất lỏng có điểm chớp cháy thấp hơn 37,8°C là chất lỏng dễ cháy. Cho bảng số liệu về điểm chớp cháy của một số chất lỏng sau:
| Chất | Isooctane | Benzene | Methanol | Formic acid | Ethylene glycol |
| Điểm chớp cháy (°C) | -12 | -11 | 11 | 50 | 111 |
Nhận định nào sau đây đúng?
A. Trong số các chất trên, có hai chất thuộc loại hợp chất arene.
B. Trong số các chất trên, ethylene glycol có khả năng gây cháy, nổ cao nhất.
C. Trong số các chất trên, có ba chất lỏng dễ cháy.
D. Methanol có điểm chớp cháy thấp hơn formic acid nên khó bốc cháy hơn.
(Xem giải) Câu 7: Khi thủy phân hoàn toàn 1 mol triglyceride thì luôn thu được
A. 1 mol glycerol. B. 3 mol muối của acid béo.
C. 3 mol acid béo. D. 1 mol ethylene glycol.
(Xem giải) Câu 8: Phát biểu nào sau đây không đúng?
A. Amylose và cellulose đều có cấu trúc mạch không phân nhánh.
B. Có thể phân biệt glucose và fructose bằng nước bromine.
C. Fructose chuyển hoá thuận nghịch thành glucose trong môi trường acid.
D. Có thể phân biệt được glucose và saccharose bằng thuốc thử Tollens.
(Xem giải) Câu 9: Cho tetrapeptide Ala-Ala-Gly-Gly vào ống nghiệp chứa Cu(OH)2 trong môi trường NaOH, sau phản ứng trong ống nghiệp xuất hiện màu
A. đỏ gạch. B. vàng. C. xanh lam. D. tím.
(Xem giải) Câu 10: Ở điều kiện thường, chất nào sau đây tồn tại ở thể rắn và dễ tan trong nước?
A. Ethanamine. B. Cellulose. C. Alanine. D. Methyl acetate.
(Xem giải) Câu 11: Peptit X có cấu tạo như sau:
H2NCH2CONHCH(CH3)CONHCH2CONHCH(COOH)[CH2]4NH2
Tên gọi của X là
A. Ala-Gly-Ala-Glu. B. Glu-Ala-Glu-Gly. C. Gly-Ala-Gly-Lys. D. Ala-Gly-Ala-Lys.
(Xem giải) Câu 12: Cho hai phản ứng tổng hợp ester như sau:
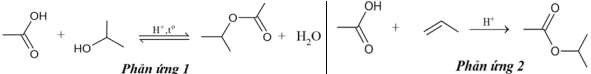
Nhận định nào sau đây đúng?
A. Sản phẩm hữu cơ thu được ở phản ứng (2) có tên gọi là isopropyl acetate.
B. Sản phẩm hữu cơ thu được ở phản ứng (1) và (2) là đồng phân của nhau.
C. Sản phẩm hữu cơ thu được ở phản ứng (1) có tên gọi là methyl isobutyrate.
D. Phản ứng (1) và (2) đều thuộc loại phản ứng ester hóa.
(Xem giải) Câu 13: Ester X có mùi đặc trưng của quả táo và có công thức phân tử C5H10O2. Thủy phân X trong dung dịch NaOH, thu được sodium butanoate và một alcohol. Công thức của X là
A. CH3CH2COOCH2CH3. B. (CH3)2CHCOOCH3.
C. CH3COOCH2CH2CH3. D. CH3CH2CH2COOCH3.
(Xem giải) Câu 14: Chất nào sau đây không tác dụng được với dung dịch NaOH?
A. C15H31COOH. B. HCOOCH3. C. CH3NHCH2CH3. D. H2NCH2COOH.
(Xem giải) Câu 15: Mùi tanh của cá là do các amine gây ra mà chủ yếu là trimethylamine. Sử dụng chất nào sau đây là thích hợp để khử mùi tanh của cá?
A. Đường ăn. B. Bột ngọt (mì chính). C. Giấm ăn. D. Muối ăn.
(Xem giải) Câu 16: Amine X có công thức phân tử C3H9N. Có bao nhiêu công thức cấu tạo bậc I của X?
A. 3. B. 2. C. 1. D. 4.
(Xem giải) Câu 17: Aniline tác dụng với hỗn hợp HNO2 và HCl ở 0 − 5°C có phương trình sau đây:
C6H5NH2 + HONO + HCl → X + 2H2O
Chất X có công thức là
A. C6H5NH3Cl. B. C6H5N2Cl. C. C6H5N2HCl. D. C6H5NH2Cl.
(Xem giải) Câu 18: Từ α-amino acid X và methyl alcohol điều chế được ester Y có công thức phân tử C4H9O2N. Công thức cấu tạo của amino acid X là
A. H2NCH2CH2COOH. B. CH3CH(NH2)COOH.
C. CH3CH2COOH. D. H2NCH2COOH.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Khi có mặt enzyme lactococcus lactis, glucose lên men thành lactic acid theo phương trình hoá học: C6H12O6 → 2CH3-CH(OH)-COOH
Để nghiên cứu sự phụ thuộc của phản ứng lên men lactic bằng enzyme lactococcus lactis vào pH của môi trường, một nhóm học sinh nêu giả thuyết như sau: “nếu pH của môi trường càng cao thì hiệu suất phản ứng lên men lactic glucose bằng enzyme lactococcus lactis càng cao.” Từ đó nhóm học sinh tiến hành thí nghiệm sau:
• Bước 1: Chuẩn bị 5 cốc chứa 50 mL (d = 1,04 g/mL) dung dịch glucose 10%, thêm hoá chất để ổn định pH của mỗi cốc lần lượt bằng 4, 5, 6, 7, 8. Hấp ở 110°C trong thời gian 20 phút để khử trùng môi trường rồi để nguội.
• Bước 2: Thêm vào mỗi cốc một lượng bằng nhau enzyme lactococcus lactis, đậy kín, để trong tủ ấm 48 giờ ở nhiệt độ 37°C.
• Bước 3: Phân tích mẫu (bằng phương pháp thích hợp) để xác định hiệu suất.
Nhóm học sinh ghi lại được biểu đồ liền quan giữa pH và hiệu suất phản ứng như hình bên.
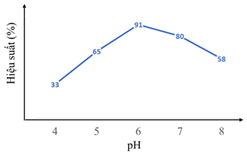
a) Từ kết quả thí nghiệm trên, tại pH = 6 khối lượng lactic acid thu được tối đa m gam. Giá trị của m là 4,7. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
b) Glucose và lactic acid là những hợp chất hữu cơ tạp chức có công thức chung dạng Cn(H2O)m.
c) Trong các môi trường pH đã thử nghiệm, hiệu suất phản ứng đạt cao nhất ở pH = 6,5.
d) Kết quả thí nghiệm chứng minh giả thuyết của nhóm học sinh là đúng.
(Xem giải) Câu 20: Triester E được tạo thành từ 3 acid béo là lauric acid (12:0, nghĩa là lauric acid chứa 12 carbon, 0 liên kết đôi C=C), linolenic acid (18:3) và palmitoleic acid (16:1). Cho bảng thông tin sau:
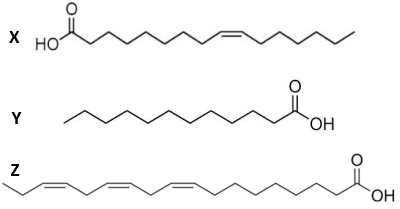
Để hydrogen hóa hoàn 1,5 mol E thì cần V L khí H2 (dùng dư 10% so với lượng phản ứng) ở điều kiện chuẩn.
a) Acid Z và X đều thuộc loại omega-3.
b) Triester E có nhiệt độ nóng chảy thấp hơn tristearin.
c) Giá trị của V là 164. (Kết quả các phép tỉnh trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
d) Z là palmitoleic acid và X là linolenic acid.
(Xem giải) Câu 21: Glycine là một loại amino acid chứa 1 nhóm COOH và 1 nhóm NH2. Tùy thuộc vào pH của dung dịch mà glycine tồn tại ion lưỡng cực, cation hay anion. Hình bên dưới cho thấy tỉ lệ phần trăm các dạng điện tích của glycine ở các giá trị pH khác nhau:
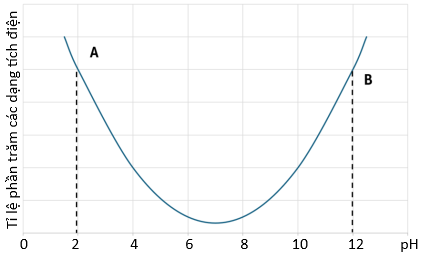
a) Từ đồ thị có thể dự đoán tại pH = 6, dạng tồn tại chủ yếu của glycine là +H3NCH2COO-.
b) Tại pH = 2 nếu đặt glycine trong điện trường thì glycine di chuyển về cực âm.
c) Dạng tồn tại chủ yếu của glycine tại điểm B có tổng điện tích bằng 0.
d) Khi pH tăng, điện tích của dạng tồn tại sẽ có xu hướng chuyển từ điện tích dương sang điện tích âm.
(Xem giải) Câu 22: Methylamine (CH3NH2) được ứng dụng rộng rãi trong nhiều ngành công nghiệp, đặc biệt là sản xuất dược phẩm, thuốc trừ sâu, thuốc diệt nấm và các hoá chất khác.
a) Methylamine thuộc loại alkylamine.
b) Cho phản ứng: CH3NH2 + H2O ⇋ CH3NH3+ + OH-, trong phản ứng nghịch thì CH3NH3+ là một base theo thuyết acid – base của Bronsted – Lowry.
c) Dung dịch methylamine có pH lớn hơn dung dịch ammonia có cùng nồng độ.
d) Nhỏ từ từ đến dư dung dịch methylamine vào dung dịch CuCl2, ban đầu thấy kết tủa, sau đó kết tủa tan tạo dung dịch màu tím.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Cho các dụng cụ (đánh số tương ứng) được dùng trong quá trình thí nghiệm điều chế ethyl acetate và thu sản phẩm: Bình cầu có nhánh (1), ống sinh hàn (2); bình tam giác (3); phễu chiết (4); bếp điện (5). Xác định dãy bốn số ứng với các dụng cụ thí nghiệm theo lần lượt thứ tự chức năng sau: ngưng tụ hơi chất lỏng; tách hai chất lỏng không trộn lẫn; thực hiện phản ứng ester hóa; cung cấp nhiệt cho phản ứng.
(Xem giải) Câu 24: Glucose được sử dụng để tạo ra năng lượng cần thiết cho sự sống, quá trình này diễn ra trong tế bào. Phản ứng oxi hóa 1 mol glucose tạo thành CO2(g) và H2O(l) giải phóng một nhiệt lượng là 2803,0 kJ. Khi thiếu hụt glucose có thể dẫn đến hạ đường huyết. Khi bị hạ đường huyết, bệnh nhân được truyền dung dịch glucose 5% (khối lượng riêng D = 1,1 g/mL). Hãy tính thể tích dung dịch glucose (L) cần dùng để cung cấp 856,47 kJ cho bệnh nhân. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
(Xem giải) Câu 25: Glucosamine hydrochloride thường được sử dụng dưới dạng thuốc uống bổ sung để điều trị viêm xương khớp. Vỏ tôm (chứa 17% chitin (C8H13NO5)n về khối lượng) bóc từ các nhà máy chế biến thủy, hải sản được tận dụng để sản xuất glucosamine hydrochloride theo sơ đồ sau:
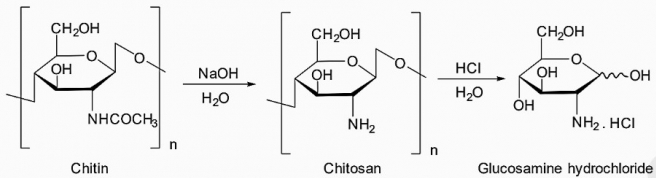
Để sản xuất 1000 hộp thuốc glucosamine hydrochloride, trong đó mỗi hộp có chứa 375 viên, với hàm lượng glucosamine hydrochloride là 1500 mg/1 viên, thì cần sử dụng bao nhiêu kg vỏ tôm. Biết hiệu suất quá trình điều chế glucosamine hydrochloride từ chitin đạt 40% và hao hụt trong quá trình sản xuất là 4%. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
(Xem giải) Câu 26: Cho công thức khung phân tử một số amino acid như sau:
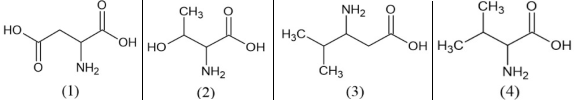
Tổng phân tử khối của các α-amino acid trong số các amino acid trên bằng bao nhiêu?.
(Xem giải) Câu 27: Tốc độ phản ứng thủy phân ester trong môi trường kiềm tỉ lệ thuận với tích nồng độ của ester và OH-: v = k[ester].[OH] Trong thí nghiệm TN0, nồng độ ester và OH- ban đầu là: [ester] = [OH-] = 0,1 mol/L. Thực hiện một số thí nghiệm khác dưới đây với nồng độ đầu của các chất thay đổi nhưng giữ nguyên các điều kiện phản ứng khác.
| Thí nghiệm | [ester] | [OH-] |
| 1 | 0,01 | 0,2 |
| 2 | 0,1 | 0,02 |
| 3 | 0,2 | 0,02 |
| 4 | 0,24 | 0,05 |
Thí nghiệm số mấy có tốc độ phản ứng lớn hơn tốc độ phản ứng của TN0?
(Xem giải) Câu 28: Cho các phản ứng hoá học sau:
(1) CH3CH2NH2 + HNO3 → CH3CH2NH3NO3
(2) C12H22O11 (saccharose) + H2O (H+) → C6H12O6 (glucose) + C6H12O6 (fructose)
(3) Gly-Ala-Ala + 2H2O (enzyme) → Gly + 2Ala.
(4) (C15H31COO)3C3H5 + 3KOH → 3C15H31COOK + C3H5(OH)3
(5) C6H12O6 (enzyme) → 2C2H5OH + CO2
Hãy cho biết có bao nhiêu phản ứng thủy phân?


Bình luận