[2026] Thi thử TN sở GDĐT Ninh Bình (Online 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 033
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2C | 3C | 4D | 5B | 6C | 7A | 8B | 9A |
| 10C | 11D | 12A | 13B | 14A | 15D | 16A | 17A | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | Đ | S | 134 | 9800 | 1 |
| (b) | S | S | Đ | Đ | 26 | 27 | 28 |
| (c) | S | Đ | Đ | Đ | 2 | 348 | 4 |
| (d) | Đ | S | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Cho cấu tạo của một đoạn mạch trong phân tử polymer X:
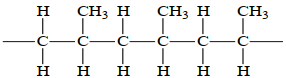
Tên gọi của polymer X là
A. poly(methyl methacrylate). B. polypropylene.
C. polyethylene. D. poly(vinyl chloride).
(Xem giải) Câu 2: Carbohydrate nào sau đây không phản ứng với thuốc thử Tollens khi đun nóng?
A. Glucose. B. Maltose. C. Saccharose. D. Fructose.
(Xem giải) Câu 3: Phát biểu nào sau đây không đúng?
A. Tơ tằm thuộc loại tơ thiên nhiên.
B. Cao su là những vật liệu polymer có tính đàn hồi.
C. Thành phần của vật liệu composite chỉ chứa polymer.
D. Nylon-6,6 thuộc loại tơ tổng hợp.
(Xem giải) Câu 4: Dynorphin là một nhóm peptide đóng vai trò quan trọng trong những thay đổi ở não liên quan đến nghiện cocaine. Một trong những peptide này, dynorphin A, chứa trình tự amino acid như sau: Tyr–Gly–Gly–Phe–Leu–Arg–Arg–Ile–Arg–Pro–Lys–Leu–Lys
Chymotrypsin là một loại enzyme đặc hiệu có khả năng cắt mạch amino acid một cách có chọn lọc, cắt đứt liên kết CO–NH (với phần carbonyl thuộc về amino acid Phe, Tyr hoặc Trp).
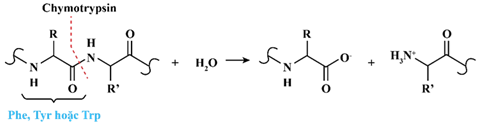
Tiến hành cắt đứt chuỗi amino acid bằng enzyme chymotrypsin đến khi hoàn toàn thì trong các chất sản phẩm thu được, có số mắt xích lớn nhất có thể là bao nhiêu?
A. 5. B. 3. C. 12. D. 9.
(Xem giải) Câu 5: “Các alkylamine …(1)… có khả năng tham gia phản ứng với …(2)… trong điều kiện thích hợp tạo sản phẩm là alcohol, khí nitrogen và nước”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A. bậc 2, nitric acid. B. bậc 1, nitrous acid.
C. bậc 1, nitric acid. D. bậc 2, nitrous acid.
(Xem giải) Câu 6: Protein tham gia phản ứng với dung dịch HNO3 đặc tạo thành hợp chất rắn có màu gì?
A. Trắng. B. Xanh. C. Vàng. D. Tím.
(Xem giải) Câu 7: Dung dịch nào sau đây có pH > 7?
A. NaOH. B. NaCl. C. CH3COOH. D. H2SO4.
(Xem giải) Câu 8: Bộ dụng cụ dưới đây được sử dụng để điện phân nước với chất điện li được sử dụng là H2SO4.
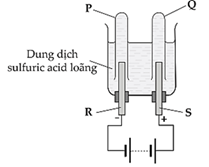
Cho các phát biểu sau:
(a) Điện cực R xảy ra quá trình khử ion H+.
(b) Ống P thu được khí H2.
(c) Thay dung dịch H2SO4 bằng dung dịch HCl thì khí thu được ở hai điện cực là không đổi.
(d) Nếu ở ống Q thu được 50 mL khí thì ống P sẽ thu được 100 mL khí (trong cùng điều kiện nhiệt độ, áp suất).
Số phát biểu đúng là
A. 4. B. 3. C. 2. D. 1.
(Xem giải) Câu 9: Sản phẩm cuối cùng của sự thủy phân tinh bột trong cơ thể người là
A. glucose. B. CO2 và H2O. C. saccharose. D. glycogen.
(Xem giải) Câu 10: Nhóm khí nào sau đây trong không khí khi vượt quá mức cho phép sẽ gây ra hiện tượng mưa acid?
A. NH3, H2S, CO2. B. CO, CH4, N2. C. SO2, NO, NO2. D. H2, SO2, N2O.
(Xem giải) Câu 11: Cho dãy sắp xếp các kim loại theo chiều giảm dần tính khử: K, Mg, Al, Fe. Cặp oxi hóa – khử nào sau đây có giá trị thế điện cực chuẩn nhỏ nhất?
A. Al3+/Al. B. Fe2+/Fe. C. Mg2+/Mg. D. K+/K.
(Xem giải) Câu 12: Trong phân tử chất nào sau đây có 1 nhóm amino (NH2) và 2 nhóm carboxyl (COOH)?
A. Glutamic acid. B. Lysine. C. Valine. D. Alanine.
(Xem giải) Câu 13: Sơ đồ hình sau đây cho biết con đường phản ứng của một phản ứng thu nhiệt.
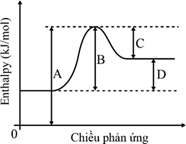
Biến thiên enthalpy của phản ứng trên là
A. ![]() = −B kJ/mol. B.
= −B kJ/mol. B. ![]() = D kJ/mol.
= D kJ/mol.
C. ![]() = −A kJ/mol. D.
= −A kJ/mol. D. ![]() = C kJ/mol.
= C kJ/mol.
(Xem giải) Câu 14: Chất nào sau đây không phản ứng với dung dịch NaOH trong điều kiện thích hợp?
A. Methanol. B. Phenol. C. Methyl acetate. D. Acetic acid.
(Xem giải) Câu 15: Ethyl propionate là ester có mùi thơm của dứa. Công thức cấu tạo của ethyl propionate là
A. HCOOC2H5. B. CH3COOC2H5. C. C2H5COOCH3. D. C2H5COOC2H5.
(Xem giải) Câu 16: Cho các chất sau: glycerol, Gly-Ala-Val, glucose, albumin (lòng trắng trứng). Số chất tác dụng với Cu(OH)2 trong NaOH cho màu tím đặc trưng là
A. 2. B. 3. C. 4. D. 1.
(Xem giải) Câu 17: Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trong đời sống: kích thích quả mau chín, điều chế nhựa làm sản phẩm gia dụng,… Phản ứng hóa học của ethylene với dung dịch Br2 như sau:
CH2=CH2 + Br2 → CH2Br–CH2Br
Cơ chế của phản ứng trên xảy ra như sau:
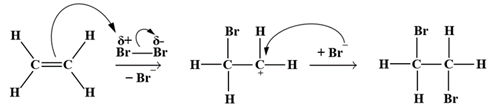
Nhận định nào sau đây không đúng?
A. Giai đoạn 1, liên kết đôi phản ứng với tác nhân Brδ- tạo thành carbocation.
B. Giai đoạn 1, có sự phân cắt dị li (cặp electron liên kết thuộc về riêng một nguyên tử Br).
C. Phản ứng trên xảy ra theo cơ chế AE.
D. Giai đoạn 2, carbocation kết hợp với anion Br- tạo thành sản phẩm.
(Xem giải) Câu 18: Hỗn hợp các muối sodium của acid béo sinh ra ở trạng thái keo. Để tách muối này ra khỏi hỗn hợp, người ta thêm chất gì vào hỗn hợp?
A. Nước. B. Acid. C. Muối ăn. D. Tinh bột.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Tại một nhà máy sản xuất rượu, cứ 10 tấn tinh bột (chứa 6,85% tạp chất trơ) sẽ sản xuất được 7,21 m³ dung dịch ethanol 40° (cho khối lượng riêng của ethanol nguyên chất là 0,8 g/cm³). Tinh bột là một polysaccharide gồm nhiều gốc α-glucose liên kết với nhau tạo ra hai dạng mạch amylose và amylopectin. Dưới đây là một đoạn cấu tạo của tinh bột:
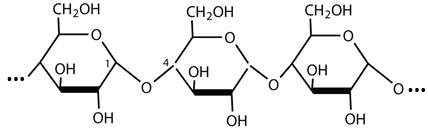
a. Amylopectin có các gốc α-glucose liên kết với nhau bởi liên kết α-1,4-glycoside và α-1,6- glycoside.
b. Tinh bột khi bị thủy phân hoàn toàn trong môi trường acid tạo thành glucose và fructose.
c. Hiệu suất của quá trình sản xuất ethanol ở trên đạt 40%. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
d. Đoạn mạch trên có các gốc α-glucose được liên kết với nhau bằng liên kết α-1,4- glycoside.
(Xem giải) Câu 20: Một nhóm học sinh tìm hiểu sự ảnh hưởng của nồng độ ion kim loại tại điện cực tới sức điện động của pin điện. Giả thuyết của nhóm học sinh đưa ra: “Nồng độ của ion kim loại trong dung dịch của bất kì điện cực nào giảm đều làm cho thế điện cực của điện cực đó giảm, dẫn đến sức điện động của pin giảm”. Để kiểm tra giả thuyết này, nhóm học sinh thiết lập một pin điện như hình bên dưới:
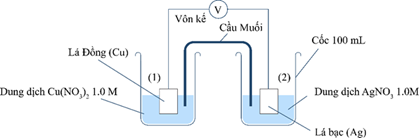
Khi pha loãng dung dịch AgNO3 tới nồng độ 0,5M ở điện cực (2) và giữ nguyên nồng độ Cu(NO3)2 ở điện cực (1) thì thấy giá trị trên vôn kế giảm. Biết thế điện cực chuẩn của các điện cực:
Ag+(aq) + 1e → Ag(s) E°Ag+/Ag = +0,8 V
Cu2+(aq) + 2e → Cu(s) E°Cu2+/Cu = +0,34 V
a. Điện cực Ag+/Ag đóng vai trò là cathode.
b. Electron di chuyển từ điện cực Ag+/Ag sang điện cực Cu2+/Cu.
c. Có thể thay dung dịch Cu(NO3)2 1 M bằng dung dịch CuSO4 1 M.
d. Khi pha loãng dung dịch AgNO3 thì giá trị trên vôn kế giảm, nên giả thuyết ban đầu là đúng.
(Xem giải) Câu 21: Phản ứng thủy phân ester trong môi trường kiềm được biểu diễn như sau: RCOOR’ + NaOH → RCOONa + R’OH
Một nhóm học sinh dự đoán “Nồng độ NaOH càng lớn thì tốc độ phản ứng thủy phân càng lớn”. Từ đó, học sinh tiến hành thí nghiệm ở nhiệt độ không đổi (60°C) nhưng thay đổi nồng độ NaOH để kiểm tra dự đoán trên như sau:
• Bước 1: Thêm 4 mL ethyl acetate (d = 0,9 g/mL) vào một ống nghiệm chứa 20 mL dung dịch NaOH nồng độ C (mol/L). Các giá trị nồng độ này không giống nhau giữa các thí nghiệm.
• Bước 2: Ngâm ống nghiệm trong nồi nước nóng (nhiệt độ nước khoảng 60°C) và đo thời gian cho
đến khi phần chất lỏng trong ống nghiệm trở lên đồng nhất. Kết quả thí nghiệm được cho ở bảng sau:
| Nồng độ NaOH (mol/L) | 4,0 | 3,6 | 3,2 | 2,8 | 2,4 | 2,0 |
| Thời gian hỗn hợp đồng nhất (phút) | 5,2 | 6,0 | 7,0 | 8,2 | 9,5 | 11,0 |
a. Phản ứng thủy phân ethyl acetate xảy ra ở bước 2 của các thí nghiệm.
b. Sau bước 1, phần chất lỏng trong các ống nghiệm tách thành hai lớp.
c. Phản ứng thủy phân hoàn toàn tại thời điểm hỗn hợp trong ống nghiệm đồng nhất.
d. Kết quả thí nghiệm chứng tỏ dự đoán của học sinh ban đầu là chính xác.
(Xem giải) Câu 22: Glycine là một loại amino acid chứa 1 nhóm COOH và 1 nhóm NH2. Biết điểm đẳng điện (pI) là giá trị pH của dung dịch mà tại đó amino acid tồn tại ion lưỡng cực và tổng điện tích dương bằng tổng điện tích âm. Hình dưới đây cho thấy tỉ lệ phần trăm các dạng điện tích của glycine ở các giá trị pH khác nhau:
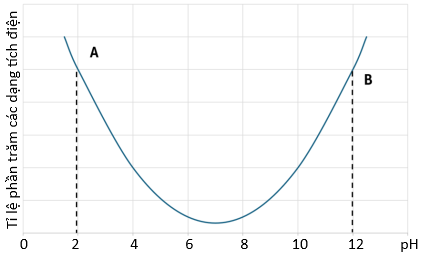
a) Dạng tồn tại chủ yếu của glycine tại điểm B có tổng điện tích là 0.
b) Từ đồ thị điểm đẳng điện gần đúng của glycine là trong khoảng pH từ 6 đến 8.
c) Khi pH tăng, điện tích của dạng tồn tại sẽ có điện tích chuyển từ dương sang âm.
d) Tại điểm A trên đồ thị, glycine chủ yếu ở dạng acid HOOCCH2NH3+.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Trong cơ thể người, tristearin (một loại triglyceride bão hòa) bị oxi hóa hoàn toàn thông qua chu trình chuẩn độ sinh học để giải phóng năng lượng cho các hoạt động sống. Phương trình nhiệt hóa học của quá trình được tóm tắt như sau: (C17H35COO)3C3H5(s) + 81,5O2(g) → 57CO2(g) + 55H2O(l)
Cho biết nhiệt tạo thành chuẩn của các chất:
| Chất | (C17H35COO)3C3H5(s) | CO2(g) | H2O(l) |
| –2344 | –393,5 | –285,8 |
Cho các phát biểu sau:
(1) Tristearin thuộc loại chất béo bão hòa, do đó nó có nhiệt độ nóng chảy cao và thường tồn tại ở trạng thái rắn trong điều kiện thường.
(2) Ở điều kiện chuẩn, cứ 1 mol tristearin bị oxi hóa hoàn toàn theo phản ứng (1) sẽ giải phóng một lượng nhiệt là 40492,5 kJ ra môi trường.
(3) Nếu một vận động viên tiêu thụ 100 gam tristearin, năng lượng sinh ra tương đương với khoảng 961 kcal (biết 1 kcal = 4,184 kJ).
(4) Hiệu suất năng lượng của tristearin (tính theo kJ/kg) đạt trên 90% so với năng suất tỏa nhiệt dầu hỏa thương phẩm (44000 kJ/kg).
Liệt kê các phát biểu đúng theo thứ tự tăng dần.
(Xem giải) Câu 24: Để mạ bạc (Ag) lên bề mặt một khối cầu kim loại có bán kính 10 cm, người ta sử dụng phương pháp điện phân với cường độ dòng điện không đổi là 500A. Lớp bạc sau khi mạ có độ dày đồng nhất là 4 mm. Biết khối lượng riêng của bạc là 10,49 g/cm³; khối lượng mol nguyên tử của bạc là 108 g/mol và hằng số Faraday F = 96500 C/mol. Giả thiết hiệu suất điện phân đạt 100%. Thời gian điện phân để hoàn thành lớp mạ trên là x giây. Giá trị của x là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị, lấy giá trị π = 3,14).
(Xem giải) Câu 25: Trong nỗ lực giảm thiểu rác thải nhựa, một nhóm nghiên cứu đã chế tạo màng bọc thực phẩm sinh học từ amylopectin chiết xuất từ tinh bột sắn. Để tăng độ bền và khả năng chống thấm, nhóm nghiên cứu thực hiện phản ứng ester hóa một phần các nhóm hydroxyl (-OH) trong amylopectin bằng acetic anhydride để tạo thành amylopectin acetate. Phân tích một mẫu polymer sau phản ứng thấy hàm lượng nguyên tố carbon chiếm 47,54% về khối lượng. Giả thiết rằng tất cả các mắt xích trong phân tử amylopectin đều bị ester hóa với cùng một số lượng nhóm acetyl (-COCH3) trung bình là n. Biết công thức cấu tạo của một mắt xích trong amylopectin acetate có dạng: [C6H7O2(OH)3-n(OCOCH3)n]. Tính giá trị của n. (Làm tròn kết quả đến hàng đơn vị)
(Xem giải) Câu 26: Glutamic acid được sử dụng bởi hầu hết các sinh vật sống trong quá trình tổng hợp ra protein, được xác định trong DNA bằng mã di truyền GAA hay GAG. Nó không phải là hoạt chất thiết yếu trong cơ thể người, có nghĩa là cơ thể có thể tự tổng hợp nó. Điểm đẳng điện pI là giá trị pH của dung dịch mà tại đó amino acid tồn tại ion lưỡng cực và tổng điện tích dương bằng tổng điện tích âm, cho glutamic acid có pI bằng 3,08. Glutamic acid có công thức cấu tạo như sau:
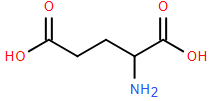
Cho các phát biểu sau:
(a) Glutamic acid là một α-amino acid.
(b) Glutamic acid có tính lưỡng tính, có thể tác dụng với acid mạnh cũng như base mạnh.
(c) Glutamic acid là một hợp chất hữu cơ đa chức có công thức phân tử là C5H9O4N.
(d) Ở pH = 10, glutamic acid di chuyển về phía cực âm.
Số phát biểu đúng là bao nhiêu?
(Xem giải) Câu 27: Trong nỗ lực giảm thiểu rủi ro từ việc vỡ vụn của thủy tinh truyền thống tại các khu vực công cộng, một doanh nghiệp đã ứng dụng Poly(methyl methacrylate) – PMMA (hay còn gọi là thủy tinh hữu cơ Plexiglass) để sản xuất các tấm chắn bảo vệ. Quy trình điều chế PMMA trong công nghiệp được thực hiện qua hai giai đoạn chính:
• Giai đoạn 1 (Ester hóa): Phản ứng giữa methacrylic acid (CH2=C(CH3)COOH) và methyl alcohol (CH3OH) với xúc tác acid để tạo thành monomer methyl methacrylate (MMA).
• Giai đoạn 2 (Trùng hợp): Monomer MMA tham gia phản ứng trùng hợp gốc tự do dưới tác dụng của chất khơi mào và nhiệt độ để tạo thành polymer PMMA.
Để sản xuất 500 tấm kính có chiều dài 20 cm, chiều rộng 15 cm có độ dày 2 cm (khối lượng riêng của tấm kính là d = 1,2 g/cm³) người ta cần tối thiểu m kg methacrylic acid. Biết trong mỗi tấm kính khối lượng PMMA chiếm 90% và hiệu suất phản ứng toàn bộ quá trình tính theo methacrylic acid là 80%. Tính giá trị của m? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị)
(Xem giải) Câu 28: Linoleic acid (có cấu tạo như hình bên) thuộc nhóm omega-n (n là số thứ tự vị trí của liên kết đôi đầu tiên tính từ đầu nhóm CH3) là một trong những acid béo có lợi cho sức khỏe tim mạch, ngăn ngừa các bệnh về tim, động mạch vành.

Cho các phát biểu sau:
(a) Công thức của chất béo trilinolein là (C17H31COO)3C3H5.
(b) Linoleic acid có mạch cacbon không phân nhánh.
(c) Linoleic acid thuộc loại omega-6.
(d) Linoleic acid phản ứng với H2 (t°, Ni) theo tỉ lệ mol 1 : 2.
Số phát biểu đúng là bao nhiêu?


Bình luận