[2026] Thi thử TN cụm 24 trường Phú Thọ (Lần 1 – Đề 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 081
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2A | 3A | 4A | 5B | 6D | 7A | 8C | 9A |
| 10C | 11C | 12D | 13C | 14B | 15B | 16C | 17A | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | S | S | 123 | 4 | 3 |
| (b) | S | Đ | Đ | S | 26 | 27 | 28 |
| (c) | Đ | Đ | S | Đ | 4 | 141 | 1,71 |
| (d) | S | S | S | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Formol được dùng làm chất tiệt trùng, thuốc trừ sâu và bảo quản xác động thực vật. Formol là dung dịch chất nào sau đây?
A. Methanol. B. Formaldehyde. C. Phenol. D. Acetone.
(Xem giải) Câu 2. Thực hiện hai thí nghiệm của cùng một lượng CaCO3 với dung dịch HCl (dư) có nồng độ khác nhau, ở cùng điều kiện và bỏ qua các quá trình ảnh hưởng. Thể tích khí CO2 thoát ra theo thời gian được ghi lại trên đồ thị sau:
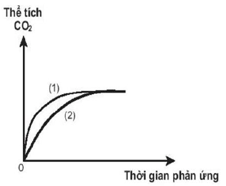
Phản ứng nào đã dùng HCl với nồng độ cao hơn ?
A. Phản ứng (1). B. Phản ứng (2).
C. Cả phản ứng (1) và (2). D. Không xác định được.
(Xem giải) Câu 3. Tiến hành thí nghiệm theo các bước:
• Bước 1: Đánh sạch lớp gỉ bên ngoài một chiếc đinh sắt rồi cho ngập vào cốc chứa dung dịch CuSO4.
• Bước 2: Sau khoảng 15 phút, quan sát màu của chiếc đinh sắt và màu của dung dịch.
Cho các nhận định sau về thí nghiệm. Nhận định đúng là
A. Đinh sắt bị phủ một lớp đồng màu đỏ.
B. Màu xanh của dung dịch không thay đổi vì đó là màu của sulfate ion.
C. Màu xanh của dung dịch đậm dần vì nồng độ của ion Cu2+ trong dung dịch giảm dần.
D. Khối lượng dung dịch trong cốc tăng so với ban đầu.
(Xem giải) Câu 4. Cá là một loại thực phẩm giàu dinh dưỡng và tốt cho cơ thể. Tuy nhiên nhiều người cảm thấy khó chịu vì cá thường có mùi tanh. Mùi tanh làm cá mất đi mùi vị và tính hấp dẫn của nó. Trong cá (đặc biệt là cá mè) có chứa một lượng hỗn hợp các amine (nhiều nhất là trimethylamine (CH3)3N) và một số chất khác. Phương pháp hóa học đơn giản để khử mùi tanh của cá trước khi nấu là rửa cá
A. bằng các chất chua tự nhiên như giấm ăn, nước chanh…
B. với dung dịch nước vôi trong, sau đó rửa lại bằng nước sạch.
C. thật kĩ bằng nước sạch.
D. với các dung dịch acid mạnh như HCl, H2SO4…, sau đó rửa lại bằng nước sạch.
(Xem giải) Câu 5. Trong y học, dung dịch glucose 5% (G-5) là dịch truyền tĩnh mạch cho những trường hợp bệnh nhân thiếu nước và năng lượng theo chỉ định của bác sĩ. Một chai chứa 600 gam dịch truyền G-5 cung cấp được tối đa x (kJ) năng lượng. Biết 1 gam glucose có thể cung cấp 10 kJ năng lượng. Giá trị của x là
A. 500. B. 300. C. 400. D. 200.
(Xem giải) Câu 6. Phát biểu nào sau đây đúng?
A. Có thể phân biệt glucose và fructose bằng thuốc thử Tollens.
B. Ở dạng mạch hở, glucose có 6 nhóm -OH liền kề.
C. Phân tử tinh bột gồm nhiều gốc -glucose liên kết với nhau.
D. Saccharose không tham gia phản ứng tráng bạc.
(Xem giải) Câu 7. Thực hiện các thí nghiệm sau:
(a) Cho một mẩu Na vào dung dịch copper (II) sulfate.
(b) Nhúng một thanh Zn vào dung dịch silver nitrate.
(c) Nhúng một thanh Al vào dung dịch iron (III) chloride.
(d) Cho bột magnesium và calcium carbonate vào dung dịch H2SO4.
Có bao nhiêu thí nghiệm xảy ra ăn mòn điện hóa?
A. 2. B. 3. C. 4. D. 1.
(Xem giải) Câu 8. Phản ứng giữa HCl với ethylene: CH2=CH2 + HCl CH3CH2Cl.
Cơ chế phản ứng qua 2 giai đoạn như sau:
Giai đoạn 1 xảy ra chậm, quyết định tốc độ phản ứng.
Nhận định nào sau đây không đúng?
A. Trong phân tử ethylene có 5 liên kết (xích ma).
B. Phản ứng trên thuộc loại phản ứng cộng.
C. Trong dãy đồng đẳng alkene, ethylene tham gia phản ứng cộng HCl dễ nhất.
D. Trong giai đoạn 1 của phản ứng trên có sự phân cắt liên kết (pi).
(Xem giải) Câu 9. Trong cơ thể người, ion Ca2+ tham gia cấu trúc xương, răng. Ở trạng thái cơ bản, cấu hình electron của nguyên tử Ca là 1s22s22p63s23p64s2. Số hạt mang điện âm của ion Ca2+là
A. 18. B. 20. C. 38. D. 40.
(Xem giải) Câu 10. Theo QCVN 01-1:2018/BYT, hàm lượng manganese (Mn) tối đa cho phép trong nước sinh hoạt không được vượt quá 0,3 mg/L. Một mẫu nước chứa Mn2+ với nồng độ chưa xác định. Để đánh giá hàm lượng manganese trong 5 m³ mẫu nước trên, người ta tiến hành tách loại manganese bằng cách sử dụng 316,5 ml dung dịch KMnO₄ 1M để oxy hóa toàn bộ Mn²⁺ thành MnO₂ kết tủa theo phản ứng:
3Mn2+ + 2MnO4- + 2H2O → 5MnO2 + 4H+
Biết rằng phản ứng xảy ra hoàn toàn và toàn bộ MnO₂ được loại bỏ. Hàm lượng manganese trong mẫu nước này cao gấp bao nhiêu lần so với ngưỡng cho phép?
A. 7,72 B. 15,6 C. 17,4 D. 20,6
(Xem giải) Câu 11. Cầu chì hoạt động dựa trên nguyên lý uốn cong hoặc tự chảy để ngắt mạch điện khi dòng điện tăng đột ngột trong mạch. Cầu chì đảm nhận vai trò bảo vệ đường dây dẫn, mạch điện và thiết bị điện khi quá dòng, quá tải, quá áp. Cầu chì thường được làm bằng các kim loại chì (Pb), thiếc trắng (Sn) hoặc cadmium (Cd).
Hình ảnh một số loại cầu chì dùng trong hệ thống điện dân dụng và công nghiệp
Ứng dụng này dựa trên tính chất nào của các kim loại trên?
A. Có độ dẫn điện cao.
B. Có tính dẻo cao.
C. Có nhiệt độ nóng chảy tương đối thấp.
D. Có độ cứng tương đối thấp.
(Xem giải) Câu 12. Cho bảng giá trị thế điện cực chuẩn của một số cặp oxi hoá – khử như sau:
| Cặp oxi hoá – khử | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Ni2+/Ni | 2H+/H2 |
| Thế điện cực chuẩn (V) | 0,340 | -0,763 | -0,440 | -0,257 | 0,000 |
Ở điều kiện chuẩn, số kim loại trong dãy Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl là
A. 2. B. 1. C. 4. D. 3.
(Xem giải) Câu 13. Insulin là hormone có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp có chứa các peptide Glu-Gln-Cys, Gly-Ile-Val, Gln-Cys-Cys, Val-Glu-Gln. Nếu đánh số thứ tự amino acid đầu N là số 1 thì amino acid ở vị trí số 4 trong X là
A. Gln. B. Cys. C. Glu. D. Val.
(Xem giải) Câu 14. Quá trình lưu hoá cao su thuộc loại phản ứng nào sau đây?
A. Cắt mạch polymer. B. Tăng mạch polymer.
C. Giữ nguyên mạch polymer. D. Phân huỷ polymer.
(Xem giải) Câu 15. Trong cơ thể người, carbohydrate có vai trò chính nào sau đây?
A. Cấu tạo màng tế bào và dự trữ năng lượng dài hạn.
B. Cung cấp năng lượng nhanh chóng cho các hoạt động sống.
C. Là thành phần chính của nhân tế bào và enzyme.
D. Tham gia vào quá trình vận chuyển oxygen trong máu.
(Xem giải) Câu 16. Một ruộng lúa có 2,0 × 10⁵ L dung dịch đất. Người nông dân bón 16 kg phân ammonium nitrate (NH₄NO₃). Giả sử toàn bộ ion NH₄⁺ (NH4+ + 2O2 → NO3- + 2H+ + H2O) trong phân bị chuyển hóa hoàn toàn trong đất, làm tăng nồng độ ion H⁺, và lượng H⁺ này phân bố đều trong dung dịch đất. Giá trị pH của dung dịch đất sau khi bón phân gần đúng nhất là
A. 2,0. B. 3,0. C. 2,7. D. 3,7.
(Xem giải) Câu 17. Hợp chất hữu cơ X có công thức cấu tạo như sau:
Phân tử X có số nguyên tử carbon và số liên kết σ lần lượt là
A. 5; 14. B. 5; 15. C. 4; 10. D. 4; 11.
(Xem giải) Câu 18. Ester X có mùi đặc trưng giống mùi táo và có công thức phân tử C5H10O2. Thuỷ phân X trong dung dịch NaOH, thu được muối của carboxylic acid không phân nhánh và methanol. Công thức của X là
A. CH3COOCH2CH2CH3. B. CH3CH2COOCH2CH3.
C. CH3CH2CH2COOCH3. D. (CH3)2CHCOOCH2CH3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 1. Hydrocarbon là nguồn nguyên liệu trong tổng hợp hữu cơ. Một trong các chuyển hóa hydrocarbon được biết đến là quá trình sản xuất xà phòng từ hydrocarbon no, mạch dài không phân nhánh. Quá trình được mô tả theo sơ đồ sau:
a) Muối sodium stearate có khả năng giặt rửa là do gốc R dễ xâm nhập vào các vết dầu mỡ.
b) Trong sơ đồ phản ứng trên cả 2 phản ứng xảy ra đều là phản ứng oxi hóa khử.
c) Trong phản ứng (2), nếu thay NaOH bằng Na2CO3 thì muối thu được không thay đổi.
d) Nếu hiệu suất quá trình là 80% thì cần 2 tấn hydrocarbon để sản xuất được 2,05 tấn sodium stearate.
(Xem giải) Câu 2. Năm 1965, trong quá trình tổng hợp thuốc chống loét dạ dày, nhà hóa học James M. Schlatter đã vô tình phát hiện một chất làm ngọt nhân tạo với tên thường gọi là “Aspartame” bằng cách kết hợp giữa aspartic acid và phenylalanine tạo thành peptide, peptide này có thể được chuyển đổi thành methyl ester gọi là aspartame. Aspartame ngọt hơn khoảng 200 lần so với đường ăn thông thường. Aspartame thường được sử dụng trong đồ uống và thực phẩm dành cho người ăn kiêng vì có ít calo hơn đường thông thường. Tổ chức y tế thế giới (WHO) thông báo xếp chất làm ngọt nhân tạo aspartame vào danh sách các chất “có thể gây ung thư cho con người” nhưng lưu ý chất này vẫn an toàn nếu được tiêu thụ trong giới hạn khuyến nghị hằng ngày.
a) Tổng số cặp electron hóa trị chưa tham gia liên kết của nguyên tử N trong một phân tử aspartame là 2.
b) Với một lon nước ngọt dành cho người ăn kiêng có chứa 300 mg aspartame. Muốn sản xuất 1 triệu lon nước ngọt trên cần 169,6 kg aspartic acid với hiệu suất quá trình 80%.((Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm)
c) Không nên sử dụng quá nhiều đồ uống có chất làm ngọt nhân tạo aspartame liên tục trong thời gian dài.
d) Aspartame là ester của methanol với dipeptide (tạo bởi amino acid HOOCCH(NH2)CH2COOH và C6H5CH(NH2)COOH).
(Xem giải) Câu 3. Để tiến hành mạ một tấm huy chương (ruột bằng sắt với lớp mạ bằng đồng) hình trụ, đáy tròn với bán kính 2,5 cm, chiều cao hình trụ 0,3 cm, với lớp mạ bằng đồng dày 0,1 cm. Người ta có thể tiến hành điện phân dung dịch X nồng độ 0,5M dư với cường độ dòng điện không đổi 2A, khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết thời gian là t giây. Biết khối lượng riêng của đồng là 8,95g/cm3 và hiệu suất điện phân là 100%, giả thiết lớp mạ huy chương dày như nhau, toàn bộ lượng Cu tạo ra đều bám hết vào tấm huy chương và cho gia trị π = 3, 14.
a) Dung dịch X có thể là FeSO4.
b) Thanh đồng là cực dương, huy chương được mạ sẽ đóng vai trò cực âm
c) Thời gian điện phân khoảng 17 giờ 57 phút 35 giây.
d) Chiều dòng điện từ nguồn điện đến thanh đồng và dòng electron di chuyển từ huân chương được mạ qua dây dẫn đến thanh đồng.
(Xem giải) Câu 4. Quá trình lên men rượu là một quá trình tỏa nhiệt. Từ 250 gam glucose, thực hiện quá trình lên men rượu trong phòng thí nghiệm, kết quả biểu thị theo đồ thị bên.
Kết quả nghiên cứu nhận thấy:
• Tốc độ phản ứng tăng lên và dung dịch trở nên đặc và ấm hơn.
• Từ ngày thứ 10, phản ứng hầu như dừng lại dù trong dung dịch vẫn còn glucose.
a) Đến ngày thứ 10, hiệu suất quá trình lên men rượu là 78%.
b) Glucose trong phản ứng lên men rượu có vai trò là chất xúc tác
c) Trong quá trình lên men, ngoài ethyl alcohol thì còn có thể tạo thành một số sản phẩm như CH3CHO, CH3COOH.
d) Glucose thuộc loại monosaccharide tồn tại chủ yếu ở dạng mạch hở .
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 1. X là một hợp chất quan trọng được hình thành trong quá trình quang hợp ở cây xanh. Quá trình quang hợp được chia thành hai pha: pha sáng và pha tối. Trong pha sáng, năng lượng ánh sáng mặt trời được hấp thụ bởi các sắc tố trong lục lạp của cây. Các sắc tố này, chủ yếu là chlorophyll, chuyển đổi năng lượng ánh sáng thành năng lượng hóa học tích lũy trong ATP và NADPH. Trong pha tối, khí CO2 được hấp thụ và chuyển hóa thành glucose nhờ năng lượng ATP và NADPH ở pha sáng. Sau đó, glucose sẽ được tổng hợp thành amylose và amylopectin. Đây là hai thành phần chính của X. Một học sinh tiến hành thí nghiệm như sau:
• Bước 1: Dùng băng giấy đen che phủ một phần lá cây ở cả hai mặt, đặt cây vào chỗ tối ít nhất hai ngày.
• Bước 2: Đem chậu cây ra để chỗ có nắng trực tiếp (hoặc để dưới ánh sáng của bóng đèn điện 500 W) từ 4 – 8 giờ.
• Bước 3: Sau 4 – 8 giờ, ngắt chiếc lá thí nghiệm, tháo băng giấy đen, cho lá vào cốc thủy tinh đựng nước cất, sau đó đun lá trong nước sôi khoảng 60 giây.
• Bước 4: Tắt bếp, dùng panh gắp lá và cho vào ống nghiệm có chứa cồn 90° đun cách thủy trong vài phút (hoặc cho đến khi thấy lá mất màu xanh lục).
• Bước 5: Rửa sạch lá cây trong cốc nước ấm.
• Bước 6: Bỏ lá cây vào cốc thủy tinh hoặc đĩa petri, nhỏ vào vài giọt dung dịch iodine pha loãng. Quan sát màu sắc của lá cây thấy phần lá không bị che chuyển màu xanh tím, phần lá bịt băng giấy đen không chuyển màu xanh tím.
(1) Học sinh trên đã dùng phản ứng tạo màu giữa tinh bột và iodine để nhận biết tinh bột vì các phân tử amylose ở dạng vòng xoắn, khi tương tác với iodine thì vòng này đã bọc (hay hấp phụ) các phân tử iodine tạo thành hợp chất bọc có màu xanh tím.
(2) Thí nghiệm chứng minh tinh bột được tạo thành trong quá trình quang hợp.
(3) Ở bước 4, chất màu xanh lục (chất diệp lục) được loại bỏ khỏi lá cây bằng phương pháp chiết.
(4) Amylose trong tinh bột được tạo bởi các gốc α-glucose liên kết với nhau bằng liên kết α-1,4-glycoside và α-1,6-glycoside.
Các phát biểu đúng được sắp xếp theo thứ tự tăng dần? (ví dụ như 124 )
(Xem giải) Câu 2. Một nhà máy sản xuất túi nylon từ HDPE cần sản xuất túi đựng hình chữ nhật có kích thước là 20cm x 30cm, bề dày của lớp nylon là 0,02cm. Biết hiệu suất phản ứng trùng hợp ethylene để điều chế HDPE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và biết khối lượng riêng của nhựa HDPE là 0,95 g/cm3. Khối lượng nguyên liệu ethylene dùng để sản xuất đơn hàng 100.000 túi trên bằng bao nhiêu tấn?
(Xem giải) Câu 3. Có bao nhiêu đồng phân alcohol C4H10O2 có thể tham gia phản ứng với Cu(OH)2 tạo dung dịch xanh lam?
(Xem giải) Câu 4. Vấn nạn ăn mòn kim loại gây ra tốn thất kinh tế lớn, theo thống kê hằng năm có khoảng 10-30% lượng kim loại bị ăn mòn so với lượng kim loại sản xuất. Sau rất nhiều thử nghiệm, thế giới đã tìm ra được một giải pháp tối ưu giúp kim loại chống lại ăn mòn, đồng thời không gây quá nhiều gánh nặng về kinh tế. Giải pháp ưu việt được đưa ra là “xi mạ kim loại”, tiêu biểu nhất phải kể đến là mạ kẽm (zinc).
Cho các phát biểu sau về đặc điểm của mạ kẽm:
(a) Giúp chống rỉ sét do lớp mạ kẽm khi gặp nước sẽ không xảy ra phản ứng hóa học.
(b) Tăng độ bền cho sản phẩm do kẽm phản ứng với oxygen trong không khí tạo lớp màng oxide mỏng bền chắc bảo vệ.
(c) Mạ kẽm là cách bảo vệ kim loại bằng phương pháp bảo vệ bề mặt.
(d) Tăng tính thẩm mỹ cho sản phẩm như mạ kẽm trắng, mạ kẽm xanh, mạ kẽm 7 màu…
Có bao nhiêu phát biểu đúng?
(Xem giải) Câu 5. Khi tiêu thụ các loại thực phẩm và đồ uống thì carbohydrate, protein và chất béo sẽ cung cấp năng lượng cho cơ thể. Hình bên là nhãn thực phẩm trên một loại coffee đóng chai. Dưới đây là giá trị nhiên liệu của một số chất có trong chai coffee. Giá trị nhiên liệu là năng lượng giải phóng khi đốt cháy hoàn toàn 1 gram chất.
| Chất | Giá trị nhiên liệu (kJ/g) |
| Carbohydrate | 17 |
| Protein | 17 |
| Chất béo | 38 |
Giả sử, trong quá trình học tập, một học sinh tiêu thụ trung bình 7 kJ năng lượng mỗi phút thì hoạt động này có thể được duy trì trong bao nhiêu phút từ năng lượng thu được từ hai khẩu phần coffee đóng chai? (làm tròn đến hàng đơn vị)
(Xem giải) Câu 6. Trong công nghiệp, nhôm được sản xuất từ quặng bauxite theo hai giai đoạn chính:
• Giai đoạn 1: Tinh chế quặng bauxite
• Giai đoạn 2: Điện phân Al2O3 nóng chảy
Để điều chế khoảng 400 kg nhôm cần dùng khoảng m tấn quặng bauxite (chứa khoảng 52% Al2O3, phần còn lại là Fe2O3, SiO2 và tạp chất trơ) với hiệu suất quá trình đạt 85%. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm)


Bình luận