[2021] Thi học kỳ 1 chuyên Trần Đại Nghĩa – Hồ Chí Minh
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Giải chi tiết và đáp án:
| 1D | 2C | 3A | 4B | 5B | 6A | 7B | 8D | 9A | 10A |
| 11D | 12D | 13A | 14D | 15B | 16D | 17A | 18A | 19A | 20C |
| 21C | 22B | 23C | 24D | 25C | 26C | 27B | 28D | 29D | 30A |
| 31C | 32C | 33A | 34D | 35C | 36B | 37C | 38D | 39B | 40C |
| 41B | 42A | 43D | 44A | 45C | 46B | 47D | 48D |
PHẦN A (32 câu trắc nghiệm): Dành cho tất cả các lớp.
(Xem giải) Câu 1. Polime X có phân tử khối là 336000 và hệ số polime hóa là 12000. X là
A. PP. B. PVC. C. Teflon. D. PE.
(Xem giải) Câu 2. Cho m gam axit glutamic tác dụng vừa đủ với 300 ml dung dịch KOH 1M. Giá trị của m là
A. 44,10. B. 21,90. C. 22,05. D. 43,80.
Câu 3. Số đồng phân thuộc loại este ứng với công thức phân tử C3H6O2 là
A. 2. B. 4. C. 3. D. 5.
(Xem giải) Câu 4. Cation M+ có cấu hình electron lớp ngoài cùng 2s2 2p6. Nguyên tử M là
A. Li (Z = 3). B. Na (Z = 11). C. Rb (2 = 37). D. K (Z = 19).
Câu 5. Kim loại nào sau đây không tan được trong dung dịch H2SO4 loãng?
A. Mg. B. Cu. C. Fe. D. Al.
Câu 6. Phát biểu nào sau đây sai?
A. Bản chất của sự ăn mòn hóa học là phản ứng oxi hóa – khử xảy ra trong đó kim loại bị oxi hóa và có phát sinh ra dòng điện.
B. Bản chất của sự điện phân là phản ứng oxi hóa – khử xảy ra trên bề mặt các điện cực dưới tác dụng của dòng điện một chiều.
C. Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh.
D. Để bảo vệ tàu biển làm bằng thép, người ta gắn những tấm Zn vào vỏ tàu ở phần chìm trong nước biển.
(Xem giải) Câu 7. Có thể dùng quỳ tím để phân biệt các dung dịch (hoặc chất lỏng) trong dãy nào sau đây?
A. valin, glyxin, alanin. B. alanin, axit glutamic, lysin.
C. metylamin, lysin, anilin. D. anilin, metylamin, alanin.
Câu 8. Phát biểu nào sau đây đúng?
A. Ở nhiệt độ thường, tất cả các amin đều tan nhiều trong nước.
B. Tất cả các amin đều làm quỳ tím ẩm chuyển màu xanh.
C. Các amin đều không độc, được sử dụng trong chế biến thực phẩm.
D. Để rửa sạch ống nghiệm có dính anilin, có thể dùng dung dịch HCl.
Câu 9. Các ion kim loại sau đây có tính oxi hóa tăng dần theo thứ tự nào?
A. Fe2+ < Ni2+ < Pb2+ < Cu2+ < Ag+. B. Ni2+ < Fe2+ < Pb2+ < Cu2+ < Ag+.
C. Fe2+ < Ni2+ < Pb2+ < Ag+ < Cu2+. D. Fe2+ < Ni2+ < Cu2+ < Pb2+ < Ag+.
(Xem giải) Câu 10. Cho các amin sau: C6H5NH2 (1), (C6H5)2NH (2), C6H5CH2NH2, (3), CH3NH2 (5). Dãy các amin xếp theo chiều tăng dần tính bazơ là
A. (2) < (1) < (3) < (5). B. (3) < (1) < (2) < (5).
C. (3) < (1) < (2) < (5). D. (1) < (2) < (3) < (5).
(Xem giải) Câu 11. Cho các polime: poli(vinyl clorua), poli(metyl acrylat), polietylen terephtalat), nilon-6,6. Số polime được điều chế bằng phản ứng trùng ngưng là
A. 1. B. 4. C. 3. D. 2.
Câu 12. Trường hợp nào sau đây, kim loại bị ăn mòn điện hóa học ?
A. Kim loại kẽm trong dung dịch HCl. B. Đốt dây sắt trong khi oxi khô.
C. Kim loại sắt trong dung dịch HNO3 loãng. D. Thép cacbon để trong không khí ẩm.
Câu 13. Tiến hành bốn thí nghiệm sau:
– Thí nghiệm 1: Nhúng thanh Fe vào dung dịch FeCl3.
– Thí nghiệm 2: Nhúng thanh Fe vào dung dịch CuSO4.
– Thí nghiệm 3: Nhúng thanh Cu vào dung dịch FeCl3.
– Thí nghiệm 4: Cho thanh Fe tiếp xúc với thanh Cu rồi nhúng vào dung dịch HCl.
Số trường hợp xuất hiện ăn mòn điện hoá là
A. 2. B. 1. C. 4. D. 3.
Câu 14. Phản ứng thủy phân este trong môi trường kiềm được gọi là phản ứng
A. tráng gương. B. este hóa. C. hidro hóa. D. xà phòng hóa.
(Xem giải) Câu 15. Cho tất cả các đồng phân đơn chức, mạch hở có cùng CTPT C3H6O2 lần lượt tác dụng với Na, NaOH, NaHCO3. Số phản ứng xảy ra là
A. 6. B. 5. C. 7. D. 4.
(Xem giải) Câu 16. Chất X được tạo thành trong cây xanh nhờ quá trình quang hợp. Ở điều kiện thường X là chất rắn vô định hình. Thuỷ phân X nhờ xúc tác axit hoặc enzim, thu được chất Y có ứng dụng làm thuốc tăng lực trong y học. Chất X và Y là
A. Saccarozơ và glucozơ. B. tinh bột và saccarozơ.
C. xenlulozơ và saccarozơ. D. tinh bột và glucozơ.
Câu 17. Cho ba dung dịch riêng biệt: Ala-Ala-Gly, Gly-Ala và hồ tinh bột. Có thể nhận biết được dung dịch Ala-Ala-Gly bằng thuốc thử Cu(OH)2 trong dung dịch NaOH nhờ hiện tượng
A. tạo hợp chất màu tím. B. xuất hiện kết tủa xanh.
C. hỗn hợp tách lớp. D. tạo hợp chất màu xanh đậm.
Câu 18. Cho các cặp oxi hoá – khử được sắp xếp theo chiều tăng dần tính oxi hoá của dạng oxi hóa như sau: Fe2+/Fe, Cu2+/Cu, Fe3+/Fe2+. Phát biểu nào sau đây là đúng?
A. Fe3+ oxi hóa được Cu thinh Cu2+. B. Cu khử được Fe3+ thành Fe.
C. Cu2+ oxi hoá được Fe2+ thành Fe3+. D. Fe2+ oxi hóa được Cu thành Cu2+.
Câu 19. Cho 4 phản ứng hóa học:
(1) Sn + Pb2+ → Pb + Sn2+. (2) Cu + 2Fe3+ → Cu2+ + 2Fe2+.
(3) 2Fe2+ + Cu → Cu2+ + 2Fe3+. (4) Fe2+ + Ag+ → Ag + Fe3+.
Các phản ứng đúng là
A. (1), (2), (4). B. (1), (2), (3). C. (1), (3), (4). D. (2), (3), (4).
(Xem giải) Câu 20. Cho 30,45 gam tripeptit mạch hở Gly-Ala-Gly vào dung dịch NaOH dư. Sau khi phản ứng hoàn toàn thấy có m gam NaOH phản ứng. Giá trị của m là
A. 20. B. 24. C. 18. D. 22.
Câu 21. Chất béo X tác dụng với H2 (xúc tác Ni, đun nóng) theo tỉ lệ mol tối đa nX : nY = 1 : 3. X là chất nào trong các chất sau?
A. tristearin. B. trilinolein. C. triolein. D. tripanmitin.
Câu 22. Khi đun nóng dung dịch protein xảy ra hiện tượng nào trong các hiện tượng sau?
A. Có khi không màu thoát ra. B. Đông tụ protein.
C. Màu của dung dịch thay đổi. D. Protein tan tốt hơn.
Câu 23. Trong công nghiệp, một lượng lớn chất béo dùng để sản xuất
A. xà phòng và ancol etylic. B. glucozơ và glixerol.
C. xà phòng và glixerol. D. glucozơ và ancol etylic.
Câu 24. Nguyên nhân tính chất vật lý chung của kim loại là do trong mạng tinh thế kim loại có
A. ít electron ở lớp ngoài cùng. B. nhiều ion kim loại.
C. các ion dương chuyển động tự do. D. các electron chuyển động tự do.
Câu 25. Các loại chai nhựa có kí hiệu số 1 (như hình bên). Kí hiệu này có ý nghĩa là

A. loại chai được sử dụng một hoặc nhiều lần.
B. loại chai có hạn sử dụng trong một năm.
C. loại chai chỉ sử dụng một lần.
D. loại chai chỉ sử dụng cho một loại thức uống.
Câu 26. Amin thuộc loại amin bậc 2 là
A. trimetylamin. B. metylamin. C. đimetylamin. D. phenylamin.
(Xem giải) Câu 27. Cho X có công thức phân tử là C4H9O2N, biết X tác dụng với NaOH tạo sản phẩm muối có công thức phân tử là C3H6O2NNa. Phát biểu đúng về cấu tạo của X là
A. X là amino axit no, mạch hở có 1 nhóm COOH, 1 nhóm NH2.
B. X là este của amino axit no, mạch hở với ancol no, đơn chức, mạch hở.
C. X là hợp chất có chứa nhóm NO2 được dùng để điều chế amin.
D. X là muối của axit không no đơn chức, mạch hở với NH3.
Câu 28. Chất nào sau đây còn có tên gọi là đường nho?
A. Tinh bột. B. Fructozơ. C. Saccarozơ. D. Glucozơ.
Câu 29. Chất có tính lưỡng tính là
A. etylamin. B. metylamin. C. anilin. D. glyxin.
Câu 30. Cấu hình electron nào sau đây là của nguyên tử kim loại?
A. 1s2 2s2 2p6 3s1. B. 1s2. C. 1s2 2s2 2p6. D. 1s2 2s2 2p2.
Câu 31. Cho hình vẽ mô tả thí nghiệm điều chế chất lỏng Y từ dung dịch X.
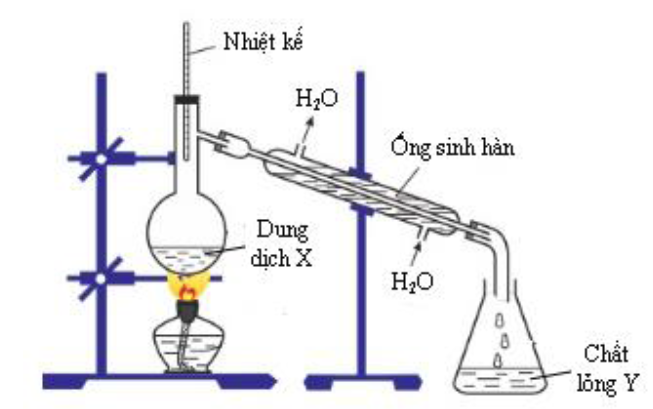
Trong thí nghiệm bên xảy ra phản ứng hóa học nào sau đây?
A. C6H5NH2 + HCl → C6H5NH3CI. B. C2H5OH → CH2=CH2 + H2O
C. CH3COOH + C2H5OH → CH3COOC2H5 + H2O. D. (C6H10O5)n + nH2O → nC6H12O6
Câu 32. Kim loại có nhiệt độ nóng chảy cao nhất và thấp nhất là
A. Cr, Hg. B. Cr, Ag. C. W, Hg. D. W, Ag.
PHẦN B (8 câu trắc nghiệm): Dành cho các lớp không chuyển hóa.
(Xem giải) Câu 33. Chất hữu cơ X mạch hở, có công thức phân tử C4H6O4, không tham gia phản ứng trán bạc. Cho a mol X phản ứng với dung dịch KOH dư, thu được m gam một muối và ancol Y. Đốt cháy hoàn toàn Y thu được 0,2 mol CO2 và 0,3 mol H2O. Giá trị của a và m lần lượt là
A. 0,1 và 16,6. B. 0,1 và 13,4. C. 0,1 và 16,8. D. 0,2 và 12,8.
(Xem giải) Câu 34. Hỗn hợp X gồm glyxin, anilin và axit glutamic (trong đó nguyên tố oxi chiếm 41,2% khối lượng). Cho m gam X tác dụng với dung dịch NaOH dư, thu được 20,532 gam muối. Giá trị của m là
A. 13,1. B. 13,8. C. 12. D. 16.
(Xem giải) Câu 35. Cho 0,01 mol Fe vào 50 ml dung dịch AgNO3 1M thi khối lượng Ag thu được là
A. 1,08 gam. B. 5,4 gam. C. 3,24 gam. D. 2,16 gam.
(Xem giải) Câu 36. Cho 61,2 gam hỗn hợp X gồm Cu và Fe3O4 tác dụng với dung dịch HNO3 loãng, đun nóng và khuấy đều. Sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí NO (là sản phẩm khử duy nhất, ở đktc), dung dịch Y và còn lại 2,4 gam kim loại. Cô cạn dung dịch Y, thu được m gam muối khan. Giá trị của m là
A. 97,5 gam. B. 151,5 gam. C. 108,9 gam. D. 137,1 gam.
(Xem giải) Câu 37. Cho 12 gam Mg vào 1 lít dung dịch chứa CuSO4 0,25M và FeSO4 0,3M. Khối lượng chất rắn sau phản ứng là
A. 16 gam Cu và 12 gam Fe. B. 12 gam Cu và 16 gam Fe.
C. 16 gam Cu và 14 gam Fe. D. 14 gam Cu và 16 gam Fe.
(Xem giải) Câu 38. Cho m gam Mg vào dung dịch chứa 0,12 mol FeCl3. Sau khi phản ứng xảy ra hoàn toàn, thu được 3,36 gam chất rắn. Giá trị của m là
A. 2,16 gam. B. 5,04 gam. C. 4,32 gam. D. 2.88 gam.
(Xem giải) Câu 39. Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 loãng, thu được 1,344 lít hidro (ở đktc) và dung dịch chứa m gam muối. Giá trị m là
A. 10,27. B. 8,98. C. 7,25. D. 9,52
(Xem giải) Câu 40. Cho 11,36 gam hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng (dư), thu được 1,344 lít khí NO (sản phẩm khử duy nhất, ở đktc) và dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là
A. 35,5. B. 34,36. C. 38,72. D. 49,09.
PHẦN C (8 câu trắc nghiệm): Dành cho lớp 12 chuyên hóa.
(Xem giải) Câu 41. Biết E°Cu2+/Cu = +0,34V; E°Cr3+/Cr = -0,74V, phản ứng hóa học xảy ra trong pin điện hóa: 2Cr + 3Cu2+ → 2Cr3+ + 3Cu. E° của pin điện hóa này là
A. 0,4V. B. 1,08V. C. 1,25V. D. 2,5V.
(Xem giải) Câu 42. Hỗn hợp X gồm Cu và Fe có khối lượng 9 gam. Tỷ lệ khối lượng giữa Fe và Cu là 7: 8. Cho lượng X trên vào lượng dung dịch HNO3, khuấy đều cho phản ứng xảy ra hoàn toàn thì thu được chất rắn Y nặng 6,48 gam, dung dịch muối sắt và khí NO (sản phẩm khử duy nhất). Khối lượng muối sắt tạo thành trong dung dịch là
A. 8,1 gam. B. 10,5 gam. C. 7,22 gam. D. 25,32 gam.
(Xem giải) Câu 43. Đốt cháy hoàn toàn 4,56 gam hỗn hợp gồm axit acrylic, vinyl axetat, metyl acrylat và axit oleic, rồi hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 (dư). Sau phản ứng thu được 24 gam kết tủa và dung dịch X. Khối lượng X so với khối lượng dung dịch Ca(OH)2 ban đầu đã thay đổi như thế nào?
A. Giảm 7,38 gam. B. Giảm 7,74 gam. C. Tăng 7,92 gam. D. Giảm 9,84 gam.
(Xem giải) Câu 44. Điện phân 200 ml dung dịch chứa đồng thời AgNO3 1M và Cu(NO3)2 2M trong thời gian 48 phút 15 giây với I = 5A (với điện cực trơ). Sau điện phân, để yên bình điện phân cho các phản ứng xảy ra hoàn toàn thu được V lít khí NO (sản phẩm khử duy nhất ở đktc). Giá trị của V là
A. 0,84 lit. B. 6,72 lit. C. 1,12 lit. D. 3,36 lit.
(Xem giải) Câu 45. Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 19,6 lít khí O2 thu được 16,8 lít khí CO2 và 13,5 gam H2O. Nếu cho m gam X tác dụng hết với 400 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 24,4 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a: b là
A. 7:1. B. 3:5. C. 3:2. D. 4:3
(Xem giải) Câu 46. Trong quá trình pin điện hóa Zn – Ag hoạt động, ta nhận thấy
A. Khối lượng của điện cực Ag giảm. B. [Zn2+] trong dung dịch tăng.
C. [Ag+] trong dung dịch tăng. D. khối lượng của điện cực Zn tăng.
(Xem giải) Câu 47. Hòa tan hoàn toàn m gam hỗn hợp 3 kim loại X, Y, Z bằng dung dịch HNO3 thu được V lít hỗn hợp khí D (ở đktc) gồm NO và NO2 (không tạo thành NH4NO3). Tỉ khối hơi của D so với H2 là 19. Khối lượng muối trong dung dịch thu được tính theo m và V là
A. (m + 8,749V) gam. B. (m + 8,96V) gam.
C. (m + 4,48V) gam. D. (m + 5,536V) gam.
(Xem giải) Câu 48. Cho một tripeptit X tạo bởi glyxin, alanin và valin tác dụng vừa đủ với 300 ml dung dịch NaOH 0,1M. Khối lượng muối thu được sau phản ứng là
A. 2,08 gam. B. 2,17 gam. C. 3,28 gam. D. 3,47 gam.

Bình luận