[2025 – 2026] Thi học sinh giỏi lớp 12 – Tỉnh Ninh Bình (Đề minh họa)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề 007-H12A năm 2025-2026
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
| 1B | 2B | 3A | 4A | 5A | 6B | 7B | 8C | 9A | 10B |
| 11A | 12B | 13C | 14D | 15A | 16D | 17A | 18C | 19A | 20C |
| (a) | (b) | (c) | (d) | ||||||
| 21 | S | Đ | S | Đ | 27 | 4,76 | |||
| 22 | S | Đ | S | Đ | 28 | 4,87 | |||
| 23 | S | S | Đ | Đ | 29 | 652 | |||
| 24 | S | S | Đ | S | 30 | 5,96 | |||
| 25 | Đ | S | Đ | Đ | 31 | 11,5 | |||
| 26 | Đ | Đ | S | S | 32 | 1072 | |||
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 20. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Liên kết cộng hoá trị được hình thành do sự xen phủ của các orbital. Cho các hình ảnh biểu diễn sự xen phủ orbital tạo liên kết hoá học sau:
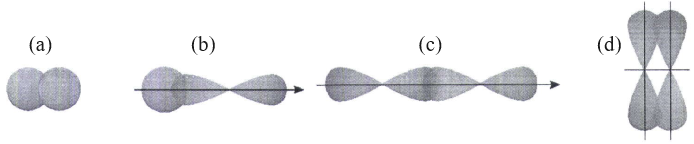
Kiểu xen phủ orbital nào xuất hiện trong phân tử HF? Biết: H (Z = 1), F (Z = 9).
A. (a) và (c). B. (b). C. (a) và (b). D. (a) và (d).
(Xem giải) Câu 2. Cho biết: enthalpy tạo thành chuẩn của các chất sau:
| Chất | SO2(g) | O2(g) | SO3(g) |
| -296,83 | -395,72 |
Biến thiên enthalpy chuẩn của phản ứng của phản ứng: 2SO2(g) + O2(g) → 2SO3(g) là
A. –98,89 kJ. B. –197,78 kJ. C. 98,89 kJ. D. 197,78 kJ.
(Xem giải) Câu 3. Trong cơ thể, một loại thuốc (X) được chuyển hoá tuân theo định luật tác dụng khối lượng trong đó bậc phản ứng của X là bậc 1. Biết rằng sau thời gian 4h, 50% lượng X đã được chuyển hoá. % lượng chất X chưa chuyển hoá sau thời gian 12h là
A. 12,5%. B. 6,25%. C. 25,0%. D. 10,0%.
(Xem giải) Câu 4. Trong dãy các hydrohalic acid, sự sắp xếp nào sau đây đúng với lực acid của các acid trong dãy?
A. HF < HCl < HBr < HI. B. HCl < HBr < HI < HF.
C. HI < HBr < HCl < HF. D. HF < HBr < HI < HCl.
(Xem giải) Câu 5. Cho dãy các phân tử: H2O, CO2, SO2, SCl2. Số phân tử có cấu trúc thẳng (các nguyên tử trong phân tử nằm trên cùng một đường thẳng) trong dãy là (Biết: H (Z = 1); C (Z = 6); O (Z = 8), S (Z = 16); Cl (Z = 17).
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 6. Cho một số phản ứng thường gặp trong công nghiệp sau:
(a) N2(g) + 3H2(g) ⇌ 2NH3(g)
(b) CaCO3(s) ⇌ CaO(s) + CO2(g)
(c) FeO(s) + CO(g) ⇌ Fe(s) + CO2(g)
(d) 2SO2(g) + O2(g) ⇌ 2SO3(g)
(e) CH4(g) + H2O(g) ⇌ CO(g) + 3H2(g)
Số phản ứng khi thực hiện ở áp suất cao có hiệu suất cao hơn khi thực hiện ở áp suất thấp (trong điều kiện nhiệt độ như nhau) là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 7. Sulfuric acid được sản xuất trong công nghiệp từ nguyên liệu sulfur theo chuỗi các phản ứng sau:
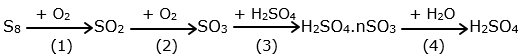
Phản ứng nào trong chuỗi các phản ứng trên sử dụng đến chất xúc tác?
A. (1). B. (2). C. (3). D. (4).
(Xem giải) Câu 8. Citric acid là hợp chất hữu cơ có mạch no, hở và phân tử chỉ chứa nhóm chứa –OH và nhóm –COOH. Công thức phân tử của citric acid là C6H8O7. Trung hoà 20 mL dung dịch citric acid cần dùng 24 mL dung dịch NaOH 0,150M. Nồng độ mol/L của citric acid là
A. 0,180M. B. 0,120M. C. 0,060M. D. 0,240M.
(Xem giải) Câu 9. Để xử lí mùi (chủ yếu là mùi khai) của tã lót trẻ sơ sinh, trong giai đoạn ngày xưa một số bà mẹ ngâm tã lót đó trong một dung dịch, giúp loại bỏ mùi của từ các tã lót đó. Cơ sở của cách làm này là
A. dung dịch được sử dụng là giấm ăn pha loãng và sẽ phản ứng với ammonia (chất gây mùi khai) và loại bỏ mùi của tã lót.
B. dung dịch được sử dụng là giấm ăn pha loãng và sẽ thay thế các chất gây mùi trong tã lót do tạo được các liên kết bền với tã lót.
C. dung dịch được sử dụng là nước muối và muối sẽ khử trùng các các vi khuẩn gây mùi để loại bỏ các vi khuẩn bám trên tã lót.
D. dung dịch được sử dụng là nước muối và muối sẽ phản ứng với ammonia (chất gây mùi khai) và loại bỏ mùi của tã lót.
(Xem giải) Câu 10. Hình vẽ dưới đây mô tả các bước tiến hành thí nghiệm tách hoặc tinh chế chất như sau:
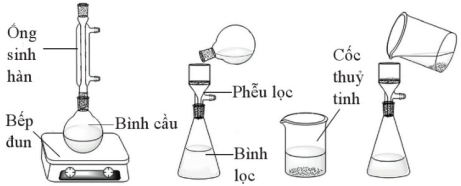
Hãy cho biết các bước trên thuộc quá trình nào sau đây?
A. Chiết. B. Kết tinh. C. Sắc kí cột. D. Chưng cất.
(Xem giải) Câu 11. Chỉ số SAP là lượng KOH cần thiết (tính bằng milligam) để phản ứng hết với 1 gam dầu, mỡ theo phản ứng xà phòng hóa và trung hòa hết carboxylic acid tự do có trong dầu, mỡ. Một loại dầu dừa có chỉ số SAP là 250 – 260 do đó người ta sử dụng giá trị SAP trung bình là 255. Khối lượng NaOH cần lấy để xà phòng hoá hoàn toàn 100 kg chất béo đó là
A. 18,2 kg. B. 19,5 kg. C. 20,4 kg. D. 17,6 kg.
(Xem giải) Câu 12. Công ty Đạm Ninh Bình sản xuất phân bón như đạm urea, NPK,…Theo số liệu được cung cấp, hàng năm công ty sản xuất khoảng 560000 tấn urea. Quá trình sản xuất urea của công ty thực hiện theo phản ứng tổng quát sau:
CO2(g) + 2NH3(g) (t°, p cao) → CO(NH2)2 + H2O
Dựa vào công nghệ tuần hoàn mà hiệu suất quá trình tổng hợp tại nhà máy đạt khoảng 98%. Khối lượng NH3 sử dụng để sản xuất được lượng urea trên gần nhất với giá trị nào sau đây?
A. 340 000 tấn. B. 323 800 tấn. C. 312 000 tấn. D. 364 800 tấn.
(Xem giải) Câu 13. Cho dãy các acid béo sau:
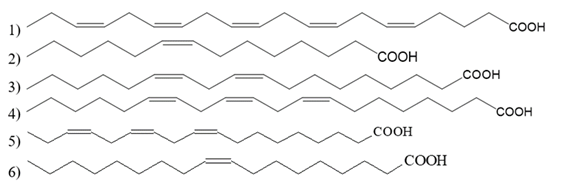
Số acid béo thuộc nhóm omega-6 là
A. 2. B. 5. C. 3. D. 4.
(Xem giải) Câu 14. Glucose phản ứng với hoá chất nào sau đây thể hiện tính chất của nhóm –OH hemiacetal?
A. Thuốc thử Tollens. B. Cu(OH)2 trong dung dịch NaOH.
C. Khí H2 (xúc tác Ni, t°). D. CH3OH (xúc tác HCl).
(Xem giải) Câu 15. Cấu tạo của một đoạn mạch polymer X như sau:
![]()
Công thức của polymer X là
A. [-CH2-CH(CH3)-]n. B. [-CH(CH3)-CH(CH3)-]n.
C. [-CH2-CH(CH2CH3)-]n. D. [-CH2-CH2-]n.
(Xem giải) Câu 16. Amine X có công thức cấu tạo là CH3CH2NHCH3. Tên thay thế của X là
A. 1-methyl ethanamine. B. ethyl methylamine.
C. N-methyl ethylamine. D. N-methyl ethanamine.
(Xem giải) Câu 17. Hải Hậu (một huyện của tỉnh Nam Định cũ) là một trong các vùng trồng lúa nổi tiếng ở Đồng bằng Bắc Bộ. Gạo Hải Hậu thơm, ngon, dẻo được nhiều gia đình yêu thích. Thành phần chính của gạo gồm 2 loại polysaccharide là amylose và amylopectin. Các đơn vị mắt xích tạo nên các polysaccharide trên là
A. α-glucose. B. β-glucose. C. α-fructose. D. β-fructose.
(Xem giải) Câu 18. Insulin, một loại hormone thuộc loại protein, được sản sinh bởi tuyến tuỵ, có chức năng điều hoà quá trình chuyển hoá glucose trong cơ thể. Insulin thúc đẩy sự hấp thu glucose của các tế bào và dự trữ glucose dư thừa trong gan và cơ. Insulin tạo từ 51 gốc amino acid phân bố trong 2 chuỗi:
• Chuỗi I: 21 gốc amino acid.
• Chuỗi II: 30 gốc amino acid.
Hai chuỗi đó liên kết với hai bằng hai cầu disulfide (–S–S–) và trên chuỗi I có thêm một cầu disulfide. Số liên kết peptide (-CONH-) có trong một phân tử insulin là
A. 50. B. 51. C. 49. D. 48.
(Xem giải) Câu 19. Acquy chì khi phóng điện được mô tả theo mô hình bên:
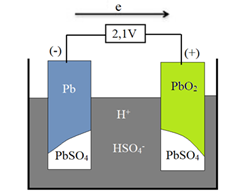
Tại anode (cực âm): Pb(s) + HSO4-(aq) → PbSO4(s) + H+(aq) + 2e
Tại cathode (cực dương): PbO2(s) + HSO4-(aq) + 3H+(aq) + 2e → PbSO4(s) + 2H2O(l)
Trong quá trình acquy phóng điện, sự thay đổi nào sau đây đúng?
A. Khối lượng các điện cực tăng.
B. Nồng độ H+ trong dung dịch tăng.
C. Nồng độ H2SO4 trong dung dịch tăng.
D. Sức điện động (E) của acquy tăng.
(Xem giải) Câu 20. Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trọng sản xuất và đời sống: Sản xuất polyethylene (PE), tổng hợp ethyl alcohol, sản xuất dung môi, kích thích quả mau chín. Phản ứng hóa học của ethylene với dung dịch Br2 như sau: CH2=CH2 + Br2 → CH2Br-CH2Br (∗)
Cơ chế của phản ứng trên xảy ra theo 2 giai đoạn như sau:
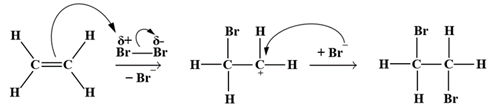
Nhận định nào sau đây là sai?
A. Ở giai đoạn 2, phần tử mang điện dương kết hợp với anion Br– tạo thành sản phẩm.
B. Giai đoạn 1 xảy ra chậm hơn giai đoạn 2 nên giai đoạn 1 quyết định tốc độ của phản ứng.
C. Sản phẩm của giai đoạn 1 có chứa một electron chưa ghép đôi.
D. Phản ứng (∗) thuộc loại phản ứng cộng.
PHẦN II. Thí sinh trả lời từ câu 21 đến câu 26. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
(Xem giải) Câu 21. Dây chuyền sản xuất NH3 như sau:
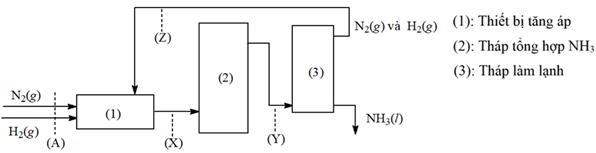
Biết rằng tỉ lệ mol N2 : H2 trong tháp tổng hợp NH3 là 1 : 3. Tốc độ dòng khí đi qua điểm (X) là 1000 mol/s; tốc độ dòng khí đi qua điểm (Y) là 900 mol/s.
a) Hiệu suất phản ứng tổng hợp NH3 ở tháp phản ứng là 10%.
b) Tốc độ dòng khí đi qua điểm (Z) là 800 mol/s.
c) Sau khi đi ra khỏi tháp (3), NH3 tách ra ở dạng lỏng chứng tỏ NH3 có nhiệt độ hoá lỏng thấp nhất.
d) Tỉ lệ mol N2 : H2 tại các điểm (X), (Y), (Z) luôn là 1 : 3.
(Xem giải) Câu 22. Một nhóm học sinh nghiên cứu ảnh hưởng của pH dung dịch đến sức điện động của pin Galvani Zn – Cu. Giả thuyết được đưa ra là: “Khi thay đổi pH của dung dịch muối sẽ thay đổi sức điện động của pin điện”. Nhóm học sinh đó tiến hành thí nghiệm như sau ở 25°C:
• Thí nghiệm 1: Lấy thanh Zn nhúng vào cốc 1 đựng 400 mL dung dịch ZnSO4 1,25M và thanh Cu nhúng cốc 2 vào 400 mL dung dịch CuSO4 1,25M, thêm nước cất vào cả hai cốc để thành 500 mL dung dịch. Nối hai dung dịch với nhau bằng cầu muối KCl nhão và hai thanh kim loại với một vôn kế như hình vẽ sau:
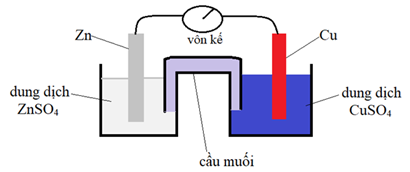
Để hệ thống ổn định khoảng 2 phút và ghi lại số chỉ vôn kế và được giá trị là 1,10 V.
Lặp lại các bước như thí nghiệm 1 nhưng thay nước cất ở một trong hai cốc bằng dung dịch H2SO4 2M. Cụ thể:
• Thí nghiệm 2: thay nước cất ở cốc 1 bằng 100 mL dung dịch H2SO4 2M, thì số chỉ vôn kế là 1,07 V.
• Thí nghiệm 3: thay nước cất ở cốc 2 bằng 100 mL dung dịch H2SO4 2M, thì số chỉ vôn kế là 1,12 V.
a) Khi pin điện hoá trên hoạt động, thanh Zn là cực dương và thanh Cu là cực âm.
b) Kết quả các thí nghiệm cho thấy giả thuyết học sinh đưa ra là đúng.
c) So sánh kết quả ba thí nghiệm cho thấy, pH ở các dung dịch càng thấp thì sức điện động của pin càng lớn.
d) Kết quả thí nghiệm chứng minh rằng: trong các dung dịch muối tồn tại nhiều cân bằng hoá học giữa các dạng tồn tại chứa kim loại.
(Xem giải) Câu 23. Glutamic acid (Glu) là một amino acid không thiết yếu và có thể được cơ thể hấp thụ từ thực phẩm chứa các chuỗi peptide hoặc muối của các amino acid. Trong dung dịch nước của glutamic acid tồn tại các cân bằng sau:
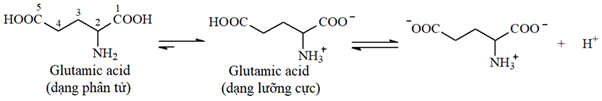
pH của dung dịch glutamic acid nồng độ 0,10M là 3,22.
a) Glutamic acid là là hợp chất hữu cơ đa chức.
b) Từ đặc điểm cấu tạo của glutamic acid (dạng lưỡng cực) chứng tỏ nhóm -COOH ở vị trí số 1 có lực acid yếu hơn nhóm -COOH ở vị trí số 5.
c) Nếu giảm pH của dung dịch glutamic acid bằng cách thêm HCl đặc vào, nhóm –COO– trong dạng lưỡng cực sẽ chuyển dần thành nhóm –COOH.
d) Khi đặt dòng điện một chiều vào dung dịch tại pH = 4, glutamic acid điện di về phía cực dương chứng tỏ glutamic acid tồn tại chủ yếu ở dạng anion.
(Xem giải) Câu 24. Chitin là một loại polymer thiên nhiên với trữ lượng rất lớn (đứng thứ hai sau cellulose). Trong tự nhiên, chitin tồn tại trong cả động vật và thực vật. Trong động vật, chitin là một thành phần cấu trúc quan trọng trong vỏ của một số động vật không xương sống như: giáp xác (tôm, cua,…), côn trùng, nhuyễn thể, giun tròn,… Đun nóng chitin với dung dịch NaOH 40 – 50%, thu được chitosan theo sơ đồ sau:
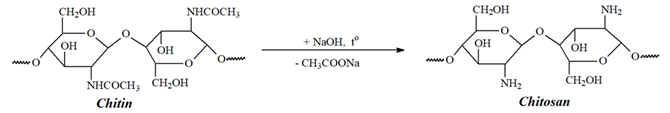
Biết rằng, chỉ cần 50% số nhóm -NHCOCH3 trong chitin chuyển thành nhóm -NH2 thì sản phẩm sẽ được gọi là chitosan.
a) Chitin và chitosan có công thức chung lần lượt là (C8H13O5N)n và (C6H11O4N)n.
b) Phản ứng giữa chitin với dung dịch NaOH tạo ra chitosan là phản ứng giảm mạch polymer.
c) Chitosan thu được sau phản ứng của chitin với NaOH có phân tử khối nhỏ hơn so với chitin.
d) Khi đun nóng 193 gam chitin với dung dịch NaOH, sản phẩm chitosan thu được có khối lượng là 167,4 gam thì có 80% số nhóm -NHCOCH3 trong chitin đã thuỷ phân.
(Xem giải) Câu 25. Ascorbic acid (hay vitamin C) được biết đến như một hợp chất quan trọng đối với con người. Nó đóng vai trò chất chống lão hoá, tăng sức đề kháng của cơ thể.
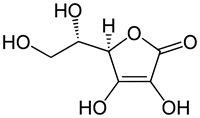
Một nhóm học sinh được giao nhiệm vụ xác định hàm lượng ascorbic acid trong một viên uống cung cấp vitamin C. Nhóm học sinh đã biết được ngoài ascorbic acid (kí hiệu là H2As), các hoạt chất còn lại coi như không có phản ứng với NaOH. Phản ứng giữa ascorbic acid với NaOH được biểu diễn bởi phương trình sau:
H2As + NaOH → NaHAs + H2O
Điểm tương đương được xác định dựa vào chỉ thị phenol đỏ (màu tại điểm tương đương là màu da cam, pH = 8,72). Nhóm học sinh tiến hành thí nghiệm theo các bước sau:
• Bước 1: Lấy một viên vitamin C, đem cân được 800 mg.
• Bước 2: Hoà tan phần đã nghiền vào nước, lọc bỏ phần không tan, thêm nước để được 100,0 mL (dung dịch X). Lấy 10 mL dung dịch X cho vào cốc sạch và nhỏ 1 – 2 giọt phenol đỏ vào, dung dịch thu được có màu đỏ.
• Bước 3: Lấy dung dịch NaOH 0,02M cho vào burette đến vạch số 0. Mở khoá burette cho dung dịch NaOH từ từ vào cốc đựng dung dịch X (lắc nhẹ cốc trong quá trình thí nghiệm) cho đến khi dung dịch trong cốc có màu da cam và dừng lại. Ghi lại thể tích dung dịch NaOH đã dùng là V1 (mL). Lặp lại bước 3 thêm 2 lần nữa, kết quả thu được như sau:
| Thí nghiệm | Lần 1 | Lần 2 | Lần 3 |
| Thể tích dung dịch NaOH (mL) | 14,20 | 14,25 | 14,15 |
a) Giả thuyết khoa học phù hợp là ” Sử dụng phản ứng chuẩn độ acid – base xác định được hàm lượng của ascorbic acid trong hoạt chất của thuốc”.
b) Trong quá trình chuẩn độ, tốc độ chảy từ burette của dung dịch NaOH được giữ không đổi để được kết quả chính xác nhất.
c) Trong quá trình chuẩn độ, việc lắc nhẹ cốc giúp cho tốc độ phản ứng giữa ascorbic acid với NaOH diễn ra nhanh hơn.
d) Kết quả thí nghiệm của nhóm học sinh xác định được hàm lượng ascorbic acid trong hoạt chất là 62,5% (Kết quả được làm tròn đến hàng phần mười).
(Xem giải) Câu 26. Để khảo sát ảnh hưởng của nhiệt độ đến quá trình tổng hợp ethyl acetate, một loạt thí nghiệm được tiến hành với hỗn hợp phản ứng gồm acetic acid và ethanol theo tỷ lệ mol 1 : 1 và H2SO4 đặc được sử dụng làm chất xúc tác với nồng độ cố định. Quá trình phản ứng được thực hiện dưới điều kiện đun hồi lưu liên tục trong thời gian 6 giờ ở các mức nhiệt độ khác nhau. Sau khi kết thúc phản ứng, hỗn hợp được làm nguội và xử lí nhằm tách sản phẩm, sau đó tiến hành phân tích để đánh giá hiệu suất tạo thành ethyl acetate ở từng điều kiện nhiệt độ. Kết quả thí nghiệm được biểu diễn ở đồ thị hình bên.
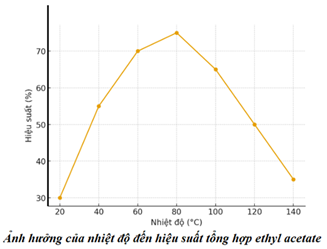
a) Phản ứng tổng hợp ethyl acetate trong thí nghiệm này được gọi là phản ứng ester hoá.
b) Hiệu suất phản ứng tổng hợp ethyl acetate lớn nhất ở 80°C.
c) Ethyl acetate được tách khỏi hỗn hợp sau phản ứng bằng phương pháp kết tinh.
d) Hiệu suất phản ứng ở nhiệt độ 20°C nhỏ hơn hiệu suất ở 80°C là do phản ứng ở 20°C xảy ra chậm hơn so với phản ứng ở 80°C.
PHẦN III. Thí sinh trả lời từ câu 27 đến câu 32.
(Xem giải) Câu 27. Cho các cân bằng trong dung dịch nước sau:
(1) NH4+(aq) ⇌ NH3(aq) + H+(aq) K1 = 10^–9,24
(2) H2O(l) ⇌ H+(aq) + OH-(aq) K2 = 10^–14,00
(3) NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH-(aq) K3 = 10^–a
Xác định giá trị của a.
(Xem giải) Câu 28. Acetic acid điều chế từ ethanol bằng phương pháp lên men theo phương trình hoá học sau: CH3CH2OH + O2 (enzyme) → CH3COOH + H2O
Để có được giấm ăn (dung dịch CH3COOH 5%) bằng phương pháp trên thì rượu ban đầu có độ rượu là x° (hay ethanol chiếm x% thể tích). Cho biết: hiệu suất lên men đạt 100% và khối lượng riêng của C2H5OH là 0,8 g/mL; của nước là 1 g/mL. Xác định giá trị của x. (Không làm tròn các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
(Xem giải) Câu 29. Steroid (X) có trong thức ăn. X là ester của stearic acid và cholestorol (phân tử có chứa 27 nguyên tử carbon và được biểu diễn ở hình sau).
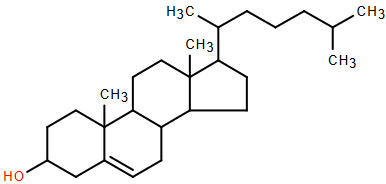
Xác định phân tử khối (M) của steroid X.
(Xem giải) Câu 30. Trong dung dịch nước của glycine, tồn tại các cân bằng sau:
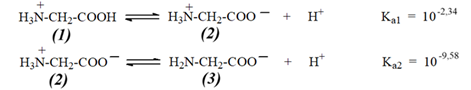
Điểm đẳng điện (kí hiệu là pI) là giá trị pH của dung dịch mà tại đó dạng tồn tại chủ yếu là dạng (2) và nồng độ cân bằng của hai dạng (1) và (3) bằng nhau ([(1)] = [(3)]). Xác định giá trị pI.
(Xem giải) Câu 31. Poly (vinyl acetate) (viết tắt là PVAc) được làm keo dán gỗ, keo dán giấy,… PVAc được tổng hợp từ ethylene theo sơ đồ sau:
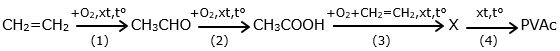
Trong các phản ứng (1), (2), (3), (4) lần lượt có 90%, 95%, 80% và 90% lượng chất hữu cơ chuyển hoá thành sản phẩm theo sơ đồ phản ứng, lượng chất hữu cơ còn lại chuyển hoá thành các sản phẩm khác hoặc không tái sử dụng được. Riêng phản ứng (3), tỉ lệ mol các chất hữu cơ được lấy theo đúng hệ số trong phương trình phản ứng. Khối lượng PVAc (theo kg) thu được từ 10 m³ ethylene (đo ở 25°C, 1 bar) là bao nhiêu? Biết: hằng số R = 0,08314 bar.L.mol-1.K-1; (Không làm tròn các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 32. Điện lượng (q) của pin điện liên hệ với số mol electron trao đổi giữa hai điện cực (ne) hoặc thời gian (t, giây) pin hoạt động theo biểu thức sau: q = ne.F = I.t
Với F là hằng số Faraday, F = 96485 C/mol; I là cường độ dòng điện của pin.
Người ta lập một pin Galvani gồm:
• Nửa pin 1: Thanh Zn có khối lượng 200 gam nhúng vào 1,00 L dung dịch Zn(NO3)2 1M
• Nửa pin 2: Thanh Cu có khối lượng 100 gam nhúng và 1,00 L dung dịch Cu(NO3)2 1M.
Hai thanh kim loại được nối với vật tiêu thụ điện và hai dung dịch nối với nhau bằng cầu muối (chứa KCl nhão). Pin trên sản sinh dòng điện có cường độ ổn định là I = 0,05A. Xác định thời gian (theo giờ) pin đó hoạt động. Biết rằng pin chỉ dừng hoạt động khi một trong các chất tham gia phản ứng hết. (Không làm tròn các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).


Bình luận