[2025] Thi thử TN sở GDĐT Nghệ An (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 072
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2D | 3D | 4C | 5A | 6A | 7A | 8C | 9D |
| 10D | 11B | 12D | 13B | 14B | 15B | 16A | 17A | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | Đ | S | 124 | 1058 | 2645 |
| (b) | S | Đ | Đ | S | 26 | 27 | 28 |
| (c) | S | S | S | Đ | 5 | 4 | 67,1 |
| (d) | Đ | Đ | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Nước cứng gây nhiều trở ngại cho đời sống thường ngày. Các nguồn nước ngầm hoặc nước ở các ao hồ, sông suối thường có độ cứng cao bởi quá trình hòa tan các ion Ca2+, Mg2+ có trong thành phần của lớp trầm tích đá vôi. Cho các phát biểu sau:
(a) Có thể dùng Na2CO3 để làm mềm nước có tính cứng toàn phần.
(b) Nước cứng làm cho xà phòng có ít bọt, giảm khả năng tẩy rửa của xà phòng.
(c) Nước tự nhiên có chứa ion Ca2+, Mg2+, HCO3- gọi là nước có tính cứng vĩnh cửu.
(d) Để loại bỏ lớp cặn trong ấm đun nước lâu ngày có thể dùng dung dịch giấm ăn.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 2. Trong quá trình hoạt động của pin Zn – Pb, quá trình xảy ra ở cathode là
A. Pb → Pb2+ + 2e. B. Zn → Zn2+ + 2e.
C. Zn2+ + 2e → Zn. D. Pb2+ + 2e → Pb.
(Xem giải) Câu 3. Eicosapentaenoic acid (EPA) có trong một số loại cá biển và tảo. Công thức của EPA như sau:
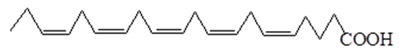
Cho các nhận định sau:
(a) Eicosapentaenoic acid có công thức phân tử là C20H30O2.
(b) Eicosapentaenoic acid thuộc nhóm acid béo omega-3.
(c) Eicosapentaenoic acid là một chất béo lỏng.
(d) Một phân tử Eicosapentaenoic acid tác dụng tối đa với năm phân tử hydrogen ở điều kiện thích hợp.
Các nhận định đúng là
A. (b), (c), (d). B. (a), (b), (c).
C. (a), (b), (c), (d). D. (a), (b), (d).
(Xem giải) Câu 4. Quá trình điện phân dung dịch NaCl bão hòa với điện cực trơ (graphite) thu được khí nào sau đây ở cathode?
A. Cl2. B. HCl. C. H2. D. O2.
(Xem giải) Câu 5. Phức chất trisoxalatoferrate(III) (hoặc ferrioxalate) có công thức cấu tạo sau:
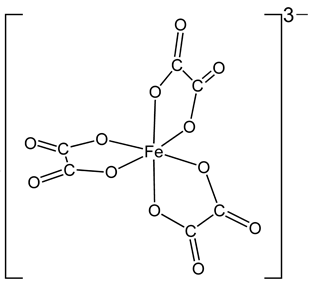
Số lượng phối tử có trong phức chất trên là
A. 3. B. 6. C. 2. D. 1.
(Xem giải) Câu 6. Trong công nghiệp, nguyên liệu thường dùng để sản xuất phân lân là quặng apatite. Thành phần chính của quặng apatite là
A. Ca3(PO4)2. B. CaCO3. C. Ca(H2PO4)2. D. CaSO4.
(Xem giải) Câu 7. Ester ethylpropionate có mùi dứa. Công thức cấu tạo thu gọn của ester này là
A. C2H5COOC2H5. B. C3H7COOC2H5. C. CH3COOCH3. D. CH3COOC2H5.
(Xem giải) Câu 8. Bơ thực vật là loại bơ nhân tạo, được chế biến từ dầu thực vật bằng cách chuyển hóa chất béo lỏng thành chất béo rắn. Để chuyển hóa dầu thực vật thành bơ thực vật người ta thực hiện quá trình
A. cô cạn dầu thực vật ở nhiệt độ cao. B. làm lạnh nhanh dầu thực vật.
C. hydrogen hóa dầu thực vật. D. xà phòng hóa dầu thực vật.
(Xem giải) Câu 9. Argentite (chứa Ag2S) là loại quặng chứa bạc trong tự nhiên. Trong công nghiệp, để tách kim loại Ag từ quặng argentite tiến hành theo sơ đồ sau:
![]()
Phương pháp điều chế kim loại nào đã được sử dụng trong quá trình sản xuất Ag theo sơ đồ trên?
A. Điện phân dung dịch. B. Điện phân nóng chảy.
C. Nhiệt luyện. D. Thuỷ luyện.
(Xem giải) Câu 10. Có thể dùng dao hoặc kéo để cắt kim loại nhóm IA một cách dễ dàng là do
A. kim loại nhóm IA dễ bị oxi hóa trong không khí.
B. kim loại nhóm IA có thế điện cực chuẩn nhỏ.
C. nhiệt độ nóng chảy của kim loại nhóm IA thấp.
D. lực liên kết kim loại trong tinh thể kim loại nhóm IA yếu.
(Xem giải) Câu 11. Trong sản xuất hợp kim, thêm chromium vào thép để tăng cường tính chất nào sau đây?
A. Tính dễ dát mỏng. B. Chống ăn mòn. C. Tính dẻo. D. Tính dẫn điện.
(Xem giải) Câu 12. Cho một số hiện tượng sau:
(a) Nhỏ nitric acid vào lỏng trắng trứng thấy xuất hiện kết tủa vàng.
(b) Luộc chín trứng gà.
(c) Mỡ lợn bị đóng rắn khi làm lạnh
(d) Khi nấu canh cua thấy có chất rắn (gạch cua) nổi lên.
Số hiện tượng có sự đông tụ protein là
A. 3 B. 4 C. 1 D. 2
(Xem giải) Câu 13. Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:

Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 3 được điều chế bằng phản ứng trùng hợp monomer nào dưới đây?
A. CH2=CH2. B. CH2=CH–Cl. C. CH2=CH–C6H5. D. CH2=CH–CH3.
(Xem giải) Câu 14. Khi đun nóng ester X (có công thức cấu tạo thu gọn CH3COOR, là ester của acetic acid với alcohol no, đơn chức, mạch hở ROH) trong dung dịch NaOH, phản ứng hoá học xảy ra như sau: CH3COOR + NaOH → CH3COONa + ROH (*)
Cơ chế của phản ứng xảy ra như sau:
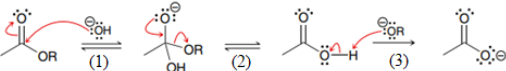
Nhận định nào sau đây không đúng?
A. Phản ứng (*) thuộc loại phản ứng xà phòng hóa.
B. Giai đoạn (1) có sự hình thành liên kết π.
C. Trong phân tử chất sản phẩm ROH chỉ có liên kết σ.
D. Trong giai đoạn (1) có sự phân cắt liên kết π.
(Xem giải) Câu 15. Tên bán hệ thống của amino acid H2N-CH(CH3)-COOH là
A. alanine. B. α-aminopropionic acid.
C. β-aminopropionic acid. D. aminoacetic acid.
(Xem giải) Câu 16. Saccharose là chất rắn có vị ngọt, dễ tan trong nước. Saccharose có công thức phân tử là
A. C12H22O11. B. (C6H10O5)n. C. C6H12O6. D. C3H6O3.
(Xem giải) Câu 17. “Chưng cất là phương pháp tách và tinh chế chất lỏng dựa trên sự khác nhau về … của các chất trong hỗn hợp ở áp suất nhất định”. Nội dung phù hợp trong dấu … là
A. nhiệt độ sôi. B. khối lượng riêng.
C. độ tan. D. nhiệt độ nóng chảy.
(Xem giải) Câu 18. Mức độ phản ứng với nước của các kim loại từ Li, Na, K biến đổi như thế nào?
A. Giảm dần. B. Không đổi.
C. Tăng dần. D. Không theo quy luật.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Một học sinh tiến hành thí nghiệm nghiên cứu sự tạo thành phức chất, phản ứng của phức chất iron(III), ghi lại hiện tượng quan sát được và đưa ra những nhận định như sau:
• Bước 1: Hòa tan iron(III) sulfate vào ống nghiệm chứa nước thu được dung dịch màu vàng nâu. Sau một thời gian, thấy có kết tủa màu nâu đỏ trong ống nghiệm.
• Bước 2: Lọc bỏ kết tủa, thêm KSCN (potassium thiocyanate) vào nước lọc thấy dung dịch chuyển sang màu đỏ máu của các phức chất bát diện chứa từ 1 đến 6 phối tử SCN-.
• Bước 3: Thêm tiếp dung dịch KF dư vào ống nghiệm thấy dung dịch nhạt màu dần và mất màu do tạo phức chất [FeF6]3-.
a) Kết tủa xuất hiện ở Bước 1 là do sự thủy phân phức aqua của ion Fe3+.
b) Các phức chất được tạo thành ở Bước 2 đều có điện tích âm.
c) Ở Bước 3 chỉ xảy ra phản ứng thay thế phối tử SCN- bằng phối tử F-.
d) Ở Bước 1 có quá trình hình thành phức chất aqua của ion kim loại.
(Xem giải) Câu 20. Học sinh A tìm hiểu quá trình làm giấm ăn từ dung dịch ethyl alcohol loãng với giả thiết “khi nhiệt độ tăng thì tốc độ lên men giấm càng nhanh”. Để kiểm tra giả thiết này, học sinh A đã tiến hành thí nghiệm như sau:
– Chuẩn bị: 1 lít rượu vang trắng (nồng độ ethyl alcohol khoảng 10°), 1 ly giấm nuôi, 5 cốc thủy tinh chia vạch loại 200 mL.
– Cách làm: Lấy 200 mL rượu vang trắng vào cốc thứ nhất (mẫu trắng). Cho giấm nuôi vào lượng rượu còn lại, rồi cho vào 4 cốc thủy tinh đến vạch định mức, đậy nắp bằng tấm bìa giấy. Bảo quản các cốc trong điều kiện ít chiếu sáng ở các nhiệt độ: 0°C (mẫu 1); 10°C (mẫu 2); 30°C (mẫu 3); 50°C (mẫu 4).
Sau 1 tháng, lấy các mẫu đem lọc sạch, để ổn định ở nhiệt độ môi trường thì thấy thể tích dung dịch trong các mẫu hầu như không thay đổi..Lần lượt lấy 5 mL các mẫu: mẫu trắng và các mẫu 1; 2; 3; 4 rồi pha loãng thành 100 mL và tiến hành chuẩn độ bằng dung dịch NaOH 0,1 M với chỉ thị phenolpthalein. Kết quả thu được như bảng sau:
| Mẫu | Mẫu trắng | Mẫu 1 | Mẫu 2 | Mẫu 3 | Mẫu 4 |
| V NaOH 0,1M (mL) | 4,8 | 5,2 | 7,4 | 25,2 | 8,6 |
Biết trong các mẫu chỉ chứa C2H5OH, CH3COOH và H2O
a) Trong thí nghiệm trên, nhiệt độ tối ưu cho quá trình lên men giấm là 30°C.
b) Trong rượu vang trắng đã có một lượng CH3COOH.
c) Từ kết quả thí nghiệm, kết luận giả thuyết của học sinh A là đúng.
d) Trong thí nghiệm trên, lượng CH3COOH được tạo thành nhiều nhất trong một mẫu (200 mL) là 4,896 gam.
(Xem giải) Câu 21. Glutamine và glutamic acid là những amino acid không thiết yếu. Tuy nhiên chúng được sử dụng bởi hầu hết các sinh vật sống trong quá trình sinh tổng hợp ra protein. Trong máu ở người, glutamine là amino acid tự do có hàm lượng cao nhất. Về cấu tao, từ phân tử glutamic acid, thay thế nhóm chức carboxyl (ở phía xa nhóm -NH2) bởi nhóm chức amide (-CONH2) ta được glutamine.
a) Công thức phân tử của glutamine là C5H10O3N2.
b) Glutamine có số loại nhóm chức nhiều hơn số loại nhóm chức của glutamic.
c) Tại pH bất kỳ, khi đặt trong điện trường, glutamine và glutamic acid sẽ di chuyển về 2 điện cực khác nhau.
d) Glutamine và glutamic acid đều thuộc loại α-amino acid.
(Xem giải) Câu 22. Một nhóm học sinh nghiên cứu sự ăn mòn kim loại của một sợi nhôm với giả thuyết: “trong cùng điều kiện, tốc độ ăn mòn điện hóa nhanh hơn tốc độ ăn mòn hóa học”. Để kiểm tra giả thuyết của mình, nhóm học sinh trên đã chuẩn bị 2 sợi nhôm (loại làm lõi dây điện đơn) đã làm sạch bề mặt, có kích thước, khối lượng như nhau và tiến hành các thì nghiệm như sau:
– Thí nghiệm 1: Nhúng một sợi nhôm vào dung dịch H2SO4 0,5M (hình 1).
– Thí nghiệm 2: Nhúng sợi nhôm còn lại vào dung dịch H2SO4 0,5M cùng với một sợi đồng và nối chúng lại qua vôn kế (hình 2).
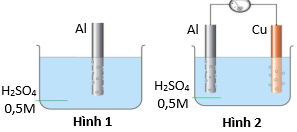
a) Ở thí nghiệm 2, quan sát thấy có bọt khí thoát ra trên bề mặt sợi đồng, chứng tỏ sợi đồng bị ăn mòn hóa học.
b) Nhóm học sinh trên quan sát thấy bọt khí thoát ra trên bề mặt sợi nhôm ở thí nghiệm 1 nhanh hơn bọt khí thoát ra trên bề mặt sợi nhôm ở thí nghiệm 2, chứng tỏ giả thuyết trên là sai.
c) Sau 3 phút, nhóm học sinh lấy 2 sợi nhôm ra cân lại, thấy khối lượng sợi nhôm ở thí nghiệm 1 lớn hơn khối lượng sợi nhôm ở thí nghiệm 2, chứng tỏ giả thuyết trên là đúng.
d) Nếu thế điện cực chuẩn E°Al3+/Al = -1,676V; E°2H+/H2 = 0V; E°Cu2+/Cu = 0,340V thì vôn kế luôn chỉ giá trị cố định là 2,016 V.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Ở điều kiện thường, hợp chất hữu cơ X tồn tại ở trạng thái lỏng. Khi phân tích thành phần nguyên tố của hợp chất hữu cơ X thu được kết quả %C; %H;, %O (theo khối lượng) lần lượt là 60,00%; 13,33%; 26,67%. Cho các nhận định sau về X:
(1) Công thức phân tử của X là C3H8O.
(2) X là alcohol.
(3) X có phản ứng iodoform.
(4) Giữa các phân tử X có liên kết hydrogen.
Hãy sắp xếp các nhận định đúng theo thứ tự tăng dần.
(Xem giải) Câu 24. Trong công nghiệp, sản xuất nước Javel xảy ra qua hai giai đoạn chính sau:
– Giai đoạn 1: điện phân dung dịch NaCl bão hòa không có màng ngăn điện cực:
2NaCl(aq) + 2H2O(l) → 2NaOH(aq) + H2(g) + Cl2(g)
– Giai đoạn 2: khí Cl2 phản ứng với dung dịch NaOH tạo ra nước Javel:
Cl2(g) + 2NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l)
Một loại nước Javel (có khối lượng riêng 1,15 g/cm³) được bán trên thị trường với chai dung tích 1,0 L có nồng độ NaClO, NaCl và NaOH lần lượt là 10%; 8% và 0,8%. Để sản xuất 1000 chai nước Javel ở trên cần bao nhiêu kg dung dịch NaCl 18,5% (làm tròn kết đến hàng đơn vị)?
(Xem giải) Câu 25. DEP (diethyl phthalatate) được dùng làm thuốc điều trị bệnh ghẻ và giảm triệu chứng sưng tấy ở vùng da bị côn trùng cắn. Có thể điều chế DEP từ o-xylene qua 2 giai đoạn (hiệu suất lần lượt là 75% và 80%) được mô tả như sau:

Một loại thuốc DEP thành phẩm trên thị trường có hàm lượng diethyl phthalatate là 95% (về khối lượng). Biết mỗi lọ thuốc có chứa 10 gam gồm diethyl phthalatate và tá dược. Hãy tính số lọ thuốc loại này sản xuất được từ 20 kg o-xylene? (làm tròn đến hàng đơn vị).
(Xem giải) Câu 26. Cho thế điện cực chuẩn của các cặp oxi hoá – khử như bảng sau:
| Cặp oxi hóa – khử | Cu2+/Cu | Ni2+/Ni | Zn2+/Zn | Fe2+/Fe | Mg2+/Mg | Fe3+/Fe2+ | Ag+/Ag |
| Thế điện cực chuẩn (V) | 0,340 | –0,26 | –0,762 | –0,440 | –2,356 | 0,771 | 0,799 |
Trong số các kim loại: Fe, Ni, Cu, Mg, Ag và Zn, ở điều kiện chuẩn có bao nhiêu kim loại tác dụng được với dung dịch Fe(NO3)3?
(Xem giải) Câu 27. Cho các hydrocarbon sau: ethylene, buta-1,3-diene, propyne, methane, styrene, propene. Có bao nhiêu chất có thể trùng hợp tạo polymer?
(Xem giải) Câu 28. Một nhà máy nhiệt điện khí có sản lượng điện 10^6 kWh/ngày (1 kWh = 3600 kJ) sử dụng khí thiên nhiên hóa lỏng LNG làm nhiên liệu đã giảm được x% khí thải CO2 so với nhà máy nhiệt điện than (sử dụng than đá làm nhiên liệu) có cùng sản lượng điện. Biết rằng:
– Khí thiên nhiên hóa lỏng LNG chứa 94% CH4 và 6% C2H6 về thể tích. Năng lượng tỏa ra khi đốt cháy hoàn toàn 1 mol CH4 là 890 kJ; 1 mol C2H6 là 1560 kJ và có 64% nhiệt lượng tỏa ra của quá trình đốt cháy hoàn toàn LNG được chuyển hóa thành điện năng.
– Than đá chứa 78% carbon về khối lượng, còn lại là các tạp chất không chứa carbon. Năng lượng tỏa ra khi đốt cháy hoàn toàn 1 tấn than đá là 3.10^7 kJ và chỉ có 40% nhiệt lượng tỏa ra của quá trình đốt cháy hoàn toàn than đá được chuyển hóa thành điện năng.
Tính giá trị của x (làm tròn đến hàng phần mười).


Bình luận