[2025] Thi thử TN sở GDĐT Quảng Nam (Lần 1 – Đề 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 075
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2D | 3D | 4A | 5C | 6D | 7B | 8B | 9B |
| 10C | 11C | 12C | 13A | 14D | 15C | 16A | 17C | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | S | S | Đ | 3 | 37,3 | 95 |
| (b) | Đ | Đ | Đ | S | 26 | 27 | 28 |
| (c) | Đ | S | Đ | Đ | 21,1 | 0,78 | 3241 |
| (d) | S | S | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Trong chế độ dinh dưỡng hàng ngày, khi cơ thể không hấp thu được hoặc thiếu nguyên tố nào sau đây sẽ dẫn đến nguy cơ loãng xương?
A. Ba. B. Mg. C. Ca. D. Be.
(Xem giải) Câu 2. Các chuyến bay thường xuyên của máy bay siêu thanh trong tầng bình lưu sản sinh ra nitrogen monoxide (NO). Chất khí này phản ứng với ozone và người ta cho rằng điều này có thể góp phần làm suy giảm tầng ozone theo phương trình: NO + O3 ⟶ NO2 + O2.
Biết đây là phản ứng đơn giản với hằng số tốc độ là 2,20.10^7. Tốc độ biến mất tức thời của NO là a.10-5 mol/L.s. Giá trị của a là bao nhiêu khi nồng độ NO, O3 lần lượt là 3,3.10^-6M và 5,9.10^-7M? (Làm tròn kết quả đến hàng phần chục).
A. 4,1. B. 4,4. C. 4,2. D. 4,3.
(Xem giải) Câu 3. Khi đun nước đường có thêm một ít nước chanh thì dung dịch sẽ ngọt hơn. Vì nước chanh có thành phần chủ yếu là citric acid, xúc tác thủy phân saccharose tạo sản phẩm fructose vị ngọt hơn. Saccharose và fructose thuộc loại nào trong số carbohydrate sau?
A. Monosaccharide, disaccharide. B. Polysaccharide, monosacharide.
C. Polysaccharide, disaccharide. D. Disaccharide, monosacharide.
(Xem giải) Câu 4. Xem xét các giá trị pH sau cho một loạt các chất.
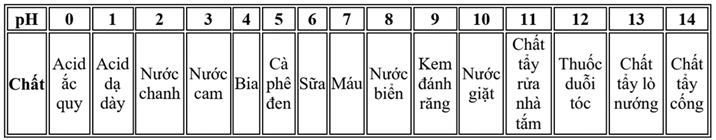
Dựa trên các giá trị pH này, phát biểu nào sau đây về nồng độ ion hydronium (H₃O⁺) là đúng?
A. Nồng độ ion hydronium trong nước biển lớn hơn 1000 lần so với chất tẩy rửa nhà tắm.
B. Nồng độ ion hydronium trong thuốc duỗi tóc lớn hơn 1 000 000 lần so với sữa.
C. Nồng độ ion hydronium trong bia lớn gấp đôi so với nước chanh.
D. Nồng độ ion hydronium trong bia lớn gấp ba lần so với thuốc duỗi tóc.
(Xem giải) Câu 5. Vật liệu polymer tổng hợp E có hình sợi dài, mảnh và giữ nhiệt tốt nên thường được dùng để dệt vải may quần áo ấm hoặc bện thành sợi “len” đan áo rét. Biết E bền với nhiệt và bền trong môi trường acid và base. Vật liệu E là
A. tơ nylon-6,6. B. tơ tằm. C. tơ nitron. D. bông.
(Xem giải) Câu 6. Trong pin Galvani X-Y có phản ứng chung như sau: X(s) + Y2+(aq) → Y(s) + X2+(aq). Quá trình xảy ra tại cathode (hay cực dương) của pin là
A. X2+(aq) + 2e → X(s). B. X(s) → X2+(aq) + 2e.
C. Y(s) → Y2+(aq) + 2e. D. Y2+(aq) + 2e → Y(s).
(Xem giải) Câu 7. Một loại muối (X) của kim loại kiềm được dùng làm phân bón, cung cấp cả hai nguyên tố dinh dưỡng đa lượng cho cây trồng. Công thức hóa học của muối X là
A. Na3PO4. B. KNO3. C. NaNO3. D. K2CO3.
(Xem giải) Câu 8. Giá trị thế điện cực chuẩn của cặp oxi hoá − khử nào được quy ước bằng 0 (V)?
A. Na+/Na. B. 2H+/H2. C. Cl2/2Cl−. D. Al3+/Al.
(Xem giải) Câu 9. M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
– Có nhiều số oxi hóa trong hợp chất, trong đó có số oxi hóa +2 và +3.
– Ở trạng thái cơ bản, nguyên tử có 4 electron độc thân.
– Ở dạng đơn chất, là kim loại nặng.
M là nguyên tố nào sau đây?
A. Cu. B. Fe. C. Cr. D. Ni.
(Xem giải) Câu 10. Cho các nhận định sau về tác hại của nước cứng:
(1) làm giảm bọt khi giặt quần áo bằng xà phòng;
(2) làm đường ống dẫn nước đóng cặn, giảm lưu lượng nước;
(3) làm thức ăn lâu chín và giảm mùi vị;
(4) làm nồi hơi phủ cặn, gây tốn nhiên liệu và có nguy cơ gây nổ.
Số nhận định đúng là
A. 2. B. 3. C. 4. D. 1.
(Xem giải) Câu 11. Tiến hành hòa tan zinc oxide (ZnO) vào dung dịch hydrochloric acid (HCl) như hình vẽ:
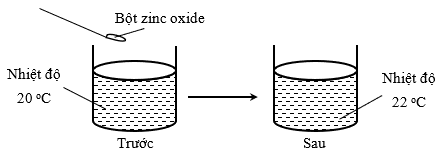
Phát biểu nào dưới đây là sai?
A. Đây là phản ứng tỏa nhiệt.
B. Trong quá trình phản ứng, nhiệt độ của phản ứng tăng.
C. Năng lượng của các chất phản ứng thấp hơn năng lượng của các chất sản phẩm.
D. Biến thiên enthalpy của phản ứng có giá trị âm.
(Xem giải) Câu 12. Thành phần chính của các loại đá vôi là calcium carbonate. Khi cho vôi sống tác dụng với carbon dioxide thì thu được calcium carbonate:
CaO(s) + CO2 (g) → CaCO3(s) (1) ![]() = x kJ
= x kJ
Biết: CaO(s) + H2O(l) → Ca(OH)2(aq) (2) ![]() = -81,9 kJ
= -81,9 kJ
Ca(OH)2(aq) + CO2(g) → CaCO3(s) + H2O(l) (3) ![]() = -96,4 kJ
= -96,4 kJ
Thạch nhũ trong hang động được hình thành dựa trên phản ứng sau đây:
Ca(HCO3)2(aq) → CaCO3(s) + H2O(l) + CO2(g) (4) ![]() = y kJ
= y kJ
Biết: Ca(OH)2(aq) + 2CO2(g) → Ca(HCO3)2(aq) (5) ![]() = -132,72 kJ
= -132,72 kJ
Giá trị x, y lần lượt là
A. -178,3 kJ và 36,42 kJ. B. 36,52 kJ và -168,25 kJ.
C. -178,3 kJ và 36,32 kJ. D. 36,62 kJ và -168,40 kJ.
(Xem giải) Câu 13. Hình ảnh nào dưới đây được dùng cho loại pin điện có thể tái sử dụng nhiều lần bằng cách sạc điện?

A. Acquy chì. B. Pin chanh. C. Pin con thỏ. D. Pin mặt trời.
(Xem giải) Câu 14. Doping là một trong những loại chất kích thích bị cấm sử dụng trong thể thao có công thức hóa học như hình bên.
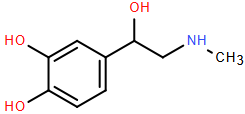
Phát biểu nào dưới đây là đúng khi nói về doping?
A. Doping tham gia phản ứng với hydrogen theo tỉ lệ mol 1:1.
B. Công thức phân tử của doping là C9H11O3N.
C. Doping có khả năng tham gia phản ứng với NaOH theo tỉ lệ mol 1:3.
D. Doping có khả năng làm mất màu nước bromine.
(Xem giải) Câu 15. Chất dẻo khó phân hủy, vì vậy gây ô nhiễm môi trường. Dưới đây là một số giải pháp để hạn chế ảnh hưởng của chất dẻo đến môi trường.
(1) Sử dụng vật liệu có thể phân hủy sinh học hoặc thân thiện với môi trường.
(2) Tái chế và tái sử dụng các sản phẩm chất dẻo.
(3) Phân loại rác theo quy định.
(4) Không tự ý đốt chất thải nhựa.
(5) Tăng cường sử dụng bao bì nhựa, túi nylon.
Các giải pháp đúng là
A. (1), (3), (4) và (5). B. (1), (2), (3) và (5).
C. (1), (2), (3) và (4). D. (1), (2), (4) và (5).
(Xem giải) Câu 16. Cellulose thuộc loại polysaccharide, là thành phần chính tạo nên màng tế bào thực vật, có nhiều trong gỗ, bông nõn. Công thức của cellulose là
A. (C6H10O5)n. B. C12H22O11. C. C6H12O6. D. C2H4O2.
(Xem giải) Câu 17. “Chất béo là các triester của…(1)… với các…(2)…, gọi chung là các triglyceride”. Nội dung phù hợp trong các vị trí (1), (2) lần lượt là
A. glycerol, carboxylic acid. B. ethylene glycol, acid béo.
C. glycerol, acid béo. D. ethylene glycol, carboxylic acid.
(Xem giải) Câu 18. Nhựa X là chất liệu khá cứng, không màu, không mùi, không vị, dễ tạo màu. Các loại hộp xốp phần lớn được làm từ nhựa X. X thuộc loại polymer nhiệt dẻo có kí hiệu là PS. Vậy X là
A. cellulose. B. poly(methyl methacrylate).
C. polystyrene. D. polypropylene.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Sự hình thành ion phức [Fe(SCN)]2+ trong dung dịch nước được biểu diễn bằng cân bằng hóa học ở dưới đây. Người ta đề xuất xác định gián tiếp nồng độ của ion Fe3+ trong dung dịch bằng cách sử dụng quang phổ UV-Vis để đo nồng độ của ion phức [Fe(SCN)]2+ có màu đỏ được tạo ra.
Fe3+(aq) + SCN⁻(aq) ⇌ [Fe(SCN)]2+ (aq) ![]() < 0 (1)
< 0 (1)
Màu vàng Màu đỏ
a) Phản ứng tạo thành ion phức [Fe(SCN)]2+ là phản ứng toả nhiệt.
b) Nếu thêm 1,0 mL dung dịch Fe(NO3)3 vào cân bằng (1), thì màu đỏ của phức sẽ đậm hơn.
c) Để xác định chính xác nhất về nồng độ của ion Fe3+ trong dung dịch ban đầu bằng cách sử dụng quang phổ UV-Vis thì cân bằng (1) phải có giá trị của hằng số cân bằng lớn, sử dụng dư SCN⁻ và phản ứng được thực hiện ở nhiệt độ thấp.
d) Khi hỗn hợp cân bằng (1) bị pha loãng, cân bằng (1) dịch chuyển theo chiều thuận.
(Xem giải) Câu 20. Trona là một khoáng vật tự nhiên, có công thức hóa học Na3H(CO3)2.2H2O. Khoáng vật Trona là một nguồn tự nhiên quan trọng để sản xuất sodium carbonate công nghiệp. Trong thành phần của Trona: NaHCO3 thường được biết đến là baking soda (làm bánh, y tế), trong khi Na2CO3 là soda (công nghiệp thủy tinh, chất tẩy rửa, làm mềm nước)…
a) Trona là hỗn hợp của 2 muối sodium bicarbonate và sodium carbonate với tỉ lệ khối lượng bằng nhau.
b) Khi nung nóng, Trona bị phân hủy thành sodium carbonate khan (Na2CO3), H2O và khí CO2.
c) Trong công nghiệp, Na2CO3 và NaHCO3 còn được sản xuất bằng phương pháp Solvay từ nguyên liệu chính là CaSO4 và NaCl.
d) Một học sinh muốn chuẩn bị một dung dịch có nồng độ cuối cùng của Na+ là 0,50 M và nồng độ cuối cùng của HCO3- là 0,10 M bằng cách lấy một ít (NaOH và Trona), pha loãng với nước đến thể tích cuối cùng là 1,00 L. Học sinh cần phải dùng 0,35 mol NaOH và 0,05 mol Trona.
(Xem giải) Câu 21. Pin “cúc áo” lithium, được sử dụng để cung cấp năng lượng cho đồng hồ bình thường và máy tính bỏ túi, là một pin sơ cấp chứa kim loại lithium. Pin lithium ion là một pin thứ cấp được sử dụng để cung cấp năng lượng cho máy tính xách tay.
Trong pin lithium ion, các ion lithium di chuyển giữa các điện cực khi pin được sạc và xả. Điện cực âm bao gồm graphite đã lithi hóa (LiC6), và điện cực dương bao gồm lithium cobalt oxide (LiCoO2). Các phản ứng hóa học diễn ra trong pin lithium ion rất phức tạp. Các phương trình sau đây trình bày một mô tả đơn giản hóa về các phản ứng xảy ra ở các điện cực khi pin được sạc.
Điện cực dương: LiCoO2 → CoO2 + Li+ + e⁻
Điện cực âm: 6C + Li+ + e⁻ → LiC6
a) Pin sơ cấp và pin thứ cấp đều là loại pin có thể được sạc lại và sử dụng nhiều lần sau khi hết điện.
b) Lithium có thế điện cực chuẩn rất âm, và là một chất khử mạnh và dễ dàng bị oxy hóa, nên lithium được sử dụng làm chất phản ứng trong pin “cúc áo” lithium.
c) Khi pin lithium ion được xả, cả electron và cation Li+ đều di chuyển về phía điện cực dương.
d) Lithium kim loại được sản xuất bằng phương pháp điện phân lithium chloride nóng chảy. Khối lượng lithium kim loại được sản xuất trong 48,0 giờ bằng dòng điện 6,50 ampe là 81,5 gam (kết quả làm tròn đến hàng phần mười).
(Xem giải) Câu 22. Enzyme là các cấu trúc protein phức tạp có chức năng như chất xúc tác sinh học. Invertase là một enzyme xúc tác cho quá trình chuyển đổi sucrose thành glucose và fructose. Invertase có nhiệt độ hoạt động tối đa khác với nhiều enzyme khác. Đồ thị dưới đây cho thấy kết quả của một nghiên cứu về ảnh hưởng của cả pH và nhiệt độ đến hoạt động của invertase trong dung dịch sucrose.
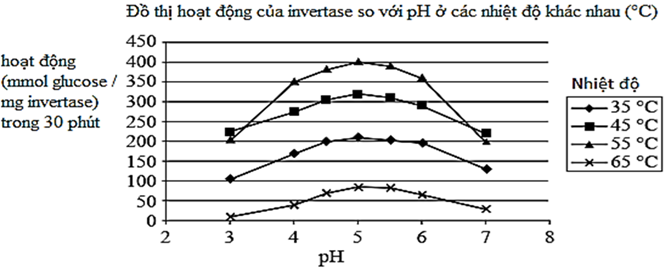
a) Do cấu trúc không gian đặc thù của enzyme, đặc biệt là trung tâm hoạt động, chỉ phù hợp để liên kết với cơ chất (chất phản ứng) tương ứng của nó.
b) Enzyme trong nghiên cứu có hoạt độ tối đa ở nhiệt độ 65°C và pH = 5
c) Ở pH quá cao hoặc quá thấp so với giá trị pH tối ưu, enzyme có thể bị biến tính và mất hoạt tính.
d) Giả sử lượng sucrose dư, có 5,4 gam glucose (M = 180) được tạo ra trong 30 phút từ dung dịch sucrose chứa 1,00.10^-4 gam invertase nếu hoạt độ đo được là 300 mmol glucose/mg invertase.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Cho các thí nghiệm sau:
(1) Glucose phản ứng thuốc thử Tollens.
(2) Glucose phản ứng với nước bromine.
(3) Glucose phản ứng với copper(II) hydroxide và NaOH đun nóng.
(4) Saccharose phản ứng với copper(II) hydroxide trong môi trường kiềm ở điều kiện thường.
(5) Cellulose phản ứng với HNO3 đặc có mặt H2SO4 đặc, đun nóng.
Có bao nhiêu thí nghiệm xảy ra phản ứng oxi hóa – khử?
(Xem giải) Câu 24. Điện phân khí carbon dioxide, trong nước là một cách để tạo ra ethanol. Sơ đồ dưới đây cho thấy một bình điện phân CO2 – H2O. Chất điện li được sử dụng trong bình điện phân là dung dịch sodium bicarbonate, NaHCO3 (aq). Phương trình phản ứng điện phân xảy ra như sau: 2CO2(g) + 3H2O(l) → C2H5OH(l) + 3O2(g)
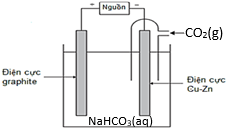
Một dòng điện 2,70 A được cho đi qua bình điện phân CO2 – H2O. Bình điện phân có hiệu suất 58%. Tính thời gian cần thiết (theo phút) để bình này tiêu thụ 6,05.10^-3 mol CO2(g). (Làm tròn kết quả đến hàng phần mười)
(Xem giải) Câu 25. C60600 là hợp kim của copper (Cu) và aluminium (Al). Phản ứng sau đây có thể được sử dụng để xác định hàm lượng Cu trong C60600.
2Cu2+(aq) + 4I-(aq) → 2CuI(s) + I2(aq)
Quy trình thực hiện thí nghiệm như sau:
• Bước 1: Hòa tan 0,5 gam mẫu hợp kim C60600 trong sulfuric acid đặc, rồi pha loãng bằng nước.
• Bước 2: Thêm dung dịch I- đến dư.
• Bước 3: Thêm dần dung dịch S2O32- 0,50 M để phản ứng iodine theo phản ứng sau:
I2(aq) + 2S2O32-(aq) → 2I-(aq) + S4O62-(aq)
Thể tích dung dịch S2O32- (aq) cần để phản ứng trên xảy ra vừa đủ là 14,85 mL. Tính hàm lượng % khối lượng Cu trong mẫu hợp kim C60600? (Làm tròn kết quả đến hàng đơn vị)
(Xem giải) Câu 26. Nước ngầm, bên cạnh nước hồ đập và nước biển khử muối, là một phần của nguồn cung cấp nước cho các hộ gia đình. Nước ngầm chứa nhiều loại hóa chất khác nhau có thể ảnh hưởng đến chất lượng nước uống. Một trong những chất gây ô nhiễm là sắt, thường được tìm thấy ở dạng iron(II) hydrogencarbonate. Iron có thể được loại bỏ bằng cách thêm khí chlorine, calcium hydrogencarbonate được thêm vào để duy trì độ pH hơi base. Phản ứng có thể được biểu diễn bằng phương trình sau:
2Fe(HCO3)2 + Cl2 + Ca(HCO3)2 → 2Fe(OH)3 + CaCl2 + 6CO2
Dẫn 7,00 gam khí chlorine được sục qua 30000 L nước ngầm chứa 38982 mg iron(II) hydrogencarbonate, trong đó đã thêm 16,2 gam calcium hydrogencarbonate. Tính khối lượng (gam) iron(III) hydroxide sẽ kết tủa, phản ứng xảy ra hoàn toàn. (Làm tròn kết quả đến hàng phần mười)
(Xem giải) Câu 27. Trong y học, oxalic acid (H2C2O4) được sử dụng để điều trị một số bệnh về da. Tuy nhiên, việc sử dụng quá liều oxalic acid có thể gây ngộ độc. Để kiểm soát chất lượng của dung dịch oxalic acid, người ta thường sử dụng phương pháp chuẩn độ bằng dung dịch KMnO4. Một dung dịch H2C2O4 được lấy ra 10,00 mL và pha loãng thành 250,0 mL dung dịch. Lấy 25,00 mL dung dịch này cho vào bình nón, thêm H2SO4 loãng dư rồi chuẩn độ bằng dung dịch KMnO4 0,02 M. Thể tích trung bình của dung dịch KMnO4 tiêu tốn sau 3 lần chuẩn độ là 15,60 mL.Tính nồng độ mol của dung dịch H2C2O4 ban đầu (làm tròn đến hàng phần trăm). Biết sản phẩm phản ứng chuẩn độ tạo ra gồm K2SO4, MnSO4, CO2.
(Xem giải) Câu 28. Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4 dưới đây:
(1) CH2=CHCOOCH3 + H2 → CH3CH2COOCH3
(2) CH2=CHCOOCH3 + NaOH → CH2=CHCOONa + CH3OH
(3) CH2=CHCOOH + NaOH → CH2=CHCOONa + H2O
(4) nCH2=CHCOOCH3 → [-CH2-CH(COOCH3)-]n
Gán số thứ tự phương trình hoá học của các phản ứng theo tên gọi: trung hoà, thủy phân, trùng hợp, cộng và sắp xếp theo trình tự thành dãy bốn số (ví dụ: 1234,4321, ….).


Bình luận