[2026] Thi thử TN chuyên Huỳnh Mẫn Đạt – An Giang (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 100
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2A | 3B | 4B | 5A | 6B | 7B | 8C | 9C |
| 10C | 11C | 12B | 13C | 14A | 15C | 16C | 17D | 18D |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | S | Đ |
| (b) | S | S | Đ | S |
| (c) | Đ | Đ | S | S |
| (d) | Đ | S | S | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 44,1 | 12,4 | 27 | 22,5 | 15 | 3,1 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Ion X2- có cấu hình electron ở trạng thái cơ bản 1s2 2s2 2p6. Nguyên tố X là:
A. O (Z = 8). B. F (Z = 9). C. Ne (Z = 10). D. Mg (Z = 12).
(Xem giải) Câu 2: Ammonia có nhiều ứng dụng như sản xuất nitric acid, sản xuất phân đạm, làm dung môi, chất gây lạnh,… Trong công nghiệp, quá trình sản xuất ammonia được thực hiện theo phản ứng sau: N2(g) + 3H2(g) ⇋ 2NH3(g) ![]() = -92 kJ.
= -92 kJ.
Lượng nhiệt tỏa ra khi tổng hợp 3,7185 lít NH3 (đkc) là:
A. 6,9 kJ. B. 92 kJ. C. 13,8 kJ. D. 41 kJ.
(Xem giải) Câu 3: Trong dung dịch muối AlCl3 tồn tại các cân bằng hóa học sau:
Al3+ + 3H2O ⇋ Al(OH)3 + 3H+ (1)
Khi thêm hỗn hợp KIO3 và KI vào dung dịch AlCl3 thì xảy ra phương trình hóa học:
IO3- + 5I- + 6H+ → 3I2 + 3H2O (2)
Cho các phát biểu sau:
(1) Dung dịch muối AlCl3 có pH > 7
(2) Trong phòng thí nghiệm, để tránh sự phân hủy của Al3+ trong dung dịch người ta thường thêm vài giọt dung dịch acid mạnh.
(3) Khi thêm hỗn hợp KIO3 và KI vào dung dịch AlCl3 thì cân bằng (1) chuyển dịch theo chiều thuận, tạo thành Al(OH)3 dạng keo màu trắng.
(4) Có thể dùng hỗn hợp KIO3 và KI để bảo quản ion Al3+
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 4: Chất nào sau đây không phải là một hợp chất ketone?
A. CH3COCH3. B. CH3CHOHCH2CH3. C. C6H5COCH3. D. CH2=CHCH2COCH3.
(Xem giải) Câu 5: Khi đặt trong bình chứa hỗn hợp alkane với halogen (thường là chlorine) hoặc bromine trong phòng tối và ở nhiệt độ phòng, phản ứng không xảy ra. Nhưng đến đun nóng hoặc chiếu ánh sáng sẽ xảy ra phản ứng thế nguyên tử hydrogen trong alkane bằng nguyên tử halogen:

Cho isopentane tác dụng với Br2 tỉ lệ số mol 1 : 1 thu được bao nhiêu sản phẩm monobromo?
A. 4. B. 3. C. 2. D. 5.
(Xem giải) Câu 6: Cho phản ứng sau

Sản phẩm chính của phản ứng trên thì -Br gắn vào vị trí carbon bao nhiêu (tính theo thứ tự đánh số trên mạch carbon)
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 7: Phản ứng hóa học đặc trưng của chất béo là:
A. phản ứng trùng hợp. B. phản ứng thủy phân. C. phản ứng cộng. D. phản ứng thế.
(Xem giải) Câu 8: Chất nào sau đây được tạo thành từ sự liên kết của một đơn vị glucose với một đơn vị fructose?
A. Maltose. B. Tinh bột. C. Saccharose. D. Cellulose.
(Xem giải) Câu 9: Dung dịch amino acid nào sau đây làm quỳ tím chuyển sang màu xanh?
A. Glycine. B. Alanine. C. Lysine. D. Glutamic acid.
(Xem giải) Câu 10: Một học sinh tiến hành thí nghiệm như sau:
• Bước 1: Nhỏ vài giọt aniline nguyên chất vào ống nghiệm chứa 5 mL nước cất, lắc đều.
• Bước 2: Cho vài giọt dung dịch HCl vào ống nghiệm, quan sát hiện tượng.
• Bước 3: Thêm tiếp từ từ dung dịch NaOH 1M cho đến dư, lắc đều và quan sát.
Xét các phát biểu sau:
(a) Aniline tan kém trong nước do phân tử có phần gốc phenyl không phân cực và làm giảm khả năng tạo liên kết hydrogen với nước.
(b) Sau bước 2, dung dịch trở nên trong suốt vì aniline chuyển thành muối tan C6H5NH3Cl.
(c) Sau bước 3, dung dịch vẫn trong suốt do base mạnh làm tăng độ phân cực của aniline.
(d) Phản ứng của aniline với HCl là phản ứng acid-base.
(e) So với NH3, aniline có lực base mạnh hơn.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 11: Cho một pin Galvani có cấu tạo như hình bên.
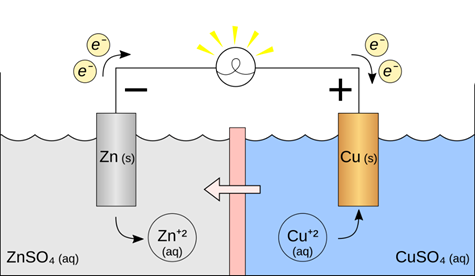
Màng bán thấm ngăn cách hai dung dịch CuSO4 và ZnSO4 và chỉ cho H2O và anion đi qua. Nhận xét nào sau đây không đúng trong quá trình pin phóng điện?
A. Dòng electron đi từ điện cực Zn sang điện cực Cu qua dây dẫn.
B. Khối lượng điện cực Zn giảm và khối lượng điện cực Cu tăng.
C. Ion SO42- chuyển từ dung dịch ZnSO4 sang dung dịch CuSO4 qua màng bán thấm.
D. Phản ứng trong pin khi pin hoạt động là: Zn(s) + Cu2+(aq) → Cu(s) + Zn2+(aq).
(Xem giải) Câu 12: Trong các kim loại cho dưới đây thì kim loại dẫn điện tốt nhất là
A. Au. B. Ag. C. Al. D. Cu.
(Xem giải) Câu 13: Kim loại nào sau đây không tan trong dung dịch H2SO4 đặc, nguội?
A. Zn. B. Cu. C. Al. D. Mg.
(Xem giải) Câu 14: Trong quá trình mạ điện, một kỹ thuật viên nhúng một tấm zinc (Zn) có khối lượng 15,625 gam vào 300 mL dung dịch CuSO4 0,2M. Sau một thời gian, lấy tấm Zn ra, rửa sạch, sấy khô và cân lại thấy khối lượng giảm 0,010 gam. Khối lượng Cu bám vào tấm Zn là bao nhiêu gam? (Giả sử toàn bộ lượng Cu sinh ra đều bám hết vào thanh Zn).
A. 0,640 gam. B. 0,512 gam. C. 0,320 gam. D. 0,960 gam.
(Xem giải) Câu 15: Thực hiện thí nghiệm như hình vẽ dưới đây:
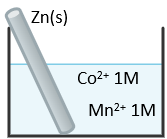
Biết thế điện cực chuẩn:
Mn2+(aq) + 2e ⇋ Mn(s) E° = -1,18V
Zn2+(aq) + 2e ⇋ Zn(s) E° = -0,76V
Co2+(aq) + 2e ⇋ Co(s) E° = -0,28V
Cho các phát biểu sau:
(1) Phản ứng xảy ra giữa Zn(s) và Co2+(aq) tạo được một pin có suất điện động là 0,48V.
(2) Năng lượng hóa học dự trữ trong các chất phản ứng chủ yếu được chuyển hóa thành năng lượng điện khi phản ứng xảy ra.
(3) Nồng độ của các ion trong dung dịch tăng.
(4) Sau một thời gian xảy ra phản ứng, thanh Zn(s) bị ăn mòn dần ở phần nhúng trong dung dịch do xảy ra phản ứng: Zn(s) + Mn2+(aq) → Zn2+(aq) + Mn(s).
Số phát biểu không đúng là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 16: Giáo viên giao nhiệm vụ cho một nhóm học sinh xác định tính cứng của một mẫu nước. Nhóm học sinh đã thực hiện hai thí nghiệm và ghi nhận kết quả như sau:
| Ống nghiệm | Cách tiến hành | Hiện tượng quan sát được |
| 1 | Đun sôi mẫu nước trong 30 giây | Xuất hiện kết tủa X |
| 2 | Thêm 1 mL dung dịch BaCl2 0,1M | Xuất hiện kết tủa Y |
Dựa trên kết quả thu được từ hai thí nghiệm, học sinh đưa ra các nhận định về tính cứng của mẫu nước:
A. Mẫu nước có tính cứng tạm thời. B. Mẫu nước có tính cứng vĩnh cửu.
C. Mẫu nước có tính cứng toàn phần. D. Mẫu nước thí nghiệm là nước mềm.
(Xem giải) Câu 17: Kim loại titanium (Ti) có nhiều ứng dụng quan trọng nhờ các đặc tính: nhẹ, rất bền, chịu nhiệt tốt và chống ăn mòn cao. Do titanium nhẹ nhưng bền gần như thép, giúp giảm khối lượng và tăng độ bền của thiết bị nên dùng chế tạo thân máy bay, cánh máy bay, động cơ phản lực, tên lửa. Ngoài ra titanium tương thích sinh học tốt, ít bị cơ thể đào thải và không bị ăn mòn trong môi trường cơ thể nên dùng chế tạo răng implant, khớp nhân tạo, vít và nẹp xương. Nguyên tố titanium thuộc chu kì 4, nhóm IVB trong bảng tuần hoàn. Cấu hình electron ở trạng thái cơ bản của titanium là
A. [Ne]3d24s2. B. [Ar]3d4. C. [Ar]4s24p2. D. [Ar]3d24s2.
(Xem giải) Câu 18: Phức chất E có nguyên tử trung tâm là X3+, phối tử là NH3. Biết E có số lượng phối tử là 6, công thức của phức chất E có dạng là
A. [X(NH3)6]3-. B. [X(NH3)6]2-. C. [X(NH3)6]2+. D. [X(NH3)6]3+.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Poly(vinyl chloride) (PVC) là một chất dẻo có tính cách điện tốt, không thấm nước, bền với acid vì vậy nó được dùng để sản xuất vật liệu cách điện, ống dẫn nước,… Khi đun nóng, PVC mềm ra rồi nóng chảy và khi để nguội nó lại đóng rắn. Hiện nay, trong công nghiệp sản xuất PVC người ta đi từ nguyên liệu là khí ethylene và chlorine. Quy trình sản xuất thực hiện theo sơ đồ khép kín như sau.
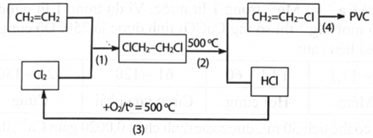
a. Phản ứng (3) giúp giảm thải khí gây ô nhiễm môi trường và tăng hiệu quả của quá trình sản xuất.
b. Trong cơ chế phản ứng của phản ứng (1) thì giai đoạn đầu hình thành gốc tự do CH2=CH•.
c. PVC thuộc loại polymer nhiệt dẻo và vật liệu làm bằng PVC có thể tái chế.
d. Biết chỉ có 1,4% lượng chlorine bị thất thoát vì vậy để sản xuất 1 tấn PVC cần 576 kg chlorine (làm tròn đến phần nguyên).
(Xem giải) Câu 20: Trong phương pháp chuẩn độ acid – base, xung quanh điểm tương đương có một sự thay đổi pH đột ngột gọi là bước nhảy chuẩn độ. Đường biểu diễn trên đồ thị chuẩn độ acid – base gọi là đường định phân. Đồ thị dưới đây biểu diễn sự biến thiên pH của dung dịch thu được khi cho từ từ dung dịch X nồng độ 0,10 M vào dung dịch chất Y (chưa biết nồng độ). Biết rằng X, Y là hai chất không theo thứ tự gồm HCl và NaOH.

a. Trong quá trình chuẩn độ trên, dung dịch X là HCl (dung dịch chuẩn), dung dịch Y là NaOH.
b. Tại điểm tương đương, giá trị pH > 7 và dung dịch thu được chứa các chất tan gồm chứa muối và kiềm dư.
c. Bước nhảy chuẩn độ ở khoảng pH từ 3,7 đến 10,3 và tại khoảng pH đó, thể tích dung dịch X ít thay đổi nhất.
d. Khi đã dùng hết 50 mL dung dịch X, dung dịch thu được có [OH–] < 10–2 M.
(Xem giải) Câu 21: Để mạ đồng cho một tấm huy chương bằng sắt với độ dày và diện tích lớp mạ lần lượt là 0,1 mm và 88,5 cm², người ta tiến hành điện phân dung dịch CuSO4 (điện cực âm là tấm huy chương và điện cực dương là lá đồng (copper) thô, hiệu suất điện phân 100%) với cường độ dòng điện 2A không đổi. Khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết t giây. Cho biết:
– Khối lượng riêng của kim loại Cu là 8,96 g/cm³ và giả thiết toàn bộ lượng kim loại Cu sinh ra đều bám hết vào tấm huy chương, nước không bị điện phân ở cả hai điện cực.
– Điện lượng: q = I.t = ne.F, trong đó: q là điện lượng (C), ne là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian điện phân (giây).
a) Lá đồng thô đóng vai trò là cathode và tại điện cực này xảy ra quá trình oxi hoá kim loại Cu.
b) Lượng CuSO4 trong dung dịch không đổi trong quá trình điện phân.
c) Tấm huy chương đóng vai trò là anode và tại điện cực này xảy ra quá trình khử ion Cu2+.
d) Giá trị của t là 23912.
(Xem giải) Câu 22: Methanol (CH3OH) là một alcohol đơn giản có nhiều ứng dụng quan trọng trong công nghiệp. Methanol được dùng để tổng hợp nhiều hóa chất khác như: Formaldehyde (sản xuất nhựa, keo, chất dẻo), dimethyl ether (nhiên liệu và chất đẩy aerosol), dùng làm nhiên liệu cho động cơ, đặc biệt trong xe đua. Ngoài ra methanol là dung môi tốt trong sản xuất sơn, mực in, nhựa và dược phẩm, làm chất chống đông trong hệ thống làm lạnh và đường ống dẫn khí tự nhiên. Trong công nghiệp, methanol (CH3OH, nhiệt độ sôi 65°C) được tổng hợp từ CO và H2 theo sơ đồ sau:

a. Phản ứng xảy khi đun nóng hỗn hợp A là: CH4 + H2O (200°C, 10 bar) → CO + 3H2
b. Chất ngưng tụ thoát ra ở giai đoạn (4) là H2O và CH4.
c. Nếu quá trình tổng hợp methanol là quá trình tỏa nhiệt, để tăng hiệu suất tổng hợp methanol thì cần tăng nhiệt độ và giảm áp suất của hệ.
d. Giả sử tốc độ lưu chuyển ban đầu của CH4 là 86 L/s và H2O là 150 L/s thì tốc độ lưu chuyển của H2O dư ở giai đoạn (4) là 56 L/s.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Trong quá trình sản xuất 2,4-D và 2,4,5-T từ phenol luôn sinh ra một lượng nhỏ dioxin. Dioxin là một hợp chất khó phân hủy trong môi trường và cơ thể con người. Dioxin cực kì độc ở nồng độ rất nhỏ (cỡ phần tỉ) gây ra những hậu quả khôn lường cho con người như ung thư, quái thai, dị tật, vô sinh,… Dioxin có công thức cấu tạo như sau:
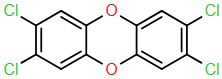
Thành phần (%) của nguyên tố chlorine trong một phân tử dioxin bằng bao nhiêu? (làm tròn kết quả đến hàng phần mười)
(Xem giải) Câu 24: Tơ nylon-6,6 có tính dai, mềm, óng mượt, ít thấm nước, giặt mau khô, được dùng để dệt vải may mặc, dệt bít tất, đan lưới, bện dây cáp, dây dù. Polymer dùng sản xuất tơ nylon-6,6 là poly(hexamethylene adipamide). Poly(hexamethylene adipamide) được tạo thành bằng phản ứng trùng ngưng giữa hexamethylene diamine (H2N[CH2]6NH2) và adipic acid (HOOC[CH2]4COOH). Phần trăm khối lượng của nitrogen trong một mắt xích poly(hexamethylene adipamide) bằng a%. Giá trị của a bằng bao nhiêu (làm tròn kết quả đến hàng phần mười)?
(Xem giải) Câu 25: Methane hydrate hay còn được gọi là “băng cháy” có công thức (CH4)x(H2O)y, là một dạng băng đặc biệt chứa khí methane hình thành sau dưới đáy biển sâu hoặc trong vùng băng vĩnh cửu. Thành phần chính của năng lượng băng cháy có 85 – 90% thể tích là khí methane. Khi đốt nó bốc cháy như than, do vậy methane hydrate có thể trở thành một nguồn năng lượng tiềm năng trong tương lai. Tuy nhiên việc khai thác hydrate gặp nhiều khó khăn vì khi giảm nhiệt độ và áp suất giảm thì sẽ bị phân hủy và giải phóng methane rất mạnh và có thể ảnh hưởng lớn đến môi trường. Giả sử khi đốt cháy hoàn toàn một mẩu methane hydrate trong bình kín với lượng dư oxygen. Sau khi làm nguội thu được 41,85 gam nước và khi tác dụng với nước vôi trong dư thì tạo ra 30 gam kết tủa CaCO3. Giá trị x + y bằng bao nhiêu?
(Xem giải) Câu 26: Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất điện là 56% (nghĩa là có 56% năng lượng của phản ứng chuyển hoá thành điện năng). Mỗi ngày nhà máy sản xuất được 500 kWh. Tính khối lượng (theo kg) khí hydrogen tiêu thụ? (Làm tròn kết quả đến hàng phần mười). Cho biết: 1 kWh = 3,6.10^6 J; MH2 = 2 g/mol và phương trình phản ứng là:
H2(g) + ½O2(g) → H2O(l) ![]() = -285,84kJ.
= -285,84kJ.
(Xem giải) Câu 27: Các khoáng chất Y1, Y2 và Y3 là các tinh thể trong suốt, không hút ẩm, đều là muối ngậm nước của cùng một kim loại hóa trị II và một gốc acid. Khi nung đến trên 200°C, tất cả chúng đều chuyển thành chất Z, cũng tồn tại ở dạng khoáng tự nhiên. Khi hòa tan 10 gam Y1 và 10 gam Y3 vào 100 gam nước, thu được dung dịch Z có nồng độ 10%. Hòa tan từ từ 26,75 gam Y2 theo từng lượng nhỏ vào 100 gam nước tạo thành dung dịch bão hòa Z ở 25°C, khi trộn lẫn dung dịch này với dung dịch BaCl2 dư thu được 29,125 gam kết tủa trắng muối sulfate. Bằng cách đun cẩn thận Y1 đến 63°C có thể thu được Y2, khối lượng bã rắn sau khi nung chỉ còn lại 85,60% so với ban đầu. Tổng số phân tử H2O trong công thức tinh thể của 3 loại tinh trên là bao nhiêu?
(Xem giải) Câu 28: Trong công nghiệp sản xuất sulfuric acid, người ta dùng dung dịch H2SO4 98% để hấp thụ hoàn toàn SO3 tạo ra sản phẩm là oleum. Lấy 5,0 gam oleum sinh ra ở trên pha loãng với nước cất thu được 1000 mL dung dịch H2SO4 loãng (dung dịch X). Để xác định nồng độ H2SO4 trong X, người ta tiến hành chuẩn độ như sau:
• Bước 1: Rửa sạch burette loại 25 mL bằng nước cất, tráng lại bằng dung dịch chuẩn NaOH 0,1M rồi lắp burette lên giá đỡ, cho dung dịch chuẩn NaOH 0,1M vào burette, điều chỉnh dung dịch trong burette đến vạch 0.
• Bước 2: Hút chính xác 10,0 mL dung dịch X cho vào bình tam giác 250 mL. Thêm 3 – 4 giọt phenolphthalein, lắc đều.
• Bước 3: Mở khóa burette để dung dịch NaOH được nhỏ từ từ xuống bình tam giác, lắc đều cho đến khi dung dịch chuyển từ không màu sang màu hồng bền trong khoảng 30 giây thì dừng lại, ghi thể tích dung dịch NaOH đã dùng. Kết quả của 3 lần chuẩn độ như sau:
| Lần chuẩn độ | Lần 1 | Lần 2 | Lần 3 |
| Thể tích dung dịch NaOH đã dùng (mL) | 11,7 | 11,8 | 11,7 |
Tính khối lượng dung dịch (theo tấn) H2SO4 98% cần dùng để sản xuất được 10 tấn oleum ở trên. (Làm tròn kết quả đến hàng phần mười.)

Bình luận