[2026] Thi thử TN chuyên Trần Phú – Hải Phòng (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 019
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2C | 3D | 4A | 5A | 6A | 7D | 8A | 9A |
| 10C | 11D | 12B | 13A | 14B | 15B | 16B | 17C | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | S | S | 5,2 | 3 | 2,8 |
| (b) | Đ | Đ | S | Đ | 26 | 27 | 28 |
| (c) | Đ | S | S | Đ | 4231 | 1402 | 63 |
| (d) | S | S | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Chất nào sau đây được dùng làm chất giặt rửa tổng hợp?
A. C17H35COONa. B. CH3C6H4ONa.
C. CH3[CH2]11C6H4SO3Na. D. C15H31COONa.
(Xem giải) Câu 2. Cho các hợp chất có công thức cấu tạo dưới đây:
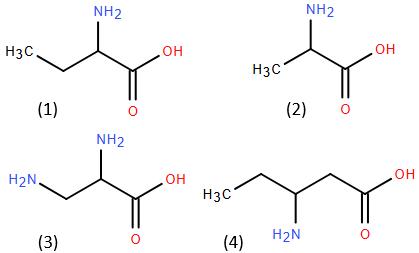
Trong số các chất trên, những hợp chất thuộc loại α-amino acid là
A. chất (1) và chất (2). B. chất (1) và chất (3).
C. chất (1), chất (2) và chất (3). D. chất (2), chất (3) và chất (4).
(Xem giải) Câu 3. Hợp chất sau thuộc loại polysaccharide là
A. peptide. B. protein. C. maltose. D. cellulose.
(Xem giải) Câu 4. Linoleic acid là một trong những acid béo có lợi cho sức khỏe tim mạch, ngăn ngừa các bệnh về tim, động mạch vành.

Phát biểu nào sau đây không đúng?
A. Trong phân tử linoleic acid có 2 liên kết π.
B. Công thức của chất béo trilinolein là (C17H31COO)3C3H5.
C. Linoleic acid thuộc loại omega-6.
D. Ở điều kiện thích hợp, 1 mol trilinolein tác dụng được tối đa với 6 mol H2.
(Xem giải) Câu 5. DHA (Docosahexaenoic acid) là một acid béo rất cần thiết cho sự phát triển trí não, thị giác của con người, giúp tăng khả năng miễn dịch và giảm nguy cơ phát triển dị ứng của trẻ. Oleic acid rất tốt cho việc hỗ trợ các vấn đề tim mạch, kiểm soát lượng đường nạp vào trong cơ thể, đồng thời cũng là chất chống oxy hóa hiệu quả. Cho cấu trúc của DHA và olecic aicd như hình sau:
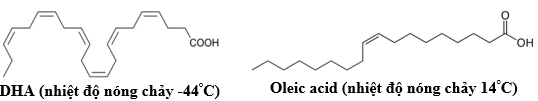
Chọn phát biểu đúng.
A. DHA có nhiệt độ nóng chảy thấp hơn oleic acid do có tương tác van der Waals yếu hơn.
B. DHA thuộc nhóm acid béo omega-3, oleic acid thuộc nhóm acid béo omega-6.
C. Phần trăm khối lượng nguyên tố carbon trong oleic acid là 80,49%.
D. Phân tử DHA có cấu hình trúc dạng trans, oleic acid có trúc dạng cis.
(Xem giải) Câu 6. Trong máu người trưởng thành, khỏe mạnh vào lúc đói (8 giờ sau ăn) có lượng đường huyết trong khoảng 4,4 – 7,2 mmol/L (theo quyết định số 5481/QĐ-BYT ngày 30 tháng 12 năm 2020 của Bộ Y tế). Cho các nhận định sau:
(a) Lượng đường huyết là lượng đường glucose trong máu.
(b) Kết quả xét nghiệm đường huyết của một người vào buổi sáng (chưa ăn) là 152 mg/dL (biết 1L = 10dL). Người đó có lượng đường huyết thấp hơn mức giới hạn bình thường.
(c) Lúc đói nếu ăn thực phẩm chứa tinh bột thì lượng đường huyết sẽ tăng trong một khoảng thời gian nhất định.
(d) Khi bị hạ đường huyết thì nên uống một cốc nước đường ấm.
Số nhận định đúng là
A. 2. B. 4. C. 3. D. 1.
(Xem giải) Câu 7. Khi điện phân NaCl nóng chảy (điện cực trơ), chất thu được ở cathode là
A. Cl2. B. HCl. C. NaOH D. Na.
(Xem giải) Câu 8. Polypropylene là polymer nhiệt dẻo, rất bền và có khả năng chịu lực tốt. Nó thường được sử dụng để làm hộp đựng thức ăn, chai lọ, và nhiều sản phẩm khác cần độ bền cao… Polypropylene được tổng hợp từ monomer nào sau đây?
A. CH3CH=CH2. B. CH2=CHCN.
C. CH2=CH2. D. CH2=CH(CH3)COOCH3.
(Xem giải) Câu 9. Ethanol sinh học là một loại nhiên liệu tái tạo thân thiện với môi trường, được sản xuất thông qua quá trình sinh học. Phương pháp nào sau đây dùng để sản xuất ethanol sinh học?
A. Lên men tinh bột.
B. Cho hỗn hợp khí ethylene và hơi nước đi qua tháp chứa H3PO4.
C. Thủy phân dẫn xuất C2H5Br trong môi trường kiềm.
D. Cộng nước vào ethylene với xúc tác là H2SO4.
(Xem giải) Câu 10. Pin Galvani Zn-Cu được biểu diễn ở hình sau
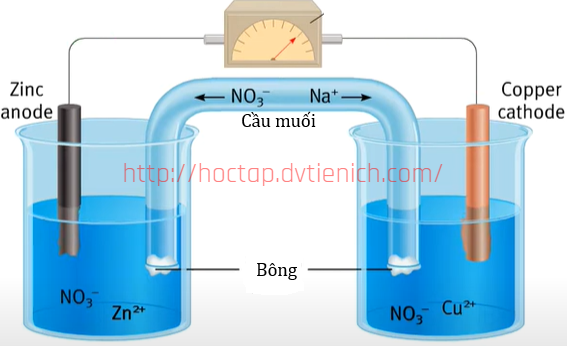
Cho các phát biểu sau:
a) Khi pin hoạt động, khối lượng thanh Zn giảm dần.
b) Điện cực âm xảy ra quá trình khử Zn, điện cực dương xảy ra quá trình oxi hóa ion Cu2+.
c) Electron chuyển từ thanh Zn qua dây dẫn đến thanh Cu. Cầu muối đóng vai trò khép kín mạch và trung hoà điện tích của dung dịch ở hai điện cực.
d) Biết thế điện cực chuẩn của cặp oxi hoá – khử Zn2+/Zn và Cu2+/Cu lần lượt là -0,76V, 0,340V. Sức điện động của pin Galvani Zn-Cu có giá trị bằng 1,10 (V).
Số phát biểu đúng là
A. 1. B. 4. C. 3. D. 2.
(Xem giải) Câu 11. Nhỏ dung dịch X vào dung dịch Y thu được kết tủa trắng. Kết tủa này hoàn toàn tan trong dung dịch HCl dư. Vậy X và Y có thể là
A. BaCl2 và H2SO4. B. Na2CO3 và HCl. C. AgNO3 và NaCl. D. CaCl2 và Na2CO3.
(Xem giải) Câu 12. Cho ba dung dịch có cùng nồng độ: hydrochloric acid (HCl), ethanoic acid (acetic acid, CH3COOH) và sodium hydroxide (NaOH). Khi chuẩn độ những thể tích như nhau của dung dịch HCl và dung dịch CH3COOH bằng dung dịch NaOH với chỉ thị phenolphtalein. Phát biểu nào sau đây đúng?
A. Giá trị pH của hai acid tăng như nhau cho đến khi đạt điểm tương đương.
B. Tại các điểm tương đương, dung dịch thu được khi chuẩn độ HCl có giá trị pH nhỏ hơn pH của dung dịch sau chuẩn độ CH3COOH.
C. Tại các điểm tương đương, dung dịch của cả hai phép chuẩn độ đều có giá trị pH bằng 7.
D. Trước khi chuẩn độ, pH của hai acid bằng nhau.
(Xem giải) Câu 13. Dung dịch glucose 5% có khối lượng riêng là 1,02 gam/mL. Khi oxy hóa 1 mol glucose tạo thành carbon dioxide và nước, quá trình tỏa ra nhiệt lượng là 2803,0 kJ. Một người bệnh được truyền một chai chứa 500 mL dung dịch glucose 5%. Năng lượng tối đa từ phản ứng oxy hóa hoàn toàn glucose mà bệnh nhân đó có thể nhận được là
A. 397,09 kJ. C. 416,02 kJ. B. 381,67 kJ. D. 389,30 kJ.
(Xem giải) Câu 14. Cho các phát biểu sau:
(a) Aldehyde bị khử bởi NaBH4, LiAlH4 tạo thành alcohol bậc I.
(b) Có thể phân biệt but-1-yne và but-2-yne bằng dung dịch AgNO3/NH3.
(c) Phân tử vinyl acetylene có 7 liên kết sigma (σ) và 3 liên kết pi (π)
(d) Acetylene được dùng trong đèn xì oxygen – acetylene để hàn cắt kim loại.
(e) Acetone, formaldehyde, acetaldehyde đều phản ứng với I2 trong môi trường kiềm tạo ra kết tủa màu vàng.
Số phát biểu đúng là
A. 5. B. 4. C. 3. D. 2.
(Xem giải) Câu 15. Cho các chất sau: C2H6 (1), C2H5OH (2), CH3COOH (3), CH3COOC2H5 (4). Trật tự tăng dần nhiệt độ sôi các chất (trái sang phải như sau):
A. (2), (1), (3), (4). B. (1), (4), (2), (3). C. (4), (1), (2), (3). D. (1), (2), (3), (4).
(Xem giải) Câu 16. Formaldehyde được sử dụng rộng rãi trong các ngành công nghiệp như dệt, nhựa, chất dẻo, xây dựng, mỹ phẩm, mực máy photocopy… Công thức phân tử của formaldehyde là
A. CH4O. B. CH2O. C. C2H6O. D. C2H4O.
(Xem giải) Câu 17. Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá – khử sau:
| Cặp oxi hoá – khử | Al3+/Al | Fe2+/Fe | Mg2+/Mg | Cu2+/Cu | Zn2+/Zn | Fe3+/Fe2+ |
| E°(V) | –1,676 | –0,440 | –2,356 | +0,340 | –0,763 | +0,771 |
Kim loại nào sau đây khi lấy dư chỉ khử được Fe3+ trong dung dịch FeCl3 thành Fe2+?
A. Al. B. Zn. C. Cu. D. Mg.
(Xem giải) Câu 18. Phân đạm là tên gọi chung của các loại phân bón vô cơ cung cấp nitrogen cho cây trồng, thúc đẩy quá trình tăng trưởng của cây, làm tăng năng suất cây trồng. Chất nào sau đây dùng làm phân đạm?
A. NaCl. B. Ca(H2PO4)2. C. (NH2)2CO. D. K2CO3.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Hòa tan hoàn toàn hai chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
• Thí nghiệm 1: Cho dung dịch NaOH dư vào V mL dung dịch Z, thu được a mol kết tủa.
• Thí nghiệm 2: Cho dung dịch NH3 dư vào V mL dung dịch Z, thu được b mol kết tủa.
• Thí nghiệm 3: Cho dung dịch AgNO3 dư vào V mL dung dịch Z, thu được c mol kim loại.
Biết các phản ứng xảy ra hoàn toàn và a < b và X, Y chỉ có thể là muối chloride của các kim loại sau: Fe, Cu, Al.
Cho các phát biểu sau:
a) Trong thí nghiệm 2, kết tủa thu được bao gồm Cu(OH)2 và Fe(OH)2.
b) Công thức của chất X, Y lần lượt là FeCl2 và AlCl3.
c) Kết tủa thu được trong thí nghiệm 3, ngoài Ag còn có AgCl.
d) Trong thí nghiệm 1, kết tủa thu được là Fe(OH)2 và Al(OH)3.
(Xem giải) Câu 20. Isopropyl myristate (IPM) là một ester thường được sử dụng trong kem dưỡng da, dầu tẩy trang và sản phẩm chăm sóc tóc như một chất làm mềm, chất kết dính và chất tăng hương thơm vì khả năng thẩm thấu tốt mà không gây nhờn rít. Ester này được tạo ra từ phản ứng giữa acid béo bão hòa myristic và isopropyl alcohol. Công thức khung phân tử của isopropyl myristate như sau:
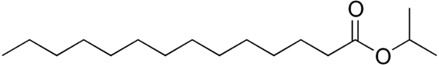
a) Một lọ kem dưỡng da có thể tích thực là 100 mL trong thành phần có chứa 3% isopropyl myristate theo khối lượng. Giả sử khối lượng riêng của kem dưỡng da đã cho là 0,85 g/mL. Lượng ester cần dùng để sản xuất 500 lọ kem trên là 1,275 kg.
b) Công thức phân tử của isopropyl myristate là C17H34O2.
c) Isopropyl myristate là một chất béo bão hòa.
d) Isopropyl myristate có phản ứng iodoform (tác dụng với I2/NaOH tạo kết tủa màu vàng).
(Xem giải) Câu 21. Đường nghịch chuyển (invert sugar) là hỗn hợp gồm các lượng như nhau (về khối lượng) của fructose và glucose, được tạo ra từ quá trình thuỷ phân saccharose. Trong đời sống, đường nghịch chuyển được điều chế ở dạng siro. Loại đường này được sử dụng rộng rãi trong sản xuất thực phẩm, đồ uống do có khả năng giữ nước cùng với có vị ngọt cao hơn từ 20% – 25% so với saccharose, mang lại hương vị mới, hữu ích cho sản phẩm.
a) Có thể dùng dung dịch AgNO3/NH3 (thuốc thử Tollens) để phân biệt glucose và fructose.
b) Phân tử saccharose gồm một đơn vị α-glucose và một đơn vị β-fructose liên kết với nhau bằng liên kết β-1,2-glycoside.
c) Khi tồn tại ở dạng mạch vòng, các carbohydrate có nhóm hemiacetal hoặc hemiketal trong phân tử được gọi là đường khử; ngược lại khi phân tử các chất này không có nhóm -OH hemiacetal hoặc hemiketal, chúng được gọi là đường không có tính khử. Maltose, saccharose, glucose, fructose đều thuộc loại đường khử.
d) Để sản xuất đường nghịch chuyển, người ta tiến hành đun sôi nhẹ dung dịch saccharose với xúc tác citric acid. Để thu được 10,5 tấn đường nghịch chuyển thì người ta phải sử dụng 10 tấn saccharose nếu quá trình nghịch chuyển saccharose xảy ra hoàn toàn. (Làm tròn kết quả đến hàng đơn vị).
(Xem giải) Câu 22. Bạc (silver) là tên của một nguyên tố kim loại có ký hiệu là Ag trong bảng tuần hoàn các nguyên tố hóa học. Đây là một kim loại chuyển tiếp có màu trắng, đặc tính mềm, dẻo và có độ dẫn điện, dẫn nhiệt cao nhất trong tất cả các nguyên tố kim loại đã được biết đến ngày nay.
a) Bạc có độ dẫn nhiệt cao nhất nên được sử dụng làm vật liệu chế tạo các bộ phận tản nhiệt trong ngành công nghiệp điện tử.
b) Trong không khí, bạc phản ứng với hợp chất chứa sulfur tạo thành hợp chất Ag2S là một chất rắn màu đen thường gây hiện tượng xỉn màu trên đồ trang sức bằng bạc.
c) Để mạ Ag lên hai mặt của một tấm kim loại bằng phương pháp điện phân, cần dùng thanh Ag (tinh khiết) làm anode và tấm kim loại cần mạ làm cathode.
d) Ion bạc có thể tạo phức với ammonia (NH3) trong dung dịch, hình thành phức chất [Ag(NH3)2]+. Phức chất này tham gia phản ứng tráng bạc.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Bột ngọt (monosodium glutamate – MSG) là loại gia vị được sử dụng rộng rãi để tăng hương vị cho món ăn. Bột ngọt hiện nay được sản xuất chủ yếu bằng phương pháp lên men vi sinh từ nguyên liệu là các hợp chất chứa tinh bột. Tiến hành các bước sau:
• Bước 1: Cho m tấn nguyên liệu (chứa 80% tinh bột) thủy phân bằng các enzyme để chuyển hóa thành glucose.
• Bước 2: Lên men glucose thành glutamic acid dưới tác dụng của vi khuẩn được kiểm soát chặt chẽ nhiệt độ, độ pH và các yếu tố khác để đảm bảo quá trình lên men diễn ra ổn định và hiệu quả. Sơ đồ lên men như sau (bỏ qua sản phẩm phụ)
C6H12O6 → HOOCCH(NH2)CH2CH2COOH
• Bước 3: Cho glutamic acid tác dụng với dung dịch NaOH, sau khi lọc bỏ tạp chất thu được dung dịch bão hòa MSG ở 60°C, làm nguội về 25°C thì khối lượng MSG kết tinh là 1,25 tấn.
Biết hiệu suất cả quá trình đạt 85%, độ tan trong nước của MSG ở 60°C là 112 gam/100 gam nước, ở 25°C là 74 gam/100 gam nước. Tính giá trị của m (làm tròn đến hàng phần mười).
(Xem giải) Câu 24. Thực hiện thí nghiệm điện phân dung dịch CuSO4 với điện cực graphite (than chì). Cho các nhận định sau:
(a) Tại cathode xảy ra sự khử Cu2+ trước, sau đó mới đến sự khử của nước.
(b) Tại anode chỉ xảy ra sự oxi hóa của nước tạo khí hydrogen.
(c) Sau điện phân, khối lượng cathode tăng lên.
(d) Theo thời gian điện phân, pH của dung dịch giảm dần.
(e) Nếu thay 2 điện cực graphite bằng 2 điện cực copper, trong quá trình điện phân khối lượng anode tăng dần, cathode giảm dần.
Có bao nhiêu nhận định đúng trong các nhận định trên?
(Xem giải) Câu 25. Trong quá trình sơ chế thủy sản, chlorine được thêm vào nước để tiêu diệt vi sinh vật. Nhưng lượng clorine cao làm tăng nguy cơ chuyển hóa thành chlorate trong sản phẩm tiềm ẩn nguy cơ cho sức khỏe người dùng. Vì vậy, công văn số 226/QLCL-CL1 (của Cục quản lý chất lượng nông lâm sản và thủy sản) về phối hợp kiểm soát thủy sản xuất khẩu cho thị trường châu Âu, chỉ tiêu dư lượng chlorine trong nước thải sau khi sơ chế thủy sản không vượt quá 1 mg/L. Phương pháp chuẩn độ iodine-thiosulfate được dùng để xác định dư lượng chlorine trong nước thải (theo QCVN 11-MT:2015/BTNMT):
– Khử hoàn toàn Cl2 trong mẫu theo phương trình: Cl2 + 2KI → 2KCl + I2.
– Lượng I2 sau đó được được nhận biết bằng hồ tinh bột, I2 bị khử bởi dung dịch chuẩn sodium thiosulfate theo phương trình: I2 + 2Na2S2O3 → 2NaI + Na2S4O6.
Dựa vào thể tích dung dịch Na2S2O3 đã phản ứng, tính được dư lượng chlorine trong dung dịch mẫu.
Tiến hành chuẩn độ 100 mL dung dịch một mẫu nước thải sau khi sơ chế thủy sản bằng dung dịch Na2S2O3 0,01M, thì thể tích Na2S2O3 đã dùng trong lần chuẩn độ lần lượt như sau
| Thí nghiệm | 1 | 2 | 3 |
| Thể tích Na2S2O3 đã dùng (mL) | 0,78 | 0,80 | 0,78 |
Tính hàm lượng chlorine (mg/L) trong mẫu nước thải trên. (Kết quả cuối cùng làm tròn đến hàng phần mười)
(Xem giải) Câu 26. Thực hiện các thí nghiệm hóa học được đánh số thứ tự từ 1 đến 4 như sau:
(1) Cho dung dịch glucose vào ống nghiệm chứa Cu(OH)2.
(2) Cho dung dịch aniline loãng vào ống nghiệm chứa 1 mL dung dịch bromine.
(3) Cho dung dịch hồ tinh bột vào ống nghiệm chứa dung dịch iodine.
(4) Cho vài giọt dung dịch HNO3 đặc vào ống nghiệm chứa 2 mL dung dịch lòng trắng trứng.
Gán số thứ tự thí nghiệm (ví dụ: 3124, 1234,…) theo hiện tượng quan sát được lần lượt như sau: xuất hiện kết tủa vàng, xuất hiện kết tủa trắng, xuất hiện dung dịch màu xanh tím, xuất hiện dung dịch màu xanh lam.
(Xem giải) Câu 27. Thuốc chữa ghẻ DEP (diethyl phtalate) được sản xuất từ nguồn nguyên liệu đầu là naphatalene và ethyl alcohol theo sơ đồ các quá trình chuyển hoá sau:
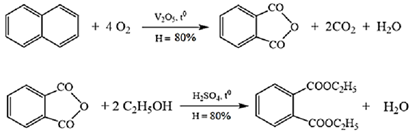
Một loại thuốc DEP trên thị trường có khối lượng dược phẩm là 10 gam, trong đó hàm lượng diethyl phtalate chiếm 95%. Tính số lọ thuốc loại này có thể sản xuất được từ 12 kg naphtalene và 7 kg ethyl alcohol. (Kết quả làm tròn đến hàng đơn vị)
(Xem giải) Câu 28. Picric acid (2,4,6 – trinitrophenol) trước đây được sử dụng làm thuốc nổ. Để tổng hợp picric acid, người ta cho 47 gam phenol phản ứng với hỗn hợp HNO3 đặc (dư)/H2SO4 đặc theo phản ứng hóa học sau:
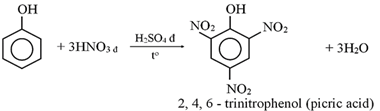
Khối lượng picric acid thu được bằng bao nhiêu gam? Biết hiệu suất phản ứng là 55%. (Kết quả làm tròn đến hàng đơn vị)


Bình luận