[2026] Thi thử TN cụm Cẩm Xuyên – Hà Tĩnh (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 060
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2C | 3C | 4C | 5A | 6D | 7A | 8B | 9A |
| 10D | 11B | 12B | 13B | 14C | 15B | 16A | 17B | 18D |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | |||||||
| (b) | 26 | 27 | 28 | ||||
| (c) | |||||||
| (d) |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Hợp chất vô cơ X có thể được sử dụng để điều trị chứng dư acid ở dạ dày, điều chỉnh vị chua của nước giải khát, làm tăng độ xốp của bánh, làm mềm thực phẩm. Chất X là
A. NaHCO3. B. NaCl. C. NaOH. D. Na2CO3.
(Xem giải) Câu 2. Ngâm hoa quả làm siro thuộc loại tách biệt và tinh chế nào?
A. Phương pháp kết tinh. B. Phương pháp chưng cất.
C. Phương pháp chiết. D. Sắc kí cột.
(Xem giải) Câu 3. Đun nóng dung dịch lòng trắng trứng, có hiện tượng
A. kết tủa màu vàng. B. tạo dung dịch màu xanh lam.
C. kết tủa màu trắng. D. tạo dung dịch màu tím.
(Xem giải) Câu 4. Phản ứng hóa học của ethylene với dung dịch Br2 được cho bởi phương trình:
CH2 = CH2 + Br2 → CH2Br – CH2Br
Cơ chế của phản ứng trên xảy ra như sau:
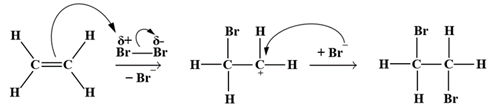
Phát biểu nào sai?
A. Hiện tượng của phản ứng là nước bromine bị mất màu.
B. Giai đoạn 1, liên kết đôi phản ứng với tác nhân Br2 tạo thành phần tử mang điện dương.
C. Phản ứng trên thuộc loại phản ứng thế.
D. Giai đoạn 2, phần tử mang điện dương kết hợp với anion Br⁻ tạo thành sản phẩm.
(Xem giải) Câu 5. Chất X là CH3COOC2H5. Tên của X là
A. ethyl acetate. B. methyl formate. C. isoamyl acetate. D. acetic acid.
(Xem giải) Câu 6. Phản ứng dùng để điều chế kim loại iron (Fe) trong công nghiệp là:
Fe2O3 + 3CO → 2Fe + 3CO2
Phương pháp tách kim loại đã được sử dụng trong quá trình trên là
A. phương pháp thủy luyện. B. phương pháp điện phân nóng chảy.
C. phương pháp điện phân dung dịch. D. phương pháp nhiệt luyện.
(Xem giải) Câu 7. Hợp chất nào sau đây là amine?
A. CH3NHCH2CH3. B. H2NCH2COOCH3. C. H2NCH2COOH. D. HOCH2COOH.
(Xem giải) Câu 8. Kim loại tungsten (W) được sử dụng làm dây tóc bóng điện. Ứng dụng này được dựa trên tính chất vật lí nào sau đây của tungsten?
A. Tính dẫn nhiệt. B. Nhiệt độ nóng chảy. C. Tính cứng. D. Tính dẻo.
(Xem giải) Câu 9. Phát biểu nào sai?
A. Bồ kết là một loại chất giặt rửa tổng hợp.
B. Các chất CH3[CH2]10CH2C6H4SO3Na và CH3[CH2]10CH2OSO3Na là chất giặt rửa tổng hợp.
C. Xà phòng bị giảm hoặc mất tác dụng giặt rửa khi dùng với nước cứng vì tạo kết tủa với cation Ca2+, Mg2+.
D. Xà phòng dễ bị các vi sinh vật phân huỷ nên thân thiện với môi trường.
(Xem giải) Câu 10. Cho các dung dịch: (1) mật ong, (2) nước mía, (3) nước ép quả nho chín, (4) nước ép củ cải đường, (5) rượu gạo. Số dung dịch có khả năng hòa tan Cu(OH)2 là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 11. Nguồn điện nào sau đây không dựa vào năng lượng từ các phản ứng hoá học?
A. Acquy. B. Pin mặt trời. C. Pin nhiên liệu. D. Pin Galvani.
(Xem giải) Câu 12. Hợp chất A là một α-amino acid, có phân tử khối 89u. A có tên gọi là
A. Valine. B. Alanine. C. Glycine. D. Aniline.
(Xem giải) Câu 13. Cho biết:
| Cặp oxi hoá – khử | Cu2+/Cu | Ag+/Ag | Fe2+/Fe | Ni2+/Ni |
| Thế điện cực chuẩn, V | +0,340 | +0,799 | -0,44 | -0,257 |
Trong các kim loại Cu, Ag, Fe và Ni. Số kim loại khử được ion H+ trong dung dịch ở điều kiện chuẩn là
A. 4. B. 2. C. 3. D. 1.
(Xem giải) Câu 14. Bơ thực vật (margarine) là loại được điều chế từ dầu thực vật. Để chuyển hoá dầu thực vật thành bơ thực vật người ta thực hiện phản ứng …(1)… nhằm chuyển chất béo không no thành chất béo no. Nội dung phù hợp với chỗ trống (1) là
A. hydrate hóa. B. oxi hóa. C. hydrogen hóa. D. xà phòng hóa.
(Xem giải) Câu 15. LDPE là một chất dẻo dễ tạo màng, có tính dai bền nên được sử dụng làm túi nylon, màng bọc, bao gói thực phẩm. LDPE thuộc nhóm nhựa PE (polyethylene). LDPE được tổng hợp từ monomer nào đây?
A. CH2=CH–Cl. B. CH2=CH2. C. CH2=CH–CH3. D. CH2=CH–C6H5.
(Xem giải) Câu 16. Phát biểu nào sau đây sai?
A. Saccharose tham gia phản ứng tráng bạc.
B. Maltose là disaccharide.
C. Fructose có nhiều trong mật ong và có vị ngọt đậm.
D. Phân tử cellulose gồm nhiều gốc β-glucose liên kết với nhau tạo thành chuỗi không có nhánh.
(Xem giải) Câu 17. Phát biểu nào sai?
A. Sự đóng cặn calcium carbonate trong bình nóng lạnh gây lãng phí điện năng.
B. Đun sôi nước có thể làm mềm nước cứng toàn phần.
C. Nước chứa nhiều Ca(HCO3)2 là nước cứng tạm thời.
D. Có thể sử dụng Na2CO3, Na3PO4 để làm mềm nước cứng vĩnh cửu.
(Xem giải) Câu 18. Khi xảy ra cháy xăng dầu, tuyệt đối không được dùng nước để dập lửa vì có thể khiến lửa lan rộng hơn. Thay vào đó, cần sử dụng bọt chữa cháy hoặc cát khô để dập tắt đám cháy. Cho các phát biểu sau:
(a) Xăng dầu nhẹ hơn nước nên sẽ nổi lên trên và tiếp tục cháy nếu dùng nước để dập lửa.
(b) Bọt chữa cháy có tác dụng cách ly nhiên liệu với không khí, giúp dập lửa hiệu quả.
(c) Khi cháy, xăng dầu có thể tạo ra các khí độc như CO, NO2, SO2.
(d) Có thể dùng chăn bông ướt dập tắt đám cháy xăng dầu nhỏ.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 1. Trong quá trình lên men glucose thành ethanol, nấm men là chất xúc tác giúp chuyển hóa glucose thành ethanol và khí CO2 trong điều kiện yếm khí (không có oxygen), quá trình lên men tỏa nhiệt. Từ 300 gam glucose, thực hiện quá trình lên men rượu trong phòng thí nghiệm, kết quả biểu diễn theo đồ thị sau:
Kết quả nghiên cứu nhận thấy:
– Tốc độ phản ứng tăng lên và dung dịch trở nên đặc và nhiệt độ dung dịch tăng dần.
– Sau ngày thứ 10, phản ứng hầu như dừng lại mặc dù trong dung dịch vẫn còn glucose chưa bị chuyển hóa hết.
a) Ngoài ethanol (C2H5OH), trong quá trình lên men, có thể sinh ra các sản phẩm phụ như acetaldehyde (CH3CHO), acetic acid (CH3COOH) hoặc ethyl acetate (CH3COOC2H5) tùy theo điều kiện của quá trình lên men.
b) Từ 300 gam glucose, sau 12 ngày thực hiện quá trình lên men rượu trong phòng thí nghiệm thì thu được 2 mol ethyl alcohol.
c) Hiệu suất của quá trình lên men tại ngày thứ 10 là 85%. (Làm tròn đến hàng đơn vị)
d) Trong quá trình trên, men rượu có tác dụng làm tăng hiệu suất phản ứng tạo ethanol.
(Xem giải) Câu 2. Bộ dụng cụ dưới đây được sử dụng để điện phân nước với chất điện li được sử dụng là H2SO4.
a) Nếu ống Q thu được 50 mL khí thì ống P sẽ thu được 100 mL khí (trong cùng điều kiện nhiệt độ, áp suất).
b) Điện cực R xảy ra quá trình khử ion H+.
c) Thay dung dịch H2SO4 bằng dung dịch HCl thì khí thu được ở hai điện cực là không đổi.
d) Ở ống Q thu được khí H2.
(Xem giải) Câu 3. Trong công nghiệp, sodium hydrogencarbonate (baking soda) và sodium carbonate (soda) được sản xuất bằng phương pháp Solvay từ nguyên liệu chính là đá vôi, muối ăn, ammonia và nước theo sơ đồ sau:
a) NH4Cl được nhiệt phân để thu hồi NH3 đưa trở lại quá trình sản xuất.
b) CO2 cung cấp cho quá trình Solvay được lấy từ nhiệt phân đá vôi.
c) Độ tan của NaHCO3 ở 20 °C và 40 °C lần lượt là 9,6 g/100 g nước và 12,7 g/100 g nước.
Khi giảm nhiệt độ của 450,8 gam dung dịch NaHCO3 bão hòa từ 40 °C về 20 °C thì khối lượng muối NaHCO3 kết tinh là 12,4 gam. (Làm tròn đến hàng phần mười)
d) Quy trình sản xuất theo sơ đồ trên không gây tiêu tốn NH3 và CO2 (bỏ qua sự thất thoát ra môi trường).
(Xem giải) Câu 4. Tơ capron là loại tơ có tính dai, độ đàn hồi và độ bóng cao, ít thấm nước và được sử dụng để dệt vải may mặc, chỉ khâu. Tơ capron được tổng hợp từ caprolactam theo phương trình hóa học sau:
a) Do tơ capron có các nhóm –CO–NH– nên tơ capron là polypeptide.
b) Khi đun nóng tơ capron trong môi trường kiềm xảy ra phản ứng cắt mạch polymer.
c) Phản ứng (1) là phản ứng trùng hợp.
d) Một loại chỉ khâu có chứa 95% về khối lượng là tơ capron. Để sản xuất được 100 cuộn chỉ khâu cùng loại, mỗi cuộn chỉ có khối lượng 500 gam (chỉ gồm chỉ khâu) thì cần 47,5 kg caprolactam với hiệu suất toàn bộ quá trình là 90%. (Làm tròn đến hàng phần mười)
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 1. Một nhà máy chuyên sản xuất thép (chứa 1%C theo khối lượng) với công nghệ lò luyện thép Martin. Sơ đồ phản ứng trong lò là:
FexOy + C → Fe + CO2
Nguyên liệu nhà máy trên sử dụng để luyện thép gồm sắt phế liệu (chứa 50%Fe3O4; 49%Fe; 1%C theo khối lượng) và gang (chứa 4% khối lượng C còn lại là Fe). Một mẻ luyện thép cần 5 tấn gang và m tấn sắt phế liệu (hiệu suất của quá trình là 100%). Tính giá trị m. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị)
(Xem giải) Câu 2. Cho các chất: methylamine, glycine, aniline, acetic acid, glutamic acid. Có bao nhiêu chất phản ứng với dung dịch HCl tạo muối?
(Xem giải) Câu 3. Khi thực hiện phản ứng ester hóa 1 mol CH3COOH và 1 mol C2H5OH, lượng ester lớn nhất thu được là 2/3 mol. Để đạt hiệu suất cực đại là 90% (tính theo acid). Khi tiến hành ester hóa 1 mol CH3COOH cần số mol C2H5OH là bao nhiêu? (biết các phản ứng ester thực hiện ở cùng nhiệt độ). (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
(Xem giải) Câu 4. Cho dãy các kim loại: Mg, Zn, Fe, Na, K, Ca. Có bao nhiêu kim loại trong dãy tác dụng được với nước ở nhiệt độ thường tạo dung dịch base mạnh?
(Xem giải) Câu 5. Cho các phát biểu sau:
(1) Aniline là amine bậc 1.
(2) Hợp chất (CH3)2NH có tên thay thế là dimethylamine.
(3) Nhúng giấy quỳ tím vào dung dịch methylamine thấy quỳ tím chuyển màu xanh.
(4) Ethylamine tan tốt trong nước do phân tử tạo được liên kết hydrogen với nước.
(5) Dung dịch methylamine có thể hòa tan được Cu(OH)2 tạo dung dịch màu tím đặc trưng.
(6) Trong phản ứng methylamine với HNO2 thì methylamine thể hiện tính base.
Sắp xếp các phát biểu đúng theo thứ tự tăng dần (ví dụ: 123, 1235…).
(Xem giải) Câu 6. Sản phẩm của quá trình nung vôi có nhiều ứng dụng trong thực tế, CaO sinh ra được sử dụng trong công nghiệp luyện kim và làm nguyên liệu cho công nghiệp hóa học, được dùng để khử chua đất trồng trọt, xử lí nước thải công nghiệp, khử độc môi trường. Còn CO2 được dùng sản xuất CO2 lỏng phục vụ cho nhu cầu công nghiệp và dân sinh. Quá trình nung vôi xảy ra theo phương trình hóa học (1) như sau:
CaCO3(s) → CaO(s) + CO2(g) (1)
Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí thiên nhiên hóa lỏng (96% methane, 4% ethane về thể tích) theo phương trình hóa học (2) và (3):
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) (2)
C2H6(g) + 3,5O2(g) → 2CO2(g) + 3H2O(g) (3)
Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của CaCO3 là 100%. Khối lượng khí thiên nhiên hóa lỏng m tấn cần thiết để sản xuất 560 tấn CaO(s) (trong giai đoạn trên). Biết 92% tổng lượng nhiệt tỏa ra từ phản ứng (2), (3) được cung cấp cho phản ứng (1) (các giá trị nhiệt tạo thành của các chất, năng lượng liên kết trung bình của một số liên kết hóa học ở điều kiện chuẩn được cho trong bảng sau).
| Chất | CaCO3(s) | CaO(s) | CO2(g) |
| -1207,6 | -634,9 | -393,5 |
Năng lượng liên kết trung bình của một số liên kết hóa học ở điều kiện chuẩn:
| Liên kết | C–H | C–C | O=O | C=O (CO2) | O–H |
| Eb (kJ/mol) | 414 | 347 | 498 | 799 | 464 |
Giá trị của m (theo tấn) là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).


Bình luận