[2026] Thi thử TN cụm trường Hải Phòng (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 022
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2C | 3A | 4A | 5A | 6A | 7D | 8A | 9D |
| 10C | 11B | 12A | 13C | 14B | 15A | 16A | 17D | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | S | S | Đ | 39 | 1,46 | 3 |
| (b) | Đ | Đ | S | S | 26 | 27 | 28 |
| (c) | S | Đ | Đ | Đ | 1342 | 3 | 3 |
| (d) | S | Đ | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Ester X được tạo bởi methyl alcohol và acetic acid. Công thức của X là
A. CH3COOC2H5. B. HCOOCH3. C. CH3COOCH3. D. HCOOC2H5.
(Xem giải) Câu 2. Tên thay thế của alcohol có công thức cấu tạo (CH3)2CH-CHOH-CH3 là
A. 2-methylbutan-3-ol. B. 2-methylbutan-2-ol.
C. 3-methylbutan-2-ol. D. isobutan-2-ol.
(Xem giải) Câu 3. Trên hộp xốp cách nhiệt, hộp đựng thức ăn mang về, cốc, chén đĩa dùng một lần… thường được in kí hiệu như hình bên. Ở nhiệt độ khoảng trên 80°C, loại vật liệu này trở nên mềm, dính. Do vậy, tránh hâm nóng thực phẩm chứa trong các loại hộp này.

Polymer dùng làm các đồ dùng đó được tổng hợp từ monomer nào sau đây?
A. C6H5CH=CH2. B. CH2=CHCl. C. CH2=CHCH3. D. CH2=CH2.
(Xem giải) Câu 4. Dung dịch chất nào sau đây có tính base?
A. CH3NH2. B. CH3CHO. C. C6H5OH D. CH3COOH.
(Xem giải) Câu 5. Cho phản ứng: Ag+(aq) + Fe2+(aq) → Ag(s) + Fe3+(aq). Cặp oxi hoá – khử của iron (sắt) trong phản ứng trên là
A. Fe3+/Fe2+. B. Fe2+/ Fe3+. C. Fe3+/Fe. D. Fe2+/Fe.
(Xem giải) Câu 6. Trong nước, thế điện cực chuẩn của kim loại Mn+/M càng nhỏ thì dạng khử có tính khử …(I)… và dạng oxi hoá có tính oxi hoá …(II)… Các cụm từ cần điền vào (I) và (II) lần lượt là
A. càng mạnh và càng yếu. B. càng yếu và càng mạnh.
C. càng mạnh và càng mạnh. D. càng yếu và càng yếu.
(Xem giải) Câu 7. Dãy chất nào sau đây chỉ chứa các hợp chất hữu cơ?
A. NH4HCO3, CH3OH, CH4, CCl4. B. CO2, K2CO3, NaHCO3, C2H5Cl.
C. (NH4)2CO3, CO2, CH4, C2H6. D. C2H4, CH4, C2H6O, C3H9N.
(Xem giải) Câu 8. Công thức của oleic acid là
A. C17H33COOH. B. CH3COOH. C. HCOOH. D. C2H5COOH.
(Xem giải) Câu 9. Cho biết: E°Mg2+/Mg = -2,356V; E°Ag+/Ag = +0,799V. Phát biểu nào sau đây là đúng?
A. Tính oxi hoá của cation Mg2+ mạnh hơn tính oxi hoá của cation Ag+.
B. Tính oxi hoá của magnesium (Mg) mạnh hơn tính oxi hoá của silver (Ag).
C. Tính khử của cation Mg2+ mạnh hơn tính khử của cation Ag+.
D. Tính khử của magnesium (Mg) mạnh hơn tính khử của silver (Ag).
(Xem giải) Câu 10. Cho các cấu hình electron sau, hình vẽ nào sau đây biểu diễn đúng cấu hình electron của N (Z = 7) theo các ô orbital?
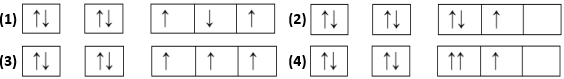
A. (1). B. (2). C. (3). D. (4).
(Xem giải) Câu 11. Glutamic acid có các dạng tồn tại và giá trị pH mà dạng tồn tại đó là chủ yếu (≈ 100%) sau:
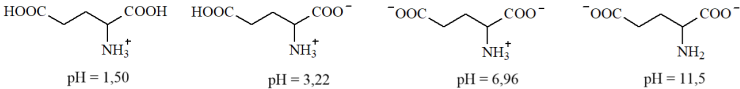
Giá trị pH của dung dịch bằng bao nhiêu thì glutamic acid hầu như không di chuyển trong điện trường?
A. 6,96. B. 3,22. C. 11,5. D. 1,50.
(Xem giải) Câu 12. Dãy nào dưới đây chỉ gồm chất điện li mạnh?
A. HNO3, KOH. B. CH3COOH, NaCl. C. HCl, Mg(OH)2. D. NaOH, H3PO4.
(Xem giải) Câu 13. Cho cơ chế phản ứng của propene với H2O như sau:
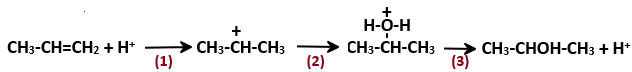
Phát biểu nào sau đây sai?
A. Nếu thay H2O bằng HBr thì cơ chế phản ứng xảy ra tương tự.
B. Giai đoạn (1) là quá trình proton hóa liên kết đôi C=C của propene tạo thành carbocation.
C. Giai đoạn (2) xảy ra quá trình tách proton để tạo thành alcohol.
D. Sản phẩm của phản ứng là sản phẩm chính theo quy tắc Markovnikov.
(Xem giải) Câu 14. Chất hữu cơ X có công thức cấu tạo như sau:
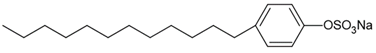
X có trong thành phần chính của
A. chất béo. B. chất giặt rửa tổng hợp.
C. xà phòng. D. ester.
(Xem giải) Câu 15. Đồ thị hình bên mô tả sự phụ thuộc giá trị nhiệt độ sôi vào số nguyên tử carbon của bốn loại hợp chất alkane, alcohol, aldehyde và carboxylic acid.
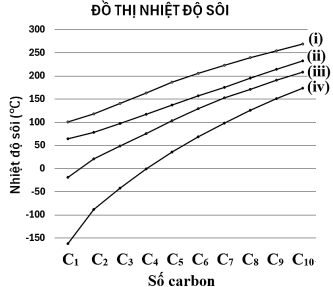
Đồ thị (i), (ii), (iii), (iv) lần lượt tương ứng với các loại hợp chất là:
A. Carboxylic acid, alcohol, aldehyde, alkane.
B. Alkane, alcohol, aldehyde, carboxylic acid.
C. Alcohol, carboxylic acid, aldehyde, alkane.
D. Carboxylic acid, aldehyde, alcohol, alkane.
(Xem giải) Câu 16. Glucose là một trong hai dạng monosaccharide phổ biến và có nhiều ứng dụng trong đời sống. Glucose có một dạng mạch hở và hai dạng mạch vòng (α và β) chuyển hóa qua lại lẫn nhau theo sơ đồ sau:
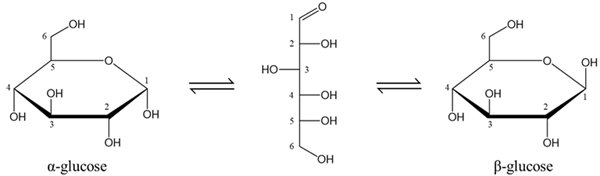
Ở dạng mạch vòng, nhóm -OH hemiacetal của glucose ở vị trí C số
A. 1. B. 6. C. 2. D. 5.
(Xem giải) Câu 17. Saccharose có phản ứng với chất nào sau đây?
A. Nước bromine. B. Cu(OH)2/NaOH tạo kết tủa đỏ gạch.
C. Thuốc thử Tollens. D. Nước (xúc tác acid, đun nóng).
(Xem giải) Câu 18. Trong các thí nghiệm sau, nếu lượng kim loại Fe được lấy bằng nhau và có kích thước như nhau thì thí nghiệm nào có tốc độ phản ứng lớn nhất?
A. Fe + dung dịch HCl 0,3M. B. Fe + dung dịch HCl 0,2M.
C. Fe + dung dịch HCl 0,5M. D. Fe + dung dịch HCl 0,1M.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Cho các phản ứng tổng hợp các polymer sau:
nCH2=CH2 (xt, t°, p) → (-CH2-CH2-)n (X)
nCH2=CHCH3 (xt, t°, p) → [-CH2-CH(CH3)-]n (Y)
nH2N(CH2)5COOH (t°) → [-NH(CH2)5CO-]n (Z) + nH2O
a) Polymer X được sử dụng rất phổ biến để tạo ra nhiều sản phẩm gia dụng như túi đựng, màng bọc, chai lọ, ống nhựa, vỏ dây điện, đồ chơi trẻ em, bình chứa.
b) Polymer X, Y thuộc loại polymer nhiệt dẻo và có thể tái chế được.
c) Polymer Z có các nhóm -CO-NH- bền với dung dịch kiềm mạnh nên dùng để sản xuất tơ tổng hợp.
d) Các phản ứng tổng hợp ra polymer X, Y, Z ở trên đều là phản ứng trùng hợp.
(Xem giải) Câu 20. Methyl cinnmate là một ester có công thức phân tử C10H10O2 và có mùi thơm của dâu tây (strawberry) được sử dụng trong ngành công nghiệp hương liệu và nước hoa. Công thức cấu tạo của methyl cinnmate được cho ở hình dưới:
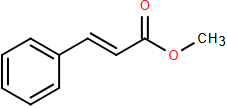
a) Khi đun nóng, methyl cinnmate phản ứng hoàn toàn với dung dịch NaOH với tỉ lệ mol tương ứng 1 : 2.
b) Phân tử khối của methyl cinnmate là 162.
c) Methyl cinnmate có đồng phân hình học.
d) Để điều chế 16,2 gam ester methyl cinnmate người ta cho 29,6 gam cinnamic acid phản ứng với lượng dư methyl alcohol (CH3OH) thì hiệu suất phản ứng ester hóa là 50%.
(Xem giải) Câu 21. Bột đá vôi (CaCO3) có thể được dùng để xử lí khí thải chứa sulfur dioxide (SO2) từ các nhà máy điện đốt than và dầu mỏ. Phương trình của phản ứng là
CaCO3(s) + SO2(g) → CaSO3(s) + CO2(g) (1)
Calcium sulfite (CaSO3) thu được thường được chuyển hoá thành thạch cao theo phản ứng:
2CaSO3 + O2 + 4H2O → 2CaSO4.2H2O (2)
a) Nếu trong khí thải có 49,59 lít SO2 (đkc), hiệu suất phản ứng (1) và (2) đều đạt 82% thì khối lượng CaSO4.2H2O thu được là 282,08 gam.
b) Phản ứng sử dụng CaCO3 ở dạng bột để phản ứng xảy ra thuận lợi hơn về năng lượng.
c) Phản ứng (2) là phản ứng oxi hóa – khử.
d) Sulfur dioxide (SO2) là một trong các tác nhân làm ô nhiễm khí quyển, gây mưa acid và viêm đường hô hấp ở người,…
(Xem giải) Câu 22. Salbutamol là hoạt chất sử dụng để sản xuất thuốc điều trị bệnh cho người (làm giãn phế quản, giãn cơn co tử cung,…), tuy nhiên chỉ được sử dụng khi có chỉ định của bác sĩ. Trong chăn nuôi, Salbutamol thúc cho gia súc, gia cầm lớn nhanh hơn, tỉ lệ nạc cao hơn, màu sắc thịt đỏ hơn. Nếu con người ăn phải thịt gia súc, gia cầm được nuôi có sử dụng Salbutamol một thời gian dài thì sẽ làm cho tim đập nhanh, tăng huyết áp, run cơ, rối loạn tiêu hóa. Thậm chí, theo một số chuyên gia, đây là một trong những hoạt chất có khả năng gây ung thư nếu bị tích lũy nhiều trong cơ thể. Salbutamol có công thức cấu tạo thu gọn nhất như sau:
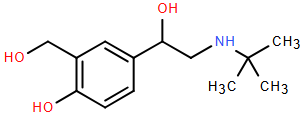
a) Trong y học, salbutamol được dùng để sản xuất thuốc làm giãn phế quản giúp người bệnh dễ thở hơn.
b) Trong dung dịch nước, a mol salbutamol có thể phản ứng tối đa với 3a mol NaOH.
c) Salbutamol tác dụng được với dung dịch nước bromine.
d) Salbutamol là hợp chất hữu cơ tạp chức, chứa đồng thời: 2 nhóm chức phenol, 1 nhóm chức alcohol và 1 nhóm chức amine bậc hai.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Sản phẩm của quá trình nung vôi có nhiều ứng dụng trong thực tế, CaO sinh ra được sử dụng trong công nghiệp luyện kim và làm nguyên liệu cho công nghiệp hoá học, được dùng để khử chua đất trồng trọt, xử lí nước thải công nghiệp, khử độc môi trường. Còn CO2 được dùng sản xuất CO2 lỏng phục vụ cho nhu cầu công nghiệp và dân sinh. Quá trình nung vôi xảy ra theo phương trình hóa học (1) như sau:
CaCO3(s) (t°) → CaO(s) + CO2(g) (1)
Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí thiên nhiên hóa lỏng (chứa 96% methane, 4% ethane về thể tích) theo phương trình hóa học (2) và (3):
CH4(g) + 2O2(g) (t°) → CO2(g) + 2H2O(g) (2)
C2H6(g) + 3,5O2(g) (t°) → 2CO2(g) + 3H2O(g) (3)
Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của CaCO3 là 100%. Khối lượng khí thiên nhiên hóa lỏng là m tấn cần thiết để sản xuất 560 tấn CaO(s) trong giai đoạn trên. Biết 92% tổng lượng nhiệt tỏa ra từ phản ứng (2), (3) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành của các chất, năng lượng liên kết trung bình của một số liên kết hóa học ở điều kiện chuẩn được cho trong bảng sau:
Nhiệt tạo thành chuẩn của các chất:
| Chất | CaCO3(s) | CaO(s) | CO2(g) |
| -1207,6 | -634,9 | -393,5 |
Năng lượng liên kết trung bình của một số liên kết hóa học ở điều kiện chuẩn:
| Liên kết | C–H | C–C | O=O | C=O (CO2) | O–H |
| Eb (kJ/mol) | 414 | 347 | 498 | 799 | 464 |
Giá trị của m (theo tấn) là bao nhiêu (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
(Xem giải) Câu 24. Xăng E5 là một loại xăng sinh học, được tạo thành khi trộn 5 thể tích C2H5OH (D = 0,8 g/ml) với 95 thể tích xăng truyền thống, giúp thay thế một phần nhiên liệu hóa thạch đang ngày càng cạn kiệt cũng như giảm thiểu ô nhiễm môi trường. Khi đốt cháy hoàn toàn 1 lít xăng E5 thì hạn chế được a phần trăm thể tích khí CO2 thải vào không khí so với đốt cháy hoàn toàn 1 lít xăng truyền thống ở cùng điều kiện nhiệt độ và áp suất. Giả sử xăng truyền thống chỉ chứa hai ankan C8H18 và C9H20 (tỉ lệ mol tương ứng 4 : 3, D = 0,7 g/ml). Giá trị của a là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
(Xem giải) Câu 25. Cho các chất sau: Glycerol (1), glucose (2), tinh bột (3), fructose (4). Có bao nhiêu chất tác dụng được với Cu(OH)2 trong môi trường kiềm ở điều kiện thường?
(Xem giải) Câu 26. Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4 dưới đây:
(1) CH3CHO + 2[Ag(NH3)2]OH (t°) → CH3COONH4 + 2Ag + 3NH3 + H2O
(2) CH3CHO + 3I2 + 4NaOH → CHI3 + HCOONa + 3NaI + 3H2O
(3) CH3COOH + NaOH → CH3COONa + H2O
(4) CH3COOH + C2H5OH (H2SO4 đặc, t°) ⇋ CH3COOC2H5 + H2O
Gán số thứ tự phương trình hoá học của các phản ứng lần lượt theo tên gọi: Phản ứng với thuốc thử Tollens, phản ứng trung hòa acid – base, phản ứng ester hóa, phản ứng tạo iodoform và sắp xếp theo trình tự thành dãy bốn số. (ví dụ: 1234, 4321,…).
(Xem giải) Câu 27. Cho các loại tơ sau: Tơ capron, tơ cellulose acetate, tơ tằm, tơ nitron, nylon-6,6. Có bao nhiêu tơ tổng hợp trong các loại tơ trên?
(Xem giải) Câu 28. Tiến hành thí nghiệm phản ứng màu biuret của protein theo các bước sau đây:
• Bước 1: Cho khoảng 1 mL dung dịch NaOH 30% vào ống nghiệm. Nhỏ thêm 2 – 3 giọt dung dịch CuSO4 2%, lắc đều.
• Bước 2: Cho khoảng 4 mL dung dịch lòng trắng trứng vào ống nghiệm, lắc đều.
Cho các phát biểu sau:
(1) Sau bước 1, xuất hiện kết tủa màu xanh.
(2) Sau bước 2, kết tủa màu xanh tan dần tạo thành dung dịch có màu tím đặc trưng.
(3) Nếu thay dung dịch CuSO4 bằng dung dịch FeSO4 thì hiện tượng không đổi sau khi kết thúc thí nghiệm.
(4) Phản trên có thể dùng để phân biệt lòng trắng trứng với Gly-Ala.
Số phát biểu đúng là bao nhiêu?


Bình luận