[2026] Thi thử TN sở GDĐT Cao Bằng (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 084
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2C | 3A | 4C | 5A | 6B | 7C | 8B | 9A |
| 10D | 11C | 12B | 13B | 14D | 15D | 16A | 17B | 18B |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | S | S | S |
| (b) | S | Đ | Đ | S |
| (c) | Đ | Đ | Đ | Đ |
| (d) | S | S | Đ | Đ |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 124 | 15,5 | 3 | 47,5 | 20 | 4 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Trong pin Galvani Cu-Ag, ở anode xảy ra quá trình
A. oxi hóa Cu. B. khử Cu2+. C. khử Ag+. D. oxi hóa Ag.
(Xem giải) Câu 2: Cho phát biểu sau: “Hầu hết các phức chất aqua của ion kim loại chuyển tiếp thứ nhất đều …(1)…, chúng thường có dạng hình học …(2)…”. Cụm từ cần điền vào (1) và (2) lần lượt là
A. không màu, tứ diện [M(OH2)4]n+. B. có màu, vuông phẳng [M(OH2)4]n+.
C. có màu, bát diện [M(OH2)6]n+. D. không màu, bát diện [M(OH2)6]n+.
(Xem giải) Câu 3: Điện phân là một ứng dụng quan trọng của dòng điện trong việc biến đổi điện năng và hóa năng. Điện phân dung dịch NaCl có màng ngăn là phương pháp chủ đạo để sản xuất các hóa chất cơ bản như NaOH và chlorine (Cl2). Cho các phát biểu sau về quá trình điện phân dung dịch NaCl có màng ngăn, sử dụng các điện cực trơ:
(a) Tại cực dương (anode), xảy ra quá trình khử ion chloride thành khí chlorine.
(b) Tại cực âm (cathode), xảy ra quá trình oxi hóa nước tạo thành khí hydrogen và ion OH-.
(c) Dung dịch thu được trong quá trình điện phân có khả năng làm quỳ tím chuyển sang màu đỏ.
(d) Màng ngăn xốp có tác dụng ngăn không cho khí Cl2 tiếp xúc và phản ứng với dung dịch NaOH.
Số phát biểu đúng là
A. 1. B. 4. C. 3. D. 2.
(Xem giải) Câu 4: Trong công nghiệp, phương pháp điện phân nóng chảy được sử dụng để sản xuất một lượng đáng kể kim loại nào sau đây?
A. Ag. B. Fe. C. Al. D. Cu.
(Xem giải) Câu 5: Aniline là nguyên liệu tổng hợp một số hợp chất quan trọng trong các lĩnh vực khác nhau như công nghiệp phẩm nhuộm, dược phẩm,… Aniline có công thức là
A. C6H5NH2. B. CH3NHCH3. C. CH3NH2. D. C6H5OH.
(Xem giải) Câu 6: Acetic acid được điều chế bằng phương pháp lên men giấm từ dung dịch chất nào sau đây?
A. CH3CHO. B. C2H5OH. C. CH3OH. D. HCOOH.
(Xem giải) Câu 7: Kim loại nào sau đây là kim loại chuyển tiếp dãy thứ nhất?
A. Na. B. K. C. Sc. D. Ba.
(Xem giải) Câu 8: Cơ chế của phản ứng cộng bromine vào liên kết đôi của ethene gồm hai giai đoạn như sau:
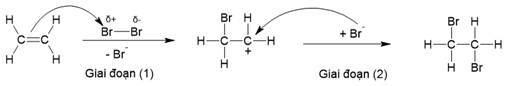
Phát biểu nào sau đây không đúng?
A. Ethene làm mất màu nước bromine.
B. Số liên kết σ (xích ma) trong một phân tử ethene là 4.
C. Giai đoạn (1) có sự phân cắt liên kết π.
D. Giai đoạn (2) có sự hình thành liên kết σ (xích ma).
(Xem giải) Câu 9: Đun nóng ethyl formate với dung dịch NaOH thu được sodium formate và alcohol X. Công thức của X là
A. C2H5OH. B. CH3COONa. C. CH3OH. D. HCOONa.
(Xem giải) Câu 10: Phát biểu nào sau đây là sai?
A. Amino acid là những hợp chất hữu cơ tạp chức.
B. Dung dịch glycine không làm đổi màu quỳ tím.
C. Dung dịch lysine làm xanh quỳ tím.
D. Ở điều kiện thường, các amino acid là những chất lỏng, dễ tan trong nước.
(Xem giải) Câu 11: Phản ứng oxi hóa không hoàn toàn ethanol bằng CuO (đun nóng) tạo ra sản phẩm hữu cơ thuộc loại
A. carboxylic acid. B. ester. C. aldehyde. D. ketone.
(Xem giải) Câu 12: Acquy chì là loại pin sạc lâu đời nhất, có nguyên tắc hoạt động như pin điện hóa. Cực dương làm từ Pb được phủ PbO2 và cực âm làm từ Pb nguyên chất dạng xốp, hai điện cực cùng nhúng vào dung dịch H2SO4 nồng độ 38%. Phản ứng xảy ra khi acquy xả điện là
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l)
Biết rằng PbSO4 sinh ra từ điện cực nào đều bám hết vào điện cực đó. Phát biểu nào sau đây sai?
A. Tại cathode, PbO2 bị khử và tạo thành PbSO4.
B. Khi acquy xả điện, khối lượng các điện cực bị giảm.
C. Tại anode, Pb bị oxi hóa và tạo thành PbSO4.
D. Khi acquy xả điện, nồng độ H2SO4 giảm.
(Xem giải) Câu 13: Để kiểm tra sự có mặt của một số cation có trong dung dịch ta tiến hành thí nghiệm sau: Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch cần xác định cation trong muối, thấy có kết tủa màu trắng xuất hiện ngay. Trong dung dịch này chứa cation nào sau đây?
A. Fe2+(aq). B. Mg2+(aq). C. Cu2+(aq). D. Fe3+(aq).
(Xem giải) Câu 14: Cho phản ứng: H2(g) + Cl2(g) → 2HCl(g). Ở điều kiện chuẩn, cứ 1 mol H2 phản ứng hết sẽ tỏa ra nhiệt lượng 184,6 kJ. Enthalpy tạo thành chuẩn của HCl(g) là
A. 184,6 kJ/mol. B. -184,6 kJ/mol. C. 92,3 kJ/mol. D. -92,3 kJ/mol.
(Xem giải) Câu 15: Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất?
A. Al. B. Na. C. Fe. D. W.
(Xem giải) Câu 16: Chlorine (Cl) là nguyên tố hóa học có trong thành phần của chất sát khuẩn, thường được sử dụng với mục đích khử trùng và tẩy trắng trong lĩnh vực thủy sản, dệt nhuộm, xử lí nước cấp, nước thải, nước bể bơi. Ở trạng thái cơ bản, cấu hình electron của nguyên tử Cl (số hiệu nguyên tử bằng 17) là
A. 1s2 2s2 2p6 3s2 3p5. B. 1s2 2s2 2p6 3p5 3s2.
C. 1s2 2s2 2p6 3s3 3p4. D. 1s2 2s2 2p6 3s1 3p6.
(Xem giải) Câu 17: Chất nào sau đây thuộc loại disaccharide?
A. Cellulose. B. Saccharose. C. Tinh bột. D. Glucose.
(Xem giải) Câu 18: Cho cân bằng: 2NO2(g, màu nâu đỏ) ⇌ N2O4(g, không màu). ![]() < 0. Nếu nhúng bình vào nước đá thì
< 0. Nếu nhúng bình vào nước đá thì
A. chuyển sang màu xanh. B. màu nâu đỏ nhạt dần.
C. giữ nguyên màu như ban đầu. D. màu nâu đỏ đậm dần.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Trong công nghiệp, sodium hydrogencarbonate (baking soda) và sodium carbonate được sản xuất bằng phương pháp Solvay từ nguyên liệu chính là đá vôi, muối ăn, ammonia và nước. Quá trình sản xuất theo phương pháp Solvay bao gồm các công đoạn như trong sơ đồ sau:
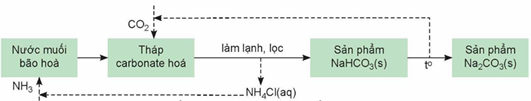
a. CaO thu được từ nhiệt phân đá vôi dùng để chuyển NH4Cl thành NH3.
b. Phản ứng xảy ra trong tháp carbonate hóa là:
2NaCl(aq) + 2NH3(aq) + H2O(l) + CO2(g) ⇌ Na2CO3(s) + 2NH4Cl(aq)
c. Nguyên liệu chính ban đầu của quá trình sản xuất soda bằng phương pháp Solvay là: NaCl, NH3, CaCO3 và H2O.
d. Để tiết kiệm chi phí, có thể thay thế dung dịch NaCl bão hòa bằng nước biển.
(Xem giải) Câu 20: Vật liệu polymer đã và đang được sử dụng rộng rãi trong rất nhiều lĩnh vực. Với những ưu điểm vượt trội về tính chất, độ bền,… vật liệu polymer được ứng dụng rộng rãi trong đời sống như làm vật liệu cách điện và đặc biệt là vật liệu xây dựng mới như: sơn chống thấm, bê tông siêu nhẹ, gỗ công nghiệp, … Các polymer được điều chế bằng phản ứng trùng hợp hoặc trùng ngưng.
a. Các polymer để sản xuất các chất dẻo đều được điều chế bằng phản ứng trùng hợp.
b. Nylon-6,6 được sử dụng phổ biến trong ngành dệt may và được điều chế từ phản ứng trùng ngưng.
c. Sự khác biệt cơ bản giữa hai phản ứng điều chế polymer là: phản ứng trùng ngưng có tạo ra các phân tử nhỏ, còn trùng hợp thì không tạo ra các phân tử nhỏ.
d. Trùng hợp buta-1,3-diene thu được polymer có cấu trúc tương tự cao su tự nhiên.
(Xem giải) Câu 21: Dung dịch acetic acid 2% – 5% trong nước gọi là giấm ăn. Một trong những phương pháp cổ nhất ngày nay vẫn dùng để sản xuất giấm ăn là lên men ethanol. Một người đã thực hiện lên men 500 mL dung dịch ethanol 4,6° với hiệu suất của quá trình lên men là 85% và khối lượng riêng của ethanol là 0,8 g/mL.
a. Công thức phân tử của acetic acid là C2H6O2.
b. Giấm ăn có pH < 7.
c. Có thể dùng giấm ăn để làm mất mùi tanh của cá khi ta chế biến các món ăn.
d. Nồng độ phần trăm acetic acid trong dung dịch thu được sau phản ứng lên men là 4,03%.
(Xem giải) Câu 22: Trong phòng thí nghiệm, một nhóm học sinh xác định thành phần của chiếc đinh sắt (đinh sắt được làm từ hợp kim của sắt với carbon và một số nguyên tố khác) đã bị oxi hóa một phần thành gỉ sắt (Fe2O3.nH2O) theo các bước sau:
• Bước 1: Hòa tan hoàn toàn đinh sắt vào dung dịch H2SO4 loãng, nóng (dùng gấp đôi lượng phản ứng), thu được 200 mL dung dịch X và 0,2225 mol H2.
• Bước 2: Cho dung dịch Ba(OH)2 dư vào 20 mL dung dịch X thu được 14,4 g kết tủa.
• Bước 3: Nhỏ từ từ dung dịch KMnO4 0,1M vào 20 mL dung dịch X đến khi phản ứng vừa đủ thì hết 46 mL.
Giả thiết toàn bộ gỉ sắt tạo ra bám trên đinh sắt; carbon và một số nguyên tố khác trong đinh sắt là những chất không tham gia phản ứng trong các bước.
a. Đinh sắt bị gỉ chủ yếu do sự ăn mòn hóa học.
b. Sau bước 1, trong dung dịch X chỉ chứa hai muối tan.
c. Phần trăm khối lượng sắt đã bị oxi hóa thành gỉ sắt là 10% (làm tròn đến hàng đơn vị).
d. Ở bước 1 và bước 3 đều xảy ra phản ứng oxi hóa – khử.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Cho các phát biểu sau:
(1) Aldehyde vừa có tính oxi hóa vừa có tính khử.
(2) Phenol tham gia phản ứng thế bromine dễ hơn benzene.
(3) Acetone phản ứng với Cu(OH)2 đun nóng tạo kết tủa màu đỏ gạch.
(4) Aldehyde tác dụng với LiAlH4 thu được alcohol bậc một.
(5) Dung dịch phenol trong nước làm quỳ tím hóa đỏ.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần.
(Xem giải) Câu 24: Gang (hợp kim Fe-C nóng chảy) được sản xuất từ quặng sắt (chứa 90% Fe2O3 theo khối lượng và tạp chất không chứa sắt), vật liệu tạo xỉ (CaO), than cốc và không khí nóng. Các phản ứng chính diễn ra trong lò cao:
C(s) + O2(g) → CO2(g) (1)
C(s) + CO2(g) → 2CO(g) (2)
Fe2O3(s) + 3CO(g) → 2Fe(s) + 3CO2(g) (3)
Fe(l) + C(s) → Gang (l) (4)
Gang thu được gồm có 95,50% sắt và 4,50% carbon (theo khối lượng). Để sản xuất 10 tấn gang thì khối lượng quặng sắt đã tiêu thụ là bao nhiêu tấn? Biết rằng có 2% lượng sắt mới sinh bị tiêu hao trong lò cao do chuyển vào xỉ. (Làm tròn kết quả đến hàng phần mười)
(Xem giải) Câu 25: Số lượng đồng phân cấu tạo mạch hở ứng với công thức phân tử C4H8 là bao nhiêu?
(Xem giải) Câu 26: Pin nhiên liệu sử dụng ethanol được đặc biệt quan tâm do có nguồn nhiên liệu sinh học dồi dào. Phản ứng chung trong pin ethanol – oxygen như sau:
C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l)
Một pin ethanol – oxygen được dùng để thắp sáng 8 bóng đèn LED, mỗi bóng có công suất 3 W (3 J/s) liên tục trong t giờ, tiêu thụ hết 230 gam ethanol. Biết rằng 60% lượng nhiệt sinh ra từ phản ứng (ở điều kiện chuẩn) được chuyển hóa thành điện năng. Cho biết nhiệt tạo thành chuẩn của các chất:
| Chất | C2H5OH(l) | O2(g) | CO2(g) | H2O(l) |
| -277,6 | -393,5 | -285,8 |
Giá trị của t bằng bao nhiêu? (Làm tròn kết quả đến hàng phần mười)
(Xem giải) Câu 27: Trong công nghiệp, ammonia được sản xuất theo phản ứng: N2(g) + 3H2(g) ⇌ 2NH3(g). Nung nóng hỗn hợp X gồm N2 và H2 trong bình kín có dung tích không đổi với xúc tác Fe (có thể tích không đáng kể) sau một thời gian đưa về nhiệt độ ban đầu thu được hỗn hợp khí Y có áp suất giảm 10% so với áp suất ban đầu và tỉ khối của Y so với H2 bằng 85/18. Hiệu suất của phản ứng tổng hợp NH3 là a%. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng đơn vị)
(Xem giải) Câu 28: Trong phân tử peptide cho dưới đây có bao nhiêu gốc alanine?
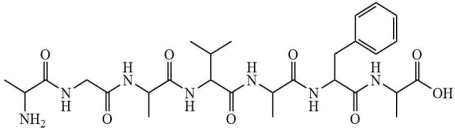


Bình luận