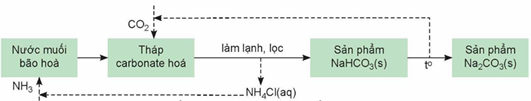
Trong công nghiệp, sodium hydrogencarbonate (baking soda) và sodium carbonate (soda) được sản xuất bằng phương pháp Solvay từ nguyên liệu chính là đá vôi, muối ăn, ammonia và nước. Quá trình sản xuất theo phương pháp Solvay bao gồm các công đoạn như trong sơ đồ sau:
Câu 1.
a) CaO thu được từ nhiệt phân đá vôi dùng để chuyển NH4Cl thành NH3.
b) Phương pháp Solvay đã tái sử dụng các sản phẩm trung gian như NH3, CO2 qua đó giảm thiểu được giá thành sản xuất.
c) Phản ứng xảy ra trong tháp carbonate hoá là
2NaCl (aq) + 2NH3 (aq) + H2O(l) + CO2(g) ⇋ Na2CO3(s) + 2NH4Cl (aq)
d) NaHCO3 là chất có độ tan kém nên dễ bị kết tinh. Độ tan của NaHCO3 trong 100 gam nước ở 20°C và ở 40°C lần lượt là 9,6 gam và 12,7 gam. Làm lạnh 90,16 tấn dung dịch NaHCO3 bão hoà ở 40°C về 20°C thì khối lượng muối NaHCO3 kết tinh là 2,48 tấn (giả thiết không có sự bay hơi của nước).
Câu 2.
a) NH4Cl được nhiệt phân để thu hồi NH3 đưa trở lại quá trình sản xuất.
b) CO2 cung cấp cho quá trình Solvay được lấy từ nhiệt phân đá vôi.
c) Độ tan của NaHCO3 ở 20°C và 40°C lần lượt là 9,6 g/100 g nước và 12,7 g/100 g nước. Khi giảm nhiệt độ của 450,8 gam dung dịch NaHCO3 bão hòa từ 40°C về 20°C thì khối lượng muối NaHCO3 kết tinh là 12,4 gam. (Làm tròn đến hàng phần mười)
d) Quy trình sản xuất theo sơ đồ trên không gây tiêu tốn NH3 và CO2 (bỏ qua sự thất thoát ra môi trường).
Câu 3. Giai đoạn tạo ra NaHCO3:
NaCl + NH3 + CO2 + H2O ⇋ NaHCO3 + NH4Cl (1)
Giai đoạn tạo ra Na2CO3:
2NaHCO3 (t°) → Na2CO3 + CO2 + H2O (2)
a) Trong quá trình phản ứng liên tục được bổ sung NaCl, CO2 và lọc lấy NaHCO3 làm cho cân bằng (1) chuyển dịch theo chiều thuận.
b) Khi làm lạnh, NaHCO3 kết tinh và được lọc, tách khỏi hệ phản ứng.
c) Phương pháp Solvay đã tái sử dụng các sản phẩm trung gian như NH3, CO2 qua đó giảm thiểu được giá thành sản xuất.
d) Trong phản ứng (2) khối lượng chất rắn giảm tối đa 39,6% sau khi nung.
Câu trả lời tốt nhất
Câu 1.
(a) Đúng: 2NH4Cl + CaO —> CaCl2 + 2NH3 + H2O
(b) Đúng, NH3 và CO2 được dẫn quay vòng khép kín, chỉ cần bổ sung lượng hao hụt từ nguồn bên ngoài, qua đó giảm thiểu được giá thành sản xuất và hạn chế xả thải.
(c) Sai, phản ứng xảy ra trong tháp carbonate hoá là
CO2(aq) + H2O(l) + NH3(aq) + NaCl(aq) → NH4Cl(aq) + NaHCO3(s)
(d) Đúng
mNaHCO3 kết tinh = x tấn, bảo toàn khối lượng NaHCO3:
90,16.12,7/(100 + 12,7) = x + (90,16 – x).9,6/(100 + 9,6)
—> x = 2,48
Câu 2.
(a) Sai, nhiệt phân không tách được khí NH3 từ NH4Cl (khí NH3 và khí HCl lại kết hợp với nhau ngay thành dạng khói trắng). Người ta dùng CaO (thu được khi nhiệt phân CaCO3) để tách NH3:
2NH4Cl + CaO —> CaCl2 + 2NH3 + H2O
(b) Đúng, quá trình Solvay cần cả CaO (vai trò như trên) và CO2 (tạo NaHCO3) nên người ta sẽ nhiệt phân CaCO3 (nguyên liệu sẵn có, giá rẻ) để thu được CaO và CO2 với tỉ lệ phù hợp.
(c) Đúng
mNaHCO3 kết tinh = x gam, bảo toàn khối lượng NaHCO3:
450,8.12,7/(100 + 12,7) = x + (450,8 – x).9,6/(100 + 9,6)
—> x = 12,4 gam
(d) Sai, nếu không tính thất thoát ra môi trường thì chỉ NH3 là đủ để quay vòng, còn CO2 vẫn phải bổ sung từ nhiệt phân CaCO3 (CO2 do nhiệt phân NaHCO3 và CO2 do nhiệt phân CaCO3 là nguyên liệu cho chu kỳ điều chế mới).
Câu 3.
(a) Đúng, theo nguyên lý chuyển dịch cân bằng Le Chatelier, việc tăng nồng độ tác chất (NaCl, CO2) và liên tục lấy bớt sản phẩm (NaHCO3 kết tủa) ra khỏi hệ sẽ làm cân bằng dịch chuyển mạnh sang chiều thuận, giúp tăng hiệu suất tạo thành NaHCO3.
(b) Đúng, trong các chất có mặt ở phản ứng (1), NaHCO3 có độ tan thấp nhất, đặc biệt là ở nhiệt độ thấp. Vì vậy, người ta làm lạnh dung dịch để NaHCO3 kết tinh dạng rắn, giúp việc lọc tách trở nên dễ dàng.
(c) Đúng, đây là ưu điểm lớn nhất của quy trình này. CO2 sinh ra từ phản ứng nung (2) và từ lò vôi được đưa ngược lại phản ứng (1). Quan trọng hơn, NH3 được tái chế từ NH4Cl bằng cách cho phản ứng với CaO. Nhờ vậy, nguyên liệu tiêu tốn thực tế chủ yếu chỉ là nước muối (NaCl) và đá vôi (CaCO3).
(d) Sai, từ 2 mol NaHCO3 tạo 1 mol Na2CO3
—> m rắn giảm = (84.2 – 106)/(84.2) = 36,9%
