[2026] Thi thử TN sở GDĐT Quảng Ninh (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 087
⇒ Tổng hợp đề thi THPT Quốc gia môn hóa theo năm học
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2D | 3B | 4D | 5D | 6D | 7A | 8D | 9A |
| 10C | 11A | 12C | 13B | 14B | 15A | 16D | 17C | 18A |
| 19 | 20 | 21 | 22 | |
| (a) | Đ | Đ | Đ | S |
| (b) | S | S | S | Đ |
| (c) | S | S | S | S |
| (d) | S | Đ | Đ | S |
| 23 | 24 | 25 | 26 | 27 | 28 |
| 4,24 | 0,17 | 1,1 | 1345 | 250 | 3,18 |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Một hydrocarbon X mạch hở trong phân tử có phần trăm khối lượng carbon bằng 85,714%. Trên phổ khối lượng của X có peak ion phân tử ứng với giá trị m/z = 42. Công thức phù hợp với X là
A. CH2=CHCH3. B. CH3CH3. C. CH≡CH. D. CH3CH2CH3.
(Xem giải) Câu 2: Tính chất vật lí chung của polymer là
A. chất lỏng, không màu, không tan trong nước.
B. chất lỏng, không màu, tan tốt trong nước.
C. chất rắn, không bay hơi, dễ tan trong nước.
D. chất rắn, không bay hơi, không tan trong nước.
(Xem giải) Câu 3: Phát biểu nào sau đây sai?
A. Hạt nhân nguyên tử cấu thành từ các hạt proton và neutron.
B. Nguyên tử có cấu trúc đặc khít, gồm vỏ nguyên tử và hạt nhân nguyên tử.
C. Vỏ nguyên tử cấu thành từ các hạt electron.
D. Đa số nguyên tử được cấu thành từ các hạt cơ bản là proton, neutron và electron.
(Xem giải) Câu 4: Các nguyên tố dinh dưỡng cho cây trồng được chia thành 3 nhóm:
– Nhóm đa lượng: Cây cần lượng lớn, gồm N, P, K.
– Nhóm trung lượng: Cây cần lượng vừa phải, gồm Ca, Mg, S.
– Nhóm vi lượng: Cây cần lượng rất nhỏ, gồm Fe, Zn, Cu, B…
Một loại phân bón hỗn hợp NPK cung cấp đồng thời ba nguyên tố Nitrogen (N), Phosphorus (P) và Potassium (K). Các nguyên tố này thuộc nhóm nào sau đây?
A. Nhóm nguyên tố trung lượng. B. Nhóm nguyên tố quý hiếm.
C. Nhóm nguyên tố vi lượng. D. Nhóm nguyên tố đa lượng.
(Xem giải) Câu 5: Nguyên nhân chính dầu mỡ thường có mùi khó chịu khi để lâu ngày trong không khí hoặc tái sử dụng nhiều lần vì dầu mỡ bị tác động nào sau đây?
A. Hydrogen hoá. B. Thuỷ phân. C. Xà phòng hoá. D. Oxi hoá.
(Xem giải) Câu 6: Số lượng phối tử có trong phức chất [PtCl4(NH3)2] là
A. 4. B. 7. C. 2. D. 6.
(Xem giải) Câu 7: Dung dịch chất nào sau đây làm quỳ tím đổi thành màu xanh?
A. Dung dịch lysine. B. Dung dịch glycine.
C. Dung dịch valine. D. Dung dịch alanine.
(Xem giải) Câu 8: Kim loại chuyển tiếp dãy thứ nhất thuộc khối nguyên tố nào sau đây?
A. Nguyên tố p. B. Nguyên tố f. C. Nguyên tố s. D. Nguyên tố d.
(Xem giải) Câu 9: Polypropylene (PP) là chất dẻo thường được sử dụng để sản xuất các sản phẩm thiết bị y tế, đồ gia dụng,… PP được tổng hợp từ monomer nào sau đây?
A. CH3-CH=CH2. B. C6H5OH và HCHO.
C. CH2=CH-CN. D. CH2=CH2.
(Xem giải) Câu 10: Khi oxi hóa không hoàn toàn alcohol bậc 1 bằng CuO nung nóng, sản phẩm thu được thường là loại hợp chất hữu cơ nào sau đây?
A. Carboxylic acid. B. Ketone. C. Aldehyde. D. Alkene.
(Xem giải) Câu 11: Cho các ester sau: ethyl formate (1); vinyl acetate (2); triolein (3); methyl acrylate (4); phenyl acetate (5). Dãy gồm các ester đều phản ứng được với dung dịch NaOH dư, đun nóng sinh ra alcohol là
A. (1), (3), (4). B. (2), (3), (5). C. (3), (4), (5). D. (1), (2), (3).
(Xem giải) Câu 12: Trong quá trình Solvay, ở giai đoạn tạo thành NaHCO3 có cân bằng hóa học sau: NaCl + NH3 + CO2 + H2O ⇋ NaHCO3 + NH4Cl. Khi làm lạnh dung dịch trên, muối đầu tiên bị tách ra khỏi dung dịch là
A. NH4Cl. B. NaCl. C. NaHCO3. D. NH4HCO3.
(Xem giải) Câu 13: Năng lượng hoạt hóa là năng lượng tối thiểu mà các chất tham gia phản ứng cần phải có để phản ứng có thể xảy ra. Cho đồ thị biểu diễn năng lượng của một phản ứng như sau:
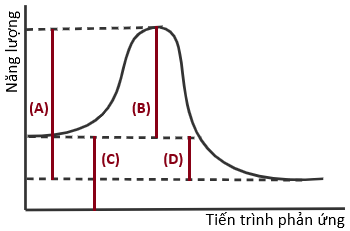
Đoạn nào trên đồ thị tương ứng với năng lượng hoạt hóa của phản ứng?
A. Đoạn (D). B. Đoạn (B). C. Đoạn (A). D. Đoạn (C).
(Xem giải) Câu 14: Cho phương trình hóa học của phản ứng nhiệt nhôm: 2Al(s) + Fe2O3(s) → Al2O3(s) + 2Fe(s). Tính biến thiên enthalpy chuẩn của phản ứng. Biết nhiệt tạo thành chuẩn của Fe2O3 và Al2O3 lần lượt là -825,5 kJ/mol và -1676,0 kJ/mol.
A. +850,5 kJ. B. -850,5 kJ. C. +2501,5 kJ. D. -2526,5kJ.
(Xem giải) Câu 15: Chất X có các đặc điểm sau: phân tử có nhiều nhóm -OH, có vị ngọt, hoà tan Cu(OH)2 ở nhiệt độ thường, phân tử có liên kết glycoside, không làm mất màu nước bromine. Chất X là
A. saccharose. B. cellulose. C. glucose. D. tinh bột.
(Xem giải) Câu 16: Có ba ống nghiệm chứa dung dịch hóa chất sau: ống (1) chứa ethyl alcohol, ống (2) chứa acetic acid và ống (3) chứa acetaldehyde. Nếu cho Cu(OH)2 trong môi trường kiềm (NaOH) lần lượt vào các dung dịch trên và đun nóng thì trong ống nghiệm nào có phản ứng hóa học xảy ra?
A. Cả ba ống. B. Ống (1).
C. Óng (1) và ống (3). D. Ống (2) và ống (3).
(Xem giải) Câu 17: Cho các quá trình nào sau đây:
(1) Hexane (t°, xt) → isohexane.
(2) Ethylbenzen (t°, xt) → 1,2-dimethylbenzene.
(3) Octane (t°, xt) → Butane + But-1-ene.
(4) Octane (t°, xt) → 2,2,4-trimethylpentane
Có bao nhiêu quá trình trong số các quá trình trên là quá trình reforming?
A. 4. B. 2. C. 3. D. 1.
(Xem giải) Câu 18: Cho cấu tạo của một pin điện như hình dưới đây:

Phát biểu nào sau đây đúng?
A. Điện cực Zn là anode, điện cực Cu là cathode.
B. Tổng thế điện cực của hai điện cực là 1,102V.
C. Điện cực Zn là cathode, điện cực Cu là anode.
D. Thế điện cực của điện cực Zn lớn hơn của điện cực Cu là 1,102V.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Tyrosine (Tyr) là một amino acid không thiết yếu nhưng đóng vai trò tiền thân quan trọng để tổng hợp các chất dẫn truyền thần kinh như dopamine và adrenaline. Cho công thức cấu tạo của Tyrosine như hình bên:
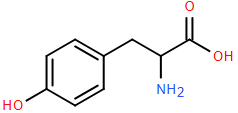
Tại pH ≈ 5,7, tyrosine tồn tại chủ yếu ở dạng ion lưỡng cực có tổng điện tích bằng không.
a) Khi đặt trong điện trường tại pH = 2, tyrosine sẽ di chuyển về phía cực âm.
b) 01 mol tyrosine có thể phản úng tối đa với 01 mol NaOH trong dung dịch.
c) Khối lượng mol phân tử của tyrosine là 179.
d) Tyrosine thuộc loại hợp chất hữu cơ tạp chức, phân tử chứa hai loại nhóm chức khác nhau.
(Xem giải) Câu 20: Ammonia có nhiều ứng dụng quan trọng trong đời sống và sản xuất. Trong công nghiệp, ammonia được tổng hợp từ nitrogen và hydrogen theo phương trình nhiệt hóa học sau: N2(g) + 3H2(g) ⇋ 2NH3(g) ![]() = -91,8 kJ. Kết quả nghiên cứu sự phụ thuộc của hiệu suất tổng hợp ammonia vào áp suất và nhiệt độ của phản ứng được thể hiện ở đồ thị hình bên:
= -91,8 kJ. Kết quả nghiên cứu sự phụ thuộc của hiệu suất tổng hợp ammonia vào áp suất và nhiệt độ của phản ứng được thể hiện ở đồ thị hình bên:
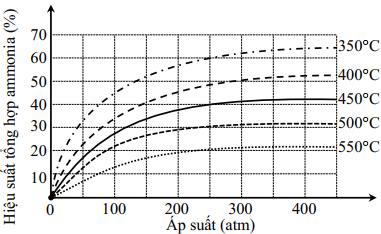
a) Ở nhiệt độ 500°C, 250 atm, 2 mol N2 tác dụng với 3 mol H2 thu được 0,6 mol NH3.
b) Nếu thực hiện phản ứng ở nhiệt độ càng thấp thì sẽ càng đạt hiệu quả kinh tế cao.
c) Hiệu suất của phản ứng ở 500°C, 300 atm cao hơn hiệu suất ở 450°C, 200 atm.
d) Để tăng hiệu suất tổng hợp ammonia có thể đồng thời tăng áp suất và giảm nhiệt độ.
(Xem giải) Câu 21: Thực hiện thí nghiệm sau:
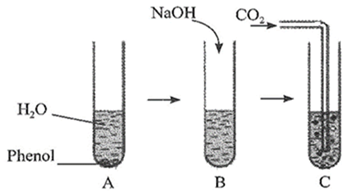
• Bước 1: Cho phenol vào ống nghiệm, thêm nước và lắc đều ống nghiệm thấy dung dịch có màu trắng đục (hình A).
• Bước 2: Tiếp tục cho dung dịch NaOH vào ống nghiệm thấy dung dịch chuyển sang trong suốt (hình B).
• Bước 3: Tiếp tục sục khí CO2 vào ống nghiệm thấy Phenol. dung dịch chuyển màu trắng đục như ban đầu (hình C).
a) Trong ống nghiệm ở bước 2 (hình B), dung dịch trong suốt vì sản phẩm tạo ra khi cho NaOH vào ống nghiệm tan tốt trong nước.
b) Trong ống nghiệm ở bước 1 (hình A), phenol tan tốt trong nước ở điều kiện thường nên dung dịch có màu trắng đục.
c) Nếu cho quỳ tím vào ống nghiệm ở bước 1 (hình A) thì quỳ tím chuyển đỏ.
d) Trong ống nghiệm ở bước 3 (hình C), dung dịch trắng đục là do có phenol tạo thành.
(Xem giải) Câu 22: Dùng panh lấy các mẫu kim loại (Li, Na hoặc K) có kích cỡ xấp xỉ nhau đã thấm khô dầu và cho vào các chậu thủy tinh đã chứa khoảng 1/3 thể tích nước. Thêm 2 – 3 giọt dung dịch phenolphthalein vào chậu sau khi kim loại tan hết.
a) Các cặp oxi hóa – khử M+/M (M: Li, Na, K) đều có giá trị thế điện cực chuẩn lớn hơn giá trị thế điện cực chuẩn của cặp oxi hóa – khử 2H2O/H2, 2OH-.
b) Các dung dịch thu được sau phản ứng đều có màu hồng.
c) Hiện tượng ở chậu thủy tinh chứa Li và K giống nhau.
d) Từ hiện tượng thí nghiệm, chứng tỏ tính khử của kim loại tăng dần theo thứ tự sau: K, Na, Li.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Trong quá trình điện phân nóng chảy hỗn hợp gồm Al2O3 và cryolite với các điện cực bằng than chì (carbon), tại cathode thu được 10,8 tấn aluminium (Al) nguyên chất. Tại anode, carbon bị oxi hóa thành hỗn hợp khí gồm CO2 (chiếm 70% về thể tích) và CO (chiếm 30% về thể tích). Giả thiết không có sản phẩm phụ nào khác và toàn bộ oxygen sinh ra từ Al2O3 đều phản ứng với carbon. Tính khối lượng carbon (theo tấn) đã bị tiêu thụ tại anode (không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
(Xem giải) Câu 24: Thủy phân m gam saccharose trong môi trường acid với hiệu suất phản ứng đạt 80%, thu được dung dịch X. Trung hòa acid dư trong X, sau đó chia dung dịch làm hai phần bằng nhau:
• Phần 1: Cho tác dụng với lượng dư dung dịch AgNO3 trong NH3 đun nóng, sau khi các phản ứng xảy ra hoàn toàn thu được 64,8 gam silver (Ag) kết tủa.
• Phần 2: Cho tác dụng với Cu(OH)2 ở nhiệt độ thường.
Giả thiết các phản ứng đều xảy ra hoàn toàn (trừ phản ứng thủy phân). Số mol Cu(OH)2 tối đa bị hòa tan ở phần 2 là bao nhiêu? (không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
(Xem giải) Câu 25: Ở điều kiện chuẩn, pin Zn-Fe có sức điện động 0,323V, pin Fe-Pb có sức điện động 0,321V, pin Pb-Cu có sức điện động 0,459V. Sức điện động chuẩn của pin Zn – Cu bằng bao nhiêu volt (V)? (không làm tròn kết quả các phép tính trung gian, chi làm tròn kết quả cuối cùng đến hàng phần mười).
(Xem giải) Câu 26: Cho các phát biểu sau:
(1) Hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn so với kim loại.
(2) Kim loại A có nhiệt độ nóng chảy cao hơn kim loại B, nhiệt độ nóng chảy của hợp kim A-B luôn cao hơn nhiệt độ nóng chảy của B.
(3) Tính chất hoá học của hợp kim thường tương tự tính chất của các kim loại thành phần.
(4) Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
(5) Hợp kim thường khó bị oxi hoá hơn các đơn kim loại thành phần.
Hãy sắp xếp các phát biểu đúng trong các phát biểu trên thành bộ số theo số thứ tự tăng dần (ví dụ 12, 134,…)
(Xem giải) Câu 27: Khí thiên nhiên là nguồn nhiên liệu quan trọng, phát thải thấp, được sử dụng phổ biến trong các nhà máy nhiệt điện hiện đại. Một loại khí thiên nhiên X (đã qua xử lý để loại bỏ tạp chất) có thành phần phần trăm về thể tích các khí như sau: 95% methane, 3% ethane, 1,5% propane và 0,5% butane. Giả thiết, khi đốt cháy hoàn toàn X ở điều kiện chuẩn chỉ xảy ra các phản ứng nhiệt hóa học sau:
(1) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
(2) 2C2H6(g) + 7O2(g) → 4CO2(g) + 6H2O(l)
(3) C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(l)
(4) 2C4H10(g) + 13O2(g) → 8CO2(g) + 10H2O(l)
Một nhà máy nhiệt điện chu trình hỗn hợp có công suất phát điện ổn định là 150 MW (150000 kJ/s). Biết rằng có 55% nhiệt lượng tỏa ra khi đốt cháy hoàn toàn khí thiên nhiên X được chuyển hóa thành điện năng. Biết giá khí thiên nhiên trên thị trường hiện nay là 372650 đồng/triệu BTU (với 1 triệu BTU = 1,055.10^6 kJ). Hãy tính số tiền (tỷ đồng) nhà máy cần chi trả để mua lượng nhiên liệu trên cho một tháng (30 ngày) hoạt động liên tục (không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
Cho biết: Nhiệt tạo thành chuẩn của các chất được cho trong bảng sau:
| Chất | CH4(g) | C2H6(g) | C3H8(g) | C4H10(g) | CO2(g) | H2O(l) |
| -74,9 | -84,7 | -105,0 | -126,1 | -393,5 | -285,8 |
(Xem giải) Câu 28: Trong quá trình một nhà máy xử lí nước sinh hoạt, đến giai đoạn xử lí tính cứng vĩnh cửu gây ra bởi Ca2+ có độ cứng tính theo CaCO3 là 300 mg CaCO3/L (quy đổi nồng độ Ca2+ tương ứng với khối lượng CaCO3 trong 1 lít nước) về nước có độ cứng không vượt quá 60 mg CaCO3/L. Tính khối lượng (kg) tối thiểu Soda công nghiệp (chứa 80% Na2CO3 về khối lượng, còn lại là tạp chất trơ) cần dùng để xử lý 10 m³ nước cứng vĩnh cửu trên (không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).


Bình luận