[2026] Thi thử TN sở GDĐT Tuyên Quang (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 062
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2A | 3C | 4A | 5C | 6A | 7A | 8D | 9D |
| 10A | 11A | 12D | 13B | 14C | 15A | 16C | 17C | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | Đ | Đ | 4 | 1342 | 960 |
| (b) | S | S | Đ | S | 26 | 27 | 28 |
| (c) | S | Đ | Đ | S | 9 | 28,8 | 3,26 |
| (d) | S | S | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Acquy chì là loại pin sạc lâu đời nhất, có nguyên tắc hoạt động như pin điện hóa. Cực dương làm từ PbO2 và cực âm làm từ Pb nguyên chất dạng xốp, hai điện cực nhúng vào dung dịch H2SO4 nồng độ 38%. Phản ứng xảy ra khi acquy xả điện là Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l). Biết rằng PbSO4 sinh ra từ điện cực nào đều bám hết vào điện cực đó. Phát biểu nào sau đây đúng?
A. Khi acquy xả điện, khối lượng các điện cực đều tăng.
B. Tại anode, Pb bị khử và tạo thành PbSO4.
C. Khi acquy xả điện, nồng độ H2SO4 tăng.
D. Tại cathode, PbO2 bị oxi hóa và tạo thành PbSO4.
(Xem giải) Câu 2. Phát biểu nào sau đây về carbohydrate là đúng?
A. Ở dạng mạch vòng, nhóm –OH hemiacetal của glucose phản ứng với methanol khi có mặt HCl khan, tạo thành methyl glucoside.
B. Carbohydrate là những hợp chất hữu cơ đa chức, thường có công thức chung là Cn(H2O)m.
C. Một phân tử amylose có cấu tạo như sau:
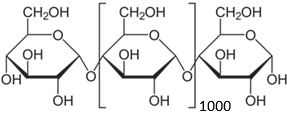
Số liên kết α–1,4–glycoside trong phân tử amylose ở trên là 1000.
D. Amylopectin được cấu tạo từ nhiều đơn vị β-glucose liên kết với nhau qua liên kết β–1,4–glycoside và β–1,6–glycoside hình thành cấu trúc mạch phân nhánh.
(Xem giải) Câu 3. Phương trình hóa học thủy phân 2-bromo-2-methylpropane trong dung dịch NaOH là
(CH3)3CBr + NaOH → (CH3)3COH + NaBr
Cơ chế phản ứng diễn ra theo 2 giai đoạn được mô tả như sau:
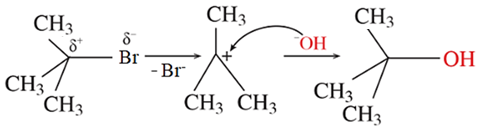
Nhận định nào sau đây đúng?
A. Phản ứng thuỷ phân 2-bromo-2-methylpropane là phản ứng tách hydrogen halide.
B. Trong giai đoạn (1) do độ âm điện C lớn hơn Br nên liên kết phân cực về phía Br.
C. Trong giai đoạn (2) có sự hình thành liên kết σ.
D. Sản phẩm thu được sau phản ứng thủy phân là alcohol bậc IV.
(Xem giải) Câu 4. Thành phần chính của “khí thiên nhiên” là methane. Công thức phân tử của methane là
A. CH4. B. C2H4. C. C2H5. D. C3H8.
(Xem giải) Câu 5. Cho dãy sắp xếp các kim loại theo chiều giảm dần tính khử: Na, Mg, Al, Fe. Trong các cặp oxi hóa – khử sau, cặp nào có giá trị thế điện cực chuẩn lớn nhất?
A. Al3+/Al. B. Mg2+/Mg. C. Fe2+/Fe. D. Na+/Na.
(Xem giải) Câu 6. Nhiều vụ ngộ độc rượu do sử dụng rượu được pha chế từ cồn công nghiệp có lẫn methanol. Công thức phân tử của methanol là
A. CH3OH. B. C2H4(OH)2. C. C2H5OH. D. C3H7OH.
(Xem giải) Câu 7. Khi cho mẩu giấy quỳ tím ẩm ướt vào bình đựng khí NH3, màu giấy quỳ tím chuyển sang màu
A. xanh. B. vàng. C. đỏ. D. nâu.
(Xem giải) Câu 8. Chlorine (Cl) là chất oxi hóa mạnh, được sử dụng làm chất tẩy trắng và khử trùng nước. Ở trạng thái cơ bản, cấu hình electron của nguyên tử Cl (số hiệu nguyên tử bằng 17) là
A. 1s2 2s2 2p6 3s2 3p4. B. 1s2 2s2 2p6 3s2 3p5 3s3.
C. 1s2 2s2 2p6 3s1 3p6. D. 1s2 2s2 2p6 3s2 3p5.
(Xem giải) Câu 9. Salbutamol là chất cấm thường bị lạm dụng trong chăn nuôi heo để tăng tỉ lệ nạc. Tồn dư của nó trong thực phẩm có thể gây ảnh hưởng đến sức khoẻ của con người. Cho công thức cấu tạo của Salbutamol:
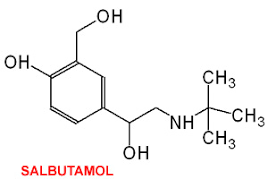
Phát biểu nào sau đây không đúng?
A. Salbutamol tác dụng được với dung dịch HCl và với dung dịch NaOH.
B. Công thức phân tử của Salbutamol là C13H21O3N.
C. Salbutamol có chứa nhóm chức amine bậc II.
D. Salbutamol có chứa 1 nhóm chức amine và 3 nhóm chức alcohol.
(Xem giải) Câu 10. “…(1)…” là các chất được tổng hợp hóa học, có tác dụng giặt rửa như xà phòng nhưng không phải là muối sodium hoặc potassium của các acid béo. Nội dung phù hợp trong chỗ trống (1) là
A. chất giặt rửa tổng hợp. B. ester.
C. xà phòng. D. chất béo.
(Xem giải) Câu 11. Trong phân tử chất nào sau đây có 2 nhóm amino (-NH2) và 1 nhóm carboxyl (-COOH)?
A. Lysine. B. Glycine. C. Glutamic acid. D. Alanine.
(Xem giải) Câu 12. Cho cân bằng: 2SO2(g) + O2(g) ⇌ 2SO3(g), ![]() < 0. Cân bằng hóa học của phản ứng trên sẽ chuyển dịch sang phải khi
< 0. Cân bằng hóa học của phản ứng trên sẽ chuyển dịch sang phải khi
A. giảm áp suất, giảm nhiệt độ. B. tăng nhiệt độ và giảm áp suất.
C. tăng nhiệt độ, tăng áp suất. D. giảm nhiệt độ và tăng áp suất.
(Xem giải) Câu 13. Cho phương trình nhiệt hóa học: H2(g) + ½O2(g) → H2O(l) ![]() = –285,84 kJ. Ở điều kiện chuẩn, khi H2(g) phản ứng vừa đủ với 4,958 L O2(g) thì phản ứng
= –285,84 kJ. Ở điều kiện chuẩn, khi H2(g) phản ứng vừa đủ với 4,958 L O2(g) thì phản ứng
A. tỏa ra nhiệt lượng 285,84 kJ. B. tỏa ra nhiệt lượng 114,336 kJ.
C. thu vào nhiệt lượng 228,672 kJ. D. thu vào nhiệt lượng 114,336 kJ.
(Xem giải) Câu 14. Methyl salicylate (C8H8O3) dùng làm chất giảm đau được điều chế từ salicylic acid (hay 2–hydroxybenzoic acid) theo phản ứng sau:
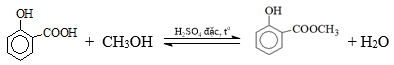
Phát biểu nào sau đây đúng?
A. Công thức phân tử của salicylic acid là C8H8O3.
B. Methyl salicylate thuộc loại hợp chất hữu cơ đa chức.
C. 1 mol methyl salicylate phản ứng tối đa với 2 mol NaOH trong dung dịch.
D. Methyl salicylate không thủy phân trong môi trường kiềm.
(Xem giải) Sử dụng thông tin dưới đây để trả lời các câu hỏi 15 – 18
Kẽm (zinc) là kim loại có nhiều ứng dụng trong công nghiệp như mạ kẽm chống ăn mòn, sản xuất hợp kim,… đồng thời kẽm còn là một vi chất thiết yếu cho sự sống. Lượng kẽm này được tách chủ yếu từ quặng zinc blende (ZnS) theo các bước sau:
• Bước 1. Làm giàu quặng: Quặng được nghiền nhỏ và cho vào nước có thổi không khí. Các hạt đất, đá lắng xuống đáy, zinc sulfide nổi lên cùng với bọt. Lớp bọt này được tách ra và sấy khô.
• Bước 2. Đốt quặng: Nung nóng zinc sulfide trong lò thu được zinc oxide.
2ZnS + 3O2 → 2ZnO + 2SO2
• Bước 3. Khử zinc oxide: ZnO được trộn với than cốc và nung ở nhiệt độ 1400°C: ZnO + C → Zn + CO
• Bước 4. Thu hồi: Kim loại kẽm tạo thành được làm nguội, khí CO sinh ra được đốt cháy, nhiệt lượng tỏa ra giúp giảm chi phí vận hành lò nung.
Biết rằng: kẽm có khối lượng riêng bằng 7,13 g/cm³, nóng chảy ở 419,5°C, sôi ở 906°C.
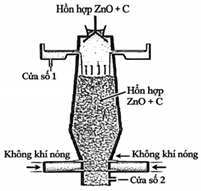
Câu 15. Phát biểu nào dưới đây đúng?
A. Khí SO2 từ nhà máy nếu không qua xử lí sẽ gây ô nhiễm môi trường nước.
B. Kẽm được tách ra theo phương pháp oxy hoá – khử trong dung dịch.
C. Quá trình thổi không khí vào hỗn hợp bột quặng và nước (bước 1) xảy ra biến đổi hoá học.
D. Cửa số (2) trong sơ đồ lò nung thu được hỗn hợp khí CO và CO2.
Câu 16. Đồng thau là hợp kim của khoảng 70% đồng và 30% kẽm. Hợp kim này tan hoàn toàn trong dung dịch nào dưới đây?
A. Dung dịch NaCl. B. Dung dịch CuCl2. C. Dung dịch HNO3. D. Dung dịch HCl.
Câu 17. Cho các nhận định sau về sản xuất và ứng dụng của kẽm:
(1) Trong mạ kẽm chống ăn mòn thép, kẽm là lớp bảo vệ bề mặt, đồng thời bảo vệ điện hoá cho thép.
(2) Cả hai phản ứng xảy ra tại bước 2 và bước 3 trong sơ đồ đều là phản ứng oxi hoá – khử.
(3) Khí thải từ bước 2 và bước 3 đều là nguyên nhân trực tiếp gây mưa axit.
(4) Kẽm được thu hồi ở bước 4 dạng lỏng (cửa số 1) do kẽm là kim loại nặng.
(5) Nhiệt độ của lò nung được cung cấp bởi đốt cháy carbon và đốt cháy khí CO.
Số phát biểu đúng là
A. 5. B. 2. C. 3. D. 4.
Câu 18. Phương pháp tách kim loại nào đã được sử dụng trong bước 3 của sơ đồ trên?
A. Điện phân. B. Kết tinh. C. Nhiệt luyện. D. Thuỷ luyện.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Học sinh A được giao nhiệm vụ tìm hiểu sự ăn mòn kim loại và bảo vệ kim loại. Bạn A đã thực hiện thí nghiệm sau:
• Bước 1: Cho dung dịch NaCl 5% vào ống thuỷ tinh chữ U như hình bên.
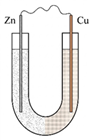
• Bước 2: Nhúng một thanh đồng và một thanh kẽm đã làm sạch vào hai đầu ống chữ U.
• Bước 3: Nối hai thanh kim loại bằng dây dẫn.
a) Sau bước 3, kẽm bị oxi hoá và đóng vai trò là anode.
b) Sau bước 3, Cu2+ bị khử thành Cu bám vào thanh đồng, làm khối lượng thanh đồng tăng dần.
c) Dung dịch quanh thanh đồng làm phenolphthalein chuyển màu hồng vì dòng điện sinh ra từ các pin điện phân dung dịch NaCl quanh thanh đồng.
d) Sau bước 3, cả hai thanh kim loại đều bị ăn mòn hoá học.
(Xem giải) Câu 20. Một nhóm học sinh nghiên cứu quá trình tinh chế đồng từ một mẫu đồng thô (chứa đồng có hàm lượng là x%) bằng phương pháp điện phân và đưa ra giả thuyết “khối lượng mẫu đồng thô giảm bằng khối lượng cathode tăng”. Để kiểm chứng giả thuyết, nhóm học sinh thực hiện thí nghiệm sau:
– Nối mẫu đồng thô với một điện cực và miếng đồng tinh khiết với điện cực còn lại của nguồn điện một chiều, rồi nhúng vào bình điện phân chứa dung dịch copper(II) sulfate trong dung dịch sulfuric acid.
– Tiến hành điện phân với cường độ dòng điện 24A. Sau t giờ, các điện cực được lấy ra, làm khô và đem cân.
– Khối lượng các điện cực trước và sau điện phân được ghi lại trong bảng sau:
| Trước điện phân | Khối lượng mẫu đồng thô (g) | Khối lượng miếng đồng tinh khiết (g) |
| 103 | 100 | |
| Sau 1 giờ | 9,56 | 182,5 |
Giả sử hiệu suất quá trình điện phân là 100% và phần tạp chất tạp chất trong mẫu đồng không tham gia vào quá trình điện phân. Biết q = ne.F = I.t, trong đó: q là điện lượng (C), ne là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian điện phân (giây), F là hằng số Faraday (F = 96500 C/mol).
a) Giả thuyết của nhóm học sinh sai.
b) Trong thí nghiệm, mẫu đồng thô được nối với cực âm, miếng đồng tinh khiết được nối với cực dương của nguồn điện.
c) Giá trị của x ≥ 80,1. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười)
d) Giá trị của t là 3,3. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười)
(Xem giải) Câu 21. Aspirin (hay acetylsalicylic acid), là một dẫn xuất của salicylic acid được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp. Cho quy trình tổng hợp Aspirin trong phòng thí nghiệm như sau:
• Bước 1: Cho 6,9 gam salicylic acid khan và 7,0 ml acetic anhydride (d = 1,08 g/mL) vào bình cầu 250 ml; thêm 3,0 ml sulfuric acid 98% vào và lắc kĩ. Sau đó, khuẩy khối phản ứng ở 50-60°C trong khoảng 45 phút cho đến khi tan hết phần chất rắn.
• Bước 2: Dùng nước đá để làm lạnh hỗn hợp phản ứng đến nhiệt độ nhỏ hơn 10°C. Thêm từ từ 750 ml nước cất và khuấy kỹ, aspirin sẽ kết tủa. Lọc lấy sản phẩm bằng phễu lọc Buchner.
• Bước 3: Hòa tan aspirin thô trong 150 ml ethanol 90° (cần đun nóng để tan hoàn toàn), sau đó đồ dungdịch này từ từ vào 375 ml nước nóng khoảng 50°C. Nếu aspirin kết tủa lại thỉ cần đun nóng cho tan hết. Để nguội dung dịch thu được đến nhiệt độ phòng. Aspirin sẽ kết tinh dưới dạng tinh thể. Lọc và hút kiệt rồi sấy khô ở 50°C.
• Bước 4: Cân sản phẩm thu được 5,04 gam aspirin
Cho biết phương trình hóa học điều chế aspirin từ salicylic acid được biểu diễn như sau:
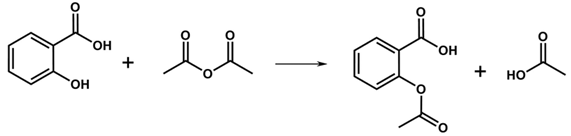
a) Có thể thay H2SO4 đặc bằng H3PO4 đặc.
b) Ở bước 2, chất rắn thu được chưa tinh khiết; bước 3 có vai trò loại bỏ acetic acid.
c) Phương pháp tinh chế được sử dụng ở thí nghiệm trên là phương pháp kết tinh lại.
d) Hiệu suất của phản ứng tổng hợp aspirin ở thí nghiệm trên là 56%.
d) Phương pháp tinh chế được sử dụng ở thí nghiệm trên là phương pháp kết tinh lại.
(Xem giải) Câu 22. Nhựa là một loại vật liệu có nhiều ứng dụng trong đời sống. Dưới đây chai hoặc các vật dụng bằng nhựa thường có kí hiệu các con số (như hình bên). Số 2 là kí hiệu của nhựa làm từ polymer X, loại nhựa mềm, nóng chảy trên 110°C, có tính khá trơ với môi trường acid, kiềm, dầu mỡ, được dùng phổ biến làm màng mỏng, bình chứa. Số 3 là kí hiệu của nhựa làm từ polymer Y, loại nhựa này được sử dụng để sản xuất ống nhựa dẫn nước, vách che mưa. Ở nhiệt độ cao, nhựa làm từ polymer Y bị phân hủy, có mùi hôi và gây ngộ độc.

a) Nhựa làm từ polymer X được đánh giá an toàn cho sức khỏe, có thể sản xuất đồ dùng đựng thực phẩm (ở điều kiện thường).
b) Nhựa làm từ polymer Y được sử dụng để sản xuất đồ dùng bọc thực phẩm hoặc sử dụng trong lò vi sóng.
c) Polymer Y được điều chế bằng phản ứng trùng ngưng vinyl chloride.
d) Polymer X được điều chế bằng phản ứng trùng hợp ethylene.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Thủy phân hoàn toàn tripeptide X thu được hai amino acid là gly, ala. Mặt khác, thủy phân không hoàn toàn X thu được dipeptide ala-gly. Có tối đa bao nhiêu công thức cấu tạo có thể có của tripeptide X?
(Xem giải) Câu 24. Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4 dưới đây:
(1) CH3CHO + 2[Ag(NH3)2]OH (t°) → CH3COONH4 + 2Ag + 3NH3 + H2O
(2) CH3CHO + 3I2 + 4NaOH → CHI3 + HCOONa + 3NaI + 3H2O
(3) CH3COOH + NaOH → CH3COONa + H2O
(4) CH3COOH + C2H5OH (H2SO4 đặc, t°) ⇋ CH3COOC2H5 + H2O
Gán số thứ tự phương trình hoá học của các phản ứng lần lượt theo tên gọi: Phản ứng với thuốc thử Tollens, phản ứng trung hòa acid – base, phản ứng ester hóa, phản ứng tạo iodoform và sắp xếp theo trình tự thành dãy bốn số. (ví dụ: 1234, 4321,…).
(Xem giải) Câu 25. Trong nước thải của một nhà máy, hàm lượng ion ammonium là 192 mg/L. Để xử lí ion ammonium đến nồng độ cho phép không vượt quá 5 mg/L (theo quy chuẩn Việt Nam), người ta tiến hành xử lí nước thải theo phương pháp Anammox (Anaerobic Ammonium Oxidation). Phương pháp này gồm 2 giai đoạn:
• Giai đoạn 1: Oxi hóa ion ammonium thành ion nitrite theo phản ứng sau: (HCO3- dùng dư 10% so với lượng phản ứng)
2NH4+ + 3O2 + 4HCO3- → 2NO2- + 4CO2 + 6H2O
• Giai đoạn 2: Diễn ra trong điều kiện yếm khí, ion ammonium sẽ được oxi hóa trực tiếp thành khí nitrogen theo phản ứng:
NH4+ + NO2- → N2 + 2H2O
Biết các phản ứng xảy ra hoàn toàn. Tính khối lượng (kg) NaHCO3 tối thiểu cần dùng để xử lí 1000 m³ nước thải trên (kết quả các phép tính trung gian không làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
(Xem giải) Câu 26. Trong hợp chất CH≡C-CH2-CH3 có bao nhiêu liên kết σ?
(Xem giải) Câu 27. Nescafe đã sản xuất thành công lon coffee tự làm nóng. Để làm nóng coffee, chỉ cần ấn nút (trên lon) để trộn nguyên liệu gồm dung dịch KOH hoặc NaOH rất loãng và CaO; 210 mL coffee trong lon sẽ được hâm nóng đến khoảng 40°C. Giả sử nhiệt dung riêng của coffee là 4,18 J/g.K (Nhiệt dung riêng là nhiệt lượng cần cung cấp để 1 gam chất tăng lên 1°C). Cho  (kJ.mol-1) của CaO, H2O(l), Ca(OH)2 lần lượt là -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Tính khối lượng CaO theo gam cần cung cấp để làm nóng 210 mL coffee từ 10°C đến 40°C (d = 1,0 g/ml). (làm tròn kết quả đến hàng phần chục)
(kJ.mol-1) của CaO, H2O(l), Ca(OH)2 lần lượt là -635; -286; -985; các giá trị này không đổi trong khoảng nhiệt độ đang xét. Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Tính khối lượng CaO theo gam cần cung cấp để làm nóng 210 mL coffee từ 10°C đến 40°C (d = 1,0 g/ml). (làm tròn kết quả đến hàng phần chục)
(Xem giải) Câu 28. Trong công nghiệp, người ta tách Al bằng phương pháp điện phân nóng chảy Al2O3 với điện cực bằng than chì. Để sản xuất được 1 tấn Al thì lượng than chì bị tiêu hao là x tấn và lượng bauxite Al2O3.2H2O là y tấn. Biết khí thoát ra ở anode gồm 40% CO và 60% CO2 về thể tích. Al2O3 được tách hoàn toàn từ quặng và hiệu suất quá trình điện phân là 90%. Tính tổng giá trị (x + y). (Kết quả làm tròn đến hàng phần trăm).
Chú ý: Do không có đề gốc nên một số bài đọc không hiểu được đề (do lỗi đánh máy) sẽ được thay thế bằng bài khác tương đương.


Câu nào đề chưa rõ Ad coi trong file này ( file này do Nguyễn Anh Phong gõ lại)
https://drive.google.com/file/d/1PYS-oBuUEFjyt-sDQ9NEEgRlfRdCuw5R/view?usp=sharing
Nhiều đề gần đây nhìn rất đẹp nhưng làm mới thấy, chữ nghĩa câu văn lộn xộn hết, vừa làm vừa đoán đề