[2024 – 2025] Thi học sinh giỏi lớp 12 – Tỉnh Khánh Hòa
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Danh sách đề học sinh giỏi năm 2024-2025
⇒ Tổng hợp đề học sinh giỏi theo năm học
⇒ Mã đề 039-H12C năm 2024-2025
⇒ Thời gian làm bài: 180 phút
Câu 1. (2,00 điểm):
(Xem giải) 1. Người ta thường tách bromine trong rong biển bằng cách sục khí chlorine vào dung dịch chiết chứa ion bromide. Phương trình ion thu gọn của phản ứng như sau:
2Br- (aq) + Cl2 (aq) → 2Cl- (aq) + Br2 (aq)
Biết enthalpy tạo thành chuẩn ![]() (kJ/mol) trong bảng:
(kJ/mol) trong bảng:
| Br- (aq) | Cl- (aq) | Br2 (aq) | Cl2 (aq) | |
| -121,55 | -167,16 | -2,16 | -17,30 |
a) Tính biến thiên enthalpy của phản ứng.
b) Phản ứng có thuận lợi về năng lượng không? Vì sao?
c) Kỹ thuật chụp PET-CT nhằm phát hiện vị trí các tế bào có tốc độ tiêu thụ glucose lớn thường là tế bào ung thư. Dược chất F-FDG trong chụp PET-CT được tạo ra khi thay nhóm -OH trong phân tử glucose bằng nguyên tử đồng vị của flourine (F) được đánh dấu. Nguyên tử khối của F trong F-FDG có giá trị bằng bao nhiêu?
(Xem giải) 2. Trong một bình kín có thể tích 1,0 lít chứa 0,5 mol H2 và 0,3 mol I2. Nung nóng bình đến nhiệt độ 430°C xảy ra phản ứng: H2(g) + I2(g) ⇋ 2HI(g) Kc = 54.
Tính nồng độ mol/L của các chất khi hệ đạt đến trạng thái cân bằng. Sau khi phản ứng đạt đến trạng thái cân bằng ở nhiệt độ 430°C, nếu giảm thể tích bình thì nồng độ mol/L của các chất trong bình có thay đổi không? Giải thích.
Câu 2. (2,00 điểm):
(Xem giải) 1. Hiện nay, mưa acid, hiệu ứng nhà kính và thủng tầng ozone là ba thảm họa môi trường toàn cầu. Một trong những tác nhân chủ yếu gây ra mưa acid là sulfur dioxide.
a) Trong bản tin dự báo thời tiết, lượng mưa tại một địa điểm là 1,0 mm nghĩa là trên diện tích 1m² có 1 lít nước mưa rơi xuống. Một cơn mưa acid xuất hiện ở khu công nghiệp có diện tích 10 km², lượng mưa trung bình 80 mm và nồng độ H2SO4 trong nước mưa là 2.10^-5 M. Tính thể tích nước mưa đã rơi xuống và khối lượng H2SO4 trong lượng nước mưa.
b) Acid trong nước mưa có thể ăn mòn các công trình bằng đá vôi. Tính khối lượng CaCO3 tối đa bị ăn mòn bởi lượng acid trên.
c) Hiện nay, hầu hết các nhà máy nhiệt điện thường thải ra các chất khi gây ô nhiễm môi trường. Nếu một nhà máy nhiệt điện thải ra 5429 lít SO2 mỗi ngày thì cần phải dùng bao nhiêu kilogam MgO để loại bỏ hết lượng SO2?
(Xem giải) 2. Hợp chất MX2 có trong một loại quặng phổ biến trong tự nhiên. Hòa tan MX2 trong dung dịch HNO3 đặc, nóng thu được dung dịch A. Cho dung dịch BaCl2 dư vào A thu được kết tủa trắng, cho A tác dụng với dung dịch NH3 dư thu được kết tủa màu đỏ nâu.
a) Xác định hợp chất MX2 và viết các phương trình phản ứng xảy ra.
b) Nước ở các khe suối, nơi có nhiều lượng chất MX2 thường có pH thấp. Giải thích hiện tượng này bằng phương trình phản ứng hóa học.
(Xem giải) Câu 3. (1,75 điểm):
Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 ml dung dịch X. Lấy chính xác 10 ml dung dịch X, thêm 10 ml dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như sau:
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích dung dịch KMnO4 (mL) | 16,0 | 16,1 | 16,0 |
a) Viết phương trình phản ứng chuẩn độ và cho biết vai trò của dung dịch H2SO4 trong thí nghiệm. Có thể thay dung dịch H2SO4 bằng dung dịch HCl hoặc HNO3 (ở cùng nồng độ) được
không? Vì sao?
b) Tính độ tinh khiết của muối Mohr trên.
Câu 4. (2,25 điểm):
(Xem giải) 1. Khí hóa lỏng (LPG) – khí gas hay còn gọi là khí dầu mỏ hóa lỏng – có thành phần chính là propane và butane được đóng trong bình “Gas” để sử dụng làm nhiên liệu. Ở điều kiện thường, propane và butane là các chất khí không màu, không mùi. Tuy nhiên, để dễ vận chuyển, người ta nén thành dạng lỏng.
a) Tại sao trong các bình gas hiện nay đang được các nhà sản xuất cung cấp cho người tiêu dùng lại có mùi? Em phải làm gì khi phát hiện khí gas bị rò rỉ?
b) Hiện nay, trên thị trường Việt Nam có nhiều loại khí gas do thành phân propane, butane khác nhau. Một loại khí gas có tỉ lệ về số mol propane : butane bằng 2 : 3 (thành phần các chất khác không đáng kể). Khi sử dụng làm nhiên liệu thì toàn bộ khí gas sẽ cháy hoàn toàn theo phương trình nhiệt hóa học của phản ứng như sau:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(g) ![]() = -2220 kJ
= -2220 kJ
C4H10(g) + 13O2(g) → 4CO2(g) + 5H2O(g) ![]() = -2874 kJ
= -2874 kJ
Tính nhiệt lượng tỏa ra khi đốt cháy hoàn toàn một bình gas 12,0 kilogam ở điều kiện chuẩn. Nếu một hộ gia đình cần 6000 kJ nhiệt mỗi ngày thì sau bao nhiêu ngày sẽ sử dụng hết một bình gas trên với hiệu suất hấp thụ nhiệt 60%?
c) Tính thể tích khí gas ở điều kiện chuẩn cần dùng để làm nóng 2,0 lít nước từ 25°C tới 100°C. Biết để làm nóng 1,0 mol nước thêm 1,0°C cần một nhiệt lượng là 75,4J; hiệu suất hấp thụ nhiệt 70%.
(Xem giải) 2. Carbon monoxide thay thế oxygen trong hemoglobin bị oxi hóa theo phản ứng:
HbO2(aq) + CO(aq) ⇋ HbCO(aq) + O2(aq) Kc = 170.
Khi phân tích một mẫu không khí bị ô nhiễm, kết quả thu được (về thể tích) có thành phần carbon monoxide chiếm 0,1%, oxygen chiếm 20,0% và các khí khác; tỉ lệ oxygen và carbon monoxide hòa tan trong máu giống với tỉ lệ của chúng trong không khí.
a) Xác định tỉ lệ về nồng độ mol HbCO so với HbO2 trong máu.
b) Dựa vào số liệu trên em có nhận xét gì về tính độc của khí CO?
Câu 5. (2,00 điểm):
(Xem giải) 1. Tiến hành thí nghiệm sau: cho hỗn hợp A gồm benzoic acid và phenol vào dung dịch NaHCO3 dư, lắc kỹ một thời gian, sau đó để yên rồi tách riêng phần dung dịch và chất không tan. Cho phần dung dịch vào phễu chiết, thêm dung dịch HCl dư, làm lạnh hỗn hợp, thêm tiếp hexane vào và lắc đều. Để yên phễu chiết để hỗn hợp phân thành 2 lớp.
a) Viết các phương trình hóa học đã xảy ra.
b) Trong thí nghiệm trên, có thể thay NaHCO3 bằng Na2CO3 được không? Vì sao?
(Xem giải) 2. Calcium là vi chất quan trọng trong cơ thể con người. Cơ thể người cần calcium dễ xây dựng và giữ cho xương chắc khỏe. Bên cạnh đó, tim, cơ, thần kinh cũng cần calcium để đảm bảo hoạt động tối ưu. Cho biết 1 mol calcium chiếm thể tích là 25,87 cm³ (các nguyên tử calcium được xem có dạng hình cầu, chiếm 74% thể tích tinh thể, còn lại là các khe trống).
Tính bán kính của nguyên tử calcium.
Câu 6. (3,25 điểm):
(Xem giải) 1. Thực hiện phản ứng reforming heptane thu được hỗn hợp sản phẩm có chứa ba hydrocarbon X1, X2, X3. Trong phân tử X1 có chứa vòng benzene, X2 là hợp chất no mạch hở có chứa một nguyên tử carbon bậc III và một nguyên tử carbon bậc IV. Hydrogen hóa hoàn toàn X1 thu được X3. Hợp chất X1 phản ứng với bromine trong điều kiện chiếu sáng thu được dẫn xuất monobromo X4, còn trong điều kiện đun nóng với xúc tác iron (III) bromide thì thu được dẫn xuất monobromo X5, X6. Khi đun nóng X1 với dung dịch potassium permanganate thu được hợp chất hữu cơ X7. X1 phản ứng với hỗn hợp nitric acid và sulfuric acid thu được hợp chất X8, là thành phần chính của một loại thuốc nổ.
Xác định các chất X1, X2, X3, X4, X5, X6, X7, X8.
(Xem giải) 2. Trinitroglycerol (TNG) là hợp chất nguy hiểm, thành phần chính trong thuốc súng không khói và được sử dụng làm chất nổ thương mại. TNG được điều chế bằng các hóa chất glycerol, H2SO4 đặc, HNO3 đặc và ở điều kiện nhiệt độ 10°C.
a) Viết phương trình phản ứng điều chế TNG và phản ứng cháy nổ xảy ra từ TNG.
b) Vì sao không được để hỗn hợp điều chế TNG ở nhiệt độ cao và cũng không được để ở nhiệt độ quá thấp?
c) Để sản xuất 10 tấn thuốc nổ chứa 90% TNG từ glycerol cần m tấn mỡ động vật có chứa các chất béo theo tỉ lệ khối lượng tương ứng tristearin : tripalmitin : triolein = 3 : 4 : 3. Biết hiệu suất toàn bộ quá trình là 80%. Tính giá trị của m.
Câu 7. (3,00 điểm):
(Xem giải) 1. Thủy phân hoàn toàn một triglyceride X trong dung dịch NaOH dư thu được glycerol và hai muối sodium stearate, sodium oleate. Viết các công thức cấu tạo của X và giải thích tại sao khi để dầu, mỡ chứa chất X trong không khí một thời gian sẽ bị ôi thiu? Em hãy để xuất 2 cách bảo quản (không dùng hóa chất) để làm chậm quá trình ôi thiu của loại dầu, mỡ trên và cho biết mỗi cách đó dựa trên nguyên tắc nào?
(Xem giải) 2. Carbohydrate là những hợp chất hữu cơ thiên nhiên có nhiều ứng dụng trong đời sống và sản xuất.
a) Viết các dạng công thức cấu tạo của glucose và phương trình phản ứng của glucose với thuốc thử Tollens và với CH3OH/khí HCl.
b) Ethanol dùng để sản xuất xăng sinh học E5 (xăng chứa 5% ethanol về thể tích) được tạo ra từ cellulose theo sơ đồ: Cellulose → Glucose → Ethanol (hiệu suất tương ứng 80% và 81%). Để tạo ra lượng ethanol đủ sản xuất được 2300 lít xăng E5 thì cần x kilogam mùn cưa (chứa 50% cellulose, các chất còn lại không tạo ra được ethanol). Biết D ethanol = 0,8 g/mL. Viết phương trình học của phản ứng theo sơ đồ trên và tính giá trị x.
Câu 8. (1,75 điểm):
(Xem giải) 1. Insulin là hormone của cơ thể có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide (X). Khi thủy phân không hoàn toàn X thu được hỗn hợp các peptide sau: Ser-His-Leu; Val-Glu-Ala; His-Leu-Val; Gly-Ser-His. Xác định công thức của peptide (X)
(Xem giải) 2. Hợp chất A là một α-amino acid. Phổ MS của ester B (được điều chế từ A và ethanol) xuất hiện peak của ion phân tử [M+] có giá trị m/z = 117.
a) Xác định các chất A và B.
b) Trong môi trường acid mạnh (pH khoảng 1 – 2) amino acid A tồn tại chủ yếu ở dạng nào? Nếu đặt hai điện cực của nguồn điện một chiều vào dung dịch A, ion trong dung dịch sẽ dịch chuyển như thế nào?
Câu 9. (2,0 điểm):
(Xem giải) 1. Viết phương trình phản ứng hóa học để hoàn thành sơ đồ sau:
(1) X + NaOH (t°) → X1 + X2 + H2O
(2) X1 + H2SO4 (t°) → Na2SO4 + X3
(3) nX2 + nX4 (t°) → poly(hexamethylene adipamide) + 2nH2O
(4) nX3 + nX5 (t°) → poly(ethylene terephthalate) + 2nH2O
(Xem giải) 2. Ascorbic acid (vitamin C) là một acid hữu cơ được kí hiệu đơn giản là HAsc. Hàm lượng HAse trong các loại đồ uống thể thao có thể xác định được bằng cách chuẩn độ với dung dịch iodine. Phương trình phản ứng có thể được biểu diễn như sau:
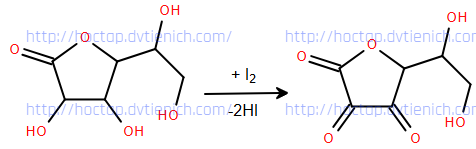
a) Xác định công thức phân tử của HAsc.
b) Tính pH của dung dịch khi hòa tan 10 gam HAsc vào 500 mL nước. Biết HAsc có hằng số phân li Ka1 = 7,9.10^-5; Ka2 = 10^-12 cho quá trình ion hóa thứ hai. Xem thể tích của dung dịch thay đổi không đáng kể.
c) Lấy 25 mL một mẫu đồ uống thể thao tiến hành chuẩn độ thì cần dùng 29,25 mL dung dịch I2 0,00125 M để đạt đến điểm tương đương. Xác định khối lượng HAsc (bằng mg) trong chai đồ uống thể thao chứa 350 mL dung dịch.


Bình luận