[2025] Thi thử TN sở GDĐT Ninh Bình (Lần 3)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 095
⇒ Đề thi, đáp án và giải chi tiết:
| 1A | 2B | 3B | 4A | 5A | 6D | 7D | 8B | 9B |
| 10A | 11B | 12B | 13D | 14A | 15A | 16B | 17D | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | Đ | S | 2,41 | 49,7 | 1 |
| (b) | Đ | Đ | Đ | Đ | 26 | 27 | 28 |
| (c) | S | S | Đ | Đ | 0,93 | 174 | 1,2 |
| (d) | S | Đ | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Một nhà máy sản xuất vôi sống từ đá vôi với lò nung vôi công nghiệp sử dụng than đá làm nhiên liệu. Để phân hủy 1 kg đá vôi cần cung cấp lượng nhiệt là 1800kJ. Khi đốt cháy 1 kg than đá giải phóng ra lượng nhiệt là 27000kJ, lượng nhiệt này được hấp thụ 50% ở quá trình phân hủy đá vôi. Biết công suất của lò nung vôi là 42 tấn vôi sống/ngày. Giả thiết đá vôi chỉ chứa CaCO3. Tổng khối lượng đá vôi và than đá mà lò nung vôi đó đã sử dụng trong 2 ngày là m tấn, giá trị của m gần nhất với giá trị nào sau đây?
A. 170. B. 85. C. 174. D. 79.
(Xem giải) Câu 2. Khi nhựa polystyrene (PS) bị cháy sẽ sinh ra nhiều khí độc. Cho các phát biểu sau về đám cháy có nhựa PS cháy:
(a) Đeo mặt nạ phòng độc có thể hạn chế hít phải khí độc.
(b) Không được cúi thấp người khi thoát khỏi đám cháy.
(c) Khói của cháy nhựa PS độc hại hơn khói của đám cháy gỗ.
(d) Dùng nước chữa cháy nhằm giảm sự lan rộng của đám cháy.
Số phát biểu đúng là
A. 2. B. 3. C. 4. D. 1.
(Xem giải) Câu 3. Phát biểu nào sau đây là không đúng?
A.Trong phân tử alkane chỉ có liên kết đơn.
B. Chỉ các alkane là chất khí ở điều kiện thường được dùng làm nhiên liệu.
C. Các alkane lỏng được dùng sản xuất xăng và làm dung môi.
D. Các alkane rắn được dùng làm sáp, nến,….
(Xem giải) Câu 4. Nhà máy phân đạm Ninh Bình có sản xuất ra thị trường một loại urea như sau:

Khối lượng nitrogen tối thiểu có trong hai bao urea như trên là bao nhiêu kg?
A. 46,30. B. 23,15. C. 1,01. D. 0,41.
(Xem giải) Câu 5. Ester X có tên gọi là ethyl acetate. X là chất lỏng, có mùi đặc trưng, được sản xuất ở quy mô lớn làm dung môi trong công nghiệp. Công thức của X là
A. CH3COOC2H5. B. C3H7COOC2H5. C. C2H5COOC2H5. D. HCOOCH3.
(Xem giải) Câu 6. Chất nào sau đây thuộc loại disaccharide?
A. Fructose. B. Cellulose. C. Tinh bột. D. Saccharose.
(Xem giải) Câu 7. Chất nào sau đây tạo kết tủa trắng với nước bromine?
A. Glucose. B. Ethanal. C. Ethyl acetate. D. Aniline.
(Xem giải) Câu 8. Phát biểu nào sau đây đúng?
A. Protein ít tan trong nước lạnh, tan nhiều trong nước nóng.
B. Các protein đơn giản thủy phân đến cùng thu được các α-amino acid.
C. Dipeptide có phản ứng màu biuret.
D. Trong phân tử Gly-Ala-Gly có 3 liên kết peptide.
(Xem giải) Câu 9. Catechin là một chất kháng oxi hoá mạnh, ức chế hoạt động của các gốc tự do nên có khả năng phòng chống bệnh ung thư, nhồi máu cơ tim. Trong lá chè tươi, catechin chiếm khoảng 25% đến 35% tổng trọng lượng. Công thức cấu tạo của catechin như hình bên:
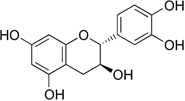
Cho các phát biểu sau:
(a) Catechin thuộc loại hợp chất hữu cơ tạp chức.
(b) Catechin có khả năng phòng chống các bệnh ung thư, tim mạch.
(c) Một phân tử catechin chứa 16 nguyên tử hydrogen.
(d) Phân tử catechin có phản ứng vừa đủ với dung dịch NaOH theo tỉ lệ mol tương ứng là 1:3.
Số phát biểu đúng là
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 10. Chất nào sau đây có thể tham gia phản ứng trùng hợp?
A. Ethylene. B. Butane. C. Toluene. D. Xylene.
(Xem giải) Câu 11. Trong công nghiệp, phương pháp điện phân nóng chảy được sử dụng để sản xuất một lượng đáng kể kim loại nào sau đây?
A. Ag. B. Al. C. Fe. D. Cu.
(Xem giải) Câu 12. Một pin điện hóa tạo bởi hai cặp oxi hóa – khử ở điều kiện chuẩn: Fe2+/Fe và Cu2+/Cu với thế điện cực chuẩn tương ứng là -0,440 V và 0,340 V. Cho các phát biểu về pin điện hóa trên như sau:
(1) Anode của pin là Fe2+.
(2) Cathode của pin là Cu.
(3) Quá trình xảy ra ở anode khi pin hoạt động là: Fe → Fe2+ + 2e.
(4) Quá trình xảy ra ở cathode khi pin hoạt động là: Cu2+ + 2e → Cu.
(5) Sức điện động chuẩn của pin đó là 0,780 V.
Số phát biểu đúng là
A. 3. B. 4. C. 1. D. 2.
(Xem giải) Câu 13. Kim loại tungsten (W) được sử dụng làm dây tóc bóng điện như hình vẽ sau:

Ứng dụng này được dựa trên cơ sở tính chất vật lí nào sau đây của tungsten?
A. Tính dẫn nhiệt thấp. B. Tỉ trọng nhỏ.
C. Tính dẻo cao. D. Nhiệt độ nóng chảy cao.
(Xem giải) Câu 14. Kim loại copper (Cu) không thể tác dụng với dung dịch nào sau đây?
A. FeCl2. B. AgNO3. C. HNO3. D. FeCl3.
(Xem giải) Câu 15. Một loại pháo hoa có chứa một số thành phần như sodium nitrate, sodium oxalate. Khi cháy, loại pháo hoa này sẽ tạo ra màu gì trên bầu trời đêm?
A. vàng. B. xanh. C. đỏ. D. tím.
(Xem giải) Câu 16. Cấu hình electron ở phân lớp ngoài cùng của ion R2+ là 2p6. Nguyên tử R là
A. Ne (Z = 10). B. Mg (Z = 12). C. Na (Z = 11). D. Ca (Z = 20).
(Xem giải) Câu 17. Kim loại nào sau đây là kim loại chuyển tiếp dãy thứ nhất?
A. Na. B. K. C. Ba. D. Sc.
(Xem giải) Câu 18. Số oxi hoá của nguyên tử trung tâm trong phức chất [Co(NH3)4(OH2)2]SO4 là
A. +3. B. +6. C. +2. D. +4.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Một chất béo X là thành phần chính của một loại dầu thực vật và có công thức cấu tạo như sau:
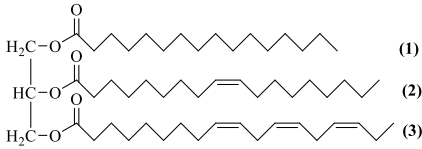
a) Công thức phân tử của X là C55H96O6 và ở điều kiện thường X là chất lỏng.
b) Có thể sử dụng chất béo X để cung cấp acid béo omega-9 cho cơ thể.
c) Trong X, các gốc acid béo không no đều có cấu hình trans-.
d) Bơ nhân tạo thường được tạo ra bằng cách hydrogen hóa dầu thực vật, làm tăng độ bão hòa của chất béo, giúp bảo quản lâu hơn. Tiến hành hydrogen hóa 427 kg X ở nhiệt độ cao, có Ni xúc tác thu được 344,8 kg chất béo no (biết hiệu suất phản ứng là 90%).
(Xem giải) Câu 20. Để xác định hàm lượng Fe2+ trong một lọ muối Mohr (có công thức (NH4)2SO4.FeSO4.6H2O) người ta tiến hành thí nghiệm như sau: Cân chính xác 10,0 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 5 mL dung dịch H2SO4 loãng nồng độ 20%, được dung dịch Y. Chuẩn độ chính xác dung dịch Y bằng dung dịch chuẩn KMnO4 0,02M. Thực hiện chuẩn độ 3 lần, kết quả thu được như sau:
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích dung dịch KMnO4 (mL) | 19,9 | 20,1 | 20,0 |
a) Dung dịch H2SO4 loãng được thêm vào nhằm tạo môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành Mn2+.
b) Thời điểm kết thúc chuẩn độ là lúc dung dịch xuất hiện màu hồng ổn định khoảng 20 giây.
c) Khi để trong không khí lâu ngày thì hàm lượng FeSO4 trong muối Mohr sẽ không thay đổi.
d) Hàm lượng (% khối lượng) Fe2+ trong mẫu muối Mohr đem phân tích ở trên là 11,2%.
(Xem giải) Câu 21. Một mẫu nước cứng có chứa đồng thời các ion Ca2+, HCO3- và Cl-.
a) Nước cứng làm giảm tác dụng của xà phòng; làm hại quần áo.
b) Mẫu nước cứng trên có tính cứng toàn phần.
c) Dùng soda sẽ làm mềm được mẫu nước cứng trên.
d) Theo quy ước, một đơn vị độ cứng ứng với 0,5 milimol Ca2+ hoặc Mg2+ trong 1,0 lít nước. Để làm mềm 10 lít nước cứng trên cần dùng vừa đủ 50 mL dung dịch chứa NaOH 0,2M và Na3PO4 0,2M. Số đơn vị độ cứng của mẫu nước trên là 5.
(Xem giải) Câu 22. Sorbic acid (hexa-2,4-dienoic acid) có thể được dùng làm chất bảo quản trong một số loại thực phẩm. Theo thông tư 24/2019/TT-BYT về mức sử dụng tối đa phụ gia trong thực phẩm (ML) thì giá trị ML của sorbic acid là 1000 mg.kg-1 đối với đồ uống từ sữa dạng lỏng có hương vị.
a) Công thức phân tử của sorbic acid là C6H8O4 .
b) Sorbic acid có thể tham gia phản ứng cộng.
c) Khi cho 16,8 gam sorbic acid phản ứng hoàn toàn với dung dịch KOH dư sẽ thu được 22,5 gam potassium sorbate.
d) Khi phân tích một lô sữa tươi có khối lượng 180 gam/hộp, thu được kết quả thành phần trong hộp sữa có 150,5 mg sorbic acid. Vậy lô sữa tươi này có lượng sorbic acid nằm trong mức cho phép theo thông tư 24/2019/TT-BYT.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Tiến hành sản xuất 2000 chai rượu vang 12° dung tích 750 mL bằng phương pháp lên men rượu với nguyên liệu là m tấn quả nho tươi (chứa 18% glucose về khối lượng).

Biết khối lượng riêng của ethyl alcohol là 0,8 g/mL. Giả thiết trong thành phần quả nho tươi chỉ có glucose bị lên men rượu; hiệu suất toàn bộ quá trình sản xuất là 65%. Giá trị của m là bao nhiêu (chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng phần trăm)?
(Xem giải) Câu 24. Magnesium (Mg) là kim loại được ứng dụng để tạo các hợp kim nhẹ, bền, đặc biệt là cho ngành công nghiệp sản xuất ô tô và hàng không vũ trụ. Magnesium được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite (chứa 92% MgCO3.CaCO3 còn lại là tạp chất). Quá trình được thực hiện qua các giai đoạn sau:
Giai đoạn 1: Nung quặng dolomite:
MgCO3.CaCO3(s) (t°) → MgO(s) + CaO(s) + 2CO2(g)
Giai đoạn 2: Dùng Si trong ferrosilicon (Fe, Si) làm chất khử trong điều kiện chân không :
2MgO(s) + 2CaO(s) + Si(s) (t°) → 2Mg(g) + Ca2SiO4(s)
Nếu hiệu suất của mỗi phản ứng đều là 91% thì cứ 500 kg quặng dolomite trên sẽ điều chế được bao nhiêu kg magnesium (chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng phần mười).
(Xem giải) Câu 25. Để bảo vệ vật bằng thép khỏi bị ăn mòn, trong thực tế người ta đã thực hiện một số cách sau:
(1) Sơn kín bề mặt cánh cửa làm bằng thép.
(2) Tráng kẽm lên bề mặt tấm thép mỏng khi sản xuất tôn.
(3) Hàn những khối kẽm lên vỏ tàu làm bằng thép.
(4) Mạ chromium lên bề mặt thép để làm vật liệu chế tạo các dụng cụ y tế.
Trong các cách trên, có bao nhiêu cách sử dụng phương pháp điện hóa?
(Xem giải) Câu 26. NaHCO3 là chất có độ tan kém nên dễ bị kết tinh. Độ tan của NaHCO3 trong 100 gam nước ở 20°C và 40°C lần lượt là 9,6 gam và 12,7 gam. Làm lạnh 33,81 tấn dung dịch NaHCO3 bão hòa ở 40°C về 20°C thì khối lượng muối NaHCO3 kết tinh là m tấn (giả thiết không có sự bay hơi của nước). Tính m (chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 27. Theo QCVN 01-1:2018/BYT, hàm lượng sắt tối đa cho phép trong nước sinh hoạt là 0,3 mg/L. Một mẫu nước có hàm lượng sắt cao gấp 40 lần ngưỡng cho phép, giả thiết sắt trong mẫu nước tồn tại ở dạng Fe2(SO4)3 và FeSO4 với tỉ lệ mol tương ứng là 1 : 8. Quá trình tách loại sắt trong 10 m³ mẫu nước trên được thực hiện bằng cách sử dụng m gam vôi tôi (vừa đủ) để tăng pH, sau đó sục không khí:
Fe2(SO4)3 + Ca(OH)2 → Fe(OH)3 + CaSO4 (1)
FeSO4 + Ca(OH)2 + O2 + H2O → Fe(OH)3 + CaSO4 (2)
Giả thiết vôi tôi chỉ chứa Ca(OH)2. Giá trị của m là bao nhiêu (chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng đơn vị)?
(Xem giải) Câu 28. Eugenol là một hợp chất thiên nhiên được tìm thấy trong một số loại cây như quế, đinh hương… Thành phần phần trăm về khối lượng các nguyên tố trong eugenol là 73,17% carbon; 7,31% hydrogen, còn lại là oxygen. Kết quả phân tích phổ MS cho thấy phân tử khối của eugenol là 164. Eugenol tác dụng được với Na và NaOH. Eugenol không có đồng phân hình học. Hydrogen hoá hoàn toàn 0,3 mol eugenol cần x mol khí H2 (Ni, t°), thu được sản phẩm là 2-methoxy-4-propylcyclohexanol (nhóm methoxy có công thức là CH3O-). Giá trị của x bằng bao nhiêu (chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng phần mười)?


Bình luận