[2025] Thi thử TN sở GDĐT Bắc Giang (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 107
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2D | 3B | 4A | 5D | 6D | 7A | 8B | 9C |
| 10B | 11D | 12C | 13C | 14C | 15C | 16B | 17C | 18A |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | S | S | 1904 | 3412 | 196 |
| (b) | Đ | Đ | Đ | S | 26 | 27 | 28 |
| (c) | S | Đ | S | S | 31,5 | 12,5 | 741 |
| (d) | S | S | S | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Nguyên tố nhôm (aluminium, Al) có số hiệu nguyên tử là 13. Ở trạng thái cơ bản, số electron ở lớp ngoài cùng trong nguyên tử Al là
A. 2. B. 5. C. 3. D. 1.
(Xem giải) Câu 2. Cho tripeptide X có công thức cấu tạo như sau: H2N-CH2-CONH-CH(CH3)-CONH-CH(COOH)-CH(CH3)2. Cho các nhận định sau:
(a) Các đơn vị amino acid tạo nên X là glycine, alanine và lysine.
(b) Trong môi trường kiềm, X tác dụng với Cu(OH)2 tạo thành dung dịch màu xanh lam.
(c) Trong phân tử X, amino acid đầu N là glycine, amino acid đầu C là valine.
(d) Thuỷ phân không hoàn toàn X thu được tối đa 2 dipeptide.
Số nhận định đúng là bao nhiêu?
A. (a), (c). B. (b), (d). C. (b), (c). D. (c), (d).
(Xem giải) Câu 3. Phân tích hợp chất hữu cơ X cho thấy thành phần nguyên tố: 38,71% carbon; 9,68% hydrogen và 51,61% oxygen về khối lượng. Trên phổ khối lượng của X có peak ion phân tử M+ ứng với m/z = 62. Công thức phân tử của X là
A. C2H2O3. B. C2H6O2. C. C2H4O2. D. C3H8O.
(Xem giải) Câu 4. Chất giặt rửa tổng hợp thường là muối sodium alkylsulfate hoặc sodium alkylbenzene sulfonate, được tổng hợp hoá học và có tác dụng giặt rửa như xà phòng. Chất nào sau đây thuộc loại chất giặt rửa tổng hợp?
A. CH3[CH2]11OSO3Na. B. CH3[CH2]14COONa.
C. CH3[CH2]16COONa. D. CH3[CH2]7CH=CH[CH2]7COONa.
(Xem giải) Câu 5. Gang bị ăn mòn điện hoá trong không khí ẩm bởi sự tạo thành vô số pin điện hoá nhỏ trong đó anode là sắt và cathode là carbon. Quá trình oxi hoá sắt xảy ra trên bề mặt của gang là
A. Fe → Fe3+ + 3e. B. Fe3+ + 3e → Fe.
C. Fe2+ + 2e → Fe. D. Fe → Fe2+ + 2e.
(Xem giải) Câu 6. Cho amine X có công thức:
![]()
Nhận định nào sau đây về X không đúng?
A. Danh pháp thay thế của X là N-methylethanamine.
B. X thuộc loại amine bậc hai.
C. Trong dung môi nước, X là một base yếu.
D. X tác dụng với dung dịch HNO2/HCl giải phóng N2.
(Xem giải) Câu 7. Độ dinh dưỡng của phân đạm được đánh giá theo tỉ lệ phần trăm về khối lượng của nguyên tố nitrogen. Loại phân đạm nào sau đây có độ dinh dưỡng lớn nhất?
A. Urea: (NH2)2CO. B. Ammonium chloride: NH4Cl.
C. Ammonium nitrate: NH4NO3. D. Ammonium sulfate: (NH4)2SO4.
(Xem giải) Câu 8. Trong công nghiệp luyện kim, phương pháp chung để tách các kim loại hoạt động mạnh như Na, K, Mg, Ca, Al,… là
A. điện phân dung dịch. B. điện phân nóng chảy.
C. thuỷ luyện. D. nhiệt luyện.
(Xem giải) Câu 9. Phát biểu nào sau đây không đúng?
A. Polypeptide có phản ứng màu biuret với Cu(OH)2 trong môi trường kiềm.
B. Protein trong thức ăn giúp bổ sung các amino acid thiết yếu cho cơ thể.
C. Dung dịch α-aminopropionic acid làm quỳ tím chuyển sang màu đỏ.
D. Trùng ngưng ε-aminocaproic acid thu được polymer thuộc loại polyamide.
(Xem giải) Câu 10. Phản ứng monochlorine hoá methane có phương trình hoá học:
(I) CH4 + Cl2 → CH3Cl + HCl
Giai đoạn tạo thành sản phẩm trong cơ chế của phản ứng (I) xảy ra như sau:
(II) •CH3 + Cl2 → CH3Cl + Cl•
Nhận định nào sau đây đúng?
A. Phản ứng (I) thuộc loại phản ứng cộng.
B. Trong giai đoạn (II), có sự tạo thành liên kết cộng hoá trị phân cực.
C. Trong giai đoạn (II), có sự hình thành liên kết π.
D. Trong phản ứng (I), dẫn xuất halogen tạo thành là chloroform.
(Xem giải) Câu 11. Ester methyl methacrylate là nguyên liệu để tổng hợp poly(methyl methacrylate), polymer được sử dụng để chế tạo thuỷ tinh hữu cơ plexiglas. Công thức của methyl methacrylate là
A. CH3COOC2H5. B. C2H5COOC2H5.
C. CH2=CHCOOCH3. D. CH2=C(CH3)COOCH3.
(Xem giải) Câu 12. Tiến hành điện phân dung dịch CuSO4 trong môi trường H2SO4, sử dụng anode bằng kim loại đồng (copper), cathode bằng điện cực trơ và dòng điện một chiều có cường độ không đổi. Nhận xét nào sau đây không đúng?
A. Ở cathode xảy ra quá trình khử ion Cu2+ thành kim loại Cu.
B. Ở anode xảy ra quá trình oxi hóa kim loại Cu thành ion Cu2+.
C. Ở cathode xảy ra quá trình khử ion H+ trước ion Cu2+.
D. Khối lượng anode giảm dần, khối lượng cathode tăng dần.
(Xem giải) Câu 13. Cho ester X có công thức:

Nhận định nào sau đây không đúng?
A. X có công thức phân tử là C4H8O2.
B. X có tên gọi là methyl propionate.
C. X tạo thành từ acetic acid và ethyl alcohol.
D. X bị thuỷ phân trong môi trường acid hoặc base.
(Xem giải) Câu 14. Một pin điện hoá Ni – H2 được thiết lập ở điều kiện chuẩn như hình vẽ sau. Cho thế điện cực chuẩn của cặp Ni2+/Ni bằng -0,257V.
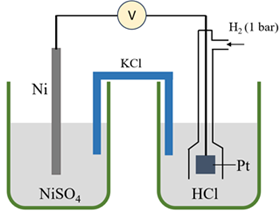
Cho các nhận định sau khi pin hoạt động:
(a) Số chỉ hiển thị trên vôn kế là -0,257V.
(b) Ở anode xảy ra quá trình oxi hoá Ni, ở cathode xảy ra quá trình khử H+.
(c) Ở cầu muối có sự di chuyển của ion K+ đi vào dung dịch HCl và ion Cl- đi vào dung dịch NiSO4.
(d) Khối lượng thanh Ni giảm dần, khối lượng thanh Pt không đổi.
Số nhận xét đúng là
A. 4. B. 1. C. 3. D. 2.
(Xem giải) Câu 15. Cho 1 mL dung dịch AgNO3 1% vào ống nghiệm, sau đó nhỏ từng giọt dung dịch NH3 cho đến khi kết tủa vừa xuất hiện lại tan hết. Thêm tiếp vào 1 mL dung dịch glucose 1%, đun nóng nhẹ, thấy thành ống nghiệm sáng bóng như gương. Vai trò của glucose trong thí nghiệm là
A. chất oxi hoá. B. acid. C. chất khử. D. base.
(Xem giải) Câu 16. Nổ bụi là vụ nổ gây ra bởi quá trình bốc cháy nhanh của các hạt bụi mịn phân tán trong không khí bên trong một không gian hạn chế, tạo ra sóng nổ. Nổ bụi xảy ra khi có đủ năm yếu tố: nguồn oxygen, nguồn nhiệt, nhiên liệu (bụi có thể cháy được), nồng độ bụi mịn đủ lớn và không gian đủ kín. Năm 2007, một vụ nổ bụi xảy ra khi các công nhân hàn để bảo trì lại bể chứa bột mì tại một phân xưởng sản xuất bột mì ở tỉnh Bình Dương khiến 5 công nhân bị bỏng nặng.
Cho các phát biểu sau:
(a) Nổ bụi là một vụ nổ vật lí.
(b) Vụ nổ bụi xảy ra khi có đủ các yếu tố nguồn oxygen, nguồn nhiệt, không gian đủ kín.
(c) Nhiên liệu trong vụ nổ bụi tại phân xưởng bột mì ở Bình Dương là bụi bột mì.
(d) Bất kỳ loại bụi mịn nào trong không gian kín cũng đều có khả năng gây nổ bụi.
Trong các phát biểu trên, số phát biểu đúng là
A. 3. B. 1. C. 2. D. 4.
(Xem giải) Câu 17. Nước cứng ảnh hưởng nhiều đến các hoạt động trong sản xuất và đời sống, vì vậy trong sinh hoạt và sản xuất cần làm mềm nước, tức là điều chỉnh lượng ion Ca2+ và Mg2+ trong nước xuống ngưỡng mà tại đó nước được coi là nước mềm. Cho các phát biểu:
(1) Đun sôi có thể làm mất tính cứng tạm thời của nước.
(2) Dùng Na2CO3 để làm mất tính cứng tạm thời và tính cứng vĩnh cửu của nước.
(3) Dùng HCl để làm mất tính cứng tạm thời của nước.
(4) Dùng Ca(OH)2 với lượng vừa đủ để làm mất tính cứng vĩnh cửu của nước.
Trong các phát biểu trên, những phát biểu đúng là
A. (3) và (4). B. (1), (2) và (3). C. (1) và (2). D. (1), (2) và (4).
(Xem giải) Câu 18. Khi trùng hợp buta-1,3-diene với acrylonitrile thu được polymer có cấu tạo như sau:
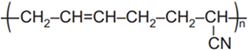
Polymer trên được dùng để sản xuất loại cao su nào sau đây?
A. Cao su buna-N. B. Cao su chloroprene.
C. Cao su buna-S. D. Cao su buna.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Trong phòng thí nghiệm, tiến hành điện phân dung dịch NaCl bão hoà với điện cực than chì để điều chế nước Javel theo sơ đồ:
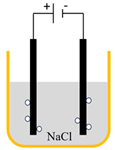
a) Dung dịch sau điện phân có khả năng diệt khuẩn và tẩy màu.
b) Khí Cl2 tác dụng với NaOH trong dung dịch tạo thành nước Javel.
c) Thứ tự điện phân ở anode là Cl-, H2O và thứ tự điện phân ở cathode là Na+, H2O.
d) Số mol khí Cl2 bay ra khỏi dung dịch bằng số mol khí H2 bay ra khỏi dung dịch.
(Xem giải) Câu 20. Một học sinh tiến hành thí nghiệm theo các bước:
• Bước 1: Cho bột Fe vào dung dịch HCl (loãng, dư) khuấy đều, lọc thu lấy dung dịch nước lọc màu xanh lá cây có chứa phức chất bát diện X.
• Bước 2: Nhỏ nước Cl2 vào nước lọc để chuyển hoá toàn bộ X thành phức chất bát diện Y màu vàng.
• Bước 3: Kết tinh dung dịch Y thu được muối Z.
Biết rằng: trong phức chất X và Y chỉ có phối tử nước, ở bước 3 toàn bộ phối tử trong Y đều chuyển vào Z.
a) X và Y đều chứa 6 phối tử nước.
b) Nguyên tử trung tâm của X, Y lần lượt là Fe2+, Fe3+.
c) Thành phần của muối Z là FeCl3.6H2O.
d) Ở bước 2, phản ứng chuyển hoá X thành Y là phản ứng thế phối tử.
(Xem giải) Câu 21. Nhiều ester có trong tự nhiên là nguyên liệu để sản xuất hương liệu, mĩ phẩm. Ester thường được điều chế bằng phản ứng ester hoá giữa carboxylic acid và alcohol với xúc tác là acid (thường dùng H2SO4 đặc) theo phương trình tổng quát như sau:
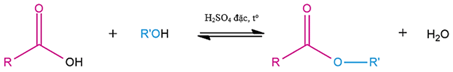
a) Có thể sử dụng phương pháp như trên (phản ứng giữa giữa carboxylic acid và alcohol với xúc tác acid) để điều chế vinyl acetate, phenyl acetate.
b) Khi thay H2SO4 đặc bằng H2SO4 loãng sẽ làm giảm hiệu suất của phản ứng ester hoá.
c) Trong phản ứng ester hóa, nguyên tử H trong nhóm -COOH của carboxylic acid được thay thế bởi gốc hydrocarbon R’.
d) Trộn a mol carboxylic acid với a mol alcohol có mặt H2SO4 đặc, rồi đun trong thời gian đủ lâu, thu được a mol ester.
(Xem giải) Câu 22. Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Cho 10 mL dung dịch H2SO4 70% vào cốc thuỷ tinh, thêm một lượng nhỏ cellulose (bông) vào cốc và dùng đũa thuỷ tinh khuấy đều. Sau đó, đặt cốc thuỷ tinh vào cốc nước nóng và khuấy trong khoảng 3 phút để cellulose tan hết tạo dung dịch đồng nhất.
• Bước 2: Trung hoà dung dịch bằng cách thêm từ từ NaHCO3 đến khi dừng sủi bọt khí, sau đó thêm tiếp 5 mL dung dịch NaOH 10%,
• Bước 3: Cho 5 mL dung dịch thu được ở trên vào ống nghiệm chứa Cu(OH)2 (được điều chế bằng cách cho 0,5 mL dung dịch CuSO4 5% vào 2 mL dung dịch NaOH 10%, lắc nhẹ). Đun nóng đều ống nghiệm khoảng 2 phút, sau đó để ống nghiệm trên giá khoảng 3 phút.
a) Ở bước 2 thêm từ từ NaHCO3 để phản ứng thủy phân diễn ra nhanh hơn.
b) Sau bước 1, thu được hai loại monosaccharide.
c) Thí nghiệm trên chứng minh cellulose có tính khử.
d) Sau bước 3, trong ống nghiệm có kết tủa đỏ gạch Cu2O.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Xà phòng hóa hoàn toàn 132,9 kg chất béo bằng dung dịch NaOH vừa đủ, thu được 13,8 kg glycerol và muối dùng để làm xà phòng. Toàn bộ lượng muối thu được ở trên được trộn với phụ gia và đóng thành k bánh xà phòng. Biết rằng mỗi bánh xà phòng nặng 100 gam trong đó muối của acid béo chiếm 72% về khối lượng. Giá trị của k bằng bao nhiêu (làm tròn kết quả đến số nguyên)?
(Xem giải) Câu 24. Cho các dung dịch có cùng nồng độ 0,1 mol/L được đánh số thứ tự như sau: (1) – alanine; (2) – glutamic acid; (3) – sodium hydroxide và (4) – lysine. Xác định bộ bốn số là dãy số thứ tự của các dung dịch được sắp xếp theo chiều pH giảm dần (ví dụ 1234, 1432,…)?
(Xem giải) Câu 25. Cho sơ đồ chuyển hoá:
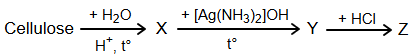
Biết X là monosaccharide; Y, Z là các hợp chất hữu cơ. Phân tử khối của Z bằng bao nhiêu?
(Xem giải) Câu 26. Hiện nay, pin nhiên liệu sử dụng hydrogen rất được quan tâm do có nguồn nhiên liệu dồi dào, sản phẩm thân thiện với môi trường. Phản ứng xảy ra khi một pin hydrogen – oxygen phóng điện ở 25°C như sau: 2H2(g) + O2(g) → 2H2O(l) ![]()
Để một pin nhiên liệu hydrogen – oxygen tạo ra điện năng 1 kWh (3600 kJ) cần tiêu thụ hết m gam hydrogen với hiệu suất quá trình oxi hoá hydrogen đạt 80%. Cho nhiệt tạo thành chuẩn của H2O(l) bằng -285,8 kJ/mol và công sinh ra của pin bằng |![]() |. Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng phần mười)?
|. Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng phần mười)?
(Xem giải) Câu 27. Trong quá trình bảo quản, muối FeSO4.7H2O thường bị oxi hoá bởi oxygen không khí tạo thành hỗn hợp X chứa các hợp chất Fe(II) và Fe(III). Để xác định lượng Fe(II) bị oxi hoá người ta hoà tan một lượng X trong dung dịch loãng chứa 0,06 mol H2SO4, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
• Thí nghiệm 1. Cho lượng dư dung dịch BaCl2 vào 25 mL dung dịch Y, lọc kết tủa, sấy khô rồi đem cân thu được 5,825 gam chất rắn.
• Thí nghiệm 2. Thêm dung dịch H2SO4 (loãng, dư) vào 25 mL dung dịch Y, thu được dung dịch Z. Chuẩn độ dung dịch Z bằng dung dịch chuẩn KMnO4 0,1 M đến khi đầu xuất hiện màu hồng (tồn tại khoảng 20 giây) thì hết 17,5 mL.
Phần trăm Fe(II) đã bị oxi hoá là a %. Tính giá trị của a (làm tròn kết quả đến hàng phần mười).
(Xem giải) Câu 28. Quy trình Downs là một phương pháp điện hoá để sản xuất kim loại sodium (Na) có thể biểu diễn theo sơ đồ:
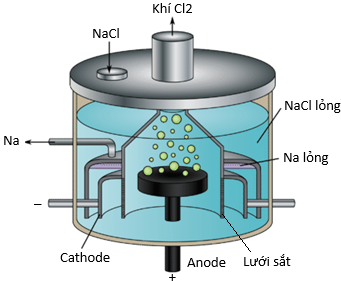
Tại một bể điện phân Downs, quá trình điện phân nóng chảy NaCl được thực hiện với cường độ dòng điện 40000 A, hiệu suất sử dụng điện năng đạt 90%. Trong mỗi ngày (24 giờ) hoạt động liên tục, bể điện phân tạo ra m kg Na ở cathode. Cho: q = It = ne F; F = 96500 C/mol. Giá trị của m bằng bao nhiêu (làm tròn kết quả đến số nguyên)?


Bình luận