[2025 – 2026] Thi học sinh giỏi lớp 12 – TP Hà Nội
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Tổng hợp đề hsg theo năm học
⇒ Mã đề 001-H12C năm 2025-2026
⇒ Thời gian làm bài: 180 phút
Câu I (4,0 điểm)
(Xem giải) 1. Nitric acid là một trong ba acid chính của công nghiệp hóa chất hiện đại.
a) Vì sao dung dịch nitric acid không màu để lâu ngoài không khí chuyển sang màu vàng?
b) Nêu cách bảo quản dung dịch nitric acid trong phòng thí nghiệm.
(Xem giải) 2. Trong cơ thể người, hemoglobin (Hb) kết hợp với khí oxygen theo phản ứng thuận nghịch được biểu diễn đơn giản như sau:
Hb(aq) + O2(g) ⇋ HbO2(aq) (1)
Tuy nhiên, Hb kết hợp với khí carbon monoxide thuận lợi hơn nhiều so với oxygen, nên khi có mặt carbon monoxide, khí này sẽ cạnh tranh và thay thế oxygen.
a) Xác định chiều ưu tiên xảy ra của phản ứng (1) ở phổi, ở tế bào.
b) Dựa vào cân bằng (1), giải thích hiện tượng một số người bị đau đầu, chóng mặt khi ở trên núi cao.
c) Một số ca nhiễm độc xảy ra do đốt than để sưởi ấm trong phòng kín. Người bị nhiễm độc có thể bị hôn mê, tổn thương thần kinh, thậm chí tử vong. Giải thích nguyên nhân gây nhiễm độc trong trường hợp này.
(Xem giải) 3. Đồng thau là hợp kim của đồng và kẽm. Để xác định phần trăm khối lượng đồng trong một mẫu đồng thau (giả sử không có tạp chất khác), một học sinh thực hiện thí nghiệm theo các bước sau:
• Bước 1: Hòa tan hoàn toàn 1,00 gam đồng thau vào bình nón A chứa dung dịch HNO3 đậm đặc (dư).
• Bước 2: Thêm từng giọt dung dịch Na2CO3 vào bình A cho đến khi xuất hiện kết tủa. Sau đó, nhỏ từng giọt dung dịch CH3COOH loãng cho đến khi kết tủa tan hoàn toàn.
• Bước 3: Chuyển toàn bộ dung dịch trong bình A sang bình định mức B và định mức đến 100 mL bằng nước cất.
• Bước 4: Chuyển 10 mL dung dịch trong bình B vào bình nón C. Thêm 10 mL dung dịch KI (dư) vào bình C.
• Bước 5: Thêm dung dịch chuẩn Na2S2O3 0,06 M vào burette, rồi chuẩn độ dung dịch trong bình C với chất chỉ thị D.
Các bước chuẩn độ được lặp lại 3 lần.
a) Viết phương trình hóa học của các phản ứng xảy ra ở bước 1 biết NO2 là sản phẩm khử duy nhất của N+5.
b) Nêu rõ mục đích của bước 2.
c) Viết phương trình hóa học xảy ra ở bước 4 và xác định tên chất chỉ thị được dùng ở bước 5.
Biết:
– Ở bước 4, chỉ có một cation bị khử bởi I- về mức oxi hoá +1 và sản phẩm khử của I- là I2 (tồn tại ở dạng KI3 trong dung dịch KI dư).
– Ở bước 5, KI3 được tạo thành sau bước 4 phản ứng với Na2S2O3 theo phương trình hóa học:
KI3 + 2Na2S2O3 → Na2S4O6 + 2NaI + KI
d) Tính phần trăm khối lượng đồng trong mẫu đồng thau. Biết tại điểm kết thúc chuẩn độ, thể tích dung dịch Na2S2O3 0,06 M của ba lần chuẩn độ có giá trị như sau:
| Lần 1 | Lần 2 | Lần 3 | |
| VddNa2S2O3 ban đầu (mL) | 24,80 | 45,35 | 22,50 |
| VddNa2S2O3 sau chuẩn độ (mL) | 4,50 | 24,80 | 2,00 |
Câu II (4,0 điểm)
(Xem giải) 1. Nguyên tố X thuộc chu kì 3, nhóm VA trong bảng tuần hoàn các nguyên tố hóa học. Đồng vị bền Y của X có số khối bằng 31.
a) Xác định nguyên tố X; số proton, số electron và số neutron của đồng vị Y.
b) Viết công thức cấu tạo và công thức Lewis của các phân tử: XH3, XCl5. Dự đoán dạng hình học phân tử của từng chất theo mô hình VSEPR và giải thích.
c) Vì sao NH3 tan trong nước tốt hơn XH3?
(Xem giải) 2. Một đám cháy bùng phát tại một kho chứa hóa chất. Đội cứu hỏa đã cố gắng dập tắt đám cháy bằng nước, nhưng đám cháy không những không tắt mà còn bùng lên dữ dội hơn. Sau khi đám cháy được kiểm soát, các chuyên gia phát hiện trong kho có một số thùng chứa một chất rắn màu xám (X) có khả năng tác dụng với nước tạo ra khí Y thường được sử dụng trong hàn cắt kim loại.
a) Xác định công thức hóa học của X và viết các phương trình phản ứng giải thích hiện tượng trên.
b) Giả sử khí sinh ra từ phản ứng của X với nước có giới hạn nổ dưới ở đkc (LEL – Lower Explosive – là nồng độ thấp nhất của khí hoặc hơi trong không khí có thể bắt lửa và gây nổ) là 2,5% thể tích; kho có thể tích 1000 m³ và được đóng kín ở đkc. Tính khối lượng (đơn vị kg) tối thiểu của X cần phản ứng với nước để thể tích khí đạt đến giới hạn nổ dưới.
(Xem giải) 3. Cho dãy chuyển hóa:
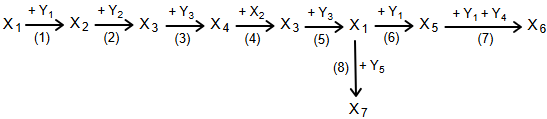
Viết phương trình hóa học của các phản ứng thực hiện dãy chuyển hóa trên.
Biết:
+ Hợp chất XOH (X2) của kim loại X là hóa chất cơ bản quan trọng trong công nghiệp giấy, dệt, xà phòng, chất tẩy rửa,…
+ Các chất X1, X3, X4, X5, X6, X7 cũng là hợp chất của X;
+ Dung dịch X7 làm quỳ tím hóa đỏ;
+ MX2 + MX4 = 96.
Câu III (4,5 điểm)
(Xem giải) 1. Lập các phương trình hóa học sau bằng phương pháp thăng bằng electron, xác định chất khử và chất oxi hóa:
a) CO + NO → CO2 + N2
b) CrCl3 + NaOH + Cl2 → Na2CrO4 + NaCl + H2O
c) CH3-CH=CH2 + KMnO4 + H2SO4 → CH3COOH + CO2 + K2SO4 + MnSO4 + H2O
(Xem giải) 2. Phân tích thành phần nguyên tố của hợp chất hữu cơ A thu được kết quả: %C = 55,81%; %H = 6,98%; còn lại là O.
a) Xác định công thức phân tử của A biết một trong những đồng phân của A có phổ khối như sau:
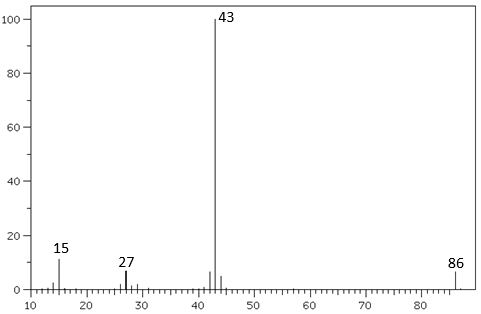
b) Viết các đồng phân cấu tạo, đơn chức, mạch hở của A.
c) A1, A2 là các đồng phân đơn chức của A và đều có đồng phân hình học. Thuỷ phân A1 trong môi trường kiềm thu được sản phẩm X1 và X2. Viết các phương trình hoá học theo sơ đồ sau (biết tác nhân trong các phản ứng đều là chất vô cơ):
A1 → X2 → X3 → X4 → A2
(Xem giải) 3. Hợp chất hữu cơ E, mạch hở có công thức tổng quát C8H12O4. Từ E thực hiện các phản ứng hóa học theo đúng tỉ lệ mol:
(1) E + 2NaOH (t°) → E1 + E2 + E3
(2) E + H2 (Ni, t°) → E4
(3) E4 + 2NaOH (t°) → 2E1 + E3
(4) E1 + HCl → NaCl + E5
Xác định công thức cấu tạo của E, E1, E2, E3, E4, E5 và viết phương trình hoá học của các phản ứng trên.
Câu IV (3,5 điểm)
(Xem giải) 1. Trong nghiên cứu khảo cổ học, để xác định tuổi của các cổ vật làm từ vật liệu hữu cơ (như xương, gỗ, …), người ta thường sử dụng một đồng vị phóng xạ của nguyên tố X. Đồng vị này được tạo thành trong khí quyển khi hạt nhân ![]() hấp thụ một hạt neutron. Trong tự nhiên, đồng vị đó không bền, phát ra tia β- (
hấp thụ một hạt neutron. Trong tự nhiên, đồng vị đó không bền, phát ra tia β- (![]() ) để trở về dạng
) để trở về dạng ![]() .
.
a) Xác định kí hiệu hạt nhân của đồng vị ![]() .
.
b) Viết phương trình hạt nhân hình thành và phân rã của đồng vị ![]() .
.
c) Giải thích vì sao có thể dùng đồng vị này để xác định tuổi của cổ vật hữu cơ.
d) Tháng 12/2024, tại Bắc Ninh, người dân phát hiện thấy hai mẫu thuyền cổ. Các nhà khảo cổ học đã cho khai quật vào tháng 4/2025. Một mảnh gỗ từ chiếc thuyền được gửi đi đo hoạt độ phóng xạ của đồng vị ![]() (theo Vnexpress ngày 04/5/2025).
(theo Vnexpress ngày 04/5/2025).

(i) Tính tuổi của con thuyền trên, nếu giả thiết phòng thí nghiệm báo kết quả hoạt độ phóng xạ của đồng vị ![]() trong mẫu là 77,26% so với hoạt độ phóng xạ của đồng vị
trong mẫu là 77,26% so với hoạt độ phóng xạ của đồng vị ![]() trong vật sống. Biết tuổi của cổ vật được tính theo phương trình:
trong vật sống. Biết tuổi của cổ vật được tính theo phương trình:
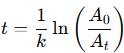
Trong đó:
– t là tuổi của cổ vật (năm);
– k là hằng số phóng xạ; với k = ln2/t½
– A₀ là hoạt độ phóng xạ của đồng vị ![]() trong vật sống;
trong vật sống;
– At là hoạt độ phóng xạ của đồng vị ![]() trong mẫu vật tại thời điểm nghiên cứu;
trong mẫu vật tại thời điểm nghiên cứu;
– t½ là chu kì bán rã của đồng vị ![]() có giá trị là 5730 năm.
có giá trị là 5730 năm.
(ii) Nêu một lí do có thể dẫn đến sai số của kết quả xác định tuổi của chiếc thuyền cổ khi sử dụng phương pháp đo hoạt độ của đồng vị phóng xạ trong trường hợp trên.
(Xem giải) 2. X là muối carbonate trung hòa, ngậm nước của một kim loại R. X có trong một loại khoáng vật được tìm thấy ở những vùng khí hậu khô cằn, trên bề mặt hoặc trong các hốc núi lửa. Hòa tan hoàn toàn 49,60 gam X trong 100,00 gam nước ở t₁°C, sau đó làm lạnh xuống t₂°C thu được 58,00 gam tinh thể Y (MY < 280 g/mol) và dung dịch Z. Khi thêm từ từ 36,5 mL dung dịch HCl 36% (d = 1,18 g/mL) vào dung dịch Z thu được 128,07 gam dung dịch T. Cho bay hơi đến khô dung dịch T thu được 17,55 gam chất rắn khan Q. Xác định công thức hóa học của X, Y.
Câu V (4,0 điểm)
(Xem giải) 1. Biodiesel (diesel sinh học) là hỗn hợp các methyl ester của acid béo (kí hiệu tổng quát là RCOOCH3). Biodiesel được sản xuất dựa trên phản ứng chuyển hóa ester (transesterification) xảy ra khi cho chất béo (kí hiệu tổng quát là (RCOO)3C3H5) tác dụng với lượng dư methanol có xúc tác là kiềm.
a) Viết phương trình hoá học tổng quát điều chế biodiesel biết sản phẩm đi kèm là glycerol.
b) Chỉ ra ba nguyên nhân khiến biodiesel thân thiện với môi trường hơn so với dầu diesel.
c) Trình bày một phương pháp thực nghiệm để tách biodiesel khỏi glycerol sau phản ứng.
d) Từ 500 kg một loại dầu ăn đã qua sử dụng có chứa 86% chất béo (phân tử khối trung bình của chất béo là 860), còn lại là tạp chất không có khả năng chuyển hóa thành biodiesel, tính khối lượng biodiesel (đơn vị kg) tối đa thu được với hiệu suất chuyển hóa là 90%.
(Xem giải) 2. Aspirin (acetylsalicylic acid) là một dẫn xuất của salicylic acid (o-hydroxybenzoic acid) được sử dụng phổ biến trên thế giới để hạ sốt, giảm đau, kháng viêm. Một nhóm học sinh, sau khi tìm hiểu kĩ đặc điểm, tính chất của các chất liên quan, đã tiến hành tổng hợp aspirin trong phòng thí nghiệm từ salicylic
acid theo các bước sau:
• Bước 1: Cân 5,0 gam salicylic acid, cho vào bình tam giác 150 mL (bình A).
• Bước 2: Thêm tiếp 7,0 mL acetic anhydride (CH3CO)2O (d = 1,08 g/mL) vào bình A rồi tiếp tục nhỏ vào bình 8 giọt dung dịch H2SO4 đặc. Thực hiện bước 2 trong tủ hút.
• Bước 3: Đặt bình A chứa hỗn hợp phản ứng vào cốc nước nóng và đun cách thủy trên bếp điện cho đến khi sôi, đun thêm 15 phút nữa.
• Bước 4: Để nguội và thêm 15,0 mL nước cất ở nhiệt độ phòng vào bình A, lắc đều. Khi các tinh thể aspirin bắt đầu hình thành thì ngâm bình A vào cốc nước đá trong 10 phút. Lọc lấy sản phẩm bằng phễu lọc chân không.
• Bước 5: Hòa tan aspirin thô trong bình B đựng 20,0 mL ethanol 90° và làm ấm bình B trên bếp điện cho đến khi aspirin tan hết. Ngay lập tức nhấc bình ra khỏi bếp và từ từ thêm 13,0 mL nước lạnh. Ngâm bình B vào trong cốc nước đá để làm lạnh rồi thu thập tinh thể bằng phễu lọc chân không.
• Bước 6: Làm khô và cân sản phẩm, thu được 4,0 gam aspirin.
a) Phản ứng giữa acetic alhydride và salicylic acid ngoài sản phẩm chính là aspirin còn thu được acetic acid. Viết phương trình phản ứng và tính hiệu suất của quá trình điều chế aspirin ở trên.
b) Phương pháp tách và tinh chế aspirin trong thí nghiệm trên là phương pháp gì? Trình bày ngắn gọn nguyên tắc của phương pháp và giải thích thông qua nội dung thí nghiệm.
c) Aspirin tan trong nước hay tan trong ethanol tốt hơn? Giải thích.


Hà Nội thi rồi ạ thầy.
Uh, năm nay thi sớm, lồng ghép thi HSG và chọn đội tuyển HSG Quốc gia luôn