[2026] Thi thử TN cụm chuyên môn số 02 Đắk Lắk
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 069
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2C | 3C | 4A | 5B | 6A | 7D | 8A | 9A |
| 10B | 11A | 12A | 13D | 14B | 15D | 16C | 17A | 18B |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | |||||||
| (b) | 26 | 27 | 28 | ||||
| (c) | |||||||
| (d) |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Cho các phát biểu sau:
(a) Dung dịch methylamine làm quỳ tím chuyển sang màu đỏ.
(b) Ester ethyl acetate ít tan trong nước.
(c) Tơ capron thuộc loại tơ tự nhiên.
(d) Trong y học saccarose được dùng làm thuốc tăng lực cho người bệnh.
Số phát biểu không đúng là
A. 2. B. 1. C. 3. D. 4.
(Xem giải) Câu 2. Cho các phát biểu sau khi nói về tính chất của ethylamine C2H5NH2:
(1) Ethylamine có khả năng tạo được liên kết hydrogen liên phân tử.
(2) Khi hòa tan vào trong nước, dung dịch ethylamine làm giấy quỳ tím hóa hồng.
(3) Khi cho ethylamine phản ứng với HNO2 ở nhiệt độ thường thu được sản phẩm chứa ethanol.
(4) Phản ứng của dung dịch CuCl2 với dung dịch ethylamine dư cho phức chất màu xanh lam.
Số phát biểu sai là
A. 3 B. 2 C. 1 D. 4
(Xem giải) Câu 3. Dung dịch protein tham gia phản ứng biuret với Cu(OH)2 trong môi trường kiềm tạo sản phẩm đặc trưng có màu
A. xanh. B. trắng. C. tím. D. vàng.
(Xem giải) Câu 4. Chất nào sau đây không bị thủy phân trong môi trường acid?
A. Glucose. B. Peptide. C. Cellulose. D. Maltose.
(Xem giải) Câu 5. Cấu hình electron ở phân lớp ngoài cùng của ion R2+ là 2p6. Nguyên tử R là
A. 11Na. B. 12Mg. C. 10Ne. D. 19K.
(Xem giải) Câu 6. Dichloromethane (DCM) là một chất lỏng không màu, dễ bay hơi với mùi thơm nhẹ và được sử dụng rộng rãi làm dung môi hữu cơ. Công thức phân tử của dichloromethane là
A. CH2Cl2. B. CCl4. C. CHCl3. D. CH3Cl.
(Xem giải) Câu 7. Chất nào dưới đây là một tripeptide?
A. Gly-Ala. B. Val.
C. Gly-Gly-Ala-Val. D. Gly-Ala-Val.
(Xem giải) Câu 8. Nhóm các khí nào sau đây trong không khí khi vượt quá mức cho phép sẽ gây ra hiện tượng mưa acid:
A. SO2; NO; NO2. B. CO2; O3; N2O.
C. NH3; H2S; O3. D. H2; CO; CH4.
(Xem giải) Câu 9. Trong các kim loại sau, kim loại nào có thể được điều chế bằng phương pháp thủy luyện?
A. Cu. B. Mg. C. Ca. D. K.
(Xem giải) Câu 10. Loại nhựa nào sau đây không phải nhựa nhiệt dẻo và không thể tái chế?
A. Nhựa PE. B. Nhựa PPF. C. Nhựa PP. D. Nhựa PS.
(Xem giải) Câu 11. Methyl propionate có công thức là
A. CH3CH2COOCH3. B. HCOOC2H5
C. CH3COOCH3. D. CH3COOCH=CH2.
(Xem giải) Câu 12. Khi điện phân dung dịch nào dưới đây tại cathode xảy ra quá trình khử nước?
A. Dung dịch MgCl2. B. Dung dịch CuCl2.
C. Dung dịch AgNO3. D. Dung dịch ZnCl2.
(Xem giải) Câu 13. Dung dịch nào sau đây làm mềm nước có tính cứng toàn phần?
A. Dung dịch NaCl. B. Dung dịch KOH.
C. Dung dịch HNO3. D. Dung dịch Na2CO3.
(Xem giải) Câu 14. Cho các phát biểu sau:
(a) Cao su thiên nhiên chứa các mắt xích isoprene, liên kết đôi trong mạch đều ở dạng cis.
(b) Thủy phân không hoàn toàn tripeptide Ala-Gly-Ala thu được tối đa 2 dipeptide.
(c) Keo dán epoxy có thành phần chính là chất hữu cơ có nhóm –COOH và -NH2 ở hai đầu.
(d) Tách tinh dầu từ hỗn hợp tinh dầu và nước bằng dung môi hexane là phương pháp chiết lỏng – lỏng.
Số phát biểu đúng là
A. 4. B. 2. C. 1. D. 3.
(Xem giải) Câu 15. Phản ứng giữa HCl với ethylene: CH2=CH2 + HCl → CH3CH2Cl.
Cơ chế phản ứng qua 2 giai đoạn như sau:
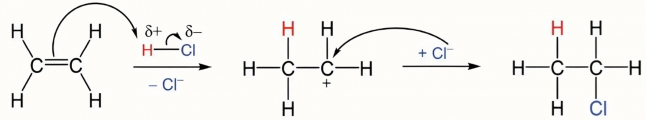
Nhận định nào sau đây không đúng?
A. Trong phân tử ethylene có 1 liên kết π (pi).
B. Giai đoạn 1 là giai đoạn hình thành carbocation (tiểu phân trung gian mang điện tích dương).
C. Phản ứng trên thuộc loại phản ứng cộng.
D. Trong giai đoạn 1 của phản ứng trên có sự phân cắt liên kết σ.
(Xem giải) Câu 16. Ion nào sau đây có tính oxi hoá mạnh nhất ở điều kiện chuẩn?
A. Al3+. B. Cu2+. C. Ag+. D. Fe2+.
(Xem giải) Câu 17. Amine nào sau đây có tính base yếu hơn ammonia ?
A. Aniline. B. Methylamine C. Propylamine D. Dimethylamine
(Xem giải) Câu 18. Trong số các chất sau đây, chất nào có nhiệt độ sôi nhỏ nhất?
A. C2H5COONa. B. CH3COOCH3. C. C2H5COOH. D. C3H7OH.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 1. Tiến hành điều chế ethyl acetate theo các bước như hình sau:
• Bước 1: Cho 10 mL C2H5OH (D = 0,78 g/mL) cùng với 10 mL CH3COOH (D = 1,05 g/mL), vài giọt dung dịch H2SO4 đặc và lắc đều bình cầu.
• Bước 2: Đun nóng bình cầu đến 70oC trong khoảng từ 5 đến 6 phút.
• Bước 3: Các chất thu được ở bình nón được thêm tiếp vào 2 mL dung dịch NaCl bão hòa.
a) Sau bước 2, các chất C2H5OH và CH3COOH vẫn còn trong bình cầu.
b) Ở bước 3, dung dịch NaCl bão hòa có vai trò làm tăng hiệu suất phản ứng ester hóa.
c) Giả sử hiệu suất của phản ứng đạt 40%, khối lượng ester thu được là 6 gam (kết quả được làm tròn đến hàng đơn vị).
d) Sau bước 2, trong bình cầu có phản ứng ester hóa sau:
(Xem giải) Câu 2. Trong quá trình làm thí nghiệm về nhận biết các cation của kim loại nhóm IIA, một học sinh làm các thí nghiệm như sau ở 20oC:
• Thí nghiệm 1: Cho 3 mL dung dịch CaCl2 vào ống nghiệm, thêm tiếp 2 mL dung dịch NaOH.
• Thí nghiệm 2: Cho 3 mL dung dịch MgCl2 vào ống nghiệm, thêm tiếp 2 mL dung dịch NaOH.
Trong cả 2 thí nghiệm học sinh đều thu được kết tủa. Để giải thích cho hiện tượng thí nghiệm này, học sinh trên đã tra cứu độ tan của các chất ở 20 oC như sau:
Chất Ca(OH)2 Mg(OH)2 NaCl
Độ tan (g/100 g H2O) 0,173 0,00125 36
a) Biết rằng ở 20oC trong dung dịch có [Ca2+].[OH-]2 > 5,4.10-6 thì xuất hiện kết tủa. Khi thực hiện thí nghiệm cho 20 mL dung dịch CaCl2 0,01 M tác dụng với 30 mL dung dịch NaOH 0,1 M ở 20oC thì có thu được kết tủa. (xem như thể tích dung dịch sau phản ứng bằng 50 mL).
b) Kết tủa thu được ở thí nghiệm 1 là Ca(OH)2.
c) Ở 20oC dung dịch bão hoà Ca(OH)2 có khối lượng riêng 1,01 g/mL thì có nồng độ Ca(OH)2 khoảng 0,02357M.
d) Ở 20oC Ca(OH)2 ít tan trong nước hơn Mg(OH)2.
(Xem giải) Câu 3. Serine là một amino acid không thiết yếu có nguồn gốc từ glycine, đóng vai trò quan trọng trong các quá trình sinh học khác nhau. Nó là một trong 20 loại amino acid tiêu chuẩn cần thiết cho sự hình thành protein trong cơ thể. Dưới đây là công thức cấu tạo của serine
a) Khối lượng phân tử của serine là 105 g/mol.
b) Serine là một hợp chất hữu cơ tạp chức, dễ tan trong nước.
c) Tên thay thế của serine là 2-amino-3-hydroxypropanoic acid
d) Serine phản ứng với NaOH theo tỉ lệ mol 1 : 2
(Xem giải) Câu 4. Một nhóm học sinh muốn khảo sát khả năng phân hủy cellulose trong điều kiện hiếu khí ở các nhiệt độ khác nhau. Nhóm học sinh đưa ra giả thuyết: “Cellulose bị phân hủy với xúc tác của enzyme cellulase do vi sinh vật tiết ra, quá trình này phụ thuộc nhiệt độ”. Để kiểm chứng giả thuyết, nhóm học sinh tiến hành thí nghiệm:
• Bước 1: Cho 2,03 gam bông tiệt trùng (chủ yếu chứa cellulose) vào mỗi ống nghiệm.
• Bước 2: Thêm 5 mL men vi sinh vào mẫu thí nghiệm, chuẩn bị một mẫu tương đương nhưng không có men vi sinh để đối chứng.
• Bước 3: Tiến hành ủ các mẫu trong 5 ngày ở các nhiệt độ: 25oC, 37oC, 45oC, 55oC.
• Bước 4: Lọc, rửa sạch, phơi khô và cân khối lượng bông còn lại.
Kết quả thí nghiệm như bảng sau:
Nhiệt độ
(oC)
Khối lượng bông còn lại
Mẫu đối chứng (gam) Mẫu có men vi sinh (gam)
25 2,03 1,21
37 2,03 0,81
45 2,03 0,92
55 2,03 1,58
a) Ở nhiệt độ tối ưu trong thí nghiệm trên, phần trăm khối lượng bông bị phân hủy lớn hơn 60%.
b) Trong thí nghiệm trên, nhiệt độ càng cao càng thuận lợi cho quá trình phân hủy cellulose.
c) Ở tất cả các nhiệt độ, khối lượng bông của mẫu đối chứng không thay đổi cho thấy môi trường nuôi cấy không chứa men vi sinh không làm phân hủy cellulose.
d) Giả thuyết đưa ra ban đầu của nhóm học sinh là đúng.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 1. Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Đánh sạch gỉ một chiếc đinh sắt rồi thả vào dung dịch CuSO4.
• Bước 2: Sau khoảng 10 phút, quan sát màu của chiếc đinh sắt và màu của dung dịch.
Cho các nhận định sau:
(a) Đinh sắt bị phủ một lớp màu đỏ.
(b) Màu xanh của dung dịch đậm hơn vì ion Fe2+ có màu xanh đậm.
(c) Màu xanh của dung dịch nhạt dần vì nồng độ của ion Cu2+ trong dung dịch giảm dần.
(d) Khối lượng dung dịch giảm so với ban đầu.
(e) Trong thí nghiệm trên có xảy ra ăn mòn điện hóa học.
Có bao nhiêu nhận định sai?
(Xem giải) Câu 2. Cho các chất sau: polybuta-1,3-diene, poly(methyl methacrylate), polyethylene, len lông cừu, polyacrylonitrile, cellulose, polyisoprene. Trong số các chất trên, có bao nhiêu chất được dùng để chế tạo cao su ?
(Xem giải) Câu 3. Trong quá trình sản xuất 2,4-D và 2,4,5-T từ phenol luôn sinh ra một lượng nhỏ dioxin. Dioxin là một hợp chất khó phân hủy trong môi trường và cơ thể con người. Dioxin cực kì độc ở nồng độ rất nhỏ (cỡ phần tỉ) gây ra những hậu quả khôn lường cho con người như ung thư, quái thai, dị tật, vô sinh,… Dioxin có công thức cấu tạo như sau:
Số nguyên tử hydrogen có trong một phân tử dioxin bằng bao nhiêu?
(Xem giải) Câu 4. Phần trăm khối lượng nguyên tố nitrogen trong alanine là a%. Giá trị của a là bao nhiêu? (Kết quả làm tròn đến hàng phần mười).
(Xem giải) Câu 5. Cho phương trình hóa học của các phản ứng (ở điều kiện phản ứng thích hợp) được đánh số thứ tự từ 1 đến 4 dưới đây:
(1) 2NaCl(l) → 2Na(l) + Cl2(g)
(2) Fe2O3(s) + 3CO(g) → 2Fe(g) + 3CO2(g)
(3) Fe(s) + CuSO4(aq) → FeSO4(aq) + Cu(s)
(4) 4AgNO3(aq) + 2H2O(l) → 4Ag(s) + O2(g) + 4HNO3(aq)
Gán số thứ tự phương trình hóa học của các phản ứng theo phương pháp tách kim loại lần lượt là: nhiệt luyện, thủy luyện, điện phân nóng chảy, điện phân dung dịch và sắp xếp theo trình tự thành dãy bốn số (ví dụ 1234, 4321…).
(Xem giải) Câu 6. Một con tàu có phần vỏ thép diện tích 1000 m². Để bảo vệ phần vỏ thép này khỏi sự ăn mòn, cần dòng điện có mật độ trung bình là 2,75 mA/m². Trong phương pháp bảo vệ cathode, người ta gắn các khối kẽm lên vỏ thép. Tính khối lượng kẽm cần sử dụng trong một năm (365 ngày) nếu lượng kẽm thất thoát bởi các quá trình khác là 12%. Cho biết công thức q = I.t = ne.F. (với q là điện lượng, I là cường độ dòng điện, F là hằng số 96485 C/mol; làm tròn kết quả đến hàng phần mười).


Bình luận