Giải đề THPT chuyên ĐH Vinh (Lần 1 – 2017)
⇒ File word đề thi, đáp án và giải chi tiết
Câu 1: Thực hiện các thí nghiệm sau:
(1) Cho lá kim loại Fe nguyên chất vào dung dịch CuSO4.
(2) Cho lá kim loại Al nguyên chất vào dung dịch HNO3 loãng, nguội.
(3) Đốt dây kim loại Mg nguyên chất trong khí Cl2.
(4) Cho lá hợp kim Fe – Cu vào dung dịch H2SO4 loãng.
Số thí nghiệm mà kim loại bị ăn mòn hóa học là
A. 4. B. 3. C. 2. D. 1.
Đáp án A. (1) và (4) lúc đầu kim loại bị ăn mòn hóa học, sau đó có ăn mòn điện hóa. Ở (2)(3) kim loại bị ăn mòn hóa học.
Câu 2: Hình vẽ sau đây mô tả thí nghiệm khí X tác dụng với chất rắn Y, nung nóng sinh ra khí Z:
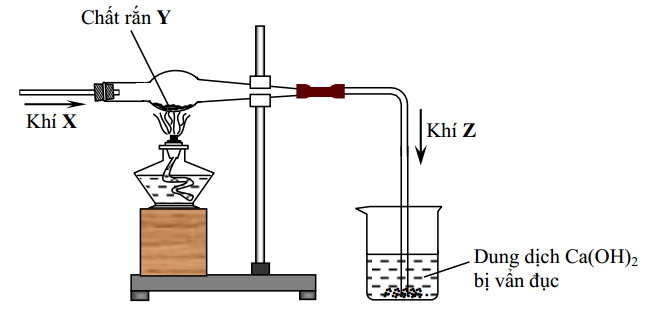
Phương trình hóa học của phản ứng tạo thành khí Z là
A. CuO + H2 → Cu + H2O B. Fe2O3 + 3H2 → 2Fe + 3H2O
C. CuO + CO → Cu + CO2 D. 2HCl + CaCO3 → CaCl2 + CO2 + H2O
Đáp án C. Nhìn hình vẽ thí nghiệm ta thấy khí X (CO) được dẫn qua chất rắn Y (CuO) nung nóng, sản phẩm là khí Z (CO2) làm đục nước vôi trong.
Câu 3: Khi thuỷ phân hoàn toàn một triglixerit X trong môi trường axit thu được hỗn hợp sản phẩm gồm glixerol, axit panmitic và axit oleic. Số công thức cấu tạo của X thoả mãn tính chất trên là
A. 8. B. 4. C. 2. D. 6.
Đáp án B. Có 4 công thức cấu tạo của X thỏa mãn tính chất trên gồm: PPO, POP, OOP, OPO (Với O là gốc axit oleic và P là gốc axit panmitic trong chất béo).
Câu 4: Este CH2=CHCOOCH3 không tác dụng với chất (hoặc dung dịch) nào sau đây?
A. Dung dịch NaOH, đun nóng. B. H2O (xúc tác H2SO4 loãng, đun nóng).
C. Kim loại Na. D. H2 (xúc tác Ni, đun nóng).
Đáp án C. Este không tác dụng với Na.
Câu 5: Cho 4,05 gam bột Al tác dụng với V lít O2 (đktc), thu được hỗn hợp rắn X. Cho X tác dụng với lượng dư dung dịch NaOH, sinh ra 1,68 lít H2 (đktc). Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V là
A. 1,68. B. 3,36. C. 6,72. D. 1,26.
Đáp án A. Bảo toàn electron: 3nAl = 4nO2 + 2nH2 —> nO2 = 0,075 —> V = 1,68 lít
Câu 6: Cho mẫu nước cứng có chứa các ion: Ca2+, Mg2+, Cl- , SO42-. Hóa chất được dùng để làm mềm mẫu nước cứng trên là
A. BaCl2. B. NaCl. C. AgNO3. D. Na3PO4.
Đáp án D. 3Ca2+ + 2PO43- —> Ca3(PO4)2; 3Mg2+ + 2PO43- —> Mg3(PO4)2
Câu 7: Phát biểu nào sau đây sai?
A. Kim loại xesi dùng để chế tạo tế bào quang điện.
B. Công thức hóa học của phèn chua là (NH4)2SO4.Al2(SO4)3.24H2O.
C. Các kim loại Na và Ba đều có cấu tạo mạng tinh thể lập phương tâm khối.
D. Thạch cao sống dùng để sản xuất xi măng.
Đáp án B. Phèn chua là K2SO4.Al2(SO4)3.24H2O
Câu 8: Phát biểu nào sau đây sai?
A. Tinh bột là lương thực của con người.
B. Xenlulozơ và tinh bột có phân tử khối bằng nhau.
C. Thành phần chính của sợi bông, gỗ, nứa là xenlulozơ.
D. Khi cho giấm ăn (hoặc chanh) vào sữa bò hoặc sữa đậu nành thì có kết tủa xuất hiện.
Đáp án B. Tinh bột và xenlulozo có độ polime hóa khác nhau, chúng không phải các đồng phân.
Câu 9: Số đồng phân cấu tạo là tetrapeptit có cùng công thức phân tử C9H16O5N4 là
A. 2. B. 1. C. 3. D. 4.
Đáp án D. Các peptit gồm:
Ala-Gly-Gly-Gly; Gly-Ala-Gly-Gly; Gly-Gly-Ala-Gly; Gly-Gly-Gly-Ala
Câu 10: Phần trăm khối lượng của nguyên tố cacbon trong phân tử anilin (C6H5NH2) là
A. 78,26%. B. 77,42%. C. 75,00%. D. 83,72%.
Đáp án B. %C = 12.6/93 = 77,42%
Câu 11: Metylamin không phản ứng với
A. dung dịch H2SO4. B. dung dịch HCl.
C. H2 (xúc tác Ni, nung nóng). D. O2, nung nóng.
Đáp án C. CH3NH2 no nên không phản ứng với H2.
Câu 12: Cho 9 gam C2H5NH2 tác dụng vừa đủ với dung dịch HCl, khối lượng muối thu được là
A. 16,10 gam. B. 12,63 gam. C. 12,65 gam. D. 16,30 gam.
Đáp án D. m muối = mC2H5NH2 + mHCl = 16,3 gam
Câu 13: Kim loại nào sau đây không phản ứng với dung dịch CuSO4?
A. Ag. B. Al. C. Fe. D. Zn.
Đáp án A. Ag đứng sau Cu trong dãy điện hóa nên không khử được Cu2+.
Câu 14: Cho m gam axit glutamic (HOOC-[CH2]2-CH(NH2)-COOH) tác dụng vừa đủ với 300 ml dung dịch KOH 1M. Giá trị của m là
A. 43,80. B. 21,90. C. 44,10. D. 22,05.
Đáp án D. nGlu = nKOH/2 = 0,15 —> mGlu = 22,05
Câu 15: Este nào sau đây khi tác dụng với dung dịch NaOH đun nóng, thu được hỗn hợp sản phẩm gồm
CH3COONa và CH3CHO?
A. CH2=CHCOOCH3. B. CH3COOCH=CH2.
C. HCOOCH=CH2. D. CH3COOCH=CHCH3.
Đáp án B.
Câu 16: Công thức phân tử của tristearin là
A. C57H104O6. B. C54H104O6. C. C54H98O6. D. C57H110O6.
Đáp án D. Tristearin là (C17H35COO)3C3H5 hay C57H110O6
Câu 17: Số đồng phân cấu tạo thuộc loại amin bậc I có cùng công thức phân tử C3H9N là
A. 1. B. 4. C. 2. D. 3.
Đáp án C. Các đồng phân amin bậc I gồm: CH3-CH2-CH2-NH2 và CH3-CH(NH2)-CH3
Câu 18: Thành phần chính của đá vôi là
A. CaCO3. B. BaCO3. C. MgCO3. D. FeCO3.
Đáp án A.
Câu 19: Cho m gam kim loại Ba vào nước dư, sau khi phản ứng xảy ra hoàn toàn thu được 4,48 lít H2 (đktc). Giá trị của m là
A. 13,70. B. 27,40. C. 54,80. D. 20,55.
Đáp án B. nBa = nH2 = 0,2 —> mBa = 27,4
Câu 20: Polime được điều chế bằng phản ứng trùng hợp là
A. poliacrilonitrin. B. poli(etylen terephtalat).
C. nilon – 6,6. D. xenlulozơ triaxetat.
Đáp án A. nCH2=CH-CN —> (-CH2-CH(CN)-)n
Câu 21: Kim loại nào sau đây là kim loại kiềm thổ?
A. Na. B. Ca. C. Fe. D. Al.
Đáp án B.
Câu 22: Cho 0,15 mol bột Fe tác dụng với 0,15 mol Cl2, nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được m gam muối. Giá trị của m là
A. 16,250. B. 19,050. C. 12,700. D. 8,125.
Đáp án A. nFeCl3 = 0,1 —> m = 16,25
Câu 23: Cho dãy các kim loại: Fe, Cu, Mg, Ag, Al, Na, Ba. Số kim loại trong dãy phản ứng được với dung dịch HCl là
A. 4. B. 3. C. 6. D. 5.
Đáp án D. Các kim loại tác dụng với dung dịch HCl: Fe, Mg, Al, Na, Ba.
Câu 24: Phương trình hóa học nào sau đây sai?
A. 2NaHCO3 —> Na2O + 2CO2 + H2O
B. NaHCO3 + NaOH —> Na2CO3 + H2O
C. 2Li + 2HCl —> 2LiCl + H2
D. 2Mg + O2 —> 2MgO
Đáp án A. Phương trình đúng là 2NaHCO3 —> Na2CO3 + CO2 + H2O
Câu 25: Trong quá trình điện phân dung dịch NaCl (điện cực trơ, có màng ngăn), ở cực âm (catot) xảy ra
A. sự oxi hóa cation Na+. B. sự oxi hóa phân tử H2O.
C. sự khử phân tử H2O. D. sự khử cation Na+.
Đáp án C.
Câu 26: Một học sinh tiến hành nghiên cứu dung dịch X đựng trong lọ không dán nhãn thì thu được kết quả sau:
– X đều có phản ứng với dung dịch NaOH và dung dịch Na2CO3.
– X đều không phản ứng với dung dịch HCl và dung dịch HNO3.
Vậy dung dịch X là dung dịch nào sau đây?
A. Dung dịch KOH. B. Dung dịch AgNO3.
C. Dung dịch Ba(HCO3)2. D. Dung dịch MgCl2.
Đáp án D.
Câu 27: Cho 0,1 mol bột Fe tác dụng với lượng dư dung dịch H2SO4 đặc, nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X và V lít SO2 (sản phẩm khử duy nhất, đktc). Giá trị của V là
A. 6,72. B. 2,24. C. 3,36. D. 4,48.
Đáp án C. Bảo toàn electron: 3nFe = 2nSO2 —> nSO2 = 0,15 —> V = 3,36 lít
Câu 28: Cho 0,2 mol bột Fe phản ứng hết với dung dịch X chứa đồng thời Cu(NO3)2 và a mol Fe(NO3)3, thu được dung dịch Y có khối lượng bằng khối lượng dung dịch X ban đầu (giả thiết nước bay hơi không
đáng kể). Giá trị của a là
A. 0,10. B. 0,15. C. 0,05. D. 0,02.
⇒ Xem giải
Câu 29: Cho 0,2 mol hỗn hợp X gồm phenylamoni clorua (C6H5NH3Cl), alanin (CH3CH(NH2)COOH) và glyxin (H2NCH2COOH) tác dụng với 300 ml dung dịch H2SO4 nồng độ a mol/lít (loãng), thu được dung dịch Y. Dung dịch Y tác dụng vừa đủ với 500 ml dung dịch NaOH 1M. Giá trị của a là
A. 2,0. B. 0,5. C. 1,5. D. 1,0.
⇒ Xem giải
Câu 30: Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:

Các dung dịch X, Y, Z, T lần lượt là
A. natri stearat, anilin, mantozơ, saccarozơ. B. natri stearat, anilin, saccarozơ, mantozơ.
C. anilin, natri stearat, saccarozơ, mantozơ. D. anilin, natri stearat, mantozơ, saccarozơ.
Đáp án A.
Câu 31: Hỗn hợp M gồm amino axit X (no, mạch hở, phân tử chỉ chứa 1 nhóm –COOH và 1 nhóm –NH2) và este Y tạo bởi X và C2H5OH. Đốt cháy hoàn toàn m gam M bằng một lượng O2 vừa đủ, thu được N2; 12,32 lít CO2 (đktc) và 11,25 gam H2O. Giá trị của m là
A. 11,30. B. 12,35. C. 14,75. D. 12,65.
⇒ Xem giải
Câu 32: Đốt cháy hoàn toàn hỗn hợp gồm CH≡C-CH=CH-CH2NH2 và (CH3)2CH-CH(NH2)COOH cần dùng x mol O2 (vừa đủ), chỉ thu được N2, H2O và 4,48 lít CO2 (đktc). Giá trị của x là
A. 0,27. B. 1,35. C. 0,54. D. 0,108.
⇒ Xem giải
Câu 33: Hợp chất X có công thức phân tử C10H8O4. Từ X thực hiện các phản ứng (theo đúng tỉ lệ mol):
C10H8O4 + 2NaOH —> X1 + X2
X1 + 2HCl —> X3 + 2NaCl
nX3 + nX2 —> Poli(etylen-terephtalat) + 2nH2O
Phát biểu nào sau đây sai?
A. Số nguyên tử H trong phân tử X3 bằng 8.
B. Dung dịch X2 hòa tan Cu(OH)2 tạo dung dịch phức chất có màu xanh lam.
C. Dung dịch X3 có thể làm quỳ tím chuyển màu hồng.
D. Nhiệt độ nóng chảy của X1 cao hơn X3.
Đáp án A.
X3: HOOC-C6H4-COOH; X2: HO-CH2-CH2-OH; X1: NaOOC-C6H4-COONa
Câu 34: Thực hiện các thí nghiệm sau:
(1) Cho kim loại K vào dung dịch HCl. (2) Đốt bột Al trong khí Cl2.
(3) Cho Na2CO3 vào dung dịch AlCl3. (4) Cho NaOH vào dung dịch Mg(NO3)2.
(5) Điện phân Al2O3 nóng chảy, có mặt Na3AlF6.
Số thí nghiệm có phản ứng oxi hóa – khử xảy ra là
A. 2. B. 1. C. 3. D. 4.
Đáp án C. Các phản ứng oxi hóa khử: (1)(2)(5)
Câu 35: Hòa tan hoàn toàn m gam hỗn hợp X gồm Ba, BaO, Al và Al2O3 vào nước dư, thu được dung dịch Y và 5,6 lít H2 (đktc). Nhỏ từ từ đến dư dung dịch HCl 1M vào dung dịch Y. Đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa Al(OH)3 theo thể tích dung dịch HCl 1M như sau:
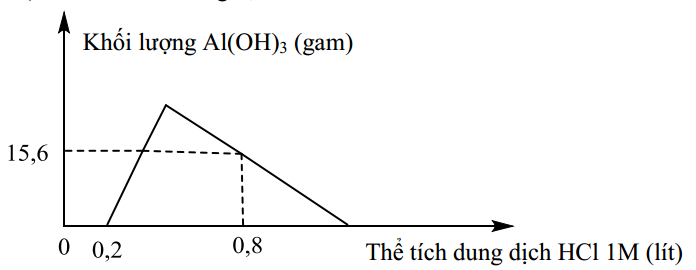
Giá trị của m là
A. 47,15. B. 56,75. C. 99,00. D. 49,55.
⇒ Xem giải
Câu 36: Cho dãy các chất: tinh bột, protein, vinyl fomat, anilin, mantozơ. Phát biểu nào sau đây đúng khi nói về các chất trong dãy trên?
A. Có 3 chất bị thủy phân trong dung dịch H2SO4 loãng, nóng.
B. Có 2 chất tham gia phản ứng tráng bạc.
C. Có 1 chất làm mất màu nước brom.
D. Có 2 chất có tính lưỡng tính.
Đáp án B. Có 4 chất bị thủy phân (1, 2, 3, 5). Có 2 chất tráng gương (3, 5). Có 3 chất làm mất màu Br2 (3, 4, 5). Không có chất nào lưỡng tính.
Câu 37: Cho hỗn hợp X gồm 0,12 mol CuO; 0,1 mol Mg và 0,05 mol Al2O3 tan hoàn toàn trong dung dịch chứa đồng thời 0,15 mol H2SO4 (loãng) và 0,55 mol HCl, thu được dung dịch Y và khí H2. Nhỏ từ từ dung dịch hỗn hợp Ba(OH)2 0,1M và NaOH 0,6M vào Y đến khi thu được khối lượng kết tủa lớn nhất, lọc kết tủa đem nung đến khối lượng không đổi, thu được m gam chất rắn khan. Giá trị của m gần nhất với giá trị nào sau đây?
A. 52,52. B. 48,54. C. 43,45. D. 38,72.
⇒ Xem giải
Câu 38: Hòa tan hoàn toàn 16,4 gam hỗn hợp X gồm FeO, Fe3O4 và Cu (trong đó FeO chiếm 1/3 tổng số mol hỗn hợp X) trong dung dịch chứa NaNO3 và HCl, thu được dung dịch Y chỉ chứa các muối clorua và 0,896 lít NO (sản phẩm khử duy nhất của N+5, đktc). Mặt khác, hòa tan hoàn toàn 16,4 gam hỗn hợp X trên trong dung dịch HCl thu được dung dịch Z chỉ chứa 3 muối có tổng khối lượng 29,6 gam. Trộn dung dịch Y với dung dịch Z thu được dung dịch T. Cho dung dịch AgNO3 tới dư vào T thu được m gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 196,35. B. 111,27. C. 160,71. D. 180,15.
⇒ Xem giải
Câu 39: Hỗn hợp M gồm 4 peptit X, Y, Z, T (đều mạch hở) chỉ tạo ra từ các α-amino axit có dạng H2NCnH2nCOOH (n ≥ 2). Đốt cháy hoàn toàn 26,05 gam M, rồi cho toàn bộ sản phẩm cháy (chỉ gồm CO2, H2O và N2) vào bình đựng 800 ml dung dịch Ba(OH)2 1M, sau khi các phản ứng xảy ra hoàn toàn thấy có 3,248 lít (đktc) một chất khí duy nhất thoát ra và thu được dung dịch E (chứa muối axit) có khối lượng giảm m gam so với khối lượng dung dịch Ba(OH)2 ban đầu. Giá trị của m gần giá trị nào nhất sau đây?
A. 90. B. 88. C. 87. D. 89.
⇒ Xem giải
Câu 40: Đun nóng 21,9 gam este đơn chức X với lượng dư dung dịch NaOH thì có tối đa 12 gam NaOH phản ứng. Mặt khác, đốt cháy hoàn toàn m gam X trên cần dùng vừa đủ 42,56 lít O2 (đktc). Giá trị của m là
A. 26,28. B. 43,80. C. 58,40. D. 29,20.
⇒ Xem giải

