[2020 – 2021] Thi học sinh giỏi lớp 12 – Tỉnh Thái Bình
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Thời gian làm bài: 90 phút
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2C | 3B | 4A | 5A | 6D | 7A | 8B | 9A | 10B |
| 11C | 12D | 13A | 14C | 15D | 16A | 17B | 18D | 19D | 20A |
| 21C | 22B | 23D | 24B | 25D | 26C | 27A | 28A | 29A | 30B |
| 31C | 32D | 33A | 34C | 35C | 36D | 37B | 38D | 39C | 40A |
| 41D | 42B | 43C | 44C | 45C | 46D | 47B | 48C | 49B | 50A |
(Xem giải) Câu 1: Cho ba hiđrocacbon mạch hở X, Y, Z (MX < MY < MZ < 62) có cùng số nguyên tử cacbon trong phân tử, đều phản ứng với dung dịch AgNO3 trong NH3 dư. Nhận xét nào sau đây không đúng?
A. Chất Y có số nguyên tử cacbon bằng số nguyên tử hiđro.
B. X, Y và Z đều có mạch cacbon không phân nhánh.
C. 1 mol X phản ứng tối đa với 4 mol H2 (Ni, t°).
D. Chất Z có tên gọi là vinyl axetilen.
(Xem giải) Câu 2: Cho sơ đồ phản ứng: FeS2 + H2SO4 (đặc, nóng) → Fe2(SO4)3 + SO2 + H2O. Sau khi phương trình phản ứng được cân bằng, tỉ lệ số nguyên tử lưu huỳnh bị khử và số nguyên tử lưu huỳnh bị oxi hóa là
A. 4:11. B. 15:4. C. 11:4. D. 4:15.
(Xem giải) Câu 3: Điện phân nóng chảy Al2O3 với các điện cực bằng than chì, thu được m gam Al ở catot và hỗn hợp khí X ở anot gồm CO và CO2. Dẫn 1/10 hỗn hợp X qua ống sứ chứa 24 gam Fe2O3 và 32 gam CuO nung nóng, thấy thoát ra khí Y duy nhất. Hấp thụ hết Y vào dung dịch nước vôi trong dư, thu được 130 gam kết tủa. Phần rắn còn lại trong ống sứ cho vào dung dịch H2SO4 đặc, nóng (dùng dư), thu được 8,96 lít khí SO2 (đktc, sản phẩm khử duy nhất của S+6). Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 432. B. 396. C. 324. D. 360.
(Xem giải) Câu 4: Cho các nhận xét sau:
(a) Khi để lâu trong không khí, các amin thơm bị chuyển từ không màu sang màu hồng vì bị oxi hóa.
(b) Este, chất béo, tinh bột, xenlulozơ, peptit, protein đều bị thủy phân trong môi trường axit và môi trường kiềm.
(c) Nhỏ vài giọt anilin vào ống nghiệm đựng nước, anilin hầu như không tan và nổi lên phía trên ống nghiệm.
(d) Tirozin (axit α-amino-β (p-hiđroxiphenyl)alanin) có thể tác dụng với NaOH trong dung dịch theo tỉ lệ mol 1:2.
(e) Peptit có thể bị thủy phân thành các peptit ngắn hơn nhờ các enzim có tính đặc hiệu vào một liên kết peptit nhất định nào đó.
(g) Tripeptit mạch hở Gly-Glu-Lys có số nguyên tử nitơ bằng số nguyên tử oxi trong phân tử.
Số nhận xét đúng là
A. 2. B. 3. C. 5. D. 4.
(Xem giải) Câu 5: Thả một viên bi hình cầu bán kính là r1 làm bằng kim loại Zn nặng 3,375 gam vào 17,782 gam dung dịch HCl 15%. Sau khi phản ứng hoàn toàn thì bán kính viên bi mới là r2 (giả sử viên bi bị mòn đều từ các phía). Biểu thức liên hệ giữa r1 và r2?
A. r1 = 1,5r2. B. r1 = 1,39r2. C. r1 = 1,75r2. D. r1 = 2r2.
Câu 6: Có 5 dung dịch A, B, C, D, E, mỗi dung dịch chứa một trong các chất: glucozơ; saccarozơ; anilin; axit glutamic; peptit Ala-Gly-Val. Để xác định chất tan trong các dung dịch, tiến hành các bước thí nghiệm theo bảng sau:
| Thuốc thử | A | B | C | D | E | |
| Bước 1 | quỳ tím | hóa đỏ | ||||
| Bước 2 | dung dịch Br2/H2O | mất màu | kết tủa trắng | |||
| Bước 3 | Cu(OH)2/OH– | dung dịch
xanh lam |
dung dịch
màu tím |
Các chất A, B, C, D, E lần lượt là
A. anilin, saccarozơ, peptit, axit glutamic, glucozơ. B. glucozơ, axit glutamic, anilin, peptit, saccarozơ.
C. glucozơ, peptit, anilin, saccarozơ, axit glutamic. D. glucozơ, axit glutamic, anilin, saccarozơ, peptit.
(Xem giải) Câu 7: Thực hiện các thí nghiệm sau:
(a) Cho a mol bột Mg vào dung dịch chứa a mol FeCl3.
(b) Cho từ từ dung dịch chứa a mol HCl vào dung dịch chứa a mol KHCO3 và 2a mol K2CO3.
(c) Cho a mol KOH vào dung dịch chứa a mol Ca(HCO3)2.
(d) Cho a mol Ba(HCO3)2 vào dung dịch chứa a mol KHSO4.
(e) Hấp thụ khí NO2 vào dung dịch NaOH dư.
(g) Hòa tan Fe3O4 vào dung dịch HI dư.
Số thí nghiệm thu được dung dịch có chứa hai muối sau phản ứng là
A. 2. B. 4. C. 3. D. 5.
(Xem giải) Câu 8: Cho các nhận xét sau:
(a) Phân đạm amoni chỉ phù hợp với đất chua.
(b) Amophot (hỗn hợp gồm (NH4)2HPO4 và NH4H2PO4) là một loại phân bón hỗn hợp.
(c) Thành phần chính của supephotphat kép gồm Ca(H2PO4)2 và CaSO4.
(d) Tro thực vật cũng là một loại phân kali vì có chứa nhiều K2SO4.
(e) Urê có công thức là (NH2)2CO và là một hợp chất vô cơ.
(g) Nguyên liệu để sản xuất phân lân là quặng photphorit hoặc apatit.
Số nhận xét không đúng là
A. 4. B. 5. C. 2. D. 3.
(Xem giải) Câu 9: Nung nóng 0,63 mol hỗn hợp X gồm Mg, Fe(NO3)2 và FeCO3 trong một bình kín đến khối lượng không đổi thu được chất rắn Y và 6,72 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ Y tác dụng với dung dịch hỗn hợp chứa 1,35 mol HCl và 0,19 mol HNO3 đun nhẹ thu được dung dịch A và V lít hỗn hợp khí B (đktc) gồm NO và N2O. Cho toàn bộ A tác dụng với lượng dư dung dịch AgNO3, thu được 0,224 lít NO (đktc) là sản phẩm khử duy nhất và 206,685 gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của V là
A. 3,584. B. 5,376. C. 4,032. D. 6,272.
(Xem giải) Câu 10: Cho anđehit X mạch hở có công thức phân tử là CxHyOz. Cho 0,15 mol X phản ứng với lượng dư dung dịch AgNO3 trong NH3 đun nóng thì thu được 64,8 gam Ag. Cho 0,125a mol X phản ứng với H2 dư (xúc tác Ni, đun nóng) thì thể tích H2 phản ứng là 8,4a lít (đktc). Mối liên hệ giữa x và y là
A. 2x – y – 2 = 0. B. 2x – y – 4 = 0. C. 2x – y + 4 = 0. D. 2x – y + 2 = 0.
(Xem giải) Câu 11: Thủy phân hoàn toàn 42,38 gam hỗn hợp X gồm hai triglixerit mạch hở trong dung dịch KOH 28% (vừa đủ), cô cạn dung dịch sau phản ứng, thu được phần hơi Y nặng 26,2 gam và phần rắn Z. Đốt cháy hoàn toàn Z thu được K2CO3 và 152,63 gam hỗn hợp CO2 và H2O. Mặt khác a mol X phản ứng tối đa với 0,24 mol Br2 trong CCl4. Giá trị của a là
A. 0,24 mol. B. 0,12 mol. C. 0,15 mol. D. 0,18 mol.
(Xem giải) Câu 12: Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở A, B (MA < MB) có số liên kết pi nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol nX : nY = 1 : 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của hiđrocacbon A trong Y gần nhất với:
A. 71%. B. 20%. C. 23%. D. 29%.
(Xem giải) Câu 13: Xét cân bằng trong bình kín có dung tích không đổi: aX (khí) ⇄ bY (khí). Ban đầu cho 1 mol khí X vào bình, khi đạt đến trạng thái cân bằng thì thấy: tại thời điểm ở 35°C trong bình có x mol X; tại thời điểm ở 65°C trong bình có y mol X. Biết a > b và x > y, nhận xét nào sau đây là đúng?
A. Khi giảm nhiệt độ thì tỉ khối hơi của hỗn hợp khí so với H2 giảm xuống.
B. Phản ứng thuận là phản ứng tỏa nhiệt.
C. Khi tăng áp suất, cân bằng chuyển dịch theo chiều nghịch.
D. Thêm xúc tác thích hợp vào hỗn hợp cân bằng thì cân bằng chuyển dịch theo chiều thuận.
(Xem giải) Câu 14: Chọn phát biểu đúng?
A. Trong các chất: CH3COONa, (NH2)2CO, C2H5OH, C2H5ONa, HCOOH, HCl, C12H22O11, C6H6. Có 4 chất khi cho thêm nước tạo thành dung dịch dẫn điện.
B. Tại catot bình điện phân xảy ra sự khử, tại catot trong ăn mòn điện hóa xảy ra sự oxi hóa.
C. Chỉ dùng phenolphtalein có thể nhận biết được tất cả dung dịch sau đây: NaCl, NaHSO4, CaCl2, AlCl3, FeCl3, Na2CO3.
D. Có 2 trong số các chất (phenol, anilin, toluen, metyl phenyl ete) tác dụng được với dung dịch brom.
(Xem giải) Câu 15: Dẫn 26,88 lít (đktc) hỗn hợp X gồm hơi nước và khí cacbonic qua than nung đỏ thu được a mol hỗn hợp khí Y gồm CO, H2, CO2; trong đó có V1 lít (đktc) CO2. Hấp thụ hoàn toàn khí CO2 vào dung dịch có chứa 0,06b mol Ca(OH)2, khối lượng kết tủa tạo ra phụ thuộc vào thể tích khí CO2 được ghi ở bảng sau:
| Thể tích khí CO2 ở đktc (lít) | V | V + 8,96 | V1 |
| Khối lượng kết tủa (gam) | 5b | 3b | 2b |
Giá trị của a có thể là
A. 1,28. B. 1,48. C. 1,36. D. 1,40.
(Xem giải) Câu 16: Cho hỗn hợp gồm Al và Fe vào dung dịch chứa FeCl3 và CuCl2, sau khi kết thúc phản ứng thu được dung dịch X và chất rắn Y. Cho dung dịch AgNO3 dư vào X thu được kết tủa Z. Cho Z vào dung dịch HNO3 dư, thấy thoát ra khí không màu hóa nâu ngoài không khí. Cho Y vào dung dịch HCl dư, thì Y chỉ tan một phần. Nhận xét nào sau đây không đúng?
A. Dung dịch X chứa tối đa ba muối.
B. Chất rắn Y gồm các kim loại Fe, Cu.
C. Kết tủa Z gồm Ag và AgCl.
D. Cho dung dịch NaOH dư vào X (không có oxi), thu được một kết tủa duy nhất.
(Xem giải) Câu 17: Hòa tan hết m gam hỗn hợp gồm Na, Na2O, Ba và BaO vào nước, thu được 0,15 mol khí H2 và dung dịch X. Sục 0,32 mol khí CO2 vào dung dịch X, thu được dung dịch Y chỉ chứa các ion Na+, HCO3-, CO32- và kết tủa Z. Chia dung dịch Y làm 2 phần bằng nhau:
– Cho từ từ đến hết phần 1 vào 200 ml dung dịch HCl 0,6M thấy thoát ra 0,075 mol khí CO2, coi tốc độ phản ứng của HCO3-, CO32- với H+ bằng nhau.
– Cho từ từ đến hết 200 ml dung dịch HCl 0,6M vào phần 2, thấy thoát ra 0,06 mol khí CO2.
Các phản ứng xảy ra hoàn toàn, H2O phân li không đáng kể. Giá trị của m là
A. 25,32. B. 25,88. C. 24,68. D. 24,66.
(Xem giải) Câu 18: Thực hiện các thí nghiệm sau:
(a) Đun nóng dung dịch Ca(HCO3)2.
(b) Nhiệt phân NaNO3 ở nhiệt độ cao.
(c) Cho dung dịch HCl vào dung dịch Fe(NO3)2.
(d) Cho dung dịch Na2CO3 vào dung dịch AlCl3.
(e) Cho dung dịch NaAlO2 vào dung dịch NH4Cl.
(g) Cho dung dịch FeCl3 vào dung dịch Na2S.
Số thí nghiệm có thể tạo thành chất khí sau phản ứng là
A. 2. B. 4. C. 3. D. 5.
(Xem giải) Câu 19: Hòa tan hoàn toàn hai chất rắn X, Y có số mol bằng nhau vào nước, thu được dung dịch Z. Tiến hành các thí nghiệm:
– Thí nghiệm 1: Cho Z phản ứng với dung dịch BaCl2, thấy có n1 mol BaCl2 phản ứng.
– Thí nghiệm 2: Cho Z phản ứng với dung dịch HCl, thấy có n2 mol HCl phản ứng.
– Thí nghiệm 3: Cho Z phản ứng với dung dịch NaOH, thấy có n3 mol NaOH phản ứng.
Biết các phản ứng xảy ra hoàn toàn và n1 < n2 < n3. Hai chất X, Y lần lượt là
A. NH4HCO3, Na2CO3. B. NaHCO3, (NH4)2CO3. C. NaHCO3, Na2CO3. D. NH4HCO3, (NH4)2CO3.
(Xem giải) Câu 20: Đốt cháy hoàn toàn m gam hỗn hợp X gồm 3 hiđrocacbon đều mạch hở cần dùng 11,76 lít khí O2, sau phản ứng thu được 15,84 gam CO2. Nung m gam hỗn hợp X với 0,04 mol H2 có xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn Y qua bình đựng dung dịch Br2 dư thấy lượng Br2 phản ứng là 17,6 gam đồng thời khối lượng của bình tăng a gam và có 0,896 lít khí Z duy nhất thoát ra. Biết các khí đo ở đktc. Giá trị của a là
A. 3,30. B. 2,75. C. 3,20. D. 2,65.
(Xem giải) Câu 21: Cho các phát biểu sau:
(a) Anilin phản ứng với HCl, đem sản phẩm tác dụng với NaOH lại thu được anilin.
(b) Oxi hóa glucozơ bằng AgNO3 trong NH3 đun nóng thu được axit gluconic.
(c) Hạn chế sử dụng túi nilon là một trong những cách để bảo vệ môi trường.
(d) Alanin tác dụng với dung dịch NaOH, lấy sản phẩm tác dụng với dung dịch HCl lại thu được alanin.
(e) Cho muối amoni fomat tác dụng với dung dịch AgNO3 trong NH3 đun nóng thu được sản phẩm chỉ gồm các chất vô cơ.
(g) Hợp chất chứa một liên kết pi trong phân tử là hợp chất không no.
Số phát biểu đúng là
A. 4. B. 2. C. 3. D. 5.
Câu 22: Dùng nước rửa tay khô là một trong những cách để phòng chống Covid-19. Thành phần hóa học của nước rửa tay khô thường bao gồm chất E, nước tinh khiết, chất giữ ẩm, chất tạo hương, chất diệt khuẩn. Chất E được dùng thay xăng làm nhiên liệu cho động cơ đốt trong. Ở nước ta đã tiến hành pha E vào xăng truyền thống với tỉ lệ 5% để được xăng E5. Chất E là
A. axit axetic. B. etanol. C. glucozơ. D. metanol.
(Xem giải) Câu 23: Hỗn hợp E gồm tinh bột và xenlulozơ. Đốt cháy hoàn toàn m gam E bằng khí O2, thu được số mol CO2 và số mol H2O hơn kém nhau 0,02 mol. Thủy phân hoàn toàn m gam E, thu được dung dịch T; trung hòa T bằng kiềm rồi tiếp tục cho tác dụng với AgNO3 dư (trong dung dịch NH3, t°), thu được tối đa a gam Ag. Giá trị của a là
A. 2,16. B. 8,64. C. 6,48. D. 4,32.
(Xem giải) Câu 24: X và Y là hai nguyên tố thuộc cùng một chu kì và ở hai nhóm A liên tiếp trong bảng tuần hoàn (số hiệu nguyên tử ZX < ZY). Tổng số hạt mang điện trong nguyên tử X và Y là 102. Số hiệu nguyên tử của X là
A. 26. B. 20. C. 25. D. 31.
(Xem giải) Câu 25: Oxi hóa m gam ancol X đơn chức thu được 1,8m gam hỗn hợp Y gồm anđehit, axit cacboxylic và nước. Chia hỗn hợp Y thành hai phần bằng nhau. Phần 1: tác dụng với Na dư, thu được 4,48 lít khí H2 (đktc). Phần 2: tác dụng với AgNO3 dư trong dung dịch NH3, thu được a gam Ag. Giá trị của m và a lần lượt là
A. 20,0 và 108,0. B. 12,8 và 64,8. C. 16,0 và 43,2. D. 16,0 và 75,6.
(Xem giải) Câu 26: Cho 3,94 gam hỗn hợp X gồm C, P, S vào dung dịch HNO3 đặc, nóng, dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp hai khí trong đó có 0,90 mol khí NO2 (sản phẩm khử duy nhất) và dung dịch Y. Đem dung dịch Y tác dụng với dung dịch BaCl2 dư thu được 4,66 gam một chất kết tủa. Mặt khác, khi đốt cháy hoàn toàn 3,94 gam hỗn hợp X trong oxi dư, lấy toàn bộ khí tạo thành hấp thụ hết vào dung dịch chứa 0,1 mol KOH và 0,15 mol NaOH thu được dung dịch chứa m gam chất tan. Giá trị của m là
A. 20,68 B. 16,15. C. 16,18. D. 15,64
(Xem giải) Câu 27: Cho các nhận xét sau:
(a) Cộng hóa trị của nguyên tố nitơ trong phân tử axit nitric là 4.
(b) Các nguyên tố trong cùng nhóm A đều có số electron lớp ngoài cùng trong nguyên tử bằng nhau.
(c) Chất X vừa tác dụng với dung dịch axit, vừa tác dụng với dung dịch bazơ chứng tỏ X lưỡng tính.
(d) Để điều chế kim loại kiềm, kiềm thổ, nhôm có thể điện phân nóng chảy muối halogenua tương ứng của chúng.
(e) Hợp kim Fe-C bị ăn mòn điện hóa trong không khí ẩm, tại catot xảy ra quá trình: O2 + 2H2O + 4e → 4OH-.
(g) Người ta tạo ra “sắt tây” (sắt tráng thiếc), “tôn” (sắt tráng kẽm) là vận dụng phương pháp điện hóa để bảo vệ sắt khỏi ăn mòn.
Số nhận xét đúng là
A. 3. B. 4. C. 2. D. 5.
(Xem giải) Câu 28: Tiến hành thí nghiệm sau:
Bước 1: Rót vào ống nghiệm 1 và 2, mỗi ống khoảng 3 ml dung dịch H2SO4 loãng cùng nồng độ và cho vào mỗi ống một mẩu kẽm như nhau. Quan sát bọt khí thoát ra.
Bước 2: Nhỏ thêm 2 – 3 giọt dung dịch CuSO4 vào ống 2. So sánh tốc độ bọt khí thoát ra ở 2 ống.
Cho các phát biểu sau:
(a) Bọt khí thoát ra ở ống 2 nhanh hơn so với ống 1.
(b) Ống 1 chỉ xảy ra ăn mòn hoá học còn ống 2 chỉ xảy ra ăn mòn điện hoá.
(c) Bọt khí thoát ra ở 2 ống tốc độ là như nhau.
(d) Ở cả hai ống nghiệm, Zn đều bị oxi hoá thành Zn2+.
(e) Ở bước 1, nếu thay kim loại kẽm bằng kim loại sắt thì hiện tượng vẫn xảy ra tương tự.
(g) Ở bước 2, nếu thay dung dịch CuSO4 bằng dung dịch MgSO4 thì hiện tượng vẫn xảy ra tương tự.
Số phát biểu đúng là
A. 3. B. 2. C. 4. D. 5.
(Xem giải) Câu 29: Cho a mol mỗi chất Fe, FeO, Fe3O4, FeCO3, Fe(NO3)2, FeI2, FeS, Fe(OH)2, KBr, Cu2O tác dụng với dung dịch HNO3 đặc, nóng, dư. Có bao nhiêu chất sau phản ứng thu được a mol khí NO2 (sản phẩm khử duy nhất)?
A. 6. B. 7. C. 5. D. 8.
(Xem giải) Câu 30: Ba dung dịch A, B, C thỏa mãn:
– A tác dụng với B thu được kết tủa X, cho X vào dung dịch HNO3 loãng dư, thấy thoát ra khí không màu hóa nâu ngoài không khí, đồng thời thu được kết tủa Y.
– B tác dụng với C thấy khí thoát ra, đồng thời thu được kết tủa.
– A tác dụng C thu được kết tủa Z, cho Z vào dung dịch HCl dư, thấy khí không màu thoát ra.
A, B, C lần lượt là các dung dịch:
A. FeCl2, AgNO3, Ba(OH)2. B. FeSO4, Ba(OH)2, (NH4)2CO3.
C. NaHSO4, Ba(HCO3)2, Fe(NO3)3. D. CuSO4, Ba(OH)2, Na2CO3.
(Xem giải) Câu 31: X, Y, Z là 3 este đều no, mạch hở và không phân nhánh. Đốt cháy 0,115 mol hỗn hợp E chứa X, Y, Z thu được 10,304 lít khí CO2 (đktc). Mặt khác đun nóng 22,34 gam E cần dùng 300 ml dung dịch NaOH 1M, thu được hỗn hợp muối và hỗn hợp F chứa các ancol. Dẫn toàn bộ F qua bình đựng Na dư thấy khối lượng bình tăng 13,7 gam. Lấy hỗn hợp muối nung với vôi tôi xút thu được một khí duy nhất có khối lượng m gam. Giá trị của m là
A. 0,81. B. 0,44. C. 0,54. D. 1,08.
(Xem giải) Câu 32: Hòa tan hoàn toàn 13,44 gam kim loại M (hóa trị không đổi) vào dung dịch axit HNO3 dư, thu được dung dịch X. Chia X thành 2 phần bằng nhau:
– Phần 1: cho tác dụng với dung dịch NaOH dư thu được kết tủa Y. Nung Y đến khối lượng không đổi thu được 11,2 gam oxit kim loại.
– Phần 2: cô cạn ở điều kiện thích hợp thu được 71,68 gam một muối A duy nhất.
Thành phần phần trăm theo khối lượng của nguyên tố oxi trong muối A gần nhất với:
A. 78%. B. 73% C. 77%. D. 74%.
(Xem giải) Câu 33: X, Y và Z là những cacbohiđrat. X là chất rắn, ở dạng bột vô định hình, màu trắng. Y là loại đường phổ biến nhất, có nhiều nhất trong cây mía, củ cải đường và hoa thốt nốt. Sự dư thừa Z trong máu người là nguyên nhân gây ra bệnh tiểu đường. Tên gọi của X, Y, Z lần lượt là
A. tinh bột, saccarozơ và glucozơ. B. xenlulozơ, saccarozơ và fructozơ.
C. tinh bột, saccarozơ và fructozơ. D. tinh bột, fructozơ và glucozơ.
(Xem giải) Câu 34: Cho hỗn hợp M gồm X (CnH2n+4O4N2) là muối của axit cacboxylic đa chức và chất Y (CmH2m+6O3N2). Đốt cháy hoàn toàn 0,6 mol M cần vừa đủ 2,9 mol O2, thu được H2O, N2 và 2,2 mol CO2. Mặt khác, cho 0,6 mol M tác dụng hết với lượng dư dung dịch NaOH đun nóng, thu được metylamin duy nhất và dung dịch chứa a gam hỗn hợp hai muối. Giá trị của a là
A. 65,2. B. 85,0. C. 74,8. D. 70,6.
(Xem giải) Câu 35: Nguyên tố X có hoá trị cao nhất đối với oxi bằng hoá trị trong hợp chất khí với hiđro. Tỉ khối hơi của oxit cao nhất so với hợp chất khí với hiđro của X là 2,75. Nguyên tố Y có hoá trị cao nhất đối với oxi bằng 3 lần hoá trị trong hợp chất khí với hiđro. Tỉ khối hơi của hợp chất khí với hiđro so với oxit cao nhất của Y là 0,425. Trong hạt nhân nguyên tử X và Y đều có số hạt mang điện bằng số hạt không mang điện. Nhận xét nào sau đây không đúng?
A. Nguyên tố Z cùng chu kì với X và cùng nhóm với Y đều có độ âm điện lớn hơn X và Y.
B. Hợp chất tạo bởi X và Y là XY2 là một chất hữu cơ.
C. Oxit cao nhất của X và Y đều là những chất khí ở điều kiện thường.
D. X ở chu kì 2, còn Y ở chu kì 3 trong bảng tuần hoàn.
(Xem giải) Câu 36: Thủy phân hoàn toàn 1 mol peptit mạch hở X thu được 2 mol Gly, 1 mol Ala và 1 mol Val. Mặt khác thủy phân không hoàn toàn X thu được các aminoaxit và các peptit (trong đó có Ala-Gly và Gly-Val). Số công thức cấu tạo phù hợp với X là
A. 2. B. 3. C. 5. D. 4.
(Xem giải) Câu 37: Hỗn hợp E gồm este X đơn chức và axit cacboxylic Y hai chức (đều mạch hở, không no có một liên kết đôi C=C trong phân tử). Đốt cháy hoàn toàn m gam E thu được 18,92 gam khí CO2 và 5,76 gam nước. Mặt khác, thủy phân hoàn toàn 46,6 gam E bằng 200 gam dung dịch NaOH 12% rồi cô cạn dung dịch thu được phần hơi Z có chứa chất hữu cơ T. Dẫn toàn bộ Z vào bình đựng Na, sau phản ứng khối lượng bình tăng 188 gam đồng thời thoát ra 15,68 lít khí H2 (đktc). Biết tỉ khối của T so với O2 là 1. Phần trăm số mol của Y trong hỗn hợp E là
A. 46,35%. B. 37,5%. C. 53,65%. D. 62,5%.
(Xem giải) Câu 38: Dùng 19,04 lít không khí ở đktc (O2 chiếm 20% và N2 chiếm 80% thể tích) để đốt cháy hoàn toàn 3,21 gam hỗn hợp A gồm hai aminoaxit no, mạch hở chứa 1 nhóm -NH2, 1 nhóm -COOH là đồng đẳng kế tiếp thu được hỗn hợp B. Dẫn B qua dung dịch nước vôi trong dư thu được 9,50 gam kết tủa. Nếu làm khô B rồi cho vào bình dung tích 2 lít, nhiệt độ 127°C thì áp suất trong bình lúc này là p atm. Biết aminoaxit khi cháy sinh khí N2. Giá trị của p gần nhất với:
A. 13. B. 16. C. 15. D. 14.
Câu 39: Trồng dâu, nuôi tằm là một nghề vất vả đã được dân gian đúc kết trong câu: “Nuôi lợn ăn cơm nằm, nuôi tằm ăn cơm đứng”. Con tằm sau khi nhả tơ tạo thành kén tằm được sử dụng để dệt thành những tấm tơ lụa có giá trị kinh tế cao, đẹp và mềm mại. Theo em, tơ tằm thuộc loại tơ nào?
A. Tơ hóa học. B. Tơ bán tổng hợp. C. Tơ thiên nhiên. D. Tơ tổng hợp.
(Xem giải) Câu 40: Hỗn hợp E chứa các chất hữu cơ mạch hở gồm tetrapeptit X; pentapeptit Y và Z là este của α-amino axit có công thức phân tử C3H7O2N. Đun nóng 36,86 gam hỗn hợp E với dung dịch NaOH vừa đủ, cô cạn dung dịch sau phản ứng thu được phần hơi chứa ancol T có khối lượng 3,84 gam và phần rắn gồm 2 muối của glyxin và alanin. Đốt cháy hết hỗn hợp muối cần dùng 1,455 mol O2, thu được CO2, H2O, N2 và 26,5 gam Na2CO3. Thành phần trăm theo khối lượng của X trong E là
A. 14,87%. B. 56,16%. C. 28,97%. D. 45,28%.
(Xem giải) Câu 41: Kết quả phân tích thành phần khối lượng của một mẫu apatit như sau:
| Thành phần | CaO | P2O5 | SiO2 | F | SO3 | CO2 |
| % khối lượng | 52,29% | 38,83% | 2,72% | 1,77% | 3,22% | 1,17% |
Hòa tan m1 gam mẫu apatit vào lượng vừa đủ 25,0 ml dung dịch H3PO4 1,0M và H2SO4 0,2M. Cô cạn cẩn thận dung dịch sau phản ứng, thu được m2 gam chất rắn gồm CaSO4.2H2O, Ca(H2PO4)2, SiO2. Tổng của m1 và m2 gần nhất với:
A. 8,4 gam. B. 8,3 gam. C. 9,1 gam. D. 8,7 gam.
(Xem giải) Câu 42: Đun 24,8 gam hỗn hợp X gồm phenol và fomanđehit (tỉ lệ mol 1 : 1, xúc tác axit) thu được hỗn hợp X gồm polime và một chất trung gian là ancol o-hiđroxibenzylic (Y). Tách polime, cho Y phản ứng vừa đủ với dung dịch Br2 thu được 2,82 gam kết tủa. Hiệu suất của phản ứng tạo polime là
A. 90%. B. 95%. C. 85%. D. 80%.
(Xem giải) Câu 43: Đốt cháy hoàn toàn a mol một este no, đơn chức mạch hở X, cần b mol O2, tạo ra c mol hỗn hợp CO2 và H2O. Biết c = 2(b – a). Số đồng phân este của X là
A. 6. B. 3. C. 4. D. 2.
(Xem giải) Câu 44: X là axit thuộc dãy đồng đẳng của axit acrylic, Y là axit no, hai chức, mạch hở; Z là este no, hai chức, mạch hở. Đun nóng 17,84 gam hỗn hợp E gồm X, Y, Z với 120 gam dung dịch MOH 12% (M là kim loại kiềm), cô cạn dung dịch sau phản ứng thu được rắn F chỉ gồm hai muối. Đốt cháy hoàn toàn F thu được H2O; 0,18 mol M2CO3 và 0,26 mol CO2. Mặt khác đốt cháy 17,84 gam hỗn hợp E thu được 0,48 mol CO2. Phần trăm khối lượng của muối có phân tử khối lớn hơn trong F là
A. 86,30%. B. 70,63%. C. 85,08%. D. 76,89%.
(Xem giải) Câu 45: Chất X có công thức C6H10O5 (trong phân tử không chứa nhóm -CH2-). Khi cho X tác dụng với NaHCO3 hoặc với Na thì số mol khí sinh ra luôn bằng số mol X đã phản ứng. Thực hiện sơ đồ chuyển hóa sau:
(1) X —> Y + H2O
(2) X + 2NaOH —> 2Z + H2O
(3) Y + 2NaOH —> Z + T + H2O
(4) 2Z + H2SO4 —> 2P + Na2SO4
(5) T + NaOH —> (t°, CaO) Na2CO3 + Q
(6) Q + H2O —> G
Biết rằng X, Y, Z, T, P, Q đều là các hợp chất hữu cơ mạch hở. Có các phát biểu sau:
(a) X chứa đồng thời nhóm chức ancol, axit, este.
(b) Y có nhiều trong sữa chua.
(c) P tác dụng Na dư cho.
(d) Q có khả năng làm hoa quả nhanh chín.
(e) Hiđro hóa hoàn toàn T (Ni, t°) thu được Z.
(g) Dùng G để sản xuất axit axetic theo phương pháp hiện đại.
Số phát biểu đúng là
A. 4. B. 2. C. 3. D. 5.
(Xem giải) Câu 46: Đốt cháy hoàn toàn 2,54 gam este A (không chứa nhóm chức khác) mạch hở, được tạo ra từ một axit cacboxylic đơn chức và ancol no, thu được 2,688 lít khí CO2 (đktc) và 1,26 gam nước. Cho 0,1 mol A tác dụng vừa đủ với 200ml NaOH 1,5M tạo ra m gam muối và ancol. Giá trị của m là
A. 32,2. B. 28,8. C. 30,0. D. 28,2.
(Xem giải) Câu 47: Hỗn hợp hơi E chứa 2 ancol đều mạch hở và một anken. Đốt cháy 0,2 mol E cần 0,48 mol O2 th được CO2 và H2O với tổng khối lượng là 23,04 gam. Mặt khác dẫn 0,2 mol E qua bình đựng Na dư thu được 1,792 lít H2 (đktc). Nếu lấy 19,2 gam E tác dụng với dung dịch Br2 1M thì thể tích dung dịch Br2 tối đa phản ứng là
A. 350 ml. B. 400 ml. C. 300 ml. D. 450 ml.
(Xem giải) Câu 48: Nhỏ từ từ V lít dung dịch chứa Ba(OH)2 0,5M vào dung dịch chứa a mol NaHCO3 và b mol BaCl2. Đồ thị sau biểu diễn sự phụ thuộc giữa số mol kết tủa và thể tích dung dịch Ba(OH)2.
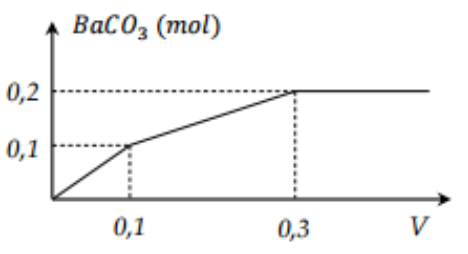
Tỉ lệ a/b có giá trị là
A. 5. B. 3. C. 4. D. 2.
(Xem giải) Câu 49: Có 4 dung dịch riêng biệt: H2SO4 1M; KNO3 2M; HNO3 4M; HCl 0,5M được đánh số ngẫu nhiên là (1), (2), (3), (4). Lấy cùng thể tích 2 dung dịch ngẫu nhiên là 5ml rồi tác dụng với Cu dư. Thu được kết quả thí nghiệm khí NO như sau: (NO sản phẩm khử duy nhất, thể tích khí đo cùng điều kiện nhiệt độ, áp suất)
| (1)+ (2) | (1) + (3) | (1) + (4) | (4) + (2) | (4) + (3) | |
| V NO (lít) | 4V | V | 8V | V1 | V2 |
Tỉ lệ V1 : V2 là
A. 5:4. B. 4:3. C. 4:5. D. 3:4.
(Xem giải) Câu 50: Thực hiện thí nghiệm như hình vẽ bên.
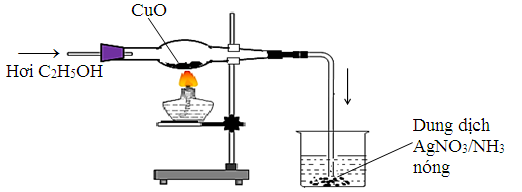
Cho các nhận xét sau:
(a) CuO từ màu đen chuyển sang màu đỏ.
(b) Nên đun nóng ống đựng CuO trước khi dẫn C2H5OH qua.
(c) Kết tủa thu được trong cốc có màu vàng.
(d) Thí nghiệm trên dùng để điều chế và thử tính chất của axetilen.
(e) Khi tháo dụng cụ, nên tháo ống dẫn ra khỏi dung dịch AgNO3/NH3 rồi mới tắt đèn cồn.
(g) Các phản ứng chính xảy ra trong thí nghiệm trên đều là phản ứng oxi hóa – khử.
Số nhận xét đúng là
A. 4. B. 2. C. 3. D. 5.

Bình luận