[2024 – 2025] Thi học sinh giỏi lớp 12 cụm Hải Dương (25/09)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề 018-H12B năm 2024-2025
⇒ Thời gian làm bài: 90 phút
⇒ Bảng đáp án phần trắc nghiệm:
Đáp án phần 1:
| 1A | 2C | 3C | 4C | 5B | 6C | 7C | 8C |
| 9C | 10B | 11A | 12D | 13B | 14A | 15D | 16A |
| 17D | 18C | 19B | 20D | 21C | 22A | 23D | 24B |
Đáp án phần 2:
| Câu 25 | Câu 26 | Câu 27 | Câu 28 | Câu 29 | Câu 30 | |
| (a) | Đ | S | Đ | Đ | S | Đ |
| (b) | S | S | Đ | Đ | Đ | Đ |
| (c) | Đ | S | S | Đ | Đ | Đ |
| (d) | Đ | Đ | Đ | S | S | S |
Đáp án phần 3:
| Câu 31 | Câu 32 | Câu 33 | Câu 34 | Câu 35 | Câu 36 | Câu 37 | Câu 38 |
| 10,0 | 1 | 9,60 | 28,5 | 0,44 | 14,6 | 160,5 | 8,16 |
⇒ Đề thi và giải chi tiết:
Phần I: Câu hỏi trắc nghiệm nhiều lựa chọn (6,0 điểm) (Mỗi câu trả lời đúng thí sinh được 0,25 điểm)
(Xem giải) Câu 1: Hiện nay, nhiều nơi ở nông thôn một số hộ gia đình đang sử dụng hầm biogas để xử lí chất thải trong chăn nuôi gia súc, cung cấp nhiên liệu cho việc đun nấu. Chất dễ cháy trong khí biogas là
A. CH4. B. Cl2. C. N2. D. CO2.
(Xem giải) Câu 2: Cho các ester sau: CH3COOC2H5, HCOOC(CH3)=CH2, C2H5COOC6H4CH3 (có vòng benzene), C6H5COOCH3. Ở điều kiện thích hợp, có bao nhiêu ester thủy phân không hoàn toàn trong môi trường acid?
A. 4. B. 3. C. 2. D. 1.
(Xem giải) Câu 3: Phản ứng với chất nào sau đây chứng tỏ glucose có nhóm -OH hemiacetal?
A. Cu(OH)2. B. Nước bromine. C. CH3OH/HCl. D. Dung dịch AgNO3/NH3, t°.
(Xem giải) Câu 4: Một mẫu nước thải của nhà máy sản xuất X có pH = 4. Để thải ra ngoài môi trường theo đúng qui định thì cần phải điều chỉnh pH nằm trong khoảng từ 6,5 đến 7,5 nên nhà máy thường sử dụng vôi sống để xử lí. Khối lượng vôi sống cần dùng cho 1m³ nước để nâng pH của nước thải từ 4 lên 7 là (Giả thiết chỉ xảy ra phản ứng giữa ion H+ và OH- cũng như bỏ qua sự thủy phân của các muối nếu có)
A. 4,20 gam. B. 0,56 gam. C. 2,80 gam. D. 0,28 gam.
(Xem giải) Câu 5: Chất béo là thức ăn quan trọng của con người, là nguồn cung cấp dinh dưỡng và năng lượng đáng kể cho cơ thể hoạt động. Ngoài ra một lượng lớn chất béo được dùng trong công nghiệp để sản xuất
A. glucose và glycerol. B. xà phòng và glycerol.
C. glucose và ethanol. D. xà phòng và ethanol.
(Xem giải) Câu 6: Trong một bình kín có cân bằng hóa học sau: 2NO2 (g) ⇋ N2O4 (g). Tỉ khối hơi của hỗn hợp khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và ở nhiệt độ T2 bằng 34,5. Biết T1 > T2. Phát biểu nào sau đây về cân bằng trên là đúng?
A. Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm.
B. Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng.
C. Phản ứng thuận là phản ứng tỏa nhiệt.
D. Phản ứng nghịch là phản ứng tỏa nhiệt.
(Xem giải) Câu 7: Xà phòng và chất giặt rửa tổng hợp đều có khả năng làm sạch bụi bẩn, dầu mỡ bám trên bề mặt. Cho các phát biểu sau:
(1) Xà phòng dễ tan trong nước hơn chất giặt rửa tổng hợp, do đó được sử dụng phổ biến.
(2) Có thể sử dụng chất giặt rửa tổng hợp với cả nước cứng, do chất giặt rửa tổng hợp không tạo muối khó tan với Ca2+, Mg2+.
(3) Chất giặt rửa tổng hợp khó bị phân hủy sinh học bởi các vi sinh vật, do đó gây ô nhiễm môi trường.
(4) Không nên dùng xà phòng giặt rửa trong nước cứng (chứa nhiều ion Ca2+, Mg2+) do muối của các kim loại này với acid béo ít tan,… và gây hại cho áo, quần sau khi giặt.
Số phát biểu đúng là:
A. 1. B. 2. C. 3. D. 4.
(Xem giải) Câu 8: Cho 20 gam CuO tác dụng vừa đủ với dung dịch H2SO4 25% đun nóng, sau đó làm nguội dung dịch đến 10°C. Khối lượng tinh thể CuSO4.5H2O đã tách ra khỏi dung dịch là (Biết rằng ở 10°C cứ 100 gam H2O hòa tan 14,4 gam CuSO4).
A. 50 gam. B. 34,33 gam. C. 48,91 gam. D. 22,5 gam.
(Xem giải) Câu 9: Cho ba dung dịch có cùng nồng độ: HCl, CH3COOH, NaOH. Khi chuẩn độ riêng một thể tích như nhau của dung dịch HCl và dung dịch CH3COOH bằng dung dịch NaOH, phát biểu nào sau đây là đúng?
A. Trước khi chuẩn độ, pH của hai acid bằng nhau.
B. Tại các điểm tương đương, dung dịch của cả hai phép chuẩn độ đều có giá trị pH bằng 7.
C. Cần cùng một thể tích NaOH để đạt đến điểm tương đương.
D. Giá trị pH của hai acid tăng như nhau cho đến khi đạt điểm tương đương.
(Xem giải) Câu 10: Hydrocarbon là nguồn nguyên liệu trong tổng hợp hữu cơ. Một trong các chuyển hóa hydrocarbon được biết đến là quá trình sản xuất xà phòng từ hydrocarbon no, mạch dài không phân nhánh. Quá trình được mô tả theo sơ đồ sau:
R-CH2-CH2-R + O2 → RCOOH + H2O (1)
RCOOH + NaOH → RCOONa + H2O (2)
(a) Trong phản ứng (1), số mol O2 phản ứng gấp 2,5 lần số mol hydrocarbon phản ứng.
(b) Trong phản ứng (2), có thể thay NaOH bằng Na2CO3 thì muối thu được không thay đổi.
(c) Muối sodium stearate có khả năng giặt rửa là do nhóm -COO- dễ xâm nhập vào các vết dầu mỡ.
(d) Nếu hiệu suất quá trình là 90% thì cần 1 tấn hydrocarbon để sản xuất được 1 tấn sodium stearate.
Số phát biểu đúng là:
A. 1. B. 2. C. 4. D. 3.
(Xem giải) Câu 11: Pin nhiên liệu cung cấp năng lượng và nhiệt giải phóng khi pin hoạt động. Ngoài ra, việc vận hành pin nhiên liệu không phát sinh tiếng ồn và giải phóng nước, không làm ô nhiễm môi trường như nhiên liệu hoá thạch. Pin nhiên liệu sử dụng tế bào nhiên liệu với nguyên liệu là khí hydrogen để chuyển hoá năng lượng thành điện năng:
Anode (+): 2H2 + 4OH- → 4H2O + 4e
Cathode (-): O2 + 4e + 2H2O → 4OH-
Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất là 56% (nghĩa là có 56% năng lượng của phản ứng chuyển hoá thành điện năng). Mỗi ngày nhà máy sản xuất được 500 kWh. Tính khối lượng (theo kg) khí hydrogen tiêu thụ? Cho biết:  (H2O(l)) = -285,84 kJ/mol, 1kWh = 3,6.10^6 J.
(H2O(l)) = -285,84 kJ/mol, 1kWh = 3,6.10^6 J.
A. 22,49. B. 22490. C. 12,59. D. 12594.
(Xem giải) Câu 12: Dẫn dòng khí gồm acethylene và ethylene lần lượt đi vào ống nghiệm (1) đựng dung dịch AgNO3 trong NH3 ở điều kiện thường, sau đó dẫn tiếp qua ống nghiệm (2) đựng dung dịch bromine. Hiện tượng thí nghiệm nào sau đây không đúng?
A. Ở ống nghiệm (1) có kết tủa màu vàng nhạt.
B. Ở ống nghiệm (2) màu của dung dịch bromine nhạt dần.
C. Ở ống nghiệm (2) chất lỏng chia thành hai lớp.
D. Ở ống nghiệm (2) thu được chất lỏng đồng nhất.
(Xem giải) Câu 13: Cho sơ đồ phản ứng sau:
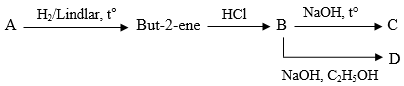
Biết các sản phẩm hữu cơ thu được đều là sản phẩm chính. Phát biểu nào sau đây là đúng?
A. Tên của A là but-1-yne.
B. Công thức cấu tạo của C là CH3CH2CH(OH)CH3
C. Tên của B là 3-chlorobutane.
D. Công thức cấu tạo của D là CH3-CH2-CH=CH2.
(Xem giải) Câu 14: Ruộng lúa mới cấy được một tháng. Lúa đã cứng cây và đang phát triển cần được bón thúc bằng phân đạm Urea để lúa phát triển tốt hơn. Nhưng rêu xanh đang phủ kín mặt ruộng, cần phải bón vôi để diệt rêu. Phương án tối ưu để giải quyết đồng thời hai vấn đề trên là
A. Bón vôi toả (Ca(OH)2) trước, vài ngày sau mới bón đạm.
B. Bón đạm trước một lát rồi bón vôi toả.
C. Trộn đều vôi toả với đạm rồi bón cùng một lúc.
D. Bón vôi toả trước một lát rồi bón đạm.
(Xem giải) Câu 15: Cho 10 mL ethyl alcohol 46° phản ứng hết với kim loại Na (dư), thu được V lít khí H2 (đkc). Biết khối lượng riêng của ethyl alcohol nguyên chất bằng 0,8 g/mL; của nước bằng 1,0 g/mL. Giá trị của V là
A. 4,256. B. 0,896. C. 3,7185. D. 4,7101.
(Xem giải) Câu 16: Số đồng phân là hợp chất thơm có công thức phân tử C8H10O tác dụng được với NaOH là:
A. 9. B. 6. C. 7. D. 8.
(Xem giải) Câu 17: Xét các phát biểu sau:
(a) Ở điều kiện thường không có alcohol no nào là chất khí;
(b) Nhiệt độ sôi của alcohol luôn nhỏ hơn nhiệt độ sôi của carboxylic acid có cùng số nguyên tử carbon;
(c) Khi đun nóng hỗn hợp các alcohol no, mạch hở, đơn chức có số nguyên tử carbon nhỏ hơn 4 với H2SO4 đặc ở 170°C chỉ tạo ra tối đa một alkene;
(d) Propenal tác dụng với Br2 dư tối đa theo tỉ lệ mol 1 : 2;
(e) Chỉ có 1 alcohol có công thức phân tử C3H6O.
(g) Formic acid tác dụng được với dung dịch AgNO3/NH3, nước bromine, dung dịch NaHCO3.
Số phát biểu đúng là:
A. 6. B. 4. C. 5. D. 3.
(Xem giải) Câu 18: Tiến hành thí nghiệm theo các bước sau:
– Bước 1: Chuẩn bị ba mẫu phân bón hóa học sau: (NH4)2SO4, KCl và Ca(H2PO4)2. Lấy mỗi loại một ít (bằng hạt ngô) vào từng ống nghiệm. Cho vào mỗi ống nghiệm 4 – 5 mL nước cất và lắc nhẹ ống nghiệm cho đến khi ba mẫu phân bón tan hết và đánh số thứ tự (NH4)2SO4 là mẫu (1), KCl là mẫu (2) và Ca(H2PO4)2 là mẫu (3).
– Bước 2: Lấy khoảng 2 mL dung dịch mỗi loại mẫu phân bón vừa pha chế vào từng ống nghiệm. Cho vào mỗi ống nghiệm 1 mL dung dịch NaOH rồi đun nóng nhẹ. Quan sát hiện tượng từng ống nghiệm
– Bước 3: Lấy khoảng 2 mL dung dịch mỗi loại mẫu phân bón của phần còn lại vào từng ống nghiệm. Cho vào mỗi ống nghiệm vài giọt dung dịch AgNO3. Quan sát hiện tượng từng ống nghiệm
Cho các nhận định sau:
(a) Ở bước 2, ống nghiệm chứa mẫu (1) có khí mùi khai bay ra.
(b) Ở bước 2, ống nghiệm chứa mẫu (2) không có hiện tượng gì.
(c) Ở bước 2, ống nghiệm chứa mẫu (3) có kết tủa vàng.
(d) Ở bước 3, ống nghiệm chứa mẫu (1) có kết tủa trắng.
(e) Ở bước 3, ống nghiệm chứa mẫu (2) có kết tủa trắng.
(g) Ở bước 3, ống nghiệm chứa mẫu (3) có kết tủa vàng.
Số nhận định đúng là
A. 3. B. 4. C. 5. D. 6.
(Xem giải) Câu 19. Cho bảng nhiệt độ sôi (°C) đo ở áp suất 1 atm như sau:
| Công thức chất | C2H5OH | CH3COOH | H2O | CH3COOC2H5 | H2SO4 |
| Nhiệt độ sôi | 78,3 | 118 | 100 | 77 | 337 |
Ethyl acetate được điều chế bằng cách đun nóng hỗn hợp gồm acetic acid, ethanol và dung dịch H2SO4 98%, đựng trong bình cầu có nhánh. Nhiệt độ bếp điện được thiết lập ở 80°C. Mô hình điều chế và tách ethyl acetate được thực hiện như sau:
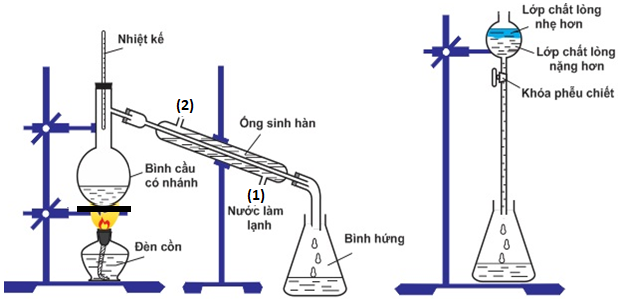
Nhận định nào sau đây không đúng?
A. Phản ứng điều chế ethyl aetate từ các nguyên liệu trên được gọi là phản ứng ester hóa.
B. Trong quá trình phản ứng, phần hơi tách ra từ bình cầu có nhánh sang bình hứng chủ yếu là ethyl acetate và nước.
C. Để tăng hiệu suất chiết ethyl acetate từ bình hứng ta thêm dung dịch muối ăn bão hòa vào.
D. Vai trò H2SO4 là xúc tác và hút nước để chuyển dịch cân bằng trong phản ứng ester hóa.
(Xem giải) Câu 20: Khi con người sử dụng thức ăn chứa tinh bột, enzyme α-amylase có trong nước bọt thúc đẩy quá trình thuỷ phân tinh bột thành các phân tử nhỏ hơn gồm dextrin và maltose. Quá trình này tiếp tục ở ruột non, nơi phần lớn tinh bột bị thuỷ phân thành glucose. Glucose được hấp thụ vào máu và di chuyển đến các tế bào trong khắp cơ thể. Glucose có thể được sử dụng cho nhu cầu năng lượng hoặc có thể được chuyển đổi thành glycogen lưu trữ trong gan và cơ.
(a) Khi ăn cơm, nếu nhai kĩ sẽ thấy vị ngọt vì tinh bột bị thuỷ phân thành glucose.
(b) Tinh bột bị thủy phân bởi enzyme α-amylase hoặc môi trường acid.
(c) Glucose chủ yếu đóng vai trò cung cấp năng lượng cho tế bào.
(d) Glycogen lưu trữ trong gan và cơ, khi cần thiết có thể chuyển hoá thành glucose để cung cấp năng lượng cho cơ thể.
Số phát biểu đúng là:
A. 1. B. 4. C. 2. D. 3.
(Xem giải) Câu 21: Phân tích nguyên tố hợp chất hữu cơ E cho kết quả phần trăm khối lượng carbon, hydrogen và oxygen lần lượt là 54,55%; 9,09% và 36,36%. Dựa vào phương pháp phân tích khối phổ (MS) xác định được phân tử khối của E là 88. Thuỷ phân hoàn toàn E trong dung dịch NaOH, thu được muối của carboxylic acid X và chất Y. Chất Y có nhiệt độ sôi (64,7°C) nhỏ hơn nhiệt độ sôi của ethanol (78,3°C) (nhiệt độ sôi đều đo ở áp suất 1 atm).
(a) Công thức phân tử của E là C4H8O2.
(b) Carboxylic acid X là propanoic acid.
(c) Chất Y được phối trộn với xăng RON 92 để tạo ra xăng sinh học.
(d) Chất E không thể được điều chế trực tiếp bằng phản ứng ester hoá.
Số nhận định đúng là
A. 1. B. 4. C. 2. D. 3.
(Xem giải) Câu 22: Đun nóng m gam hỗn hợp E chứa triglyceride X và các acid béo với 200 mL dung dịch NaOH 1M (vừa đủ), thu được glycerol và hỗn hợp muối Y. Hydrogen hóa hoàn toàn Y cần vừa đủ 0,1 mol H2, chỉ thu được muối sodium palmitate. Đốt cháy 0,07 mol E, thu được 1,645 mol CO2. Biết các phản ứng xảy ra hoàn toàn và 1 gam E cung cấp khoảng 9 kcal. Số kcal m gam E cung cấp có giá trị gần nhất là
A. 471. B. 521. C. 417. D. 554.
(Xem giải) Câu 23: Tiến hành thí nghiệm theo các bước sau:
– Bước 1: Cho khoảng 50 mL dung dịch CuSO4 1M vào cốc 250 mL. Thêm 20 mL dung dịch NaOH 20% vào, khuấy đều.
– Bước 2: Lọc tách kết tủa, cho vào cốc thuỷ tinh 250 mL. Thêm khoảng 50 mL dung dịch NH3 đặc, khuấy đều đến khi kết tủa tan hết thu được nước Schweizer.
– Bước 3: Thêm một lượng nhỏ bông vào khoảng 30 mL nước Schweizer và khuấy đều trong khoảng 5 phút.
(a) Sau bước 1, thu được là kết tủa Cu(OH)2 có màu xanh.
(b) Ở bước 2, xảy ra phản ứng tạo nước Schweizer: Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2.
(c) Sau bước 3, thu được chất rắn màu vàng.
(d) Trong sợi bông, cellulose chiếm khoảng 50%.
Số phát biểu đúng là:
A. 1. B. 4. C. 3. D. 2.
(Xem giải) Câu 24: Từ một loại tinh bột (chứa 5% tạp chất trơ về khối lượng), người ta thủy phân rồi xử lý, thu được glucose ở dạng ngậm nước gọi là glucose monohydrate (gọi là X), có công thức hóa học là C6H12O6.H2O. Hiệu suất quá trình đạt 85%. Pha 27,5 gam X với nước cất pha tiêm (nước cất để pha thuốc tiêm) và tá dược vừa đủ thì thu được 250 mL dung dịch glucose 10% (dung dịch Y). Y dùng truyền vào tĩnh mạch, liều dùng đối với bệnh nhân (người lớn) tối đa 30 mL/kg thể trọng/ngày. Với khối lượng tinh bột là 5 kg thì có thể pha chế được lượng dung dịch Y truyền cho bao nhiêu bệnh nhân người lớn có thể trọng 60 kg trong một ngày?
A. 30. B. 25. C. 14. D. 17.
Phần 2: Câu hỏi trắc nghiệm dạng Đúng/Sai (6,0 điểm)
(Xem giải) Câu 25. (1,0 điểm): Trong công nghiệp, một lượng lớn NaHCO3 và Na2CO3 được sản xuất theo phương pháp Solvay bằng cách cho khí CO2 (lấy từ nhiệt phân đá vôi) vào dung dịch chứa sodium chloride (NaCl) bão hoà và ammonia (NH3) bão hoà.
CO2(aq) + H2O(l) + NH3(aq) + NaCl(aq) → NH4Cl(aq) + NaHCO3(s) (1)
NaHCO3 tách ra đem nhiệt phân thu được soda:
2NaHCO3 → Na2CO3 + CO2 + H2O (2)
và NH4Cl được sử dụng để tái tạo NH3 bằng cách tác dụng với Ca(OH)2 tạo ra từ CaO.
Chọn đúng hoặc sai trong mỗi phát biểu sau:
a. Phản ứng (1) xảy ra được là do NaHCO3 có độ tan kém hơn nên bị kết tinh trước.
b. Trong thực tế sản xuất, người ta đun nóng hỗn hợp các chất tham gia phản ứng (1) để thu được Na2CO3 ngay.
c. Nguyên liệu chính ban đầu của quá trình sản xuất soda bằng phương pháp Solvay là NaCl và CaCO3.
d. NaHCO3 được ứng dụng làm bột nở là do phản ứng (2).
(Xem giải) Câu 26. (1,0 điểm): Thực hiện thí nghiệm điều chế và thử tính chất của khí X như sau:
• Bước 1: Cho vào ống nghiệm khô (ống số 1) có nút và ống dẫn khí khoảng 4 – 5 gam hỗn hợp bột mịn đã được trộn đều gồm sodium acetate và vội tôi xút theo tỉ lệ 1 : 2 về khối lượng.
• Bước 2: Lắp ống số 1 lên giả thí nghiệm rồi nhúng ống dẫn khi vào dung dịch nước bromine đựng trong cốc thủy tinh.
• Bước 3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ xung quanh phần dưới của ống nghiệm, sau đó đun tập trung vào vị trí có hỗn hợp phản ứng).
Chọn đúng hoặc sai trong mỗi phát biểu sau:
a. Ở bước 2, lắp ống số 1 sao cho miệng ống hướng lên.
b. Sau khi thực hiện bước 3 một thời gian, màu của dung dịch trong cốc thủy tinh bị nhạt dần.
c. Kết thúc thí nghiệm, tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong cốc thủy tinh.
d. Muốn thu khí X vào bình tam giác mà ít lẫn tạp chất ta phải thu bằng phương pháp đẩy nước.
(Xem giải) Câu 27. (1,0 điểm): Cho 3 chất hữu cơ X, Y, Z (mạch thẳng, chỉ chứa C, H, O) đều có khối lượng mol là 82 (trong đó X và Y là đồng phân của nhau). Biết 1,0 mol X hoặc Z tác dụng vừa đủ với 3,0 mol AgNO3 trong dung dịch NH3; 1,0 mol Y tác dụng vừa đủ với 4,0 mol AgNO3 trong dung dịch NH3.
Chọn đúng hoặc sai trong mỗi phát biểu sau:
a. Số liên kết π trong X, Y và Z lần lượt là 4, 4 và 3.
b. Số nhóm chức -CHO trong X, Y và Z lần lượt là 1, 2 và 1.
c. Phần trăm khối lượng của hydrogen trong X là 7,32% và trong Z là 2,44%.
d. Phần trăm khối lượng oxygen trong X là 39,02% và trong Z là 19,51%.
(Xem giải) Câu 28. (1,0 điểm): Muscone là hợp chất tạo nên mùi thơm đặc trưng của xạ hương; có công thức cấu tạo như sau:
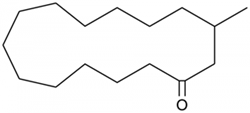
Chọn đúng hoặc sai trong mỗi phát biểu sau:
a. Muscone thuộc hợp chất ketone.
b. Muscone có công thức phân tử là C16H30O.
c. Muscone có phản ứng với cộng với HCN.
d. Muscone tham gia phản ứng tráng bạc với thuốc thử Tollens.
(Xem giải) Câu 29. (1,0 điểm): Cho hai chất hữu cơ mạch hở E, F có cùng công thức đơn giản nhất là C3H4O2. Các chất E, F, X, Z tham gia phản ứng theo đúng tỉ lệ mol như sơ đồ dưới đây:
(1) E + NaOH → X + Y
(2) F + NaOH → Z + T
(3) X + HCl → J + NaCl
(4) Z + HCl → G + NaCl
Biết: X, Y, Z, T, J, G là các chất hữu cơ, trong đó T đa chức; MT > 88 và ME < MF < 146.
Chọn đúng hoặc sai trong mỗi phát biểu sau:
a. Đun 0,72 gam E với 15 mL dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng thu được 0,68 gam rắn khan.
b. Ở nhiệt độ thường, T tác dụng với Cu(OH)2 tạo dung dịch xanh lam.
c. E và F đều tạo kết tủa khi cho tác dụng với AgNO3 trong dung dịch NH3.
d. Nung nóng chất rắn Z với hỗn hợp với tôi xút thu được khi ethylene.
(Xem giải) Câu 30. (1,0 điểm): Cho sơ đồ chuyển hóa sau:
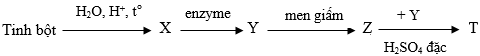
Chọn đúng hoặc sai trong mỗi phát biểu sau:
a. Chất X và Z đều có thể hoà tan Cu(OH)2 trong điều kiện thích hợp.
b. Có thể dùng chất T để tách chiết như tách caffeine khỏi cà phê.
c. Thủy phân chất T bằng dung dịch NaOH vừa đủ thu được hai chất có cùng số nguyên tử carbon..)
d. Chất X có thể là glucose hoặc fructose.
Phần 3: Câu hỏi trắc nghiệm dạng trả lời ngắn (2,0 điểm)
(Xem giải) Câu 31. (0,25 điểm): Hỗn hợp X gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 3. Nung nóng X trong bình kín (450°C, xúc tác Fe) một thời gian, thu được hỗn hợp khí có số mol giảm 5% so với ban đầu. Hiệu suất của phản ứng tổng hợp NH3 là bao nhiêu? (kết quả làm tròn đến hàng phần mười).
(Xem giải) Câu 32. (0,25 điểm): X có công thức đơn giản nhất là C2H3 và 150 < MX < 170. X không làm mất màu dung dịch nước bromine, không tác dụng với chlorine khi có bột sắt xúc tác, đun nóng, nhưng tác dụng với chlorine theo tỉ lệ mol 1 : 1 có chiếu sáng thì cho 1 sản phẩm hữu cơ duy nhất. Có bao nhiêu chất thỏa mãn điều kiện bài toán trên?
(Xem giải) Câu 33. (0,25 điểm): Khi đốt cháy 1 mol propane toả ra lượng nhiệt là 2220 kJ. Để đun nóng 1 gam nước tăng thêm 1°C cần cung cấp nhiệt lượng là 4,2 J. Tính khối lượng propane cần dùng để đun 1 L nước từ 25°C lên 100°C. Cho biết 65% nhiệt lượng toả ra khi đốt cháy propane dùng để nâng nhiệt độ của nước. Khối lượng riêng của nước là 1 g/mL. (kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 34. (0,25 điểm): Hỗn hợp X gồm phenol, glycerol, ethanol. Cho a gam hỗn hợp X tác dụng với Na dư, thu được 1,2395 lít khí H2. Mặt khác, đốt cháy a gam hỗn hợp X cần dùng vừa đủ V lít không khí, thu được 4,4622 lít CO2 và 3,6 gam H2O. Biết O2 chiếm 20% thể tích không khí và các thể tích khí đo ở điều kiện chuẩn. Giá trị của V là bao nhiêu? (kết quả làm tròn đến hàng phần mười).
(Xem giải) Câu 35. (0,25 điểm): Phân bón NPK là hỗn hợp các muối NH4NO3, (NH4)2HPO4, KCl và một lượng phụ gia không chứa các nguyên tố dinh dưỡng. Trên các bao bì phân NPK thường có kí hiệu bằng những chữ số nhằm cho biết tỉ lệ khối lượng các thành phần trong phân bón. Việc bón phân NPK cho cây cà phê sau khi trồng 4 năm được chia thành ba thời kì như sau:
| Thời kì | Lượng phân bón |
| Bón thúc ra hoa | 0,5 kg phân NPK 10.12.5/cây |
| Bón đậu quả, ra quả | 0,7 kg phân NPK 12.8.2/cây |
| Bón thúc quả lớn, tăng dưỡng chất cho quả | 0,6 kg phân NPK 16.16.16/cây |
Tổng khối lượng đạm (N) và lân (P2O5) đã cung cấp cho cây cà phê trong cả ba thời kì là bao nhiêu kg? (kết quả làm tròn đến hàng phần trăm).
(Xem giải) Câu 36. (0,25 điểm): Thủy phân hoàn toàn m1 gam ester X mạch hở bằng dung dịch NaOH dư, thu được m2 gam alcohol Y (không có khả năng phản ứng với Cu(OH)2) và 15 gam hỗn hợp muối của hai carboxylic acid đơn chức. Đốt cháy hoàn toàn m2 gam Y bằng oxygen dư, thu được 0,3 mol CO2 và 0,4 mol H2O. Tính giá trị của m1. (kết quả làm tròn đến hàng phần mười).
(Xem giải) Câu 37. (0,25 điểm): Một vận động viên thể hình “gymer” cần luyện tập với cường độ cao và bổ sung dinh dưỡng đầy đủ hơn để thi đấu. Một trong các thực phẩm bổ sung không thể thiếu là omega-3 để hỗ trợ tim mạch trong quá trình tập luyện. Vận động viên trước đây kết hợp các thực phẩm giàu omega-3 kèm theo sử dụng 5 viên “Now Omega-3 Fish Oil” mỗi ngày tuy nhiên thương hiệu Now foods của Hoa Kì đã sản xuất một sản phẩm với hàm lượng EPA và DHA cao hơn đó là “Now Ultra Omega-3 Fish Oil” với hàm lượng và giá thành của hai sản phẩm như sau:
| Loại sản phẩm | Tên sản phẩm | 1000 mg dầu cá/viên | Giá thành 1 lọ | |
| EPA (mg) | DHA (mg) | |||
| Loại 1 | Now Omega-3 Fish Oil (200 viên) | 180 | 120 | 450.000 VNĐ |
| Loại 2 | Now Ultra Omega-3 Fish Oil (180 viên) | 500 | 250 | 710.000 VNĐ |
Vì lượng “body fat” (chỉ số mỡ trên cơ thể) của vận động viên tương đối cao nên thời gian luyện tập với cường độ cao và bổ sung dinh dưỡng đầy đủ suốt trong vòng 3 tháng (mỗi tháng coi như có 30 ngày). Nếu sử dụng viên uống dầu cá loại 2 thay cho loại 1 trong vòng 3 tháng thì vận động viên đó tiết kiệm được chi phí được bao nhiêu ngàn VNĐ?
(Xem giải) Câu 38. (0,25 điểm): Một ruột phích có diện tích bề mặt là 0,35 m². Để tráng được 2000 ruột phích như trên với độ dày lớp bạc là 0,1 μm thì cần dùng m kg glucose 10% tác dụng với lượng dư dung dịch AgNO3 trong NH3. Biết hiệu suất phản ứng tráng bạc là 75% và khối lượng riêng của silver là 10,49 g/cm³. Giá trị của m là bao nhiêu? (kết quả làm tròn đến hàng phần trăm).
Phần 4: Tự luận (6,0 điểm): Thí sinh trình bày lời giải câu hỏi tự luận, gồm 3 câu ra giấy thi
Câu 1. (2,0 điểm):
(Xem giải) 1. Lấy 233 mg hợp chất A (tạo bởi một kim loại nhóm IIA; C; O; H) được đưa đi phân tích bằng nhiệt; người ta đo sự thay đổi khối lượng theo nhiệt độ được kết quả:
| Khoảng nhiệt độ phân tích (°C) | 20-250 | 20-530 | 20-800 |
| Độ giảm khối lượng (mg) | 41 | 83 | 149 |
Chất rắn còn lại ở thí nghiệm cuối cùng là một oxide màu trắng của kim loại. Lấy 12 mg A được đem đi oxi hoá bằng oxygen dư ở 900°C; sản phẩm oxi hoá được hấp thụ bởi anhydrone (chất hút ẩm có công thức Mg(ClO4)2) và sau đó là NaOH (tẩm trong lưới xốp). Khối lượng chất bị hấp thụ bởi anhydrone là 2,09 mg; khối lượng bị hấp thụ bởi NaOH là 6,813 mg. Khối lượng chất rắn còn lại là 4,335mg.
a. Giải thích kết quả thí nghiệm trên.
b. Hãy xác định công thức chất A.
(Xem giải) 2. Sulfuric acid là một trong những hoá chất quan trọng nhất được sử dụng trong công nghiệp; được sản xuất hàng trăm triệu tấn mỗi năm, chiếm nhiều nhất trong ngành công nghiệp hoá chất. Phương pháp sản xuất sulfuric acid phổ biến nhất là phương pháp tiếp xúc, theo đó acid có thể được điều chế qua các giai đoạn sau:
(1) FeS2(s) + O2(g) → Fe2O3(s) + SO2(g)
(2) SO2(g) + O2(s) → SO3(g)
(3) H2SO4(aq) + SO3(g) → H2SO4.nSO3(1)
(4) H2SO4.nSO3(l) + H2O(l) → H2SO4(aq)
Hòa tan 12,45 gam 1 oleum vào nước được dung dịch A. Để trung hòa hết dung dịch A cần 300 mL dung dịch NaOH nồng độ 1 M. Xác định công thức của oleum. Cần bao nhiêu gam oleum nói trên hòa tan vào 500 gam nước để tạo thành dung dịch H2SO4 10%.
Câu 2. (2,0 điểm):
(Xem giải) 1. Hợp chất hữu cơ (E) có kết quả đo phổ khối lượng (MS) và phổ hồng ngoại (IR) của hợp chất (E) được cho như hình bên dưới:
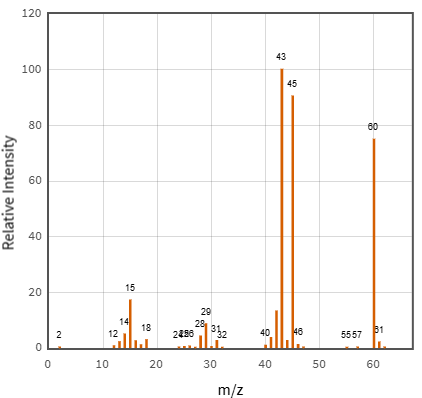 |
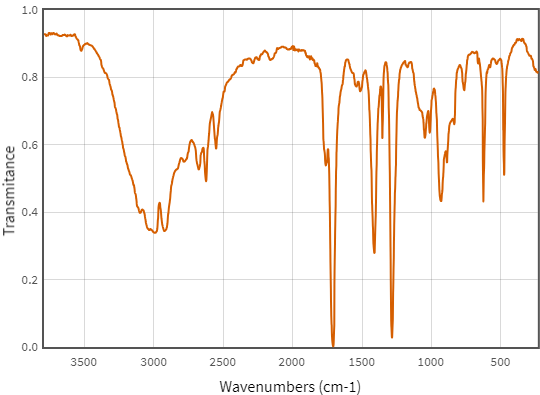 |
Dựa vào bảng đối chiếu tín hiệu phổ hồng ngoại của các nhóm chức:
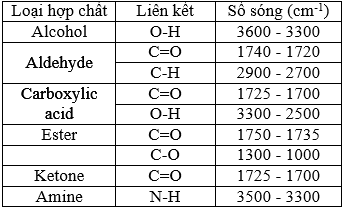
a. Hãy xác định công thức cấu tạo của E?
b. Ethanol phản ứng với E trong môi trường H2SO4 đặc tạo thành chất hữu cơ F theo phương trình hoá học sau:
C2H5OH(l) + E(l) ⇋ F(l) + H2O(l)
Ở 50°C, giá trị Kc của phản ứng trên là 7,5. Nếu cho 23,0 g ethanol phản ứng với 30,0 g E ở 50°C thì khối lượng F thu được trong hỗn hợp ở trạng thái cân bằng là bao nhiêu? (Coi tổng thể tích của hệ phản ứng không đổi).
(Xem giải) 2. Chất hữu cơ X chứa C, H, O và có phân tử khối bằng 206. Trong X, tỉ lệ khối lượng của C và O tương ứng là 33 : 16. Từ X thực hiện các phản ứng theo đúng tỉ lệ mol:
(1) X + 3KOH (t°) → Y + Z + T + M;
(2) Y + H2 (Ni, t°) → Y1
(3) Z + HCl → Z1 + KCl;
(4) Y1 + O2 (xt) → Z1 + M;
(5) T + 2HCl → T1 + 2KCl;
(6) Y + 2AgNO3 + 3NH3 + H2O (t°) → Y2 + 2Ag + 2NH4NO3.
a) Tìm công thức phân tử của X.
b) Xác định công thức cấu tạo của X, Y, Z, T, Y1, Y2, Z1, T1 và viết phương trình hóa học của các phản ứng xảy ra
(Xem giải) Câu 3. (2,0 điểm):
Cumene (isopropylbenzene) là một arene ở thể lỏng trong điều kiện thường, có mùi dễ chịu. Cumene được sản xuất từ quá trình chưng cất nhựa than đá và các phân đoạn dầu mỏ hoặc bằng cách alkyl hoá benzene với propene, xúc tác là acid.
Khoảng 95% cumene được sử dụng làm chất trung gian trong sản xuất phenol và acetone. Các ứng dụng khác như trong sản xuất styrene, α-methylstyrene, acetophenone, chất tẩy rửa; làm chất pha loãng cho sơn; làm dung môi cho chất béo và nhựa; in ấn và sản xuất cao su. Một lượng nhỏ được sử dụng trong pha chế xăng và là thành phần của nhiên liệu hàng không có chỉ số octane cao.
Đã có bằng chứng rõ rệt về khả năng gây ung thư của cumene đối với chuột, ở người, cumene thuộc nhóm có thể gây ung thư. Cumene được thải ra từ quá trình đốt cháy không hoàn toàn nhiên liệu hoá thạch từ các phương tiện giao thông, dầu tràn, vận chuyển và phân phối nhiên liệu hoá thạch hoặc bốc hơi từ các trạm xăng. Ngoài ra, các nguồn thải khác từ việc sử dụng cumene làm dung môi, từ các nhà máy dệt và kể cả từ khói thuốc lá,… cũng là một trong những nguyên nhân gây nên bệnh ung thư ở người.
Bảng sau đây thống kê một số nguồn sản sinh cumene trong đời sống, sinh hoạt, sản xuất.
| Nguồn | Tỉ lệ phát thải | Ghi chú |
| Sản xuất | 0,08 kg/tấn cumene | Được kiểm soát |
| 0,27 kg/tấn cumene | Không được kiểm soát | |
| Xe chạy động cơ xăng | 0,0002-0,0009 g/km | Có bộ chuyển đổi xúc tác |
| 0,002 g/km | Không có bộ chuyển đổi xúc tác | |
| Máy photocopy | 140-220 pg/h | Hoạt động liên tục |
a. Bộ chuyển đổi xúc tác trong động cơ xăng có khả năng giảm thiểu tối đa bao nhiêu phần trăm cumene so với trường hợp không có bộ chuyển đổi xúc tác?
b. Tính khối lượng cumene tối đa phát thải từ 1000000 xe ô tô chạy động cơ xăng (có bộ chuyển đổi xúc tác) trong 1,5 năm. Giả sử bình quân một tháng, mỗi xe ô tô chạy 3000 km.
c. Một cửa hàng có 20 máy photocopy. Bình quân mỗi máy sử dụng liên tục 12 giờ/ngày. Trong một tháng (30 ngày), khối lượng cumene tối đa phát thải từ 1000 cửa hàng có quy mô trên là bao nhiêu?
d. Thị trường tiêu thụ phenol trên toàn thế giới khoảng 11,37 triệu tấn trong năm 2021, dự kiến sẽ tăng lên 14,07 triệu tấn vào năm 2029. Phenol được sử dụng để sản xuất nhiều loại hoá chất như bisphenol A, nhựa phenolformaldehyde, picric acid và các chất khác. Khoảng 90% lượng phenol được sản xuất từ cumene (bằng phương pháp cumene, chu trình cumene,…). Để cung cấp đủ sản lượng tiêu thụ của phenol trong năm 2021, khối lượng cumene đã dùng để sản xuất phenol là bao nhiêu? (Chỉ tính trên lượng phenol đã tiêu thụ, không bao gồm lượng cumene thực tế sản xuất phenol chưa tiêu thụ).


Bình luận