[2024] Thi thử TN trường Đội Cấn – Vĩnh Phúc (Lần 5)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Giải chi tiết và đáp án:
⇒ Mã đề: 134
| 41B | 42A | 43B | 44D | 45C | 46B | 47D | 48B | 49A | 50C |
| 51B | 52B | 53A | 54C | 55C | 56C | 57A | 58A | 59B | 60B |
| 61B | 62D | 63D | 64A | 65A | 66D | 67D | 68C | 69B | 70C |
| 71A | 72A | 73A | 74D | 75D | 76A | 77B | 78C | 79A | 80A |
Câu 41. Khi nung CaCO3 ở nhiệt độ khoảng 1000°C, thu được chất rắn E thường dùng để khử chua đất trong nông nghiệp. Chất E là
A. CO2. B. CaO. C. Ca. D. CaC2.
(Xem giải) Câu 42. Cho các dung dịch: glucozơ, saccarozơ, etanol, glixerol, axit axetic. Số dung dịch hòa tan được Cu(OH)2 ở nhiệt độ thường là
A. 4. B. 2. C. 5. D. 3.
(Xem giải) Câu 43. Phát biểu nào sau đây sai?
A. Etyl axetat có công thức phân tử là C4H8O2.
B. Phân tử metyl metacrylat có một liên kết π trong phân tử.
C. Metyl acrylat có khả năng tham gia phản ứng cộng Br2 trong dung dịch.
D. Etyl fomat có khả năng tham gia phản ứng tráng bạc.
(Xem giải) Câu 44. Cho từ từ dung dịch NH3 đến dư vào dung dịch chứa chất nào sau đây thì thu được kết tủa?
A. NaCl. B. H2SO4. C. HCl. D. AlCl3.
Câu 45. Chất nào sau đây thuộc loại đisaccarit?
A. Glucozơ. B. Xenlulozơ. C. Saccarozơ. D. Tinh bột.
(Xem giải) Câu 46. Cho kim loại Fe lần lượt phản ứng với các dung dịch: FeCl3, Cu(NO3)2, AgNO3, MgCl2. Số trường hợp xảy ra phản ứng hóa học là
A. 4. B. 3. C. 1. D. 2.
(Xem giải) Câu 47. Phát biểu nào sau đây không đúng?
A. Trong môi trường kiềm, peptit có từ 2 liên kết peptit trở lên tác dụng với Cu(OH)2 cho hợp chất màu tím.
B. Ở điều kiện thường, amino axit là chất rắn kết tinh, tương đối dễ tan trong nước.
C. Mì chính (bột ngọt) là muối mononatri của axit glutamic.
D. Nhúng quỳ tím vào dung dịch anilin, màu quỳ tím chuyển thành xanh.
Câu 48. Thủy phân este X trong môi trường kiềm, thu được natri axetat và ancol etylic. Công thức của X là
A. C2H5COOCH3. B. CH3COOC2H5. C. C2H3COOC2H5 D. CH3COOCH3
Câu 49. Phản ứng nhiệt phân không đúng là
A. NaHCO3 (t°) → NaOH + CO2. B. NH4NO2 (t°) → N2 + 2H2O.
C. NH4Cl (t°) → NH3 + HCl. D. 2KNO3 (t°) → 2KNO2 + O2.
Câu 50. Chất X có nhiều trong mật ong, ngoài ra còn có trong các loại hoa quả và rau xanh như ổi, cam, xoài, rau diếp xoắn, cà chua…rất tốt cho sức khỏe. Chất X là
A. Xenlulozơ. B. Saccarozơ C. Fructozơ D. Glucozơ
Câu 51. Các tính chất vật lí chung của kim loại gây ra do
A. các kim loại đều là chất rắn. B. các electron tự do trong mạng tinh thể.
C. các ion kim loại. D. các electron hóa trị.
(Xem giải) Câu 52. Cho 7,5 gam glyxin phản ứng vừa đủ với V ml dung dịch HCl 0,2M. Giá trị của V là
A. 150. B. 500. C. 200. D. 300.
Câu 53. Quặng sắt manhetit có thành phần chính là
A. Fe3O4. B. FeS2. C. FeCO3. D. Fe2O3.
(Xem giải) Câu 54. Một mẫu nước cứng chứa các ion: Ca2+, Mg2+, HCO3-, Cl-, SO42-. Chất được dùng để làm mềm mẫu nước cứng trên là
A. H2SO4. B. NaHCO3. C. Na2CO3. D. HCl.
(Xem giải) Câu 55. Phát biểu nào sau đây đúng?
A. Chất béo lỏng khó bị oxi hóa bởi không khí hơn chất béo rắn.
B. Amilozơ có cấu trúc mạch phân nhánh.
C. Tơ nilon-6,6 được dùng dệt vải may mặc, bện dây dù, đan lưới.
D. Amin CH3-NH-CH3 có tên thay thế là đimetylamin.
Câu 56. Trong công nghiệp, quặng boxit dùng để sản xuất kim loại nhôm. Thành phần chính của quặng boxit là
A. Al(OH)3.H2O. B. Al(OH)3.2H2O. C. Al2O3.2H2O. D. Al2(SO4)3.H2O.
(Xem giải) Câu 57. Triolein không tác dụng với chất (hoặc dung dịch) nào sau đây?
A. Cu(OH)2 (ở điều kiện thường).
B. Dung dịch NaOH (đun nóng).
C. H2O (xúc tác H2SO4 loãng, đun nóng).
D. H2 (xúc tác Ni, đun nóng).
(Xem giải) Câu 58. Hợp chất Ba(HCO3)2 tác dụng với dung dịch nào sau đây không sinh ra kết tủa?
A. HCl. B. Na2CO3. C. Na2SO4. D. NaOH.
(Xem giải) Câu 59. Thủy phân hoàn toàn m gam tinh bột thành glucozơ. Cho toàn bộ glucozơ tham gia phản ứng tráng bạc (hiệu suất 100%), thu được 30,24 gam Ag. Giá trị của m là
A. 50,40. B. 22,68. C. 25,20. D. 45,36.
Câu 60. Tro thực vật được sử dụng như một loại phân bón cung cấp nguyên tố kali cho cây trông do chứa muối kali cacbonat. Công thức của kali cacbonat là
A. NaCl. B. K2CO3. C. KHCO3. D. KCl.
Câu 61. Chất nào dưới đây có tính chất lưỡng tính?
A. CrO. B. Cr2O3. C. CrO3. D. Fe2O3.
(Xem giải) Câu 62. Khi điện phân dung dịch hỗn hợp Cu(NO3)2; AgNO3, điều khẳng định nào sau đây là đúng?
A. Tại catot xảy ra quá trình khử Cu2+ trước.
B. Khối lượng dung dịch giảm là khối lượng của kim loại thoát ra bám vào catot.
C. Ngay từ đầu đã có khí thoát ra tại catot.
D. Tại anot xảy ra quá trình oxi hóa H2O.
Câu 63. Polime nào sau đây dùng làm chất dẻo?
A. Xenlulozơ. B. Polibutadien. C. Poliacrilonitrin. D. Poli (vinyl clorua).
Câu 64. Số nguyên tử hiđro trong phân tử tristearin là
A. 110. B. 99. C. 105. D. 104.
(Xem giải) Câu 65. Phát biểu nào sau đây không đúng?
A. Nhôm tan trong dung dịch axit mạnh và dung dịch kiềm, do đó nhôm có tính lưỡng tính.
B. Trong các phản ứng hóa học, kim loại Al chỉ đóng vai trò chất khử.
C. Nhôm là kim loại nhẹ, dẫn điện và dẫn nhiệt tốt.
D. Muối sunfat kép của nhôm và kali ngậm nước (K2SO4.Al2(SO4)3.24H2O) gọi là phèn chua.
(Xem giải) Câu 66. Phát biểu nào sau đây đúng?
A. Xenlulozơ và tinh bột là đồng phân của nhau.
B. Có thể dùng phản ứng tráng bạc để phân biệt glucozơ và fructozơ.
C. Saccarozơ có tính chất của ancol đa chức và andehit đơn chức.
D. Trong môi trường bazơ, fructozơ chuyển hóa thành glucozơ.
Câu 67. Tên gọi của polime có công thức (-CH2-CH(CN)-)n là
A. tơ nilon-6. B. tơ nilon-7. C. tơ nilon-6,6. D. tơ olon.
Câu 68. Trong các ion sau đây, ion nào có tính oxi hóa mạnh nhất?
A. Pb2+. B. Ba2+. C. Fe3+. D. Cu2+.
(Xem giải) Câu 69. Cho sơ đồ chuyển hóa sau:
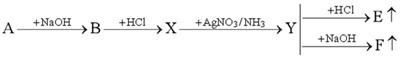
Trong đó A là hợp chất hữu cơ có khối lượng mol là 86. Công thức cấu tạo thu gọn của A là
A. CH2=CHCOOCH3. B. HCOO-CH=CH-CH3.
C. HCOOCH2CH2CH3. D. CH3COOCH=CH2.
(Xem giải) Câu 70. Cho a mol hỗn hợp X gồm CO2 và hơi nước qua than nóng đỏ (đến khi C phản ứng hết 0,03 mol), thu được 0,18 mol hỗn hợp Y gồm CO, H2 và CO2. Hấp thụ toàn bộ Y vào 300 ml dung dịch Z gồm NaOH 0,25M và Ba(OH)2 đến phản ứng hoàn toàn thu được dung dịch T và m gam kết tủa. Cho từ từ dung dịch HCl vào T, phản ứng được biểu diễn theo đồ thị sau:

Giá trị của m là
A. 11,820. B. 13,298. C. 14,775. D. 10,343.
(Xem giải) Câu 71. Tiến hành thí nghiệm sau:
Bước 1: Rót vào ống nghiệm 1 và 2, mỗi ống khoảng 3 ml dung dịch H2SO4 loãng cùng nồng độ và cho vào mỗi ống một mẩu kẽm như nhau. Quan sát bọt khí thoát ra.
Bước 2: Nhỏ thêm 2 – 3 giọt dung dịch CuSO4 vào ống 2. So sánh tốc độ bọt khí thoát ra ở 2 ống.
Cho các phát biểu sau:
(a) Bọt khí thoát ra ở ống 2 nhanh hơn so với ống 1.
(b) Ống 1 chỉ xảy ra ăn mòn hoá học còn ống 2 chỉ xảy ra ăn mòn điện hoá.
(c) Bọt khí thoát ra ở 2 ống tốc độ là như nhau.
(d) Ở cả hai ống nghiệm, Zn đều bị oxi hoá thành Zn2+.
(e) Ở bước 1, nếu thay kim loại kẽm bằng kim loại sắt thì hiện tượng vẫn xảy ra tương tự.
(g) Ở bước 2, nếu thay dung dịch CuSO4 bằng dung dịch MgSO4 thì hiện tượng vẫn xảy ra tương tự.
Số phát biểu đúng là
A. 3. B. 2. C. 4. D. 5.
(Xem giải) Câu 72. Cho 2,24 gam bột sắt vào 100 ml dung dịch chứa hỗn hợp gồm AgNO3 0,2M và Cu(NO3)2 0,4M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
A. 4,08. B. 0,64. C. 2,80. D. 2,16.
(Xem giải) Câu 73. Tiến hành điện phân dung dịch chứa x mol NaCl và y mol CuSO4 với điện cực trơ, màng ngăn xốp; cường độ dòng điện không đổi I = 7,5A, trong thời gian t = 4632 giây, thu được dung dịch X; đồng thời ở anot thoát ra 0,12 mol hỗn hợp khí. Nếu thời gian điện phân là 1,5t giây thì tổng số mol khí thoát ra ở hai cực là 0,215 mol. Giả sử trong quá trình điện phân nước bay hơi không đáng kể, hiệu suất điện phân đạt 100%, các khí sinh ra không tan trong nước, bỏ qua sự thủy phân của muối.
Cho các phát biểu sau:
(a) Tổng khối lượng hai muối trước điện phân là 45,48 gam.
(b) Dung dịch X chỉ có hai chất tan.
(c) Đến thời điểm 1,5t giây, số mol H+ sinh ra ở anot là 0,32 mol.
(d) Nếu thời gian điện phân là 1,25t giây thì nước đã điện phân ở cả hai điện cực.
(đ) Giá trị của x, y lần lượt là 0,12 và 0,22.
Số phát biểu sai là
A. 3. B. 1. C. 2. D. 4.
(Xem giải) Câu 74. Hỗn hợp E gồm este X đơn chức và este Y hai chức (X, Y chỉ chứa nhóm chức este, mạch hở). Đốt cháy hoàn toàn m gam E trong oxi dư thu được 0,925 mol CO2. Mặt khác, m gam E tác dụng vừa đủ với dung dịch NaOH thu được 18,5 gam hỗn hợp Z gồm 2 muối và hỗn hợp T gồm 2 ancol (2 ancol đều có khả năng tách nước tạo anken). Đốt cháy hoàn toàn 18,5 gam hỗn hợp Z thu được H2O; 0,1375 mol CO2 và 0,1375 mol Na2CO3. Phần trăm khối lượng của X trong E gần nhất với giá trị nào sau đây?
A. 35%. B. 25%. C. 34% D. 26%.
(Xem giải) Câu 75. Nhiệt phân hoàn toàn m gam hỗn hợp E chứa ba muối của axit nitric và axit cacbonic (trong bình kín không chứa không khí) thu được chất rắn X và 0,8 mol hỗn hợp khí Y gồm NO2, O2 và CO2. Hấp thụ toàn bộ Y vào bình đựng dung dịch NaOH dư, thì thấy khối lượng bình tăng 35 gam và có 0,9 mol NaOH tham gia phản ứng. Mặt khác, để hòa tan hết chất rắn X cần dùng vừa đủ 500 ml dung dịch HCl 2M, sau phản ứng thu được 51,5 gam hỗn hợp hai muối clorua có cùng nồng độ mol. Phần trăm khối lượng của hợp chất có số mol lớn nhất trong E gần nhất với giá trị nào sau đây?
A. 30,5. B. 82,0. C. 41,0. D. 28,5.
(Xem giải) Câu 76. Khi làm lạnh 220 gam dung dịch FeCl2 bão hoà ở 90°C xuống 10°C, thu được tinh thể FeCl2.4H2O và dung dịch X. Cho X tác dụng với lượng dư dung dịch AgNO3 ở điều kiện thường, thu được m gam kết tủa. Biết độ tan của FeCl2 ở 90°C là 100 và ở 10°C là 64. Giá trị của m gần nhất với giá trị nào sau đây?
A. 148,92 B. 39,50 C. 59,25 D. 16,20
(Xem giải) Câu 77. Cho X, Y, Z, T là các chất khác nhau trong số 4 chất: CH3COOH, C2H5OH, CH3OH, HCOOH và giá trị nhiệt độ sôi được ghi trong bảng sau:
| Chất | X | Y | Z | T |
| Nhiệt độ sôi (°C) | 100,5 | 118,2 | 78,3 | 65 |
Nhận xét nào sau đây là đúng ?
A. X là C2H5OH. B. Y là CH3COOH. C. Z là CH3OH. D. T là HCOOH.
(Xem giải) Câu 78. Một loại phân bón hỗn hợp trên bao bì ghi tỉ lệ 10 – 20 – 15. Các con số này chính là độ dinh dưỡng của phân đạm, phân lân, phân kali tương ứng. Để sản xuất loại phân bón này, nhà máy Z cần trộn ba loại hóa chất Ca(NO3)2, KH2PO4, KNO3 với nhau. Trong phân bón đó Ca(NO3)2 chiếm x% về khối lượng. Biết tạp chất không chứa N, P, K. Giá trị của x là
A. 38,3. B. 3,8. C. 55,5. D. 45,5.
(Xem giải) Câu 79. Khí SO2 do các nhà máy sinh ra là nguyên nhân quan trọng nhất gây ô nhiễm môi trường. Theo tiêu chuẩn quốc tế quy định nếu lượng SO2 vượt quá 10.10-6 mol/m³ không khí thì bị coi là ô nhiễm. Kết quả phân tích 50 lít không khí ở một số khu vực như sau:
| Khu vực | X | Y | Z |
| Khối lượng SO2 | 0,036 mg | 0,01 mg | 0,019 mg |
Không khí của khu vực bị ô nhiễm là
A. X. B. X và Y C. X, Y và Z. D. X và Z.
(Xem giải) Câu 80. Cho các phản ứng sau theo đúng tỉ lệ số mol:
(1) X (C9H20N2O4) + 2NaOH → X1 + X2 + X3↑ + H2O
(2) X1 + 3HCl → X4 + 2NaCl
(3) X2 (H2SO4 đặc, 170°C) → C2H4 + H2O
(4) X2 + O2 (lên men) → X5 + H2O
(5) X5 + X3 → X6
Biết X3 có cùng số nguyên tử cacbon với X2. Cho các phát biểu sau:
(a) X6 tác dụng được với dung dịch NaOH.
(b) Đốt cháy hoàn toàn 1 mol X1 thu được 7 mol hỗn hợp khí và hơi.
(c) Dung dịch X4 phản ứng với dung dịch NaOH, đun nóng nhẹ cho khí.
(d) X3 có 1 công thức cấu tạo.
Số phát biểu đúng là
A. 1. B. 4. C. 2. D. 3.


Bình luận