[2025] Thi thử TN chuyên ĐH Vinh – Nghệ An (Chính thức – Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 051
⇒ Đề thi, đáp án và giải chi tiết:
| 1C | 2B | 3D | 4A | 5B | 6C | 7D | 8C | 9D |
| 10A | 11C | 12C | 13A | 14A | 15D | 16D | 17D | 18B |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | S | Đ | Đ | Đ | 157 | 16 | 447 |
| (b) | Đ | Đ | S | S | 26 | 27 | 28 |
| (c) | S | Đ | Đ | S | 4 | 126 | 402 |
| (d) | S | S | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Chất nào sau đây thuộc loại disaccharide?
A. Glucose. B. Fructose. C. Maltose. D. Cellulose.
(Xem giải) Câu 2. Trên bao bì một loại phân bón NPK của công ty phân bón Việt Nhật có ghi độ dinh dưỡng là 16 – 16 – 8. Khối lượng phosphorus có trong 355 kg phân bón NPK này là
A. 28,4 kg. B. 24,8 kg. C. 12,4 kg. D. 56,8 kg.
(Xem giải) Câu 3. Cho bảng độ tan (gam/100 gam nước) ở 20°C của một số muối sulfate và nitrate của kim loại nhóm IIA như sau:
| Ion | Mg2+ | Ca2+ | Sr2+ | Ba2+ |
| NO3- | 69,5 | 152 | 69,5 | 9,02 |
| SO42- | 33,7 | 0,20 | 0,0132 | 0,0028 |
Một học sinh hoà tan hoàn toàn 150 gam muối X vào 200 gam H2O ở 20°C, thu được dung dịch Y. Vậy muối X có thể là
A. Sr(NO3)2. B. Ba(NO3)2. C. MgSO4. D. Ca(NO3)2.
(Xem giải) Câu 4. Poly(vinyl chloride) được điều chế từ phản ứng trùng hợp chất nào sau đây?
A. CH2=CHCl. B. CH3COOCH=CH2. C. CH2=CH2. D. CH2=CH-CH3.
(Xem giải) Câu 5. Tyrosine là một trong những loại amino acid cần thiết và có thể bổ sung cho cơ thể thông qua các thực phẩm ăn uống hàng ngày. Tyrosine làm tăng mức độ chất dẫn truyền thần kinh dopamine, adrenaline và norepinephrine giúp điều chỉnh tâm trạng, cải thiện trí nhớ, giúp tỉnh táo đầu óc và tăng khả năng tập trung. Với mỗi môi trường có giá trị pH bằng 0,10; 5,65; 9,59 và 12,90, coi tryrosine chỉ tồn tại ở dạng cho dưới đây:
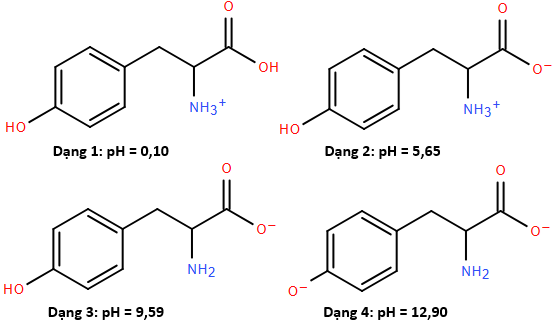
Trong quá trình điện di, ion sẽ chuyển về phía điện cực trái dấu với ion. Cho các nhận định sau về quá trình điện di của tyrosine:
(a) Với môi trường pH = 0,10 thì dạng (1) di chuyển về phía cực âm.
(b) Với môi trường pH = 5,65 thì dạng (2) hầu như không di chuyển về phía các điện cực.
(c) Với môi trường pH = 9,59 thì dạng (3) di chuyển về phía cực dương.
(d) Với môi trường pH = 12,90 thì dạng (4) di chuyển về phía cực âm.
Các nhận định đúng là
A. (b), (c), (d). B. (a), (b), (c). C. (a), (b), (d). D. (a), (c), (d).
(Xem giải) Câu 6. Glycine là một amino acid được cơ thể sử dụng để tạo ra protein và tạo ra các chất quan trọng khác gồm hormone, enzyme, … Cho m gam glycine tác dụng vừa đủ với 200 mL dung dịch NaOH 1 M, thu được dung dịch X. Phổ khối lượng của glycine như sau:
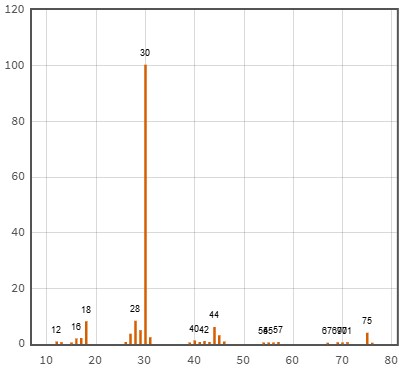
Phát biểu nào sau đây sai?
A. Công thức phân tử của glycine là C2H5O2N.
B. Glycine có tính lưỡng tính.
C. Giá trị của m là 7,5.
D. Phổ khối lượng của glycine có peak ion phân tử [Gly+] có giá trị m/z = 75.
(Xem giải) Câu 7. Một nhà kho chứa các đồ vật gia dụng làm từ nhựa polypropylene (PP) như hộp bảo quản thực phẩm, chai đựng nước, bình sữa trẻ nhỏ, đồ chơi trẻ em, dụng cụ học tập (vỏ bút bi, thước kẻ, hộp đựng bút), ghế nhựa, giá nhựa, tủ, bàn học, … bị bốc cháy, tạo nên khói đám cháy có nhiệt độ rất cao và chứa các khí độc như CO, CO2,… Cho các phát biểu sau:
(a) PP là polymer mạch không nhánh, bền trong môi trường acid và môi trường base, khó phân hủy sinh học.
(b) Trong khi di chuyển ra xa đám cháy, cần cúi thấp người (nhằm tránh khói đám cháy), đồng thời dùng khăn ướt che mũi và miệng (để hạn chế khí độc đi vào cơ thể).
(c) Nguyên tắc chữa cháy là cách li chất cháy, cách li hoặc làm giảm ảnh hưởng của nhiệt độ, nồng độ oxygen.
(d) Để dập tắt đám cháy trên ta có thể dùng nước và khí carbon dioxide.
Số phát biểu đúng là
A. 2. B. 3. C. 1. D. 4.
(Xem giải) Câu 8. Tiến hành các thí nghiệm sau:
(a) Điện phân MgCl2 nóng chảy.
(b) Nhiệt phân hoàn toàn BaCO3.
(c) Cho kim loại K vào dung dịch CuSO4 dư.
(d) Dẫn khí CO dư đi qua bột Fe2O3 nung nóng.
(e) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kim loại là
A. 4. B. 5. C. 3. D. 2.
(Xem giải) Câu 9. Chất hữu cơ X được dùng trong sản xuất thuốc chữa bệnh, các chất phòng trừ dịch hại, chất dẫn dụ côn trùng, chất tăng tốc lưu hoá cao su và chất ức chế ăn mòn kim loại. Dung dịch X làm quỳ tím hoá xanh. Kết quả phân tích phổ khối lượng cho thấy phân tử khối của X là 45. Chất X có thể là
A. methyl formate. B. methylamine. C. formic acid. D. ethylamine.
(Xem giải) Câu 10. Chất nào sau đây là amine bậc hai?
A. CH3NHCH3. B. CH3CH2N(CH3)2. C. CH3CH2NH2. D. CH3NH2.
(Xem giải) Câu 11. Chất nào sau đây gọi là xút ăn da?
A. Na2CO3. B. NaNO3. C. NaOH. D. NaHCO3.
(Xem giải) Câu 12. Phát biểu nào sau đây sai?
A. Kim loại có tính ánh kim là do các electron tự do trong mạng tinh thể kim loại phản xạ hầu hết những tia sáng mà con người nhìn thấy được.
B. Kim loại có tính dẻo là nhờ lực hút tĩnh điện giữa các cation kim loại và các electron hoá trị tự do trong mạng tinh thể.
C. Tungsten (vonfram) được dùng làm dây tóc bóng đèn vì là kim loại dẫn điện tốt nhất trong số các kim loại.
D. Ở nhiệt độ phòng, các đơn chất kim loại ở thể rắn và có cấu tạo tinh thể (trừ thuỷ ngân).
(Xem giải) Câu 13. Ethyl butyrate là ester có mùi thơm của dứa. Công thức của ethyl butyrate là
A. CH3CH2CH2COOCH2CH3. B. C2H5COOCH2CH2CH2CH3.
C. CH3CH2COOCH2CH3. D. CH3CH=CHCOOCH2CH3.
(Xem giải) Câu 14. Kim loại nào sau đây tan trong nước ở điều kiện thường?
A. Na. B. Cu. C. Al. D. Fe.
(Xem giải) Câu 15. Một trong các phương pháp bảo vệ chống ăn mòn kim loại được sử dụng rộng rãi là phương pháp điện hoá. Trong phương pháp này, người ta nối hoặc cho kim loại cần bảo vệ tiếp xúc với kim loại hoạt động hoá học mạnh hơn (kim loại hi sinh). Phát biểu nào sau đây sai?
A. Để bảo vệ vỏ tàu bằng thép, người ta gắn các lá kẽm vào phía ngoài vỏ tàu ở phần chìm trong nước biển.
B. Các electron chuyển từ kim loại hi sinh tới kim loại cần bảo vệ.
C. Sắt bị gỉ nhanh hơn khi tiếp xúc với đồng trong không khí ẩm.
D. Kim loại hi sinh luôn có thế điện cực chuẩn cao hơn kim loại cần được bảo vệ.
(Xem giải) Câu 16. Phản ứng nào sau đây được gọi là phản ứng xà phòng hoá?
A. H2NCH2COOH + NaOH → H2NCH2COONa + H2O.
B. C17H35COONa + HCl → C17H35COOH + NaCl.
C. CH3COOH + NaOH → CH3COONa + H2O.
D. CH3COOC2H5 + NaOH (t°) → CH3COONa + C2H5OH.
(Xem giải) Câu 17. Cho phản ứng: CH3-CH2-CH=O + HCN → CH3-CH2-CHOH-CN
Cơ chế của phản ứng trên như sau:
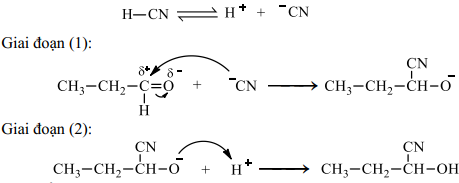
Phát biểu nào sau đây sai?
A. Trong giai đoạn (1), có sự phân cắt liên kết π và hình thành liên kết σ.
B. Trong giai đoạn (2), có sự tạo thành liên kết O-H.
C. Phản ứng trên là phản ứng cộng nucleophile vào hợp chất carbonyl.
D. Thay CH3CH2CHO bằng CH3COCH3 thì phản ứng trên không xảy ra.
(Xem giải) Câu 18. Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hoá – khử như sau:
| Cặp oxi hoá – khử | Zn2+/Zn | Fe2+/Fe | Cu2+/Cu | Ag+/Ag | Ni2+/Ni |
| Thế điện cực chuẩn (V) | -0,762 | -0,440 | +0,340 | +0,799 | -0,257 |
Dãy gồm các ion có tính oxi hoá tăng dần từ trái sang phải ở điều kiện chuẩn là
A. Ag+, Cu2+, Ni2+, Fe2+, Zn2+. B. Zn2+, Fe2+, Ni2+, Cu2+, Ag+.
C. Zn2+, Ni2+, Fe2+, Cu2+, Ag+. D. Zn2+, Fe2+, Cu2+, Ag+, Ni2+.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Để mạ đồng cho một tấm huy chương bằng sắt với độ dày và diện tích lớp mạ lần lượt là 0,1 mm và 88,5 cm², người ta tiến hành điện phân dung dịch CuSO4 (điện cực âm là tấm huy chương và điện cực dương là lá đồng (copper) thô, hiệu suất điện phân 100%) với cường độ dòng điện 2A không đổi. Khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết t giây. Cho biết:
– Khối lượng riêng của kim loại Cu là 8,96 g/cm³ và giả thiết toàn bộ lượng kim loại Cu sinh ra đều bám hết vào tấm huy chương, nước không bị điện phân ở cả hai điện cực.
– Điện lượng: q = I.t = ne.F, trong đó: q là điện lượng (C), ne là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian điện phân (giây).
a) Lá đồng thô đóng vai trò là cathode và tại điện cực này xảy ra quá trình oxi hoá kim loại Cu.
b) Lượng CuSO4 trong dung dịch không đổi trong quá trình điện phân.
c) Tấm huy chương đóng vai trò là anode và tại điện cực này xảy ra quá trình khử ion Cu2+.
d) Giá trị của t là 23912.
(Xem giải) Câu 20. Ethyl benzoate là hợp chất chính tạo mùi thơm của quả anh đào (cherry). Một học sinh tiến hành tổng hợp ethyl benzoate từ benzoic acid và ethyl alcohol theo phương trình hoá học sau: C6H5COOH + C2H5OH (H2SO4 đặc, t°) ⇋ C6H5COOC2H5 + H2O
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của ethyl benzoate, benzoic acid và ethyl alcohol. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O-H (alcohol) | O-H (carboxylic acid) | C=O (ester, carboxylic acid) |
| Số sóng (cm-1) | 3650 – 3200 | 3300 – 2500 | 1780 – 1650 |
a) Phổ hồng ngoại có số sóng hấp thụ đặc trưng ở 3391 cm-1 là phổ của ethyl alcohol.
b) Phổ hồng ngoại có số sóng hấp thụ đặc trưng ở 1726 cm-1 mà không có số sóng hấp thụ đặc trưng của liên kết O-H là của ethyl benzoate.
c) Dựa vào phổ hồng ngoại phân biệt được benzoic acid, ethyl alcohol và ethyl benzoate.
d) Phản ứng ester hoá ở trên có sự tách nguyên tử H từ phân tử benzoic acid và nhóm OH từ phân tử ethyl alcohol.
(Xem giải) Câu 21. Tiến hành thí nghiệm phản ứng màu biuret theo các bước sau:
Bước 1: Cho vào ống nghiệm khoảng 1 mL dung dịch NaOH 30%, thêm vài giọt dung dịch CuSO4 2%, lắc đều.
Bước 2: Thêm tiếp vào ống nghiệm khoảng 3 mL dung dịch protein (lòng trắng trứng), lắc đều hỗn hợp, rồi đặt lên giá ống nghiệm khoảng 2 – 3 phút.
a) Sau bước 1, trong ống nghiệm xuất hiện kết tủa màu xanh.
b) Sau bước 2, kết tủa trong ống nghiệm bị hoà tan và tạo thành dung dịch có màu vàng.
c) Thí nghiệm này còn được dùng để nhận biết dung dịch protein.
d) Kết quả thí nghiệm chứng tỏ phân tử protein có nhiều liên kết peptide.
(Xem giải) Câu 22. Một pin Galvani được thiết lập ở điều kiện chuẩn theo sơ đồ như hình sau:
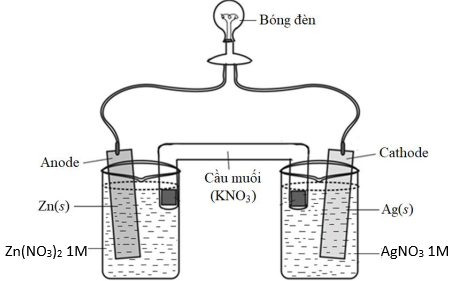
Cho biết:
– Thế điện cực chuẩn: E°Zn2+/Zn = -0,762V; E°Ag+/Ag = +0,799V.
– Điện lượng mà pin đã cung cấp: q = ne.F
– Điện năng cực đại (công cực đại) mà pin đã cung cấp cho bóng đèn ở điều kiện chuẩn:
A max pin cung cấp = q.E°pin = P.t
Trong đó: Amax là điện năng cực đại (J hay Ws), q là điện lượng (C hay As), ne là số mol electron đi qua dây dẫn, E°pin là sức điện động chuẩn của pin (V), P là công suất của bóng đèn (W), t là thời gian bóng đèn được thắp sáng liên tục (s).
a) Khối lượng Zn cần sử dụng trong pin để pin cung cấp một điện lượng bằng 17370 mAh là 21,06 gam (giả thiết hiệu suất các quá trình đều bằng 100%).
b) Coi toàn bộ điện năng cực đại (công cực đại) do pin sinh ra khi tiêu thụ hết 65 gam Zn ở điều kiện chuẩn dùng để thắp sáng một bóng đèn với công suất 20 W thì thời gian bóng đèn được thắp sáng liên tục là 75531 giây.
c) Ở cathode xảy ra quá trình oxi hoá ion Ag+.
d) Sức điện động chuẩn của pin là 0,037 V.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Sodium carbonate (Na2CO3) là chất thường dùng để làm mềm nước cứng theo phương pháp kết tủa. Độ cứng của nước có thể được tính theo số mg CaCO3 trong 1 lít nước, trong đó độ cứng không vượt quá 60 mg/L là nước mềm. Để xử lí một mẫu nước cứng vĩnh cửu có độ cứng a (mg CaCO3/L) người ta cho 1 lít dung dịch Na2CO3 0,020 M vào 19 lít mẫu nước cứng, lắc đều, thu được kết tủa CaCO3 và nước mềm Y. Nồng độ Ca2+ và CO32- có trong nước mềm Y lần lượt là 5,00.10^-4 M và 8,93.10-6 M. Giả thiết rằng, mẫu nước cứng chứa Ca2+ và các ion khác, các ion khác này không tham gia phản ứng, ion CO32- và ion Ca2+ không bị thuỷ phân trong nước. Tính giá trị của a (làm tròn đến hàng đơn vị).
(Xem giải) Câu 24. Xà phòng là hỗn hợp muối sodium hoặc potassium của các acid béo và các chất phụ gia. Hỗn hợp X gồm tristearin, tripalmitin, stearic acid và palmitic acid (tỉ lệ mol ntristearin : ntripalmitin = 1 : 1 và n palmitic acid : n stearic acid = 2 : 1). Để sản xuất b bánh xà phòng (mỗi bánh đều nặng 75 gam và chứa 75% muối của các acid béo theo khối lượng), người ta cho 863,92 gam hỗn hợp X tác dụng vừa đủ với 306 gam dung dịch NaOH 40%, đun nóng. Biết hiệu suất toàn bộ quá trình sản xuất xà phòng là 100%. Tính giá trị của b (làm tròn đến hàng đơn vị).
(Xem giải) Câu 25. Cho sơ đồ điều chế ethanol bằng phương pháp lên men tinh bột như sau:
![]()
Lên men 121,5 kg sắn khô (chứa 36% khối lượng là tinh bột, còn lại là các chất không có khả năng lên men thành ethanol) với hiệu suất mỗi quá trình (1) và (2) lần lượt là 90% và 80%. Dùng toàn bộ lượng ethanol sinh ra để pha chế xăng E5 (có chứa 5% thể tích ethanol). Biết khối lượng riêng của ethanol nguyên chất là 0,8 g/mL. Tính thể tích xăng E5 thu được sau pha trộn (theo lít, làm tròn đến hàng đơn vị).
(Xem giải) Câu 26. Có tổng số bao nhiêu đồng phân amine ứng với công thức phân tử C3H9N?
(Xem giải) Câu 27. Calcium oxide (CaO) còn được gọi là vôi sống, phần lớn được dùng làm vật liệu xây dựng. Ngoài ra, nó còn được dùng để làm chất hút ẩm trong công nghiệp, khử chua, tẩy uế,… Có thể sản xuất vôi sống bằng cách nung đá vôi (CaCO3) trong lò nung theo phương trình hoá học (1) như sau:
CaCO3(s) → CaO(s) + CO2(g) (1)
Phản ứng (1) là phản ứng thu nhiệt. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn carbon trong lò nung theo phương trình hoá học (2):
C(graphite) + O2(g) → CO2(g) (2)
Xét các phản ứng ở điều kiện chuẩn, hiệu suất chuyển hoá calcium carbonate thành calcium oxide là 100%. Tính khối lượng calcium oxide sản xuất được (theo tấn, làm tròn đến hàng đơn vị) trong các quá trình trên khi đốt cháy hoàn toàn 14,4 tấn carbon (graphite). Biết có 85% nhiệt lượng toả ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành của các chất ở điều kiện chuẩn được cho trong bảng sau:
| Chất | CaCO3(s) | CO2(g) | CaO(s) | C(graphite) |
| -1206,9 | -393,5 | -635,1 | 0,0 |
(Xem giải) Câu 28. Trong công nghiệp, aluminium được sản xuất bằng phương pháp điện phân aluminium oxide nóng chảy với hai điện cực bằng than chì, hiệu suất điện phân 100%. Quá trình điện phân được tiến hành với dòng điện có hiệu điện thế 5 V không đổi. Cho biết: 1 kWh = 3,6.10^6 J.
– Điện lượng: q = ne.F.
– Điện năng tiêu thụ: A tiêu thụ = q.U, trong đó: q là điện lượng (C), A tiêu thụ là điện năng tiêu thụ (J), U là hiệu điện thế (V), ne là số mol electron đi qua dây dẫn.
Tính điện năng tiêu thụ để sản xuất được 27 kg aluminium (theo kWh, làm tròn đến hàng đơn vị).

Bình luận