[2025] Thi thử TN sở GDĐT Thái Bình (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 076
⇒ Đề thi, đáp án và giải chi tiết:
| 1D | 2B | 3C | 4A | 5D | 6D | 7C | 8C | 9B |
| 10C | 11B | 12D | 13C | 14B | 15D | 16C | 17C | 18C |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | Đ | Đ | 25,4 | 125 | 5 |
| (b) | Đ | S | S | Đ | 26 | 27 | 28 |
| (c) | Đ | Đ | Đ | S | 134 | 42 | 37 |
| (d) | S | S | Đ | Đ |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Cho dung dịch glucose vào ống nghiệm chứa copper (II) hydroxide và NaOH rồi đun nóng nhẹ thấy xuất hiện …(1)… Cho dung dịch lòng trắng trứng vào ống nghiệm chứa copper (II) hydroxide và NaOH rồi khuấy đều thấy xuất hiện …(2)… Nội dung phù hợp trong các ô trống (1) và (2) lần lượt là
A. (1) dung dịch màu xanh lam, (2) dung dịch màu xanh lam.
B. (1) kết tủa màu đỏ gạch, (2) dung dịch màu xanh lam.
C. (1) dung dịch màu xanh lam, (2) dung dịch màu tím.
D. (1) kết tủa màu đỏ gạch, (2) dung dịch màu tím.
(Xem giải) Câu 2: Khi dẫn CO2 vào dung dịch sodium chloride bão hòa và ammonia bão hòa (phương pháp Solvay), thu được dung dịch chứa NaCl, NH4Cl, NaHCO3. Để tách NaHCO3 khỏi dung dịch hỗn hợp cần dùng phương pháp nào sau đây?
A. Lọc. B. Kết tinh. C. Chiết. D. Nung nóng.
(Xem giải) Câu 3: Thực hiện thí nghiệm về tính điện di ở pH = 6 của các amino acid gồm arginine, glycine, glutamic acid. Xét các thông tin dưới đây:
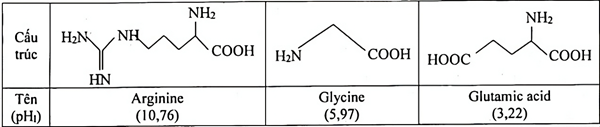
Kết quả thí nghiệm tính điện di ở pH = 6:
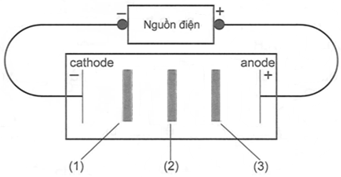
pI là giá trị pH mà tại đó aminoacid tồn tại ở dạng ion lưỡng cực có tổng điện tích dương bằng tổng điện tích âm. Cho các phát biểu sau:
(a) Tại pH = 6 thì arginine tồn tại chủ yếu ở dạng anion.
(b) Các vệt (1), (2), (3) lần lượt là glutamic acid, glycine, arginine.
(c) Nếu tại pH = 10,76 thì glycine và glutamic acid đều di chuyển về cực dương.
(d) Tại pH = 6 có thể dùng tính điện di để tách ba amino acid trên.
Số phát biểu đúng là
A. 3. B. 4. C. 2. D. 1.
(Xem giải) Câu 4: Công thức cấu tạo nào sau đây biểu diễn một ester?
A. HCOOCH2CH3. B. CH3CH2COOH. C. CH3COCH3. D. CH3COONH4.
(Xem giải) Câu 5: Hai nguyên tố Na (Z = 11) và Al (Z = 13) cùng đứng trong một chu kì trong bảng tuần hoàn do chúng có cùng đặc điểm nào sau đây?
A. Số electron ở lớp ngoài cùng. B. Số electron ở phân lớp ngoài cùng.
C. Số electron độc thân. D. Số lớp electron.
(Xem giải) Câu 6: Đạm (NH4)2SO4 được khuyến cáo không nên bón cho đất có pH thấp (đất chua). Nguyên nhân chính của khuyến cáo là
A. làm tăng khả năng bị rửa trôi dinh dưỡng. C. tăng NH3 gây độc hại cho cây trồng.
B. làm đất mất độ tơi xốp. D. làm tăng độ chua của đất.
(Xem giải) Câu 7: Cho chất X có công thức cấu tạo CH3CH2NHCH3. Tên của X là
A. isopropylamine. B. dimethylamine. C. ethylmethylamine. D. propan-2-amine.
(Xem giải) Câu 8: Vôi sống (một hợp chất chứa calcium) dùng làm chất khử chua cho đất. Tên hóa học của hợp chất này là
A. Calcium carbonate. B. Calcium hydrogen carbonate.
C. Calcium oxide. D. Calcium hydroxide.
(Xem giải) Câu 9: Chất X có công thức cấu tạo là CH3CH2CH2OH. Chất Y là một đồng phân của X. Chất Y có thể có công thức cấu tạo là
A. CH3CH(OH)CH2OH. B. CH3CH2OCH3. C. CH3CH2CHO. D. CH3CH2OH.
(Xem giải) Câu 10: Kim loại có thể bị uốn cong, dễ rèn, dễ dát mỏng và dễ kéo sợi. Tính chất vật lý nào giúp kim loại có những đặc điểm trên?
A. Tính dẫn nhiệt. B. Khối lượng riêng lớn.
C. Tính dẻo. D. Tính dẫn điện.
(Xem giải) Câu 11: Điện phân là một quá trình …(1)… xảy ra tại các điện cực khi có dòng điện …(2)… với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li. Nội dung phù hợp trong các ô trống (1) và (2) lần lượt là
A. khử, một chiều. B. oxi hóa-khử, một chiều.
C. oxi hóa, một chiều. D. oxi hóa-khử, xoay chiều.
(Xem giải) Câu 12: Chất X có công thức cấu tạo là CH3CH2COOCH3. Tên gọi của X là
A. ethyl acetate. B. propyl acetate.
C. methyl butyrate. D. methyl propionate.
(Xem giải) Câu 13: Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trọng đời sống: kích thích quả mau chín, điều chế nhựa làm sản phẩm gia dụng,… Phản ứng hóa học của ethylene với dung dịch Br2 như sau: CH2=CH2 + Br2 → CH2Br – CH2Br. Cơ chế của phản ứng trên xảy ra như sau:
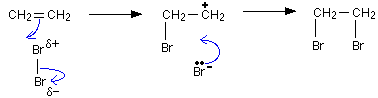
Nhận định nào sau đây không đúng?
A. Phản ứng trên thuộc loại phản ứng cộng.
B. Hiện tượng của phản ứng là dung dịch bromine bị mất màu.
C. Giai đoạn 1, liên kết đôi phản ứng với tác nhân nucleophile Brσ- tạo thành phần tử mang điện dương.
D. Giai đoạn 2, phần tử mang điện dương kết hợp với anion Br- tạo thành sản phẩm.
(Xem giải) Câu 14: Thí nghiệm về phản ứng của protein.
• Bước 1: Ống nghiệm 1: cho khoảng 1 mL dung dịch HNO3 đặc vào ống nghiệm.
• Bước 2: Ống nghiệm 2: cho khoảng 1 mL dung dịch NaOH 30% vào ống nghiệm, nhỏ thêm 3-4 giọt dung dịch CuSO4 2%, lắc đều.
• Bước 3: Cho khoảng 1 mL lòng trắng trứng vào ống nghiệm 1; cho khoảng 1 mL dung dịch lòng trắng trứng vào ống nghiệm 2, khuấy đều.
Cho các phát biểu sau:
(a) Thí nghiệm ở ống nghiệm 1 chứng tỏ trong protein có chứa vòng benzene.
(b) Sau bước 2 thu được kết tủa có màu trắng.
(c) Thí nghiệm ở ống nghiệm 1 có thể giải thích khi da tay tiếp xúc với HNO3 đặc thấy màu da chuyển sang vàng.
(d) Thí nghiệm ở ống nghiệm 2 có thể dùng để phân biệt dung dịch lòng trắng trứng với dung dịch đường saccharose.
Số phát biểu đúng là
A. 1. B. 3. C. 4. D. 2.
(Xem giải) Câu 15: Carbohydrate nào sau đây không phản ứng với thuốc thử tollens khi đun nóng?
A. Maltose. B. Fructose. C. Glucose. D. Saccharose.
(Xem giải) Câu 16: Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:

Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng… để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 5 được điều chế bằng phản ứng trùng hợp monomer nào dưới đây?
A. CH2=CH2. B. CH2=CH-C6H5. C. CH2=CH-CH3. D. CH2=CH-Cl
(Xem giải) Dựa vào thông tin dưới đây để trả lời các câu hỏi từ câu 17 – 18:
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
| Cặp | Al3+/Al | Zn2+/Zn | Fe2+/Fe | Cu2+/Cu | Ag+/Ag |
| E° (V) | -1,676 | -0,763 | -0,440 | 0,340 | 0,799 |
Câu 17. Dựa trên bảng thế điện cực chuẩn cho ở trên thì phản ứng nào dưới đây là sai?
A. Zn + Fe2+ → Zn2+ + Fe. B. Al + 3Ag+ → Al3+ + 3Ag.
C. Cu + Fe2+ → Fe + Cu2+. D. Fe + Cu2+ → Fe2+ + Cu.
Câu 18. Sức điện động chuẩn của một pin Galvani được thiết lập từ hai cặp oxi hóa – khử trong số các cặp trên có giá trị 2,475V. Hai cặp oxi hóa – khử hình thành pin lần lượt là
A. Al3+/Al và Cu2+/Cu. B. Zn2+/Zn và Al3+/Al.
C. Al3+/Al và Ag+/Ag. D. Fe2+/Fe và Cu2+/Cu.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Cao su thiên nhiên không dẫn điện, không thấm nước và khí, có tính đàn hồi tốt. Tuy nhiên, cao su thiên nhiên dễ bị lão hoá dưới tác động của không khí, ánh sáng, nhiệt. Ngoài ra, tính đàn hồi của cao su chỉ tồn tại trong một khoảng nhiệt độ hẹp. Cao su lưu hóa (loại cao su được tạo thành khi cho cao su thiên nhiên tác dụng với sulfur) có chứa khoảng 2,0% sulfur về khối lượng. Hãy cho biết những phát biểu sau là đúng hay sai?
a) Bản chất của quá trình lưu hoá cao su là phản ứng tăng mạch polymer, tạo ra cầu disulfide (-S-S-) giữa các phân tử polyisoprene tạo thành polymer có cấu tạo mạng lưới không gian.
b) Trong loại cao su lưu hóa trên, cứ trung bình khoảng 46 mắt xích isoprene có một cầu disulfide (-S-S-).
c) Cao su đã được lưu hoá có các ưu điểm tốt hơn về độ đàn hồi, chống thấm khí, chịu ma sát, bền với nhiệt và các tác nhân khác hơn với cao su thiên nhiên và cao su buna.
d) Cao su lưu hóa không tham gia phản ứng cộng.
(Xem giải) Câu 20: Thành phần dịch vị dạ dày gồm 95% là nước, enzyme và hydrochloric acid. Sự có mặt của hydrochloric acid làm cho pH của dịch vị trong khoảng từ 2 – 3. Khi độ acid trong dịch vị dạ dày tăng thì dễ bị ợ chua, ợ hơi, ói mửa, buồn nôn, loét dạ dày, tá tràng. Để làm giảm bớt lượng acid dư trong dịch vị dạ dày người ta thường uống thuốc muối dạ dày “Nabica” từng lượng nhỏ và cách quãng.
a) Công thức hoá học của thuốc muối dạ dày “Nabica” là NaHCO3.
b) Khi uống thuốc muối dạ dày “Nabica” thì sẽ sinh ra khí carbonmonooxide.
c) Khi uống thuốc muối dạ dày “Nabica” từng lượng nhỏ và cách quãng thì pH của dịch vị dạ dày sẽ tăng từ từ.
d) Nếu có 10 mL dịch vị dạ dày và coi pH của dạ dày hoàn toàn do hydrochloric acid gây ra, để nâng pH của dạ dày từ pH = 1 lên pH = 2 cần dùng hết 0,756 gam thuốc muối dạ dày Nabica (với giả thiết Nabica là nguyên chất và thể tích dung dịch vẫn giữ nguyên sau khi dùng thuốc).
(Xem giải) Câu 21: Điều chế ethyl acetate trong phòng thí nghiệm được tiến hành như sau:
• Bước 1: Cho khoảng 5 mL ethanol và 5 mL acetic acid tuyệt đối vào ống nghiệm, lắc đều hỗn hợp.
• Bước 2: Thêm khoảng 2 mL dung dịch H2SO4 đặc, lắc nhẹ để các chất trộn đều với nhau.
• Bước 3: Đặt ống nghiệm vào cốc nước nóng (khoảng 60°C − 70°C) trong khoảng 5 phút, thỉnh thoảng lắc đều hỗn hợp.
• Bước 4: Lấy ống nghiệm ra khỏi cốc nước nóng, để nguội hỗn hợp rồi rót sang ống nghiệm khác chứa 10 mL dung dịch muối ăn bão hòa thì thấy chất lỏng trong ống nghiệm tách thành hai lớp, lớp trên có mùi thơm đặc trưng.
• Bước 5: Đem đo phổ hồng ngoại (IR) của chất lỏng có mùi thơm đặc trưng.
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O-H (alcohol) | O-H (carboxylic acid) | C=O (ester, carboxylic acid) | C-O (ester) |
| Số sóng (cm-1) | 3650-3200 | 3300-2500 | 1780-1650 | 1300-1000 |
a) Dung dịch NaCl bão hoà làm giảm độ tan của ester trong nước để ester dễ dàng tách lớp nổi lên trên tốt hơn.
b) Phản ứng xảy ra trong bước 3 có sự tách nhóm -OH của phân tử alcohol.
c) Sulfuric acid đặc vừa là chất xúc tác, vừa có tác dụng hút nước, làm tăng hiệu suất tạo ester.
d) Ở bước 5, phổ hồng ngoại xuất hiện peak với số sóng 1780 – 1650 cm-1.
(Xem giải) Câu 22: Nghiên cứu ảnh hưởng của hiệu điện thế đến phản ứng điện phân, một nhóm học sinh cho rằng, dòng điện có hiệu điện thế càng lớn thì tổng khối lượng chất rắn và chất khí sau điện phân càng lớn. Để thực hiện điều đó, nhóm học sinh tiến hành như sau:
• Bước 1: Lấy cốc thể tích 100 mL, thêm vào đó 2,5 gam CuSO4.5H2O và thêm nước vào cho đến khi thể tích dung dịch là 25 mL.
• Bước 2: Thêm tiếp dung dịch H2SO4 1M vào dung dịch cho đến khi thể tích dung dịch đạt 40 mL. Đem cân toàn bộ cốc thì thấy khối lượng là m gam.
• Bước 3: Lấy hai điện cực than chì, nhúng vào dung dịch trong cốc (hai điện cực không tiếp xúc với nhau) và nối một điện cực với cực dương và nối một điện cực với cực âm của pin điện 2V.
• Bước 4: Thực hiện điện phân trong khoảng thời gian 10 phút, sau đó lấy hai điện cực ra và đem cân lại cốc đựng dung dịch sau điện phân thì khối lượng cốc là m2 gam.
Lặp lại thí nghiệm khi thay dòng điện 2V bằng các dòng điện 4V, 6V, 8V, 10V. Kết quả thí nghiệm:
| Hiệu điện thế (V) | 2 | 4 | 6 | 8 |
| Δm = m1 – m2 | 1,5 | 1,2 | 1,0 | 0,8 |
a) Các quá trình khử ion Cu2+ thành Cu và khử ion H+ thành H2 xảy ra tại điện cực than chì nối với cực âm.
b) Quá trình oxi hóa H2O tạo thành khí O2 và ion H+ xảy ra tại điện cực than chì nối với cực dương.
c) Sự chênh lệch khối lượng trước và sau điện phân đúng bằng khối lượng chất trong dung dịch đã điện phân.
d) Kết quả thí nghiệm chứng tỏ nhận định ban đầu của nhóm học sinh là sai.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Soda (Na2CO3) được dùng trong công nghiệp thủy tinh, đồ gốm, bột giặt…. Làm lạnh 100 gam dung dịch Na2CO3 bão hòa ở 20°C đến khi thu được dung dịch bão hòa ở 10°C thì tách ra m gam tinh thể Na2CO3.10H2O. Biết 100 gam nước hòa tan được tối đa lượng Na2CO3 ở 20°C và 10°C lần lượt là 21,5 gam và 12,5 gam. Tính giá trị của m. (Làm tròn kết quả đến 1 chữ số sau dấu phảy).
(Xem giải) Câu 24: Theo QCVN 01-1-2018/BYT, hàm lượng ion sắt tối đa cho phép trong nước sinh hoạt là 0,30 mg/L. Một mẫu nước có hàm lượng ion sắt cao gấp 28 lần ngưỡng cho phép, giả thiết sắt trong mẫu nước tồn tại ở dạng Fe2(SO4)3 và FeSO4 với tỉ lệ mol tương ứng là 1 : 6. Quá trình loại bỏ hoàn toàn ion sắt trong 10 m³ mẫu nước trên được thực hiện bằng cách sử dụng m gam vôi tôi (vừa đủ), sau đó sục không khí. Các quá trình diễn ra theo sơ đồ sau:
Fe2(SO4)3 + Ca(OH)2 → Fe(OH)3 + CaSO4 (1)
FeSO4 + Ca(OH)2 + O2 + H2O → Fe(OH)3 + CaSO4 (2)
Giả thiết vôi tôi chỉ chứa Ca(OH)2. Giá trị của m là bao nhiêu? (Kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 25: Cho các thông tin sau đây về tinh bột:
(1) Là một polysaccharide.
(2) Chứa liên kết α-1,4-glycoside.
(3) Thủy phân đến cùng trong môi trường acid, thu được glucose.
(4) Phản ứng được với thuốc thử tollens.
(5) Hồ tinh bột phản ứng với dung dịch iodine tạo hợp chất màu xanh tím.
(6) Trong cơ thể, enzyme α-amilase thúc đẩy quá trình thủy phân tinh bột.
Có bao nhiêu phát biểu đúng?
(Xem giải) Câu 26: Cho các nhận định sau:
(1) Aniline phản ứng với dung dịch Br2 thu được chất kết tủa trắng.
(2) CH3CH(NH2)CH3 là amine bậc hai.
(3) CH3CH2NH2 phản ứng với HNO2 ở nhiệt độ thường thu được chất khí không màu.
(4) Để khử mùi tanh của cá (thường do trimethylamine gây ra) có thể dùng giấm ăn.
Sắp xếp các nhận định đúng theo số thứ tự tăng dần (ví dụ 123, 1234,….).
(Xem giải) Câu 27: Xét quá trình đốt cháy ethanol C2H5OH(l): C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l). Cho biết enthalpy tạo thành của các chất như sau:
| Chất | CO2(g) | H2O(l) | C2H5OH(l) |
| -393,5 | -285,8 | -267 |
Cần x gam C2H5OH đốt cháy để cung cấp nhiệt dùng để đun 1,5 lít nước từ 25°C đến 100°C biết rằng có 40% lượng nhiệt đốt cháy bị thất thoát ra ngoài môi trường; biết rằng để tăng nhiệt độ của 1 gam nước thêm 1°C cần 4,2 J nhiệt; khối lượng riêng của nước là 1 g/mL.
Xét quá trình đốt cháy propane C3H8(g) và butane C4H10(g):
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(l) ![]() = -2220kJ
= -2220kJ
C4H10(g) + 6,5O2(g) → 4CO2(g) + 5H2O(l) ![]() = -2874kJ
= -2874kJ
Nếu thay lượng nhiệt do C2H5OH đốt cháy ở trên bằng lượng nhiệt lấy từ quá trình đốt cháy y gam khí hóa lỏng LPG chứa hỗn hợp propane và butane theo tỉ lệ mol tương ứng 2 : 3, hiệu suất nhiệt không đổi. Tính tổng x + y ? (Kết quả làm tròn đến hàng đơn vị).
(Xem giải) Câu 28: Cho công thức cấu tạo của phân tử chất giặt rửa sodium laurylsulfate sau đây:
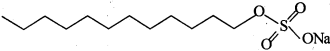
Phần kị nước của phân tử trên có tổng số nguyên tử là bao nhiêu?


Bình luận