[2025] Thi thử TN sở GDĐT Tuyên Quang (Lần 2)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 065
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2B | 3A | 4C | 5C | 6A | 7C | 8D | 9B |
| 10D | 11C | 12A | 13B | 14C | 15B | 16A | 17B | 18B |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | S | S | 389 | 1,38 | 58,3 |
| (b) | S | Đ | S | Đ | 26 | 27 | 28 |
| (c) | Đ | Đ | Đ | Đ | 6 | 23 | 1234 |
| (d) | S | Đ | S | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1. Methyl acetate có công thức cấu tạo thu gọn là
A. CH3COOC2H5. B. CH3COOCH3. C. C2H5COOCH3. D. CH2=CHCOOCH3.
(Xem giải) Câu 2. Ester X có công thức phân tử C4H8O2. Thủy phân X trong dung dịch NaOH vừa đủ, thu được sản phẩm gồm sodium propionate và alcohol Y. Số nguyên tử H trong phân tử Y là
A. 3. B. 4. C. 5. D. 7.
(Xem giải) Câu 3. Xà phòng có thể chứa chủ yếu chất nào sau đây?
A. CH3[CH2]14COONa. B. CH3[CH2]10CH2OSO3Na.
C. CH3[CH2]10CH2C6H4SO3Na. D. C3H5(OH)3.
(Xem giải) Câu 4. Chất nào sau đây thuộc loại polysaccharide?
A. Glucose. B. Saccharose. C. Cellulose. D. Fructose.
(Xem giải) Câu 5. Cho các dung dịch: (1) mật ong, (2) nước mía, (3) nước ép quả nho chín, (4) nước ép củ cải đường. Số dung dịch có khả năng hòa tan Cu(OH)2 là
A. 3. B. 1. C. 4. D. 2.
(Xem giải) Câu 6. Chất nào sau đây là amine bậc một?
A. CH3NH2. B. C2H5NHCH3. C. (C6H5)2NH. D. (CH3)3N.
(Xem giải) Câu 7. Cho các dung dịch: C6H5NH2, CH3NH2, H2NCH2COOH và H2N-[CH2]4-CH(NH2)-COOH (trong đó -C6H5 là gốc phenyl). Trong các dung dịch trên, có bao nhiêu dung dịch làm đổi màu quỳ tím?
A. 4. B. 3. C. 2. D. 1.
(Xem giải) Câu 8. Một thí nghiệm được mô tả như hình bên dưới:
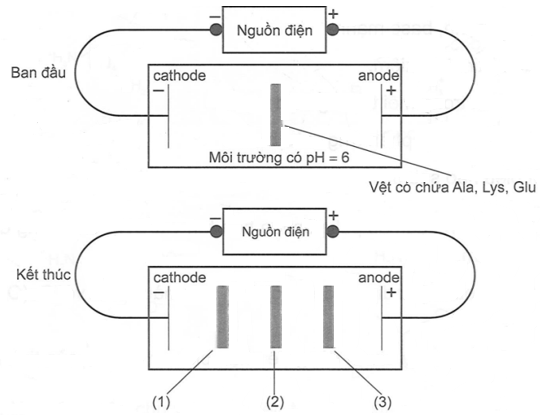
Giá trị pH mà khi đó amino acid có nồng độ ion lưỡng cực là cực đại được gọi là điểm đẳng điện (kí hiệu là pI). Mỗi amino acid có điểm đẳng điện khác nhau: Alanine (pI = 6,0), Lysine (pI = 9,74) và glutamic acid (pI = 3,08). Khi pH < pl thì amino acid đó tồn tại chủ yếu ở dạng cation, còn khi pH > pI thì amino acid đó tồn tại chủ yếu ở dạng anion. Cho các nhận định sau:
(a) Thí nghiệm trên biểu diễn tính điện li của amino acid.
(b) Ion tồn tại chủ yếu đối với Lys là cation, sẽ di chuyển về cực âm của nguồn điện nên vệt (1) là cation của Lys.
(c) Ion tồn tại chủ yếu đối với Ala là ion lưỡng cực, không di chuyển nên vệt (2) là Ala.
(d) Ion tồn tại chủ yếu đối với Glu là anion, sẽ di chuyển về cực dương của nguồn điện nên vệt (3) là anion của Glu.
Các nhận định đúng là:
A. (a), (b), (d). B. (a), (b), (c).
C. (a), (c), (d). D. (b), (c), (d).
(Xem giải) Câu 9. Polymer nào sau đây được sử dụng làm chất dẻo?
A. Nylon-6,6. B. Polyethylene. C. Nylon-6. D. Polybuta-1,3-diene.
(Xem giải) Câu 10. Xét phản ứng: Fe(s) + CuSO4(aq) → FeSO4(aq) + Cu(s). Kí hiệu cặp oxi hoá – khử của Fe trong phản ứng trên là
A. Fe3+/Fe. B. Fe/Fe2+. C. Fe3+/ Fe2+. D. Fe2+/Fe.
(Xem giải) Câu 11.Tiến hành thí nghiệm như sơ đồ dưới đây:
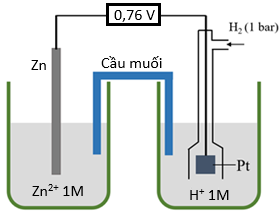
Cho thanh kẽm vào dung dịch ZnCl2 1 M. Nối thanh kẽm với điện cực hydrogen tiêu chuẩn thông qua vôn kế (voltmeter). Điện áp đo được là 0,76V. Phát biểu nào sau đây về thí nghiệm trên không đúng?
A. Zn là cực âm (anode) và điện cực hydrogen tiêu chuẩn là cực dương (cathode).
B. Tại cực âm, Zn nhường electron và tại cực dương, ion H+ nhận electron thành khí H2.
C. Nếu quy ước thế điện cực chuẩn của hydrogen bằng 0 V thì thế điện cực chuẩn của cặp Zn2+/Zn là +0,76V.
D. Phương trình hóa học của phản ứng xảy ra trong pin là: Zn(s)+ 2H+ (aq) → Zn2+(aq) + H2(g).
(Xem giải) Câu 12. Kim loại cơ bản trong hợp kim dural là
A. Al. B. Zn. C. Cu. D. Mg.
(Xem giải) Câu 13. Có bao nhiêu trường hợp xảy ra ăn mòn điện hoá trong các quá trình sau?
(a) Vỏ tàu bằng thép có gắn các khối kẽm, neo đậu tại một cảng biển.
(b) Dây chảy cầu chì làm bằng hợp kim Pb – Sn đứt khi cường độ dòng điện tăng đột ngột.
(c) Tấm tôn trầy xước trên mái nhà tiếp xúc với nước mưa.
(d) Một cổ vật làm bằng đồng thau (hợp kim Cu – Zn) chìm trong nước biển.
A. 1. B. 3. C. 2. D. 4.
(Xem giải) Câu 14. Để bảo quản sodium (Na), người ta phải ngâm sodium trong
A. nước. B. ethyl alcohol. C. dầu hỏa. D. phenol lỏng.
(Xem giải) Câu 15. Trong công nghiệp, NaOH được điều chế bằng cách điện phân dung dịch NaCl bão hòa, thùng điện phân có cực âm bằng sắt, cực dương bằng than chì, giữa hai điện cực có màng ngăn xốp (như sơ đồ bên dưới).
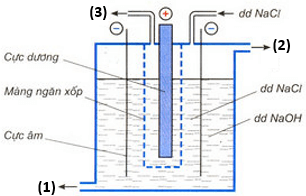
Theo sơ đồ thì dung dịch NaOH được lấy ra tại cửa ở vị trí
A. (1) và (2). B. (1). C. (2). D. (3).
(Xem giải) Câu 16. Urea là một loại phân bón quan trọng và phổ biến trong nông nghiệp, có công thức hóa học là (NH2)2CO. Urea thuộc loại
A. phân đạm. B. phân NPK. C. phân lân. D. phân kali.
(Xem giải) Câu 17. Phát biểu nào sau đây không đúng?
A. Trong vụ nổ vật lí không xảy ra phản ứng hóa học.
B. Nổ bom mìn, thuốc nổ là một dạng nổ vật lí.
C. Nổ vật lí xảy ra thường do áp suất cao.
D. Nổ hóa học bắt nguồn từ các phản ứng hóa học.
(Xem giải) Câu 18. Lycopen là hoạt chất có hoạt tính chống oxi hóa mạnh, được tìm thấy trong nhiều loại rau quả có màu đỏ như gấc, cà chua, dưa hấu… Một nghiên cứu đã chiết tách thành công lycopen từ màng hạt gấc Việt Nam, không những mang lại ý nghĩa trong việc tạo ra sản phẩm nâng cao sức khỏe cộng đồng mà còn giúp nâng cao giá trị kinh tế cho người trồng gấc. Sơ đồ quy trình chiết tách và tinh chế lycopen:
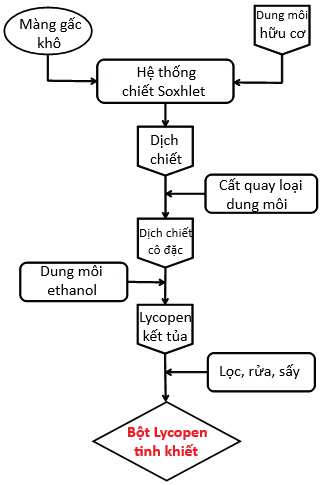
Lycopen tinh khiết được chiết tách từ quả gấc bằng phương pháp Soxhlet, sử dụng dung môi hữu cơ là dichloromethane, tinh chế lycopen bằng dung môi ethanol. Lượng lycopen chiết tách được là khoảng 3,2-4,4g/kg màng hạt gấc khô, có độ tinh khiết cao trên 98%. Cho các phát biểu sau:
(a) Dichloromethane là dung môi chiết, còn ethanol là dung môi kết tinh.
(b) Chiết lycopen từ màng hạt gấc dựa theo nguyên tắc chiết lỏng – rắn.
(c) Có thể thay dichloromethane bằng toluen do có nhiệt độ sôi tương tự.
(d) Thí nghiệm trên sử dụng 2 phương pháp là chiết và kết tinh.
Số phát biểu đúng là
A. 4. B. 3. C. 1. D. 2.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19. Phân tích phần trăm khối lượng các nguyên tố của ester X cho thấy X chứa 60% carbon, 8% hydrogen, còn lại là oxygen. Thủy phân X trong môi trường acid thu được methyl alcohol (Y) và carboxylic acid Z. Phổ khối lượng và phổ hồng ngoại của X được cho trong hình dưới đây:
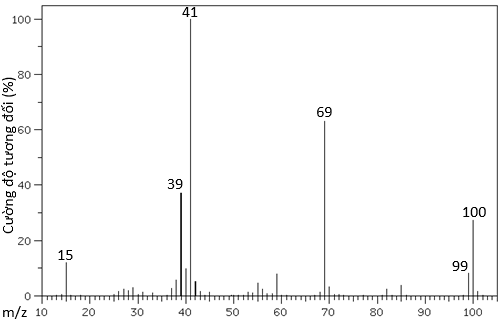
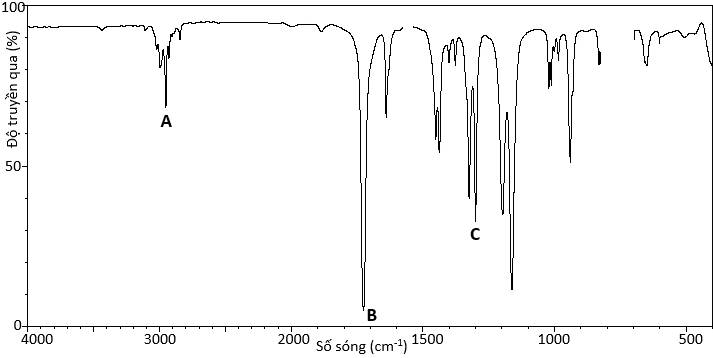
a. Khối lượng phân tử của X là 100.
b. Tổng số nguyên tử hydrogen và oxygen trong phân tử X là 12.
c. Tín hiệu hấp thụ đặc trưng cho liên kết C=O (ester) của X trên phổ hồng ngoại là điểm B.
d. Điều chế X trong phòng thí nghiệm bằng cách đun nóng 0,099 mol alcohol Y với 8,00 mL carboxylic acid Z (D = 1,02 g/mL), có dung dịch H2SO4 đặc làm xúc tác, thu được 5,58 gam ester X. Hiệu suất của phản ứng ester hóa là 50% (kết quả làm tròn đến hàng đơn vị). Cho H = 1, C = 12, O = 16.
(Xem giải) Câu 20. Để tiến hành kiểm chứng tính chất hóa học của tinh bột, một học sinh đã tiến hành thí nghiệm như sau:
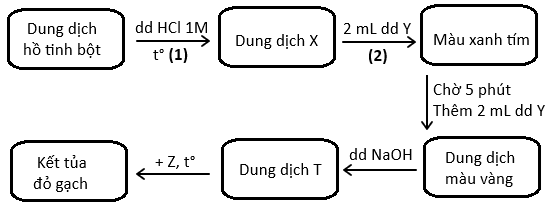
a. Thí nghiệm trên chứng minh tinh bột bị thủy phân trong môi trường acid.
b. Chất Z có thể lựa chọn là dung dịch CuSO4.
c. Dung dịch Y ở bước (2) được sử dụng để kiểm tra xem tinh bột đã thủy phân hoàn toàn hay chưa.
d. Dung dịch NaOH 10% được thêm vào từ từ từng giọt đến khi dung dịch T làm giấy quỳ tím chuyển sang màu xanh.
(Xem giải) Câu 21. Trong công nghiệp, sodium được điều chế bằng cách điện phân nóng chảy sodium chloride trong bình điện phân Downs với điện áp khoảng 7V, cường độ dòng điện từ 25000A đến 40000A với các điện cực là than chì và sắt theo sơ đồ như hình dưới đây:
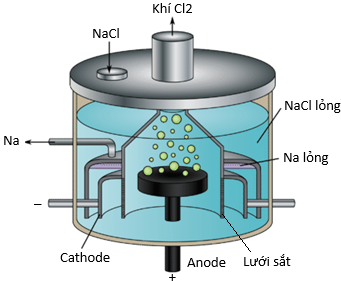
a. Ở anode xảy ra quá trình Na+ + 1e → Na.
b. Điện cực anode được làm bằng sắt, điện cực cathode được làm bằng than chì.
c. Lưới thép giúp ngăn cho Na (ở trạng thái nóng chảy) không phản ứng lại với Cl2.
d. Khi sử dụng cường độ dòng điện là 30000 A thì sau 24 giờ sản xuất được 618 kg sodium (hiệu suất của cả quá trình đạt 80%). Cho Na = 23; F = 96500 C/mol.
(Xem giải) Câu 22. Cho các giá trị thế điện cực chuẩn trong một loại pin cúc áo được sử dụng rộng rãi trong đồng hồ và các thiết bị như sau:
ZnO22- + 2H2O + 2e ⇋ Zn + 4OH- E° = -1,216V
Ag2O + H2O + 2e ⇋ 2Ag + 2OH- E° = +0,342V
Một viên pin có chứa 0,4875 gam zinc và có khả năng chạy được cho đến khi 80% lượng zinc được tiêu thụ ở cường độ dòng điện 0,03 mA. Cho O = 16; Zn = 65; Ag = 108.
a. Bán phản ứng xảy ra ở cực âm của pin là: ZnO22- + 2H2O + 2e ⇋ Zn + 4OH-
b. Phản ứng hóa học xảy ra trong pin khi pin hoạt động:
Zn(s) + Ag2O(s) + 2OH-(aq) → ZnO22- (aq) + 2Ag(s) + H2O(l)
c. Khối lượng Ag2O đã tiêu thụ khi pin dừng hoạt động là 1,392 gam.
d. Thời gian pin hoạt động được tối đa 347 ngày.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23. Glucose (C6H12O6) là một loại monosaccharide được tạo ra bởi thực vật và các loại tảo từ quá trình quang hợp. Dung dịch glucose 5% (100 mL dung dịch chứa 5 gam glucose) là dung dịch đường tiêm tĩnh mạch, dùng để cung cấp nước và năng lượng cho cơ thể, đặc biệt là khi cơ thể ốm yếu, mệt mỏi… Phương trình nhiệt hóa học của phản ứng oxi hóa glucose như sau:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l) ![]() = -2803 kJ.
= -2803 kJ.
Tính năng lượng tối đa (kJ) thu được từ glucose khi một người bệnh được truyền dịch trong 2 ngày, mỗi ngày 1 chai 250mL dung dịch glucose 5%. (Kết quả được lấy đến hàng đơn vị). Cho H = 1, C = 12, O = 16.
(Xem giải) Câu 24. Để sản xuất m tấn xà phòng (có chứa 75% khối lượng là muối sodium của acid béo, còn lại là chất độn), người ta xà phòng hóa hoàn toàn 1 tấn chất béo trung tính bằng dung dịch chứa 150 kg NaOH vừa đủ. Xác định giá trị m. (Kết quả được lấy đến hàng phần trăm). Cho H = 1, C = 12, O = 16, Na = 23.
(Xem giải) Câu 25. Một tấm kính hình chữ nhật chiều dài 2,4 m, chiều rộng 2,0 m được tráng lên một mặt bởi lớp bạc có bề dày là 0,1 µm. Để tráng bạc lên 1000 tấm kính trên người ta phải dùng V lít dung dịch glucose 0,5 M. Biết hiệu suất tráng bạc tính theo glucose là 80%, khối lượng riêng của bạc là 10,49 gam/cm³. Tính giá trị của V. (Kết quả được lấy đến hàng phần mười). Cho H = 1, C = 12, O = 16, Ag = 108.
(Xem giải) Câu 26. Số nguyên tử oxygen có trong peptide Gly-Ala-Val-Gly-Ala là bao nhiêu?
(Xem giải) Câu 27. Người ta tách kim loại Ag bằng phương pháp cyanide qua các giai đoạn sau:
• Giai đoạn 1: Nghiền nhỏ quặng silver sulfide (Ag2S), hoà tan bằng dung dịch sodium cyanide (NaCN), rồi lọc để thu được dung dịch chứa phức chất tan của bạc:
Ag2S + 4NaCN → 2Na[Ag(CN)2] + Na2S
• Giai đoạn 2: Khi có mặt oxygen, bạc trong quặng tan được trong dung dịch NaCN:
4Ag + O2 + 8NaCN + 2H2O → 4Na[Ag(CN)2] + 4NaOH
• Giai đoạn 3: Sau đó ion Ag+ trong phức được khử bằng kim loại kẽm:
2Na[Ag(CN)2] + Zn → Na2[Zn(CN)4] + 2Ag
(1) Giai đoạn 1 và giai đoạn 2 quặng được xử lí bằng cả quá trình vật lí và quá trình hoá học.
(2) Bản chất của giai đoạn 3 là sử dụng phương pháp thủy luyện để tách kim loại bạc.
(3) Trong công nghiệp, phương pháp trên thường được dùng để điều chế các kim loại quý như Au, Ag.
(4) Sau giai đoạn 3, người ta dùng dung dịch HCl, H2SO4 đặc để loại bỏ kẽm dư.
Gắn số thé tự theo chiều tăng dần các phát biểu đúng (ví dụ: 123; 134; 234;…).
(Xem giải) Câu 28. Cho sơ đồ Solvay sản xuất sodium hydrogencarbonate và sodium carbonate như sau:
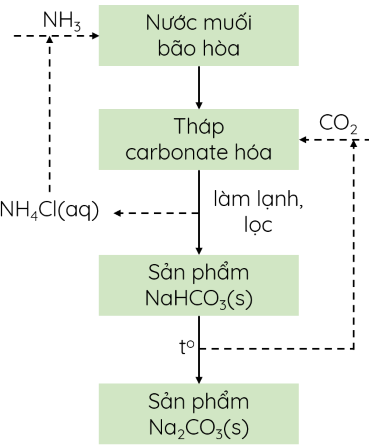
Cho các phát biểu sau:
(1) Trong quy trình trên, CO2 và NH3 được tái sử dụng.
(2) Sau khi làm lạnh, NaHCO3 kết tinh do có độ tan thấp.
(3) Trong công nghiệp, quá trình thu hồi NH3 có thể dùng vôi sống.
(4) Quy trình Solvay đã giảm thiểu được tác động đến môi trường bằng cách quay vòng các sản phẩm trung gian để tái sử dụng trong quy trình sản xuất.
Gắn số thứ tự theo chiều tăng dần các phát biểu đúng (ví dụ: 123; 234; 1234).

Bình luận