[2025] Thi thử TN trường Quảng Xương 1 – Thanh Hóa (Lần 1)
⇒ File word đề thi, đáp án và giải chi tiết
⇒ Mã đề: 141
⇒ Đề thi, đáp án và giải chi tiết:
| 1B | 2D | 3A | 4C | 5B | 6A | 7C | 8B | 9B |
| 10B | 11D | 12D | 13B | 14A | 15B | 16C | 17D | 18D |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| (a) | Đ | Đ | Đ | Đ | 2,5 | 499 | 4 |
| (b) | Đ | Đ | Đ | S | 26 | 27 | 28 |
| (c) | Đ | Đ | Đ | Đ | 234 | 4 | 67,3 |
| (d) | S | S | Đ | S |
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Xem giải) Câu 1: Nguyên tố magnesium (Mg) có số hiệu nguyên tử là 12. Ở trạng thái cơ bản, cấu hình electron của ion Mg2+ là
A. 1s2 2s2 2p6 3s2. B. 1s2 2s2 2p6. C. 1s2 2s2 2p5. D. 1s2 2s2 2p4.
(Xem giải) Câu 2: Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá – khử sau:
| Cặp oxi hoá – khử | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Ni2+/Ni | 2H+/H2 |
| Thế điện cực chuẩn (V) | 0,340 | –0,763 | –0,440 | –0,257 | 0,000 |
Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
A. 1. B. 4. C. 2. D. 3.
(Xem giải) Câu 3: Sắn là một loại thực phẩm có thành phần chủ yếu là tinh bột. Mặc dù vậy, một số loại sắn có chứa lượng chất độc cũng rất cao. Chất độc có trong sắn là cyanhydric acid (HCN), đây là một chất có thể gây độc chết người. Cách đơn giản để chuyển hóa HCN là cho HCN kết hợp nhóm carbonyl (C=O) để chuyển thành hợp chất chứa nhóm -C(OH)CN. Loại thực phẩm nào sau đây có thể cung cấp nhóm carbonyl để giải độc nhanh nhất cho người ngộ độc?
A. đường glucose. B. giấm ăn. C. gạo trắng. D. dầu ăn.
(Xem giải) Câu 4: Dung dịch saccharose tham gia phản ứng nào sau đây?
A. Phản ứng với thuốc thử Tollens.
B. Phản ứng với mước bromine.
C. Phản ứng với Cu(OH)2, tạo dung dịch màu xanh lam.
D. Phản ứng thuỷ phân trong môi trường kiềm.
(Xem giải) Câu 5: Polypropylene là chất dẻo bền, có khả năng chịu lực tốt, thường được sử dụng để làm hộp đựng thức ăn, chai lọ…. Polypropylene được tổng hợp từ monomer nào sau đây?
A. CH2=CH(CH3)-COOCH3. B. CH3CH=CH2.
C. CH2=CH2. D. CH2=CHCN.
(Xem giải) Câu 6: Hợp chất hữu cơ là hợp chất của …(1)… Trong phân tử hợp chất hữu cơ, liên kết hóa học chủ yếu giữa các nguyên tử là liên kết …(2)… Các cụm từ phù hợp nhất điền vào chỗ trống (1), (2) lần lượt là
A. carbon, cộng hóa trị. B. hydrogen, cộng hóa trị.
C. hydrogen, ion. D. carbon, ion.
(Xem giải) Câu 7: Chất nào sau đây thuộc loại amino acid?
A. Glucose. B. Methyl amine. C. Glycine. D. Acetic acid.
(Xem giải) Câu 8: Cho 1 mol chất béo X tác dụng với dung dịch NaOH dư, thu được 1 mol glycerol, 1 mol sodium palmitate và 2 mol sodium stearate. Khối lượng mol phân tử của X là
A. 890 gam. B. 862 gam. C. 888 gam. D. 834 gam.
(Xem giải) Câu 9: Trong tự nhiên, hầu hết các kim loại tồn tại ở dạng hợp chất (oxide, muối,…) trong quặng, chỉ một số kim loại kém hoạt động như vàng, bạc, platinum,… tồn tại dưới dạng đơn chất. Để tách kim loại ra khỏi hợp chất của chúng cần dựa vào mức độ hoạt động, độ bền của hợp chất và độ phổ biến của hợp chất chứa kim loại. Cho các phát biểu sau
(a) Nguyên tắc chung điều chế kim loại là khử ion kim loại thành nguyên tử.
(b) Để điều chế các kim loại hoạt động mạnh như K, Na, Mg, Al,… người ta sử dụng phương pháp điện phân nóng chảy muối chloride của chúng.
(c) Để tách kim loại Cu ra khỏi dung dịch CuSO4 ta có thể sử dụng phương pháp là điện phân dung dịch hoặc thủy luyện.
(d) Tái chế kim loại là giải pháp giúp ngăn chặn việc khai thác cạn kiệt các mỏ quặng kim loại và hạn chế phát thải ra môi trường.
(e) So với phương pháp nhiệt luyện thì phương pháp điện phân có ưu điểm là thu được kim loại có độ tinh khiết cao hơn.
Số phát biểu đúng là
A. 2. B. 4. C. 3. D. 5.
(Xem giải) Câu 10: Phản ứng nào sau đây là phản ứng tỏa nhiệt?
A. Phản ứng quang hợp của cây xanh.
B. Phản ứng oxi hóa glucose trong cơ thể.
C. Phản ứng nung đá vôi.
D. Phản ứng nhiệt phân muối KNO3.
(Xem giải) Câu 11: Phản ứng monobromo hóa ethane xảy ra theo cơ chế thế gốc: CH3CH3 + Br2 → CH3CH2Br + HBr (∗). Giai đoạn (1) trong cơ chế của phản ứng trên xảy ra như sau: Br-Br → 2Br• (1). Nhận định nào sau đây không đúng?
A. Giai đoạn (1) xảy ra sự phân cắt đồng li.
B. Phản ứng monobromo hóa ethane thuộc loại phản ứng thế.
C. Sản phẩm của giai đoạn (1) có chứa electron độc thân.
D. Sản phẩm của phản ứng (∗) là các chất tan tốt trong nước.
(Xem giải) Câu 12: Trong quá trình điện phân NaCl nóng chảy với anode bằng than chì và cathode bằng thép. Phát biểu nào sau đây sai?
A. Sodium (Na) sinh ra ở dạng lỏng.
B. Quá trình điện phân diễn ra ở nhiệt độ cao.
C. Tại anode xảy ra quá trình oxi hóa Cl- thành khí Cl2.
D. Anode bị ăn mòn trong quá trình điện phân.
(Xem giải) Câu 13: Trường hợp nào sau đây kim loại bị phá hủy chủ yếu do ăn mòn hóa học?
A. Vỏ tàu biển bằng thép bị gỉ sau một thời gian sử dụng.
B. Nhúng lá Zn vào dung dịch H2SO4 loãng.
C. Thép xây dựng bị gỉ khi để ngoài không khí ẩm.
D. Ống dẫn nước làm bằng gang bị gỉ khi chôn dưới đất.
(Xem giải) Câu 14: Cho các chất giặt rửa ở cột (I) và các ưu điểm và nhược điểm ở cột (II) sau:
| Cột (I): | Cột (II): |
| 1) Xà phòng 2) Chất giặt rửa tổng hợp 3) Chất giặt rửa tự nhiên |
a) Ưu điểm: lành tính với da, dễ phân hủy bởi vi sinh vật nên không gây ô nhiễm môi trường. Nhược điểm: Giá thành cao, khó sản xuất ở quy mô công nghiệp. b) Ưu điểm: Dùng được với nước cứng. Giá thành thấp. Nhược điểm: có gốc hydrocarbon phân nhánh hoặc chứa vòng benzene sẽ gây ô nhiễm môi trường do chúng rất khó bị vi sinh vật phân hủy. c) Ưu điểm: có thể bị phân hủy bởi vi sinh vật nên ít gây ô nhiễm môi trường. Nhược điểm: khi dùng với nước cứng tạo ra kết tủa bám trên bề mặt vải, ảnh hưởng đến chất lượng vải, đồng thời làm giảm tác dụng giặt rửa. |
Hãy lựa chọn các ghép cặp phù hợp với chất giặt rửa phù hợp và ưu điểm, nhược điểm của chúng.
A. 1-c); 2-b); 3-a). B. 1-a); 2-c); 3-b). C. 1-b); 2-c); 3-a). D. 1-a); 2-b); 3-c).
(Xem giải) Câu 15: Docosahexaenoic acid (DHA) rất quan trọng với việc phát triển trí não, giúp cho quá trình phát triển hoàn hảo của hệ thần kinh và chỉ số IQ của trẻ. Nguồn cung cấp DHA phong phú và dễ hấp thu nhất là thịt cá và dầu cá. Công thức khung phân tử của (DHA) như sau:

Vậy DHA là
A. acid béo omega-6. B. acid béo omega-3. C. acid béo no. D. chất béo.
(Xem giải) Câu 16: Cryolite (còn gọi là băng thạch) có công thức phân tử Na3AlF6, được thêm vào Al2O3 trong quá trình điện phân Al2O3 nóng chảy để sản xuất nhôm. Cryolite không có tác dụng nào sau đây?
A. Làm giảm nhiệt độ nóng chảy của Al2O3.
B. Nhẹ hơn nổi lên trên để bảo vệ Al nóng chảy không tiếp xúc với không khí.
C. Bảo vệ điện cực khỏi bị ăn mòn.
D. Làm tăng độ dẫn điện của Al2O3 nóng chảy.
(Xem giải) Sử dụng thông tin dưới đây để trả lời các câu 17 – 18:
Geranyl acetate là hợp chất hữu cơ có trong tinh dầu hoa hồng và được sử dụng nhiều trong mĩ phẩm. Trong công nghiệp, geranyl acetate được điều chế theo sơ đồ sau:
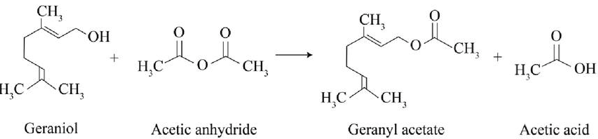
Câu 17: Công thức phân tử của geranyl acetate là
A. C12H18O2. B. C12H22O2. C. C11H18O2. D. C12H20O2.
Câu 18: Trong các điều kiện tối ưu, hiệu suất tối đa của phản ứng ester hóa giữa geraniol và acetic anhydride để tạo ra geranyl acetate có thể đạt đến 98-99%. Khối lượng geranyl acetate thu được từ 100 kg geraniol với hiệu suất chuyển hóa theo geraniol đạt 98% là
A. 128,24 kg. B. 122,54 kg. C. 112,52 kg. D. 124,73 kg.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
(Xem giải) Câu 19: Aniline (nhiệt độ nóng chảy –6,3°C; nhiệt độ sôi 184,13°C, độ tan là 3,6 g/100g nước ở 20°C) là hóa chất được sử dụng nhiều trong lĩnh vực phẩm nhuộm, dược phẩm. Trong phòng thí nghiệm, quá trình điều chế aniline từ nitrobenzene được thực hiện theo sơ đồ phản ứng sau:
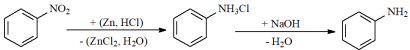
a. Trong phản ứng khử nitrobenzene bằng (Zn + HCl), tác nhân khử là hydrogen mới sinh [H].
b. Nitrobenzene được điều chế trực tiếp từ benzene bằng phản ứng nitro hóa.
c. Phương pháp có thể sử dụng để tách aniline ra khỏi hỗn hợp sau kiềm hóa là phương pháp chiết lỏng – lỏng.
d. Độ tan của aniline trong nước lớn hơn độ tan của aniline trong dung dịch acid và dung dịch kiềm.
(Xem giải) Câu 20: Tiến hành thí nghiệm theo các bước sau:
• Bước 1: Cho một nhúm bông (khoảng 2 gam) vào cốc chứa 20 mL dung dịch H2SO4 70%, dùng đũa thủy tinh khuấy nhẹ cho đến khi bông tan hết, thu được dung dịch (1).
• Bước 2: Thêm tiếp dung dịch NaOH 1M vào dung dịch (1) cho đến khi quỳ tím chuyển sang màu xanh. Thêm khoảng 1 mL dung dịch CuSO4 5% vào và 1 mL dung dịch NaOH 1 M nữa, thu được dung dịch (2).
• Bước 3: Ngâm cốc đựng dung dịch (2) trong nồi nước nóng trong khoảng thời gian 10 phút.
a. Sau bước 2, dung dịch thu được có màu xanh lam.
b. Phản ứng thủy phân cellulose xảy ra ở bước 1.
c. Sau bước 3, trong cốc xuất hiện kết tủa màu đỏ gạch.
d. Tại bước 1, có thể thay dung dịch H2SO4 70% bằng dung dịch H2SO4 98% thì kết quả các bước sau tương tự.
(Xem giải) Câu 21: Hai nhóm học sinh tiến hành thí nghiệm điện phân dung dịch CuSO4 với một điện cực than chì và một điện cực bằng đồng (bỏ qua sự thay đổi thể tích của dung dịch khi điện phân).
Nhóm 1: Nối điện cực than chì với cực dương và điện cực đồng với cực âm của nguồn điện.
Nhóm 2: Nối điện cực than chì với cực âm và điện cực đồng với cực dương của nguồn điện.
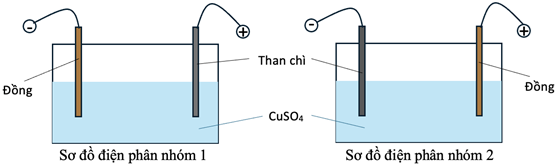
Hai nhóm đều đưa ra giả thuyết sau: trong quá trình điện phân, nồng độ ion Cu2+ giảm dần ứng với màu xanh của dung dịch nhạt dần.
a) Ở nhóm thứ hai, tại anode xảy ra quá trình oxi hoá đồng.
b) Đối với cả hai nhóm đều có kim loại đồng bám vào cathode.
c) Ở nhóm thứ nhất, pH của dung dịch điện phân giảm dần.
d) Giả thuyết đúng với nhóm thứ nhất và sai với nhóm thứ hai.
(Xem giải) Câu 22: Gang là hợp kim chứa khoảng 95% sắt, 2% đến 5% carbon và một số nguyên tố khác. Gang được sản xuất trong lò cao với nhiều phản ứng xảy ra liên tiếp nhau như hình sau
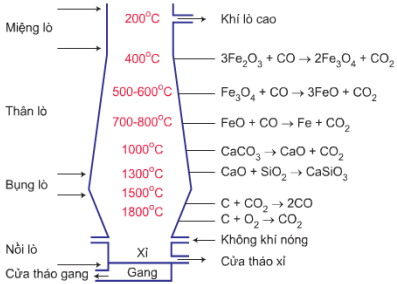
a. Quặng sắt dùng sản xuất gang là quặng hematit (thành phần chính là Fe2O3) và manhetit (thành phần chính là Fe3O4).
b. Gang được tạo ra ở nhiệt độ 800°C.
c. Xỉ có thành phần chính là CaSiO3 và có khối lượng riêng nhẹ hơn gang.
d. Để sản xuất thép người ta sử dụng nguyên liệu là sắt thép phế liệu (chứa 75% Fe, 23% Fe2O3 và 2% C) phối trộn với gang (chứa 95% Fe và 5% C). Nếu trộn 3,5 tấn sắt thép phế liệu với 6 tấn gang thì sẽ luyện được loại thép chứa 1,6% C. Biết phản ứng trong lò luyện thép như sau: 2Fe2O3 + 3C → 4Fe + 3CO2
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 23 đến câu 28.
(Xem giải) Câu 23: Một nhà máy sản xuất túi nylon từ HDPE cần sản xuất túi đựng hình chữ nhật có kích thước là 30 cm x 50 cm, bề dày của lớp nylon là 0,005 cm. Biết hiệu suất phản ứng trùng hợp ethylene để điều chế HDPE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và biết khối lượng riêng của nhựa HDPE là 0,95 g/cm³. Khối lượng nguyên liệu ethylene dùng để sản xuất đơn hàng 100.000 túi này là bao nhiêu tấn? (Kết quả làm tròn đến hàng phần mười)
(Xem giải) Câu 24: Để mạ đồng một vật dụng kim loại có tổng diện tích bề mặt là 100 cm², người ta tiến hành điện phân dung dịch CuSO4 với điện cực âm là vật dụng cần mạ và cực dương là thanh đồng thô. Biết cường độ dòng điện không đổi là 2 A, hiệu suất điện phân là 90%, khối lượng riêng của Cu là 8,94 g/cm³ và lượng đồng tạo ra được tính theo công thức Faraday là m = A.I.t/n.F (với A là NTK của Cu = 64; F là hằng số Faraday = 96485 C/mol). Thời gian điện phân để lớp mạ có độ dày đồng nhất 0,2 mm là bao nhiêu phút? (Làm tròn kết quả đến hàng đơn vị).
(Xem giải) Câu 25: Cho các kim loại sau: Ca, Pb, Mg, Fe, Cu, Al, K, Zn. Số kim loại được điều chế trong công nghiệp bằng phương pháp nhiệt luyện là?
(Xem giải) Câu 26: Cho các phát biểu sau:
(1) Trong công nghiệp, maltose được sử dụng làm nguyên liệu để sản xuất bia.
(2) Thành phần chính của giấy viết là cellulose.
(3) Insulin, một loại hormone thuộc loại protein, được sản sinh bởi tuyến tụy.
(4) PVC được dùng làm vật liệu cách điện, ống dẫn nước.
(5) Cao su buna –S được tổng hợp bằng phản ứng trùng hợp buta-1,3-diene với bột sulfur.
Liệt kê các phát biểu đúng theo thứ tự tăng dần.
(Xem giải) Câu 27: Cho các ester: Ethyl acetate, vinyl formate, iso amyl acetate; benzyl propionate, metyl acrylate và iso propyl formate. Có bao nhiêu ester khi thủy phân trong môi trường kiềm, đun nóng thu được muối và alcohol bậc 1?
(Xem giải) Câu 28: Magnetit là một khoáng vật quan trọng trong ngành công nghiệp và khai thác quặng sắt, có thành chính là Fe3O4. Hàm lượng sắt trong quặng này có thể được xác định bằng phương pháp chuẩn độ. Người ta tiến hành thí nghiệm như sau:
• Bước 1: Cân chính xác 5,0 gam mẫu quặng magnetit đã nghiền mịn và chuyển toàn bộ sang cốc thủy tinh 100 mL.
• Bước 2: Thêm 50 mL dung dịch H2SO4 loãng vào cốc, đun nhẹ để hòa tan quặng. Sau khi hòa tan hoàn toàn, lọc lấy dung dịch và loại bỏ phần không tan. Sau đó định mức thành 100 mL dung dịch.
• Bước 3: Hút chính xác 10,00 mL dung dịch sau khi định mức cho vào bình tam giác, thêm 4 mL dung dịch H2SO4 loãng và thêm tiếp 10 giọt dung dịch H3PO4 (để che màu vàng của ion Fe3+).
Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 nồng độ 0,02M đến khi xuất hiện màu hồng nhạt bền trong 10 giây thì dừng lại.
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
Lặp lại bước 3 thêm hai lần nữa. Thể tích trung bình của dung dịch KMnO4 sau ba lần chuẩn độ là 20,04 mL. Phần trăm khối lượng sắt trong quặng magnetit là bao nhiêu phần trăm? (Làm tròn kết quả đến hàng phần mười).


Bình luận